Координационная химия, 2022, T. 48, № 1, стр. 29-36
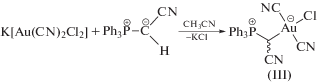
Синтез и строение комплексов золота [Ph3PR][Au(CN)2Cl2] (R = CH2CH=CHCH3, CH2CN) и Ph3PC(H)(CN)Au(CN)2Cl
Д. П. Шевченко 1, *, А. Е. Хабина 1, В. В. Шарутин 1, О. К. Шарутина 1, В. С. Сенчурин 1
1 Южно-Уральский государственный университет
(национальный исследовательский университет)
Челябинск, Россия
* E-mail: Shepher56@gmail.com
Поступила в редакцию 23.05.2021
После доработки 14.07.2021
Принята к публикации 23.07.2021
- EDN: BYNWAJ
- DOI: 10.31857/S0132344X22010054
Аннотация
Взаимодействием хлоридов органилтрифенилфосфония с дихлородицианоауратом калия в воде с последующей перекристаллизацией из ацетонитрила получены ионные комплексы [Ph3PR][Au(CN)2Cl2] (R = CH2CH=CHCH3 (I), CH2CN (II)). Наряду с основным продуктом II, были выделены кристаллы молекулярного комплекса Ph3PC(H)(CN)Au(CN)2Cl (III). Полученные соединения охарактеризованы методами рентгеноструктурного анализа (CIF files CCDC № 1957185 (I), 2060227 (II), 2066549 (III)), ЯМР- и ИК-спектроскопии. По данным РСА, комплексы I и II состоят из органилтрифенилфосфониевых катионов со слабоискаженными тетраэдрически-координированными атомами фосфора и центросимметричных квадратных анионов [Au(CN)2Cl2]−, которые в случае комплекса II образуют координационные псевдополимерные цепи посредством межанионных контактов Au∙∙∙Cl (3.40 Å). В комплексе III атомы фосфора и золота также тетраэдрически и квадратно координированы; илидный атом углерода располагается у золота в транс-положении относительно атома хлора.
При разработке новых потенциально полезных соединений значительное внимание уделяется возможности участия молекул и других структурных единиц в нековалентных взаимодействиях, которые играют важную роль в определении физико-химических свойств, а также биологической активности данных соединений [1–6]. Кроме того, в настоящее время немалый интерес у исследователей вызывают металлоорганические координационные полимеры (МОКП) [7–12].
Среди обилия строительных блоков для МОКП важное место занимают цианидные комплексы, в частности соединения одновалентного и трехвалентного золота, обладающие такими свойствами, как люминесценция [13–16], двойное лучепреломление [17–19], вапохромизм [20–22], отрицательный коэффициент термического расширения [23, 24] и магнетизм [13, 25–27]. Стратегический выбор вспомогательных лигандов и противоионов позволяет модифицировать указанные свойства.
С целью обнаружения новых цианоауратных координационных полимеров и в продолжение ряда исследований, посвященных изучению строения и свойств дигалогенодицианоауратных комплексов [28–33], мы осуществили синтез комплексов [Ph3PCH2CH=CHCH3][Au(CN)2Cl2] (I) и [Ph3PCH2CN][Au(CN)2Cl2] (II) (в смеси с побочным продуктом Ph3PC(H)(CN)Au(CN)2Cl (III)), а также описали особенности их строения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез проводили на воздухе. Коммерчески доступные хлориды (бут-2-енил)трифенилфосфония (97%, Alfa Aesar) и цианометилтрифенилфосфония (98%, Alfa Aesar), а также ацетонитрил (о. с. ч., Криохром) использовали без дополнительной очистки. Дихлородицианоаурат калия и цианометилид трифенилфосфония получали по методикам [17, 34].
Синтез дихлородицианоаурата (бут-2-енил)трифенилфосфония (I). К раствору 0.100 г (0.28 ммоль) дихлородицианоаурата калия в 10 мл воды прибавляли при перемешивании водный раствор 0.094 г (0.28 ммоль) хлорида (бут-2-енил)трифенилфосфония. Образовавшийся желтый осадок отфильтровывали, промывали водой и сушили. Перекристаллизацией из ацетонитрила получили кристаллы светло-желтого цвета. Выход комплекса I 0.160 г (90%). Tпл = 146°С.
ИК-спектр (ν, см–1): 3065, 3053, 3030, 2990, 2945, 2905, 2851, 2216, 1638, 1616, 1585, 1485, 1435, 1398, 1377, 1339, 1315, 1180, 1159, 1111, 1055, 997, 970, 922, 839, 795, 746, 737, 723, 689, 615, 540, 503, 486, 451, 426.
Соединение II – дихлородицианоаурат цианометилтрифенилфосфония – синтезировали по методике, аналогичной для I. Получили светло-желтые кристаллы. Выход 71%. Tпл = 121°С.
ИК-спектр (ν, см−1): 3061, 3024, 2930, 2866, 2766, 2259, 1587, 1483, 1441, 1393, 1319, 1252, 1186, 1113, 995, 843, 756, 743, 723, 689, 550, 503, 453, 428.
Молекулярный комплекс III получили в качестве побочного продукта (6%) при синтезе комплекса II, а также встречным синтезом, для которого приведена методика.
Синтез (цианометилтрифенилфосфоний)хлородицианозолота (III). К раствору 0.100 г (0.28 ммоль) дихлородицианоаурата калия в 10 мл ацетонитрила прибавляли при перемешивании 0.084 г (0.28 ммоль) цианометилилида трифенилфосфония. После испарения растворителя из фильтрата выделили бесцветные кристаллы. Выход III 0.134 г (82%). Tпл = 112°С.
ИК-спектр (ν, см−1): 3059, 3024, 2930, 2866, 2766, 2257, 2156, 2143, 1587, 1483, 1439, 1395, 1339, 1317, 1250, 1186, 1113, 997, 843, 756, 743, 723, 689, 547, 500, 428.
ИК-спектры соединений I−III записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S; образцы готовили таблетированием с KBr (область поглощения 4000−400 см−1).
РСА кристаллов I−III проводили на дифрактометре D8 QUEST Bruker (MoKα-излучение, λ = = 0.71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [35]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [36] и OLEX2 [37]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структур приведены в табл. 1, основные длины связей и валентные углы – в табл. 2.
Таблица 1.
Кристаллографические данные, параметры эксперимента и уточнения структуры соединений I−III
| Параметр | Значение | ||
|---|---|---|---|
| I | II | III | |
| М | 637.27 | 1244.44 | 585.76 |
| Сингония | Моноклинная | Моноклинная | Моноклинная |
| Пр. гр. | P2/c | P21 | P21/c |
| a, Å | 16.983(8) | 8.710(5) | 8.370(5) |
| b, Å | 8.483(3) | 14.036(6) | 14.984(8) |
| c, Å | 17.082(7) | 19.376(9) | 17.232(13) |
| α, град | 90.00 | 90.00 | 90 |
| β, град | 91.18(2) | 90.10(3) | 92.63(3) |
| γ, град | 90.00 | 90.00 | 90 |
| V, Å3 | 2460.4(18) | 2368.7(19) | 2159(2) |
| Z | 4 | 2 | 4 |
| ρ(выч.), г/см3 | 1.720 | 1.745 | 1.802 |
| μ, мм–1 | 6.275 | 6.517 | 7.024 |
| F(000) | 1232.0 | 1192.0 | 1120.0 |
| Размер кристалла, мм | 0.34 × 0.27 × 0.11 | 0.44 × 0.31 × 0.22 | 0.65 × 0.5 × 0.46 |
| Область сбора данных по θ, град | 5.86–65.66 | 5.9–54.28 | 5.93–56.996 |
| Интервалы индексов отражений | –25 ≤ h ≤ 25, –12 ≤ k ≤ 12, –25 ≤ l ≤ 25 |
–11 ≤ h ≤ 11, –18 ≤ k ≤ 18, –24 ≤ l ≤ 24 |
–11 ≤ h ≤ 11, –20 ≤ k ≤ 20, –23 ≤ l ≤ 23 |
| Измерено отражений | 75 175 | 36 915 | 43 689 |
| Независимых отражений (Rint) | 8951 (0.0425) | 10 456 (0.0313) | 5463 (0.0611) |
| Отражений с I > 2σ(I) | 8951 | 10 456 | 5463 |
| Переменных уточнения | 274 | 523 | 254 |
| GOOF | 1.074 | 1.077 | 1.060 |
| R-факторы по F 2 > 2σ(F 2) | R1 = 0.0357, wR2 = 0.0681 |
R1 = 0.0395, wR2 = 0.0959 |
R1 = 0.0460, wR2 = 0.1149 |
| R-факторы по всем отражениям | R1 = 0.0593, wR2 = 0.0775 |
R1 = 0.0438, wR2 = 0.0990 |
R1 = 0.0508, wR2 = 0.1192 |
| Остаточная электронная плотность (max/min), e/Å3 | 1.42/–1.72 | 1.31/–2.86 | 2.71/–3.69 |
Таблица 2.
Длины связей (d) и валентные углы (ω) в структурах I−III
| Связь | d, Å | Угол | ω, град |
|---|---|---|---|
| I | |||
| Au(1)–Сl(1) | 2.2947(13) | Cl(1)Au(1)Cl(1a) | 177.81(7) |
| Au(2)–Cl(2) | 2.2808(12) | C(7)Au(1)C(7a) | 179.0(2) |
| Au(1)–C(7) | 2.002(4) | C(7a)Au(1)Cl(1a) | 90.45(12) |
| Au(2)–C(8) | 2.015(4) | C(7)Au(1)Cl(1a) | 89.57(12) |
| P(1)–C(1) | 1.793(3) | Cl(2)Au(2)Cl(2b) | 180.0 |
| P(1)–C(11) | 1.797(3) | C(8)Au(2)C(8b) | 179.999(1) |
| P(1)–C(21) | 1.793(3) | C(8b)Au(2)Cl(2b) | 89.65(12) |
| P(1)–C(27) | 1.812(3) | C(8)Au(2)Cl(2b) | 90.35(12) |
| Преобразования симметрии: (a) –x, y, 3/2 – z; (b) 1 – x, 2 – y, 1 – z |
C(1)P(1)C(11) | 108.18(15) | |
| C(1)P(1)C(27) | 111.17(16) | ||
| II | |||
| Au(1)–Cl(1) | 2.281(2) | Cl(1)Au(1)Cl(2) | 178.28(10) |
| Au(1)–Cl(2) | 2.286(2) | C(9)Au(1)C(10) | 178.9(5) |
| Au(1)–C(9) | 1.955(12) | C(9)Au(1)Cl(1) | 89.6(3) |
| Au(1)–C(10) | 2.054(12) | C(9)Au(1)Cl(2) | 89.8(3) |
| Au(2)–Cl(3) | 2.275(2) | C(10)Au(1)Cl(1) | 90.0(3) |
| Au(2)–Cl(4) | 2.280(2) | C(10)Au(1)Cl(2) | 90.7(3) |
| Au(2)–C(39) | 2.023(13) | Cl(3)Au(2)Cl(4) | 178.49(10) |
| Au(2)–C(40) | 2.021(12) | C(39)Au(2)C(40) | 178.7(4) |
| Р(1)–C(1) | 1.792(7) | C(39)Au(2)Cl(3) | 90.8(3) |
| P(1)–C(11) | 1.786(7) | C(39)Au(2)Cl(4) | 89.9(3) |
| P(1)–C(21) | 1.792(7) | C(40)Au(2)Cl(3) | 90.5(3) |
| P(1)–C(7) | 1.827(7) | C(40)Au(2)Cl(4) | 88.9(3) |
| Р(2)–C(31) | 1.797(6) | C(1)P(1)C(21) | 111.7(3) |
| Р(2)–C(41) | 1.765(7) | C(11)P(1)C(7) | 106.1(3) |
| Р(2)–C(51) | 1.789(7) | C(41)P(2)C(31) | 112.3(3) |
| P(2)–C(37) | 1.826(7) | C(41)P(2)C(37) | 105.8(3) |
| III | |||
| Au(1)–Cl(1) | 2.318(2) | C(7)Au(1)Cl(1) | 177.76(15) |
| Au(1)–C(9) | 1.997(8) | C(9)Au(1)C(10) | 176.3(3) |
| Au(1)–C(10) | 2.006(7) | C(9)Au(1)C(7) | 93.7(2) |
| Au(1)–C(7) | 2.121(5) | C(9)Au(1)Cl(1) | 88.5(2) |
| C(7)–C(8) | 1.427(9) | C(10)Au(1)C(7) | 88.2(2) |
| P(1)–C(1) | 1.786(6) | C(10)Au(1)Cl(1) | 89.7(2) |
| P(1)–C(11) | 1.801(7) | P(1)C(7)Au(1) | 113.8(3) |
| P(1)–C(21) | 1.791(7) | C(8)C(7)Au(1) | 111.1(4) |
| P(1)–C(7) | 1.851(6) | C(8)C(7)P(1) | 112.7(4) |
| C(8)–N(1) | 1.137(10) | C(11)P(1)C(7) | 105.4(3) |
| C(9)–N(2) | 1.124(11) | C(21)P(1)C(7) | 113.9(3) |
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1957185 (I), 2060227 (II), 2066549 (III) для структур I−III соответственно, deposit@ ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Комплексы I и II были получены в результате взаимодействия водных растворов дихлородицианоаурата калия с хлоридами органилтрифенилфосфония (1 : 1 мольн.) с последующей перекристаллизацией из ацетонитрила.
Наряду с основным продуктом – ионным комплексом II светло-желтого цвета – был выделен минорный продукт в виде неокрашенных кристаллов цианометилтрифенилфосфоний)хлородицианозолота (III) с выходом 6%. Вероятно, в реакционной смеси в условиях синтеза происходит образование цианометилида трифенилфосфония Ph3PC(H)CN, атакующего анионы [Au(CN)2Cl2]– с образованием комплекса III.
Нами был осуществлен встречный синтез III взаимодействием дихлородицианоаурата калия с цианометилидом трифенилфосфония, специально полученным по методике [34]. В данном слу-чае основным продуктом реакции был комплекс III, выделенный с выходом 82%.
Отметим, что вследствие высокой подвижности метиленового атома водорода хлорида цианометилтрифенилфосфония образование илидного комплекса также возможно в ходе прямого C–H-аурирования, однако данный процесс более характерен для соединений золота(I) и обычно проходит в присутствии оснований [38–40].
В ИК-спектрах соединений I–III полосы поглощения валентных колебаний связей C≡N наблюдаются при 2216 (I), 2259 (II), 2257, 2156 и 2143 (III) см–1 и имеют низкую интенсивность. Колебаниям связей P–CPh соответствуют полосы поглощения в области 1450−1435 и 1005–995 см–1 (1435, 997 (I), 1441, 995 (II), 1439, 997 (III) см–1). Также в ИК-спектре комплекса I наблюдаются полосы поглощения, которые можно отнести к колебаниям связей ν(C=С) (1683 см–1) и δ(HC=СH) (970 см–1) бут-2-енильного фрагмента [41].
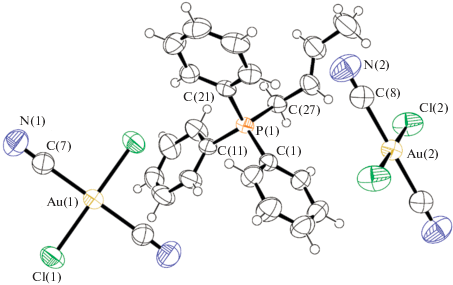
По данным РСА, кристаллы комплексов I и II состоят из органилтрифенилфосфониевых катионов и центросимметричных квадратных дихлородицианоауратных анионов (рис. 1 и 2 соответственно). Координация атомов фосфора незначительно искажена: углы CPC изменяются в интервалах 108.18(15)°–111.17(16)° (I) и 105.8(3)°–112.3(3)° (II). Бут-2-енильний заместитель в комплексе II присутствует в форме транс-изомера, углы C(27)C(28)C(29) и C(28)C(29)C(30) в котором составляют 123.5(4)° и 123.8(5)° соответственно. Атомы золота в анионах [Au(CN)2Cl2]– имеют практически неискаженную квадратную геометрию с транс-углами CAuC и цис-углами CAuCl, близкими к 180° и 90°.
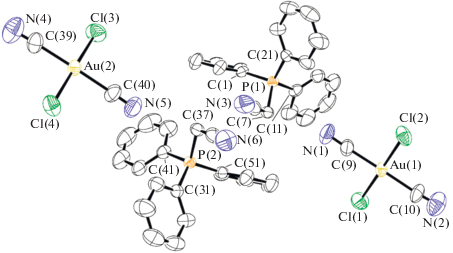
Рис. 2.
Общий вид комплекса II (термические эллипсоиды приведены с 50% вероятностью; атомы водорода не показаны).
Связи P–CAlk (1.812(3) Å (I), 1.826(7) и 1.827(7) Å (II)) длиннее связей P–CPh (1.793(3)−1.797(3) Å (I) и 1.765(7)−1.797(6) Å (II)). Расстояния Au–C 2.002(4), 2.015(4) Å (I) и 1.955(12)–2.054(12) Å (II) меньше суммы ковалентных радиусов атомов золота и sp-гибридизованного углерода (2.05 Å [42]). Длины связей Au–Cl (2.2808(12), 2.2947(13) Å (I), 2.275(2)–2.286(2) Å (II)) также меньше суммы ковалентных радиусов атомов золота и хлора (2.38 Å [42]).
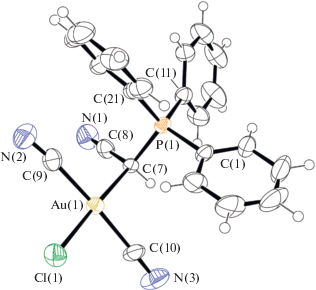
В комплексе III атомы фосфора и золота имеют тетраэдрическую и квадратную координацию соответственно, при этом транс-положение относительно атома хлора у золота занято илидным атомом углерода (рис. 3). Углы CPC (105.4(3)°–113.9(3)°) незначительно отличаются от таковых для II и III; углы P(1)C(7)Au(1), C(8)C(7)Au(1) и C(8)C(7)P(1) равны 113.8(3)°, 111.1(4)° и 112.7(4)° соответственно. Связи P(1)–CPh короче, чем P(1)–C(7) (1.851(6) Å), и варьируются в интервале 1.786(6)–1.801(7) Å.
Значения транс-углов CAuC 176.3(3)° и 177.76(15)° свидетельствует о незначительном искажении квадратной координации атома золота; цис-углы CAuC и CAuCl равны 93.7(2)°, 88.2(2)° и 88.5(2)°, 89.7(2)° соответственно. Расстояния Au(1)–CCN (1.997(8), 2.006(7) Å) практически не отличаются от таковых в ионных комплексах; расстояние Au(1)–C(7) составляет 2.121(5) Å и совпадает с суммой ковалентных радиусов атома золота и sp3-гибридизованного атома углерода (2.12 Å [42]). Связь Au(1)–Cl(1) (2.318(2) Å) на 0.035 Å длиннее среднего значения длин связей Au–Cl в I и II (2.283 Å), что обусловлено транс-влиянием илидного лиганда. Следует отметить, что в структурно охарактеризованном комплексе Ph3PC(H)(CN)AuCl3 сходного строения аналогичные длины связей атома золота с атомами углерода и хлора имеют меньшие значения (Au–C 2.083(4), Au–Cl 2.3095(13) Å) [43].
Структурная организация в кристаллах I–III обусловлена водородными связями С–H∙∙∙N≡C (2.58, 2.64 Å (I), 2.28–2.43 Å (II), 2.40–2.55 Å (III)) и С–H∙∙∙Cl–Au (2.83 Å (I), 2.81, 2.84 Å (II), 2.81 Å (III)). В кристалле II анионы [Au(CN)2Cl2]– образуют координационные псевдополимерные цепи, ориентированные вдоль кристаллографической оси a (рис. 4) и построенные на основе межанионных контактов Au(1)∙∙∙Cl(3) и Au(2)∙∙∙Cl(1) (3.40 Å), длины которых меньше суммы ван-дер-ваальсовых радиусов атомов золота и хлора (3.41 Å [44]).
Таким образом, взаимодействием хлорида (бут-2-енил)трифенилфосфония с дихлородицианоауратом калия получен ионный мономерный комплекс – дихлородицианоаурат (бут-2-енил)трифенилфосфония. В аналогичной реакции с участием хлорида цианометилтрифенилфосфония наблюдается образование дихлородицианоаурата цианометилтрифенилфосфония, структура которого содержит обусловленные контактами Au∙∙∙Cl псевдополимерные цепи из анионов [Au(CN)2Cl2]–, а также минорного продукта реакции – илидного комплекса (цианометилтрифенилфосфоний)хлородицианозолота.
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Janiak C. // Dalton Trans. 2003. № 14. P. 2781. https://doi.org/10.1039/B305705B
Desiraju G.R. // Angew. Chem., Int. Ed. 2007. V. 46. № 44. P. 8342. https://doi.org/10.1002/anie.200700534
Dunitz J.D., Gavezzotti A. // Chem. Soc. Rev. 2009. V. 38. № 9. P. 2622. https://doi.org/10.1039/B822963P
Sculfort S., Braunstein P. // Chem. Soc. Rev. 2011. V. 40. № 5. P. 2741. https://doi.org/10.1039/C0CS00102C
Alkorta I., Elguero J., Frontera A. // Crystals. 2020. V. 10. № 3. P. 180. https://doi.org/10.3390/cryst10030180
Rodina T.A., Loseva O.V., Ivanov A.V. // J. Struct. Chem. 2021. V. 62. P. 123. https://doi.org/10.1134/S0022476621010157
Batten S.R., Champness N.R. // Phil. Trans. R. Soc. A. 2017. V. 375. № 2084. ID 20160025. https://doi.org/10.1098/rsta.2016.0032
Furukawa H., Cordova K.E., O’Keeffe M., Yaghi O.M. // Science. 2013. V. 341. № 6149. ID 1230444. https://doi.org/10.1126/science.1230444
Liu J., Chen L., Cui H. et al. // Chem. Soc. Rev. 2014. V. 43. № 16. P. 6011. https://doi.org/10.1039/C4CS00094C
Liu J.-Q., Luo Z.-D., Pan Y. et al. // Coord. Chem. Rev. 2020. V. 406. P. 213145. https://doi.org/10.1016/j.ccr.2019.213145
Baranov A.Yu., Rakhmanova M.I., Samsonenko D.G. et al. // Inorganica Chim Acta. 2019. V. 494. P. 78. https://doi.org/10.1016/j.ica.2019.05.015
Petrovskii S.K., Paderina A.V., Sizova A.A. et al. // Dalton Trans. 2020. V. 49. № 38. P. 13430. https://doi.org/10.1039/D0DT02583F
Kumar K., Stefańczyk O., Chorazy S. et al. // Inorg. Chem. 2019. V. 58. № 9. P. 5677. https://doi.org/10.1021/acs.inorgchem.8b03634
Nicholas A.D., Bullard R.M., Pike R.D., Patterson H. // Eur. J. Inorg. Chem. 2019. V. 2019. № 7. P. 956. https://doi.org/10.1002/ejic.201801407
Belyaev A., Eskelinen T., Dau T. et al. // Chem. Eur. J. 2017. V. 24. № 6. P. 1404. https://doi.org/10.1002/chem.201704642
Ovens J.S., Christensen P.R., Leznoff D.B. // Chem. Eur. J. 2016. V. 22. № 24. P. 8234. https://doi.org/10.1002/chem.201505075
Ovens J.S., Geisheimer A.R., Bokov A.A. et al. // Inorg. Chem. 2010. V. 49. № 20. P. 9609. https://doi.org/10.1021/ic101357y
Katz M.J., Leznoff D.B. // J. Am. Chem. Soc. 2009. V. 131. № 51. P. 18435. https://doi.org/10.1021/ja907519c
Thompson J.R., Goodman-Rendall K.A.S., Leznoff D.B. // Polyhedron. 2016. V. 108. P. 93. https://doi.org/10.1016/j.poly.2015.12.026
Lefebvre J., Korčok J.L., Katz M.J., Leznoff D.B. // Sensors. 2012. V. 12. № 3. P. 3669. https://doi.org/10.3390/s120303669
Varju B.R., Ovens J.S., Leznoff D.B. // Chem. Commun. 2017. V. 53. № 48. P. 6500. https://doi.org/10.1039/C7CC03428H
Ovens J.S., Leznoff D.B. // Chem. Mater. 2015. V. 27. № 5. P. 1465. https://doi.org/10.1021/cm502998w
Ovens J.S., Leznoff D.B. // Inorg. Chem. 2017. V. 56. № 13. P. 7332. https://doi.org/10.1021/acs.inorgchem.6b03153
Ovens J.S., Leznoff D.B. // CrystEngComm. 2018. V. 20. № 13. P. 1769. https://doi.org/10.1039/C7CE02167D
Lefebvre J., Chartrand D., Leznoff D.B. // Polyhedron. 2007. V. 26. № 9–11. P. 2189. https://doi.org/10.1016/j.poly.2006.10.045
Lefebvre J., Tyagi P., Trudel S. et al. // Inorg. Chem. 2009. V. 48. № 1. P. 55. https://doi.org/10.1021/ic801094m
Geisheimer A.R., Huang W., Pacradouni V. et al. // Dalton Trans. 2011. V. 40. № 29. P. 7505. https://doi.org/10.1039/C0DT01546F
Sharutin V.V., Sharutina O.K., Tarasova N.M., Efremov A.N. // Russ. J. Inorg. Chem. 2020. V. 65. № 2. P. 169. https://doi.org/10.1134/S0036023620020151
Sharutin V.V., Sharutina O.K., Efremov A.N., Eltsov O.S. // Russ. J. Coord. Chem. 2020. V. 46. № 9. P. 631. https://doi.org/10.1134/S1070328420090031
Шарутин В.В. // Вест. Южно-Урал. гос. ун-та. Сер. хим. 2020. Т. 12. № 2. С. 74 (Sharutin V.V. // Bull. South Ural State Univ., Ser. Chem. 2020. V. 12. № 2. P. 74). https://doi.org/10.14529/chem200208
Sharutin V.V., Sharutina O.K., Tarasova N.M. et al. // Russ. Chem. Bull. 2020. V. 69 № 10. P. 1892. https://doi.org/10.1007/s11172-020-2975-4
Efremov A.N., Sharutin V.V., Sharutina O.K. et al. // Изв. вузов. Сер. хим. технол. 2020. Т. 63. № 3. С. 10. https://doi.org/10.6060/ivkkt.20206303.6097
Шевченко Д.П., Хабина А.Е. // Вест. Южно-Урал. гос. ун-та. Сер. хим. 2021. Т. 13. № 1. С. 58 (Shevchenko D.P., Khabina A.E. // Bull. South Ural State Univ. Ser. Chem. 2021. V. 13. № 1. P. 58). https://doi.org/10.14529/chem210106
Johnson A. Doctoral Thesis. Zaragoza: Zaragoza University, 2018. 401 p.
SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Madison (WI, USA): Bruker AXS Inc., 1998.
SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Madison (WI, USA): Bruker AXS Inc., 1998.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. A-ppl. Cryst. 2009. V. 42. P. 339. https://doi.org/10.1107/S0021889808042726
Vicente J., Chicote M.T. // Coord. Chem. Rev. 1999. V. 193–195. P. 1143. https://doi.org/10.1016/S0010-8545(99)00083-1
Djordjevic B., Schuster O., Schmidbaur H. // Z. Naturforsch. B. 2005. V. 60. № 2. P. 169. https://doi.org/10.1039/C3CY00240C
Ahlsten N., Perry G.J.P., Cambeiro X.C. et al. // Catal. Sci. Technol. 2013. V. 3. № 11. P. 2892. https://doi.org/10.1515/znb-2005-0207
Преч Э., Бюльманн Ф., Аффольтер К. Определение строения органических соединений. М.: Мир, 2006. 440 с.
Cordero, B., Gómez V., Platero-Prats A.E. et al. // Dalton Trans. 2008. № 21. P. 2832. https://doi.org/10.1039/B801115J
Johnson A., Marzo I., Gimeno M.C. // Chem. Eur. J. 2018. № 45. P. 11693. https://doi.org/10.1002/chem.201801600
Mantina M., Chamberlin A.C., Valero R. et al. // J. Phys. Chem. A. 2009. V. 113. № 19. P. 5806. https://doi.org/10.1021/jp8111556
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия