Координационная химия, 2022, T. 48, № 8, стр. 500-505
Кадмий(II)-органические координационные полимеры, содержащие лиганд 1,3-бис-(2-метилимидазолил)пропан
П. В. Бурлак 1, К. А. Коваленко 1, Д. Г. Самсоненко 1, В. П. Федин 1, *
1 Институт неорганической химии им. А.В. Николаева СО РАН
Новосибирск, Россия
* E-mail: cluster@niic.nsc.ru
Поступила в редакцию 08.12.2021
После доработки 03.02.2022
Принята к публикации 12.03.2022
- EDN: OHCRNX
- DOI: 10.31857/S0132344X22080023
Аннотация
Методом монокристального рентгеноструктурного анализа определена кристаллическая структура двух новых изоретикулярных металл-органических координационных полимеров [Cd3(Bdc-X)3(Bmip)2] (X = = Br, Bdc-Br2− – 2-бромотерефталат) (I); X = NO2, Bdc-${\text{NO}}_{2}^{{2 - }}$ – 2-нитротерефталат) (II); Bmip – 1,3-бис(2-метилимидазолил)пропан). Соединения I и II содержат трехъядерные карбоксилатные строительные блоки {Cd3(COO)6N4}, в которых атомы кадмия координированы донорными атомами азота лигандов Bmip с образованием непористых трехмерных каркасов (CCDC № 2126695 (I), 2126696 (II) соответственно). Соединение I охарактеризовано методами порошковой рентгеновской дифракции, ИК-спектроскопии, элементного CHN- и термогравиметрического анализов, a также для него исследованы сорбционные характеристики и получены спектры люминесценции.
Металл-органические координационные полимеры (МОКП, MOF) построены из неорганических и органических строительных блоков/фрагментов, при этом органические политопные лиганды-линкеры играют роль мостиков между моноядерными катионами металлов или кластерами/полиядерными комплексами. Изучение МОКП является одним из ведущих направлений в современной химии и материаловедении [1–4]. МОКП рассматриваются как перспективные материалы для катализа, хранения газов, сенсорных материалов, для разработки лекарств пролонгированного действия, суперконденсаторов, новых проводящих материалов и т.д. [5–15].
Несмотря на многие интересные функциональные свойства, указанные выше, на наш взгляд, по-прежнему актуальным является развитие методов направленного синтеза МОКП с прогнозируемой структурой и свойствами. Известно, что использование стерически жестких органических лигандов при синтезе МОКП часто приводит к повышению стабильности каркаса и позволяет получать ряды изоретикулярных соединений. Поэтому часто для синтеза металл-органических координационных полимеров используются поликарбоксилатные лиганды, в частности терефталевая кислота (H2Bdc). На основе терефталатов построено большое число широко известных каркасов, таких как MIL-101 [16], MIL-53 [17], MOF-5 [18], UiO-66 [19] и пр. С другой стороны, использование органических лигандов, способных легко менять свою конформацию, может приводить к образованию структурно нежестких/гибких металл-органических координационных полимеров [20]. Такие соединения могут найти применение в селективной адсорбции, для создания разнообразных умных материалов, отклик которых вызывается активирующим внешним воздействием [21]. Примером структурно гибкого лиганда для синтеза МОКП является 1,3-бис(2-метилимидазолил)пропан (Bmip) [22]. Благодаря алкильной группе, объединяющей имидазольные группы, данный лиганд может изменять свою конформацию, сгибаться и растягиваться; при этом расстояния между донорными атомами азота в МОКП может меняться от 5.6 [23] до 8.8 Å [24]. Необходимо отметить, что химия МОКП на основе 1,3-бис(2-метилимидазолил)пропана изучена недостаточно, и на сегодняшний день известно 18 МОКП на основе Bmip (по данным Кембриджской базы структурных данных) [24, 25]. Такое ограниченное число примеров может быть связано в том числе с высокой конформационной подвижностью гибкого лиганда, что затрудняет поиск оптимальных условий получения монокристаллов МОКП.
В настоящей работе сообщается об определении кристаллической структуры двух новых изоретикулярных металл-органических координационных полимеров кадмия(II) – [Cd3(Bdc-Br)3(Bmip)2] (I) и [Cd3(Bdc-NO2)3(Bmip)2] (II), содержащих одновременно два типа лигандов: структурно жесткий 2-бромо- (Bdc-Br) и 2-нитротерефталат (Bdc-NO2), соответственно, и структурно гибкий лиганд (Bmip).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все реагенты и растворители были чистоты не ниже “х.ч.” и использовали без дополнительной очистки. Синтез лиганда Bmip проводили по модифицированной методике, описанной в [26–28].
Спектры ЯМР 1H записывали на ЯМР-спектрометре Bruker Advance 500. ИК-спектры в диапазоне 4000–400 см–1 регистрировали на Фурье-спектрометре Bruker Scimitar FTS 2000. Элементный анализ выполняли на CHNS-анализаторе VarioMICROcube. Данные РФА получали на порошковом дифрактометре Shimadzu XRD 7000S (CuKα-излучение, λ = 1.54056 Å). Термогравиметрический анализ проводили на термоанализаторе NETZSCH TG 209 F1 Iris при линейном нагревании образцов в атмосфере He со скоростью 10°/мин. Спектры твердотельной люминесценции записывали на спектрометре Horiba Jobin Yvon Fluorolog 3, оснащенном 450 Вт Xe-лампой и детектором PM-1073 PMT. Для определения квантового выхода люминесценции твердых образцов использовали Spectralon с G8 интеграционной сферой (GMP SA). Сорбционные измерения проводили на автоматическом адсорбционном анализаторе Quantachrome Autosorb iQ с приставкой CryoCooler для измерений при 195 К.
РСА. Дифракционные данные для монокристалла I получены при 100 К на синхротронной станции “Белок” Национального исследовательского центра “Курчатовский институт”, используя двухкоординатный детектор Rayonix SX165 CCD (λ = 0.79313 Å, φ-сканирование с шагом 1.0°). Интегрирование, учет поглощения, определение параметров элементарной ячейки проведены с использованием пакета программ XDS [29]. Дифракционные данные для монокристалла II получены при 150 К на автоматическом дифрактометре Agilent Xcalibur, оснащенном двухкоординатным детектором AtlasS2 (графитовый монохроматор, λ(MoKα) = 0.71073 Å, ω-сканирование с шагом 0.5°). Интегрирование, учет поглощения, определение параметров элементарной ячейки проведены с использованием пакета программ CrysAlisPro [29]. Структуры расшифрованы с использованием программы SHELXT [30] и уточнены полноматричным МНК в анизотропном (за исключением атомов водорода) приближении с использованием программы SHELXL [31]. Позиции атомов водорода органических лигандов рассчитаны геометрически и уточнены по модели “наездника”. В структурах I и II некоторые гостевые молекулы сильно разупорядочены и не могут быть уточнены как набор дискретных позиций. В связи с этим окончательный состав определен на основании данных процедуры SQUEEZE/PLATON [32] (59 e в 359 Å3 для I и 89 e в 438 Å3 для II). Кристаллографические данные и детали уточнения структуры приведены в табл. 1.
Таблица 1.
Кристаллографические данные, параметры эксперимента и уточнения структуры I и II
| Параметр | Значение | |
|---|---|---|
| I | II | |
| Брутто-формула | C46H45N8O14Br3Cd3 | C46H45N11O20Cd3 |
| M | 1510.83 | 1409.13 |
| Сингония | Моноклинная | Моноклинная |
| Пр. группа | C2/c | C2/c |
| a, Å | 26.455(5) | 27.6407(4) |
| b, Å | 12.276(6) | 11.82254(15) |
| c, Å | 16.530(4) | 16.7692(2) |
| β, град | 91.097(8) | 90.1829(13) |
| V, Å | 5367(3) | 5479.87(12) |
| Z | 4 | 4 |
| F(000) | 2952 | 2808 |
| ρ, г см−3 | 1.870 | 1.708 |
| µ, мм−1 | 4.577 | 1.238 |
| Размер кристалла, мм | 0.11 × 0.10 × 0.09 | 0.27 × 0.24 × 0.08 |
| Число измеренных, независимых и наблюдаемых (I > 2σ(I)) отражений | 36 064, 6069, 5926 | 17 163, 6218, 5734 |
| Rint | 0.0321 | 0.0178 |
| Область сканирования по θ, град | 2.04–30.99 | 1.87–28.85 |
| Интервалы индексов отражений | −34 ≤ h ≤ 34, −15 ≤ k ≤ 15, −21 ≤ l ≤ 21 | −36 ≤ h ≤ 32, −14 ≤ k ≤ 15, −22 ≤ l ≤ 11 |
| Добротность по F 2 | 1.172 | 1.046 |
| R-факторы (I > 2σ(I)) | R1 = 0.0440, wR2 = 0.1023 | R1 = 0.0421, wR2 = 0.1080 |
| R-факторы (по всем отражениям) | R1 = 0.0447, wR2 = 0.1026 | R1 = 0.0454, wR2 = 0.1099 |
| Остаточная электронная плотность (max/min), e Å−3 | 0.927/−1.040 | 1.693/−0.877 |
Полные таблицы межатомных расстояний и валентных углов, координаты атомов и параметры атомных смещений депонированы в Кембриджском банке структурных данных (CCDC № 2126695 (I), 2126696 (II); https://www.ccdc.cam.ac.uk/structures/).
Синтез 1,3-бис(2-метилимидазолил)пропана. Суспензию 3.28 г (40 ммоль) 2-метилимидазола (2-mIm), 3.36 г (60 ммоль) порошкообразного КОН и 10 мл ДМСО интенсивно перемешивали при 80°C в течение 30 мин. Затем реакционную колбу погружали в баню с холодной водой и после охлаждения до комнатной температуры в течение 30 мин по каплям добавляли 2.1 мл (20 ммоль) 1,3-дибромпропана в 10 мл ДМСО. Реакционную смесь перемешивали и кипятили с обратным холодильником в течение ночи, затем добавляли 200 мл воды и упаривали в вакууме на роторном испарителе. Из полученного твердого остатка продукт экстрагировали этилацетатом (3 × 15 мл). Удаление этилацетата в вакууме на роторном испарителе дает продукт в виде светло-желтых кристаллов. Выход 88%. Чистота образца была подтверждена методом ЯМР 1H и элементным CHN-анализом:
ЯМР 1H (CDCl3; δ, м.д.): 6.90 (д., J = 1.3 Гц, 2H, H4-2-mIm), 6.75 (д., J = 1.3 Гц, 2H, H5-2-mIm), 3.81 (т., J = 7.1 Гц, 4H, 2-mImCH2CH2), 2.26 (с., 6H, CH3-Im), 2.16 (к., J = 7.1 Гц, 2H, 2-mImCH2CH2).
Синтез [Cd3(Bdc-Br)3(Bmip)2] (I). Смесь Cd(NO3)2 ∙ 4H2O (0.25 ммоль, 77 мг), 2-бромтерефталевой кислоты H2Bdc-Br (0.25 ммоль, 62 мг), Bmip (0.25 ммоль, 51 мг), ДМФА (13.75 мл), этилового спирта (12 мл) нагревали при 373 К в течение 24 ч в стеклянном флаконе с завинчивающейся крышкой. Полученные кристаллы отделяли декантацией, промывали ДМФА (3 × 5 мл), этанолом (3 × 5 мл) и сушили на воздухе. Выход 54% (66 мг).
ИК-спектр, (KBr; ν, см–1): 3502 сл.ш ν(O–H), 1596 ср, 1544 с νas(C=O), 1504 ср γ(С–С), 1480 ср νs(СОО–), 1378 с νs(C=O), 1298 сл, 1279 сл, 1272 сл, 1151 сл, 1081 сл, 1035 сл, 999 сл, 941 сл, 880 сл, 863 сл, 841 ср, 821 ср, 766 с, 737 ср, 665 ср, 624 сл, 558 сл, 517 ср, 466 сл, 440 сл, 420 сл.
Синтез монокристаллов [Cd3(Bdc-NO2)3(Bmip)2] (II). Смесь Cd(NO3)2 ∙ 4H2O (0.025 ммоль, 7.7 мг), нитротерефталевой кислоты H2Bdc-NO2 (0.025 ммоль, 5.3 мг), Bmip (0.025 ммоль, 5.1 мг), ДМФА (1.2 мл), этилового спирта (1.2 мл) и воды (0.175 мл) нагревали при 373 К в течение 24 ч в стеклянном флаконе с завинчивающейся крышкой. Состав и строение получившихся кристаллов определяли методом РСА. Для получения представительных количеств аналитически чистого образца требуется дальнейшая оптимизация методики синтеза.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
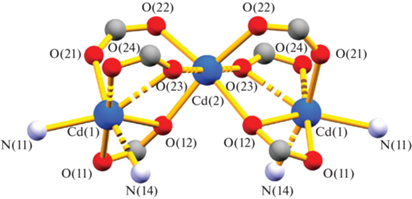
Соединение [Cd3(Bdc-Br)3(Bmip)2] (I) кристаллизуется в моноклинной пространственной группе C2/c. Независимая часть структуры I содержит два катиона кадмия. Cd(2) находится в октаэдрическом координационном окружении из шести атомов кислорода шести карбоксилатных групп. Расстояния Cd(2)–O лежат в диапазоне 2.205(3)–2.353(3) Å. В структуре I присутствуют два типа бромтерефталатных лигандов. Один из них располагается в частной позиции на центре инверсии, другой располагается в позиции общего типа. Атом брома в обоих бромтерефталатах разупорядочен по двум позициям (0.5/0.5 и 0.75/0.25). Координационное окружение Cd(1) содержит два атома азота двух лигандов Bmip, и пять атомов кислорода трех карбоксилатных групп, две из которых координируются бидентатно. Фрагмент лиганда Bmip разупорядочен по двум ориентациям с относительными весами 0.643(8)/0.357(8). Расстояния Cd(1)–N лежат в диапазоне 2.278(4)–2.297(6) Å, расстояния Cd(1)–O – в диапазоне 2.343(3)–2.573(4) Å. Координационное число Cd(1) можно описать как 5 + 2. Катион Cd(2) и два катиона Cd(1) объединяются посредством мостиковых карбоксилатных групп в трехъядерный координационный фрагмент {Cd3(Bmip)4(μ-RCOO-κ1,κ1)2- (μ-RCOO-κ1,κ2)4} (рис. 1). Такие трехъядерные фрагменты соединяются между собой посредством мостиковых лигандов Bdc-Br с образованием полимерных слоeв, параллельных плоскости bc (рис. 2а). Соседние слои соединяются между собой мостиковыми лигандами Bmip, образуя трехмерный металл-органический каркас (рис. 2б), содержащий только небольшие изолированные полости (6% объема элементарной ячейки, рассчитано по программе Mercury).
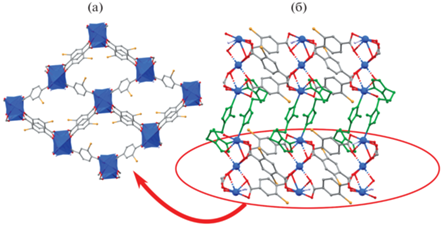
Рис. 2.
Структура [Cd3(Bdc-Br)3(Bmip)2]: двумерный слой, построенный трехъядерными кластерами кадмия и лигандами Bdc-Br2− (а); 3D-структура, двумерные слои, объединенные лигандами Bmip (б).
Соединение [Cd3(Bdc-NO2)3(Bmip)2] (II) изоструктурно соединению I. Отличия заключаются в том, что вместо 2-бромтерефталата в структуре II присутствует 2-нитротерефталат. При этом нитрогруппа разупорядочена только у одного из двух лигандов Bdc-${\text{NO}}_{2}^{{2 - }}$, расположенного в частной позиции на центре инверсии. Также в структуре II не наблюдается разупорядочения нейтрального лиганда Bmip. Расстояния Cd(2)–O находятся в диапазоне 2.177(3)–2.347(3) Å. Расстояния Cd(1)–O лежат в диапазоне 2.332(3)–2.675(3) Å, а расстояния Cd(1)–N составляют 2.273(3) и 2.287(4) Å. Структура II, так же как и I, является плотной, и объем свободного пространства, рассчитанный по программе Mercury, составляет только 4%.
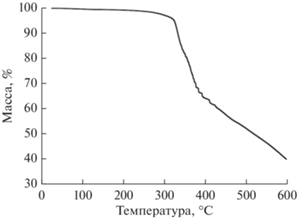
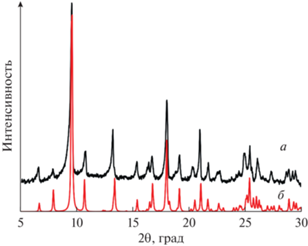
Соединение I было охарактеризовано методами РФА, ИК-спектроскопии, ТГ-анализа, элементного анализа. Было показано, что порошкограмма образца I полностью соответствует порошкограмме, рассчитанной из данных монокристального РСА (рис. 3). По данным термического анализа была показана высокая термическая стабильность I. При его нагревании до температуры 300°С не происходит изменение массы образца (рис. 4).
Рис. 3.
Рентгенограмма [Cd3(Bdc-Br)3(Bmip)2]: экспериментальная (a) и рассчитанная из данных монокристального эксперимента (б).
В литературе описан другой металл-органический координационный полимер близкого состава [Cd3(Bdc)3(Bmip)2] (III) [33], полученный с использованием незамещенной терефталевой кислоты (H2Bdc). Соединения I–III являются изоретикулярными, кристаллизуются в моноклинной пространственной группе С2/c, построены на основе схожих по строению трехъядерных неорганических строительных блоков и имеют одинаковую топологию трехмерных каркасов. Однако резко различаются объемы элементарных ячеек (5367(3) Å3 для I, 5479.87(12) Å3 для II и 6220.0(9) Å3 для III). В отличие от I и II каркас III является перманентно пористым, а объем, доступный для включения гостевых молекул, составляет 32.4%. Сравнение структур показывает, что в I и II расстояние между донорными атомами азота гибкого лиганда 1,3-бис(2-метилимидазолил)пропана составляет 6.924 и 6.837 Å, соответственно, против 7.363 Å в III. Такие резкие различия в структуре лиганда, вызванные его конформационной подвижностью, приводят к значительным изменениям сорбционных свойств: каркас III сорбирует заметное количество углекислого газа, тогда как изотермы низкотемпературной адсорбции углекислого газа при 195 К для соединение I показывают практически нулевую емкость.
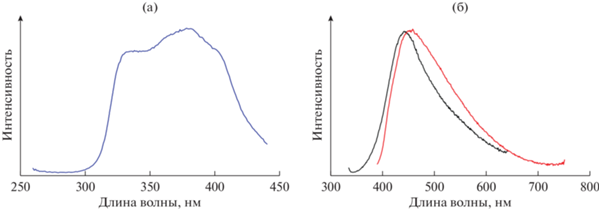
Для соединения I были исследованы фотофизические свойства. В спектре возбуждения I наблюдаются две широкие полосы (рис. 5). На основании литературных данных наблюдаемые максимумы возбуждения можно отнести к поглощению 2‑бромтерефталата (325 нм) и 1,3-бис(2-метилимидазолил)пропана (375 нм). Спектры фотолюминесценции регистрировали при двух различных длинах волн возбуждения. В обоих случаях образец демонстрирует синее излучение с широкой полосой эмиссии с максимумом 440 нм при длине волны возбуждения 325 нм и с максимумом 450 нм при длине волны возбуждения 375 нм. Комплексы Cd(II) c электронной конфигурацией d10 не являются редокс-активными, для них не реализуется механизм переноса заряда от металла к лиганду (MLCT) или от лиганда к металлу (LMCT). В нашем случае реализуется лиганд-центрированная люминесценция, и наблюдаемая эмиссия может быть отнесена к внутрилигандым переходам π* → π и/или π* → n в органических лигандах. Квантовый выход для I составил 19% при λэм = = 375 нм. Довольно высокое значение квантового выхода может быть результатом более высокой механической стабильности (жесткости) непористого каркаса I. Действительно, плотная структура препятствует возможным колебаниям органических линкеров и каркаса в целом, тем самым уменьшая вероятность релаксации фотовозбужденного электронного состояния через последовательные колебательные состояния.
Рис. 5.
Спектры твердотельного возбуждения при 450 нм (а); спектры твердотельной эмиссии при λвозб = 325 нм (черная) и 375 нм (красная) (б).
Таким образом, семейство изоретикулярных металл-органических координационных полимеров кадмия(II) построено на основе двух типов лигандов – структурно жестких терефталатов и структурно-гибкого 1,3-бис(2-метилимидазолил)пропана. Показано, что введение заместителей в терефталатный лиганд приводит к непористым каркасам, за счет изменения конформации гибкого лиганда.
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Furukawa H., Cordova K.E., O’Keeffe M. et al. // Science. 2013. V. 341. № 6149. P. 1230444.
Zhou H.-C., Kitagawa S. // Chem. Soc. Rev. 2014. V. 4.
Czaja A.U., Trukhan N., Müller U. // Chem. Soc. Rev. 2009. V. 38. № 5. P. 1284.
Cui Y., Li B., He H. et al. // Acc. Chem. Res. 2016. V. 49. № 3. P. 483.
Corma A., Garcia H., Xamena F.X.L. // Chem. Rev. 2010. V. 110. № 8. P. 4606.
Wang A., Li J., Zhang T. // Nature Rev. Chem. 2018. V. 2. P. 65.
Suh M.P., Park H.J., Prasad T.K. et al. // Chem. Rev. 2012. V. 112. № 2. P. 782.
Sumida K., Rogow D.L., Mason J.A. et al. // Chem. Rev. 2012. V. 112. № 2. P. 724.
He Y., Zhou W., Qian G. et al. // Chem. Soc. Rev. 2014. V. 43. № 16. P. 5657.
Tsivadze A.Y., Aksyutin O.E., Ishkov A. et al. // Russ. Chem. Rev. 2019. V. 88. № 9. P. 925.
Kreno L.E., Leong K., Farha O.K. et al. // Chem. Rev. 2012. V. 112. № 2. P. 1105.
Ponomareva V.G., Kovalenko K.A., Chupakhin A.P. et al. // J. Am. Chem. Soc. 2012. V. 134. № 38. P. 15640.
Lim D.-W., Kitagawa H. // Chem. Soc. Rev. 2021. V. 50. № 11. P. 6349.
Yan J., Wang Q., Wei T. et al. // Adv. Energy Mater. 2014. V. 4. P. 1300816.
Horcajada P., Gref R., Baati T. et al. // Chem. Rev. 2012. V. 112. № 2. P. 1232.
Férey G., Mellot-Draznieks C., Serre C. et al. // Science. 2005. V. 309. № 5743. P. 2040.
Serre C., Millange F., Thouvenot C. et al. // Nature. 2002. V. 124. № 45. P. 13519.
Li H., Eddaoudi M., O’Keeffe M. et al. // Nature. 1999. V. 402. P. 276.
Cavka J., Jakobsen S., Olsbuy U. et al. // J. Am. Chem. Soc. 2008. V. 130. № 42. P. 13850.
Schneemann A., Bon V., Schwedler I. et al. // Chem. Soc. Rev. 2014. V. 43. № 16. P. 6062.
Xu L., Liu B., Zheng F. K. et al. // J. Solid State Chem. 2005. V. 178. № 11. P. 3396.
Hao H. J., Liu F., Su H. et al. // CrystEngComm. 2012. V. 14. № 20. P. 6726.
Altaf M., Mansha M., Sohail M. et al. // New J. Chem. V. 41. № 8. P. 2980.
Wang J., Lu L., He J. et al. // J. Mol. Struct. 2019. V. 1182. № II. P. 79.
Xue L.P., Li Z.H., Maet L.F. et al. // CrystEngComm. 2015. V. 17. № 33. P. 6441.
Barsukova M.O., Sapchenko S.A., Kovalenko K.A. et al. // New J. Chem. 2018. V. 42. № 8. P. 6408.
Barsukova M.O., Samsonenko D.G., Goncharova T.V. et al. // Russ. Chem. Bull. 2016. V. 65. P. 2914.
Barsukova M., Goncharova T., Samsonenko D. et al. // Crystals. 2016. V. 10. P. 132.
CrysAlisPro 1.171.38.46. Rigaku Oxford Diffraction. The Woodlands (TX, USA), 2015.
Sheldrick G.M. // Acta Crystallogr. A. 2015. V. 71. P. 3.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Spek A.L. // Acta Crystallogr. C. 2015. V. 71. № 1. P. 9.
Shi J.-T., Yue K., Liu B. et al. // CrystEngComm. 2014. V. 16. № 15. P. 3097.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия