Координационная химия, 2022, T. 48, № 9, стр. 551-557
Перенос спинового порядка с молекулы параводорода на противоион в комплексе иридия в условиях SABRE
В. В. Гараева 1, 2, К. А. Спиридонов 1, 3, И. А. Никовский 1, А. С. Перегудов 1, А. С. Кирютин 4, 5, А. В. Юрковская 4, 5, А. А. Полежаев 1, 6, В. В. Новиков 1, 2, *
1 Институт элементоорганических соединений РАН им. А.Н. Несмеянова
Москва, Россия
2 Московский физико-технический институт
(национальный исследовательский университет)
Долгопрудный, Россия
3 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
4 Международный томографический центр СО РАН
Новосибирск, Россия
5 Новосибирский государственный университет
Новосибирск, Россия
6 Московский государственный технический университет им. Н.Э. Баумана
(национальный исследовательский университет)
Москва, Россия
* E-mail: novikov84@ineos.ac.ru
Поступила в редакцию 14.12.2021
После доработки 16.01.2022
Принята к публикации 17.01.2022
- EDN: ERRXDM
- DOI: 10.31857/S0132344X22080035
Аннотация
На примере новых комплексов иридия, полученных при обратимом связывании с субстратом (пиридином) и параводородом, впервые показана возможность создания спиновой поляризации ядер 19F в противоионах, не образующих ковалентной связи с металлоцентром. Это позволило обнаружить интегральную поляризацию ядер 19F в слабо координирующихся тетрафторборат- и гексафторфосфат-анионах. На основе зависимости интенсивности сигналов в спектрах ЯМР для двух полученных комплексов иридия от магнитного поля определены оптимальные параметры напряженности магнитного поля для максимального усиления сигнала 19F в двух фторсодержащих анионах.
Спектроскопия ЯМР, являясь одним из основных методов определения строения вещества, нашла широкое применение в различных областях химии [1], биологии [2] и медицины [3]. В последнем случае, разумеется, необходимо упомянуть возможность неинвазивной медицинской диагностики внутренних органов при помощи магнитно-резонансной томографии (МРТ) [4–6]. Основное ограничение спектроскопии ЯМР для указанных применений связано с ее низкой чувствительностью, вызванной исключительно малой разницей заселенностей ядерных спиновых состояний при комнатной температуре [7, 8]. Как результат, существующие подходы к увеличению чувствительности основаны на существенном увеличении указанной разницы заселенностей, т.е. достижении гиперполяризации.
Одно из прорывных направлений в решении данной задачи связано с переносом спинового порядка с молекулы параводорода на изучаемую молекулу для создания неравновесной поляризации исследуемых ядер, так называемой индуцированной параводородом гиперполяризации ядер (ИППЯ). В отличие от большинства других подходов, направленных на создание ядерной гиперполяризации (таких как оптическая накачка благородных газов [9–11] и динамическая поляризация ядер [12, 13]), ИППЯ не требует дорогостоящего оборудования и подходит для получения широкого класса поляризованных молекул, в том числе контрастных агентов для МРТ.
Параводород является одним из двух спиновых изомеров молекулярного водорода, который можно легко получить охлаждением газообразного водорода до температур жидкого азота или гелия в присутствии подходящего парамагнитного катализатора. Хотя сам по себе параводород не дает сигналов в спектре ЯМР [14], нарушение магнитной эквивалентности атомов в молекуле параводорода при их парном присоединении к субстрату приводит к продуктам реакции, в которых неравновесное распределение заселенностей ядерных уровней, присущее паре спинов протонов параводорода, наблюдается как аномальное (иногда на несколько порядков) увеличение интенсивности сигналов в спектре ЯМР [14].
Для достижения подобного результата, кроме классических эффектов ИППЯ, связанных с каталитическим гидрированием непредельных субстратов в присутствии гомогенных [15] или гетерогенных [16] катализаторов, относительно недавно [17] был предложен подход SABRE (Signal Amplification by Reversible Exchange, усиление сигнала за счет обратимого обмена). В его основе лежит обратимое присоединение молекулярного водорода, содержащего определенный процент параводорода, и субстрата к металлоцентру гомогенного иридийсодержащего катализатора. В результате магнитных взаимодействий между спинами в полученном комплексе происходит перенос поляризации с гидридных протонов на другие спины ядер лиганда [18, 19] без его химической трансформации (без реакции гидрирования).
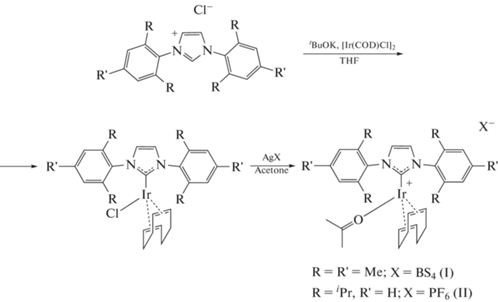
Подавляющее большинство катализаторов SA-BRE являются заряженными комплексами иридия, в состав которых входит слабо координирующийся противоион. Однако в научной литературе нам не удалось обнаружить сведений о возможности переноса поляризации на ядра, входящие в состав такого противоиона. Для того чтобы заполнить этот пробел, в рамках настоящей работы мы синтезировали два комплекса иридия с родственными карбеновыми лигандами (схема 1 ) и внешнесферными тетрафторборат- или гексафторфосфат-анионами – [Ir(COD){acetone}(IPr)]BF4 (тетрафтороборат[1,3-бис[2,6-диизопропилфенил]-2-имидазол-2-илиден]-[(η4)-1,5-циклооктадиен](2-пропанон)иридия) (I) и [Ir(COD){acetone}(IMes)]PF6 (гексафторфосфат [1,3-бис[2,4,6-триметилфенил]-2-имидазол-2-илиден]-[(η4)- 1,5-циклооктадиен](2-пропанон) иридия) (II). Входящие в состав последних магнитно-активные ядра 11B, 19F и 31P позволили нам изучить перенос спинового порядка с молекулы параводорода в условиях SABRE.
Схема 1 .
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все операции, связанные с синтезом и выделением комплексов, выполняли в атмосфере азота в перчаточном боксе. Соединения 1,3-бис(2,6-диизопропилфенил)имидазолий хлорид (IPr . HCl) и 1,3-бис(2,4,6-триметилфенил)имидазолий хлорид (IMes . HCl) использовали без дополнительной очистки (Sigma-Aldrich), (IrCODCl)2 получали по ранее описанной методике [20]. Синтез ранее описанных соединений [IrCl(COD)(IPr)] и [IrCl(COD)(IMes)] [21, 22] проводили по модифицированной методике генерации карбена in si-tu. Элементный анализ на углерод, азот и водород проводили на микроанализаторе Carlo Erba, модель 1106.
Синтез комплекса [IrCl(COD)(IPr)]. В перчаточном боксе смешивали [IrCl(COD)]2 (537 мг, 0.80 ммоль) и tBuOK (180 мг, 1.60 ммоль), к cмеси добавляли сухой ТГФ (10 мл) и полученный темно-красный раствор перемешивали при комнатной температуре в течение 10 мин. При добавлении к раствору IPr . HCl (680 мг, 1.60 ммоль) его цвет менялся с темно-красного на темно-желтый. Реакционную смесь перемешивали в течение 16 ч. Затем ТГФ удаляли в вакууме, остаток очищали методом колоночной хроматографии, элюируя продукт смесью EtOAc и петролейного эфира в соотношении 1 : 1. Выход 799 мг (69%).
ЯМР 1H (CDCl3; 400 МГц; δ, м.д.): 0.85 (м., 2Н, СН2), 1.11 (д., 12Н, СН3), 1.54–1.11 (м., 16Н, СН2, СН3), 1.64 (м., 2Н, СН2), 2.74 (м., 2Н, СН), 2.85 (м., 2Н, СН), 3.40 (м. 2Н, СН), 4.14 (м., 2Н, СН), 7.03 (с., 2Н, IPr), 7.36 (м., 4Н, IPr), 7.44 (т., 2Н, IPr).
Синтез комплекса [IrCl(COD)(IMes)]. В перчаточном боксе смешивали [Ir(Cl)(COD)]2 (537 мг, 0.80 ммоль) и tBuOK (180 мг, 1.60 ммоль), добавляли сухой ТГФ (10 мл) и полученный темно-красный раствор перемешивали при комнатной температуре в течение 5 мин. При добавлении к раствору IMes . HCl (545 мг, 1.60 ммоль) его цвет менялся с темно-красного на темно-желтый. Реакционную смесь перемешивали в течение 16 ч. Затем ТГФ удаляли в вакууме, остаток очищали методом колоночной хроматографии, элюируя продукт смесью дихлорметана и ацетона в соотношении 8 : 1. Выход 875 мг (73%).
ЯМР 1H (CDCl3; 400 МГц; δ, м.д.): 1.24 (м., 4H, CH2), 1.64 (м., 4H, CH2), 2.10 (с., 6H, CH3), 2.29 (с., 12H, CH3), 2.90 (м., 2H, CH), 4.09 (м., 2H, CH), 6.97 (с., 2H, CH), 7.00 (с., 2H, CH), 7.03 (с., 2H, CH).
Синтез комплекса [Ir(COD){acetone}(IPr)]BF4 (I). К раствору [IrCl(COD)(IPr)] (586 мг, 0.81 ммоль) в ацетоне (10 мл) добавляли 1 экв. AgBF4 (157 мг, 0.81 ммоль) и перемешивали в темноте при комнатной температуре в течение 30 мин. Полученную суспензию отфильтровывали и упаривали до 0.5 мл, к остатку добавляли диэтиловый эфир. Затем осадок отфильтровывали и высушивали в вакууме. Выход 506 мг (75%).
ЯМР 1H (CD2Cl2; 400 МГц; δ, м.д.): 1.14 (д., 24Н, CH3) 1.42 (д., 24Н, CH3), 2.11 (с., 6H, CH3), 2.67 (м., 4H, CH), 3.04 (м., 4H, CH), 4.11 (м., 4H, CH), 7.16 (с., 2H, CH), 7.39 (д., 4H, IPr), 7.58 (т., 2H, IPr).
Синтез комплекса [Ir(COD){acetone}(IMes)]PF6 (II). К раствору [IrCl(COD)(IMes)] (589 мг, 0.92 ммоль) в ацетоне (10 мл) добавляли 1 экв. AgPF6 (233 мг, 0.92 ммоль) и перемешивали в темноте при комнатной температуре в течение 30 мин. Полученную суспензию отфильтровывали, упаривали до 0.5 мл, к остатку добавляли диэтиловый эфир. Осадок отфильтровывали и высушивали в вакууме. Выход 531 мг (77%).
ЯМР 1H (CDCl3; 600 МГц; δ, м.д.): 1.56 (м., 4H, CH2), 1.72 (м., 4H, CH2), 2.18 (с., 12H, CH3) 2.41 (с., 6H, CH3), 2.46 (с., 6H, CH3), 3.46 (м., 2H, CH), 4.01 (м., 2H, CH), 7.08 (м., 2H, CH), 7.12 (с., 4H, CH). ЯМР 13С{1H} (CDCl3; 600 МГц; δ, м.д.): 18.32 (CH3), 21.13 (CH3), 29.03 (CH2), 32.79 (COCH3), 33.22 (CH2), 66.00 (CH), 82.61 (CH), 124.31 (CH), 129.34 (CH), 134.89 (C), 134.97 (C), 139.92 (C), 173.67 (COCH3).
Спектры ЯМР в условиях SABRE регистрировали на спектрометре Bruker Ascend 400 МГц (Ларморова частота по протонам 400.13 МГц) в метаноле-d4. В ходе эксперимента параводород пропускали под давлением 4 бар в течение 10 с через образец внутри стандартной цилиндрической ампулы ЯМР (5 мм) с помощью изготовленной в МТЦ СО РАН автоматизированной газовой системы. После барботирования образца в заданном магнитном поле его быстро переносили в датчик спектрометра и регистрировали спектры ЯМР. Варьирование напряженности магнитного поля осуществляли путем механического позиционирования ампулы с образцом в поле рассеяния криомагнита спектрометра вдоль его теплого отверстия с помощью шагового двигателя. Детальное описание установки с быстрым переключением магнитного поля приведено в [23, 24].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
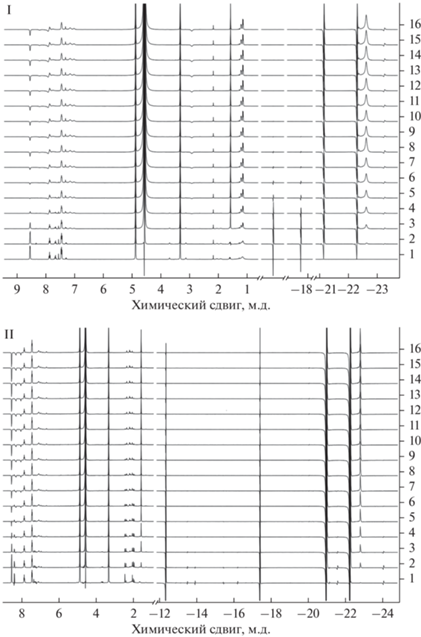
Спектры ЯМР 1H и 13С полученных комплексов иридия [Ir(COD){acetone}(IPr)]BF4 (I) и [Ir(COD)- {acetone}(IMes)]PF6 (II) (схема 1 ) полностью соответствовали ожидаемым. Для изучения переноса поляризации с молекулы параводорода в условиях SABRE соответствующие спектры ЯМР регистрировали при барботировании параводорода через растворы указанных комплексов в метаноле-d4 в присутствии пиридина. При этом в дополнение к интенсивному сигналу газообразного ортоводорода (химический сдвиг δ = 4.57 м.д.) наблюдали появление интенсивных сигналов гидридных интермедиатов в отрицательной области спектра (рис. 1). В сильном магнитном поле антифазная природа большинства из указанных сигналов характерна для гидридных интермедиатов, полученных в условиях SABRE [25, 26]. Стоит также отметить наблюдаемое изменение фазы сигналов протонов пиридина, что свидетельствует об успешном переносе поляризации с молекулы параводорода на данный лиганд (рис. 1).
Рис. 1.
Cпектры ЯМР 1H комплексов I (1.2 ммоль) и II (1.2 ммоль) в дейтерированном метаноле в присутствии пиридина (12.4 ммоль) при пропускании параводорода (~95% пара-Н2). Каждый последующий спектр регистрировали после 10 с барботирования параводорода через раствор.
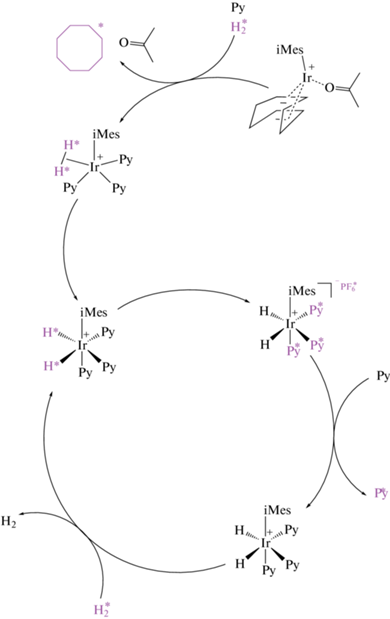
В действительности каталитический цикл, протекающий в условиях SABRE, более сложен и включает образование большего числа гидридных интермедиатов с разной степенью сольватации [27], чем приведено на упрощенной схеме 2 . Однако в большинстве случаев перенос поляризации на ядра самого катализатора и лиганда происходит по цепочке химических связей за счет скалярного спин-спинового взаимодействия. Тем не менее тетрафторборат- или гексафторфосфат-анион, не связанный непосредственно с металлоцентром, в органическом растворителе может образовывать с ним тесную ионную пару, в результате чего возможен перенос поляризации на их ядра.
(поляризованные фрагменты выделены цветом и знаком *)
Схема 2 .
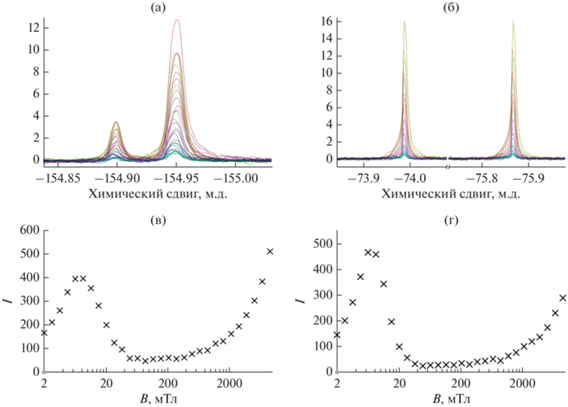
Для установления возможности такого переноса поляризации с параводорода на противоион мы изучили зависимость коэффициентов усиления сигналов ядер 19F в указанных фторсодержащих противоионах при проведении реакции в магнитном поле, изменяющемся в диапазоне от 2 мТл до 9 Тл (рис. 2). Так, в зависимости от выбранной величины магнитного поля наблюдались значительные изменения интенсивности сигнала в спектрах ЯМР 19F, что свидетельствовало о переносе поляризации на противоион, непосредственно не связанный с металлоцентром комплекса (рис. 2в, 2г). В то время как увеличение интенсивности сигнала при увеличении магнитного поля выше 0.2 Тл вызвано ростом термической разницы заселенностей спиновых уровней, расщепленных магнитным полем, в графиках полевой зависимости наблюдался максимум поляризации ядра 19F в обоих комплексах в слабом магнитном поле 6.4 мТл. Поскольку вероятность даже кратковременного образования прямой связи Ir–F очень мала, перенос поляризации на ядро 19F, вероятнее всего, достигается за счет диполь-дипольного механизма.
Рис. 2.
Спектры ЯМР 19F комплексов I и II при переносе поляризации на тетрафторборат-анион (а) и гексафторфосфат-анион (б) при проведении реакции SABRE в магнитом поле от 2 мТл до 9 Тл и зависимости сигналов ЯМР 19F тетрафторборат-аниона (в) и гексафторфосфат-аниона (г) от напряженности магнитного поля.
Показательно, что нам не удалось зарегистрировать перенос поляризации на ядра 31P и 11B противоионов, что может быть связано как с большей их удаленностью от металлоцентра, так и с более короткими (особенно в случае ядра бора) временами магнитной релаксации.
В заключение отметим, что перенос спиновой поляризации с молекулы параводорода на органические молекулы с использованием катализаторов на основе иридия в условиях SABRE является надежным способом повышения чувствительности спектроскопии ЯМР, в том числе – для создания гиперполяризованных зондов для функциональной магнитно-резонансной томографии. Хотя большинство проводимых исследований посвящено изучению переноса поляризации на ядра обменивающегося лиганда (например, пиридина), присутствие несвязанного противоиона, такого как тетрафторборат- и гексафторфосфат-анионы, в составе молекулярного комплекса также может привести к переносу поляризации на его ядра.
В результате проведенного исследования для двух комплексов иридия [Ir(COD){acetone}(IPr)]BF4 и [Ir(COD){acetone}(IMes)]PF6 нам впервые удалось продемонстрировать перенос спинового порядка с молекул параводорода на ядра 19F слабо координирующихся противоионов в условиях SABRE и определить оптимальную величину магнитного поля, обеспечивающую максимальное увеличение интенсивности в спектрах ЯМР. Механизм обнаруженного эффекта в настоящий момент не полностью ясен, но, вероятно, он имеет диполь-дипольную природу. Логичным дальнейшим шагом является получение катализатора SABRE, в котором противоион, с одной стороны, может координироваться к иону металла для увеличения степени поляризации, а с другой, является биологически-совместимым, как, например, пируват-анион. Такие исследования в данный момент проводятся в наших научных группах.
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Atkinson K.D., Cowley M.J., Duckett S.B. et al. // Inorg. Chem. 2009. V. 48. P. 663.
Terreno E., Castelli D.D., Viale A., Aime S. // Chem. Rev. 2010. V. 110. P. 3019.
Bhattacharya P., Ross B.D., Bünger R. // Exp. Biol. Med. 2009. V. 234. P. 1395.
Golman K., in’t Zandt R., Thaning M. // Proc. Natl. Acad. Sci. 2006. V. 103. P. 11270.
Ardenkjaer-Larsen J., Boebinger G., Comment A., et al. // Angew. Chem. Int. Ed. 2015. V. 54. P. 9162.
Larive C.K., Larsen S.C. // Anal. Chem. 2017. V. 89. P. 1391.
Natterer J., Bargon J. // Prog. Nucl. Magn. Reson. Spectrosc. 1997. V. 31. P. 293.
Hövener J., Pravdivtsev A.N., Kidd B. et al. // Angew. Chem. Int. Ed. 2018. V. 57. P. 11140.
Becker J., Bermuth J., Ebert M. et al. // Nucl. Instrum. Methods Phys. Res. A. 1998. V. 402. P. 327.
Frossati G. // Nucl. Instrum. Methods Phys. Res. A. 1998. V. 402. P. 479.
Bouchiat M.A., Carver T.R., Varnum C.M. // Phys. Rev. Lett. 1960. V. 5. P. 373.
Ardenkjaer-Larsen J.H., Fridlund B., Gram A. et al. // Proc. Natl. Acad. Sci. 2003. V. 100. P. 10158.
Kaptein R., Oosterhoff L.J. // Chem. Phys. Lett. 1969. V. 4. P. 214.
Bowers C R., Weitekamp D.P. // Phys. Rev. Lett. 1986. V. 57. P. 2645.
Bowers C.R., Weitekamp D.P. // J. Am. Chem. Soc. 1987. V. 109. P. 5541.
Kovtunov K.V., Beck I.E., Bukhtiyarov V.I., Koptyug I.V. // Angew. Chem. 2008. V. 120. P. 1514.
Adams R.W., Aguilar J.A., Atkinson K.D. et al. // Science. 2009. V. 323. P. 1708.
Rayner P.J., Duckett S.B. // Angew. Chem. Int. Ed. 2018. V. 57. P. 6742.
Spiridonov K.A., Kozinenko V.P., Nikovsky I.A. et al. // Mendeleev Commun. 2021. V. 31. P. 475.
Shen M.-H., Ren X.-T., Pan Y.-P., Xu H.-D. // Org. Chem. Front. 2018. V. 5. P. 46.
Kownacki I., Kubicki M., Szubert K., Marciniec B. // J. Organomet. Chem. 2008. V. 693. P. 321.
Kelly III R.A., Clavier H., Giudice S. et al. // Organometallics. 2008. V. 27. P. 202.
Hadjiali S., Bergmann M., Kiryutin A. et al. // J. Chem. Phys. 2019. V. 151. P. 244201.
Knecht S., Kiryutin A.S., Yurkovskaya A.V., Ivanov K.L. // J. Magn. Reson. 2018. V. 287. P. 10.
Knecht S., Hadjiali S., Barskiy D.A. et al. // J. Phys. Chem. 2019. V. 123. P. 16288.
Limbach H.-H., Ulrich S., Gründemann S. et al. // J. Am. Chem. Soc. 1998. V. 120. P. 7929.
Fekete M., Bayfield O., Duckett S.B. et al. // Inorg. Chem. 2013. V. 52. P. 13453.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия