Кристаллография, 2019, T. 64, № 3, стр. 380-385
Компьютерное моделирование гетеросистемы Zr0.8Sc0.2O1.9/Ce0.9Gd0.1O1.95
А. К. Иванов-Шиц 1, *, И. Ю. Готлиб 2, М. З. Галин 3, Г. Н. Мазо 4, И. В. Мурин 2
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
2 Санкт-Петербургский государственный университет, Институт химии
Санкт-Петербург, Россия
3 Институт проблем химической физики РАН
Черноголовка, Россия
4 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
* E-mail: alexey.k.ivanov@gmail.com
Поступила в редакцию 26.04.2018
После доработки 26.04.2018
Принята к публикации 15.05.2018
Аннотация
Двухслойная гетеросистема Zr0.8Sc0.2O1.9/Ce0.9Gd0.1O1.95 моделировалась методом молекулярной динамики в ячейке, содержащей около 27 тысяч атомов. Показано, что в целом в системе сохраняются кристаллографические характеристики слоев допированных оксидов циркония и церия со структурой флюорита. Искажения кристаллической структуры наблюдаются в узком граничном слое толщиной несколько ангстрем. Анализ парных корреляционных функций указывает на разупорядоченность кислородной подрешетки в гетеросистеме. Рассчитанные значения послойных коэффициентов диффузии кислорода, а также энергии активации диффузии сравниваются с данными как прямых физических, так и компьютерных экспериментов.
ВВЕДЕНИЕ
Твердооксидные топливные элементы (ТОТЭ) по сравнению с традиционными источниками энергии обладают такими преимуществами, как высокая эффективность и низкий уровень выброса загрязняющих веществ [1–6]. В качестве твердого электролита в ТОТЭ чаще всего используется стабилизированный иттрием (YSZ) или скандием (ScSZ) диоксид циркония, который характеризуется высокой кислород-ионной проводимостью как в окислительной, так и в восстановительной атмосфере и при этом сохраняет хорошие физико-химические и механические свойства. Отметим, что эффективность топливных элементов во многом определяется свойствами электродных материалов [3, 5]. Для улучшения характеристик анода предлагается использовать [7, 8] легированный оксид церия, например, с гадолинием в качестве допанта (GDC). Слой GDC играет защитную роль: подавляет диффузию катионов и предотвращает протекание химических реакций на границе анод–материал электролита. Кроме того, в восстановительной атмосфере в допированном оксиде церия отмечается смешанная электронно-ионная проводимость [9, 10], которая “расширяет” реакционную зону и тем самым повышает эффективность анодных материалов.
Аналогичная ситуация отмечается для катодных материалов, использующих сложные оксиды лантана–стронция [11–13]. На межфазной границе катод–электролит возможно образование таких непроводящих фаз, как La2Zr2O7 и/или SrZrO3 [13–15]. В этом случае на твердоэлектролитную мембрану также наносят слой допированного гадолинием или самарием оксида церия [16–18], который в зависимости от толщины и микроструктуры границы раздела и рабочей температуры улучшает характеристики катода ТОТЭ [19, 20].
Настоящая работа является продолжением серии работ по компьютерному моделированию двухслойных структур типа электрод/электролит в топливных элементах [21, 22]. Выбор границы раздела CDC/ScSZ обусловлен как использованием указанных материалов в реальных ТОТЭ, так и возможностью изучить особенности ионного транспорта в наноструктурных материалах.
КОМПЬЮТЕРНЫЙ ЭКСПЕРИМЕНТ
Построение модели границы. Гетеросистема GDC/ScSZ “собиралась” из тонких пленок допированных оксидов церия и циркония, причем конкретные составы GDC и ScSZ отвечали максимальным экспериментальным значениям проводимости [24–26]. Начальные размеры пленки Zr0.8Sc0.2O1.9 отвечали размерам пленки YSZ, изученной ранее [23], и составляли 102.560 × × 102.560 × 15.444 Å3. На эту пленку сверху помещался слой Ce0.9Gd0.1O1.95 размером 102.942 × × 102.942 × 16.254 Å3 (который был получен 19-кратным размножением элементарной ячейки с параметром a = = 5.418 Å вдоль a- и b-осей и 3-кратным – вдоль с-оси). В построенной таким образом двухслойной пленке находилось 26 699 атомов, в том числе 3898 ионов Ce4+, 434 – Gd3+, 3840 катионов Zr+4, 960 – Sc3+ и 17 567 анионов O2–. Частичное замещение четырехзарядных катионов церия и циркония трехвалентными катионами гадолиния и иттрия с введением кислородных вакансий в начальной конфигурации осуществлялось случайным образом.
Все выполненные расчеты проведены в рамках модели жестких ионов c использованием программного комплекса DL_POLY [27]. Потенциальная энергия взаимодействия между ионами, U(rij), рассчитывалась как сумма кулоновского (электростатического) и короткодействующего парного потенциала: $U({{r}_{{ij}}}) = \frac{{{{q}_{i}}{{q}_{j}}}}{{4\pi {{\varepsilon }_{0}}{{r}_{{ij}}}}}$ + ${{A}_{{ij}}}\exp \left( { - \frac{{{{r}_{{ij}}}}}{{{{\rho }_{{ij}}}}}} \right) - \frac{{{{C}_{{ij}}}}}{{r_{{ij}}^{6}}}$, где rij – расстояние между ионами i и j; qi, qj – эффективные заряды ионов, Aij, ρij и Cij – параметры короткодействующего потенциала для частиц сорта i и j; ε0 – диэлектрическая постоянная. При расчете короткодействующей составляющей потенциальной энергии ограничивались рассмотрением взаимодействия пар типа катион–анион и анион–анион [28, 29].
При расчетах использовали формальные заряды ионов: +4.0, +3.0, +4.0, +3.0, –2.0 для Ce4+, Gd3+, Zr4+, Sc3+ и O2– соответственно. Значения параметров короткодействующего потенциала приведены в таблице 1 [23, 30–32].
Таблица 1.
Значения параметров модельного потенциала
| Тип пары i–j | Ce4+–O2– | Gd3+–O2– | Zr4+–O2– | Sc3+–O2– | O2––O2– |
|---|---|---|---|---|---|
| ${{\rho }_{{ij}}}$, Å | 0.3547 | 0.3399 | 0.3580 | 0.3211 | 0.21916 |
| ${{A}_{{ij}}}$, эВ | 1809.68 | 1885.75 | 1234.73 | 1575.85 | 9547.96 |
| ${{C}_{{ij}}}$, эВ Å6 | 20.40 | 20.34 | 0 | 0 | 32.00 |
Использовались стандартные “орторомбические” периодические граничные условия. В отличие от предыдущих расчетов [22] в настоящей работе для верхнего и нижнего края моделируемой ячейки (расчетного бокса) в модельной системе устанавливались отталкивающие стенки, перпендикулярные оси c, на расстоянии ±18.35 Å от проходящей через начало координат плоскости xy (в среднем соответствующей поверхности раздела между двумя фазами). Потенциал отталкивания при $z < - 18.35{ {\AA}}$ и $z > 18.35{ {\AA}}$ имеет вид
Ранее было показано, что для моделирования бислойных гетеросистем CeO2/YSZ [32] и GDC/YSZ [23] эффективно использование процедуры высокотемпературного отжига исследуемой системы с последующей перекристаллизацией (процедура ОПК). Такой подход был применен и в настоящей работе для двухслойной системы GDC/ScSZ.
Расчет проводился по следующей схеме:
– строилась исходная конфигурация в расчетном боксе 102.946 × 102.946 × 40.00 Å, полученная из начальной конфигурации с атомами в узлах идеальной решетки путем введения между моделируемыми слоями дополнительного зазора толщиной 1 Å и уменьшения расстояния между всеми атомами внутри одного слоя на 15%. Данная исходная конфигурация уравновешивалась в NVT-ансамбле при 3400 K в течение 200 пс;
– полученная на предыдущем шаге конечная конфигурация использовалась в качестве начальной для прогона в течение 250 пс в изотропном NpT-ансамбле и затем в течение 400 пс в анизотропном NpT-ансамбле с сохранением ортогональности ребер ячейки при 3400 K и давлении 20 ГПа. В результате была получена конфигурация в расчетной ячейке размером 94.563 × 94.563 × × 36.743 Å;
– полученная на предыдущем шаге конфигурация уравновешивалась в изотропном NpT-ансамбле при 3400 K (происходил “отжиг” системы) и нулевом давлении в течение 300 пс. В результате была получена конфигурация в моделируемой ячейке размером 98.137 × 98.137 × 37.931 Å.
– полученная на предыдущем шаге (“отожженная”) конфигурация использовалась в качестве начальной при дальнейшем охлаждении системы в анизотропном NpT-ансамбле с сохранением ортогональности ребер ячейки при нулевом давлении до 1 K по алгоритму 3000 K (расчет в течение 50 пс) → 2500 K (50 пс) → 2000 K (50 пс) → → 1500 K (50 пс) → 1000 K (50 пс) → 500 K (50 пс) → → 1 K (100 пс). В результате была создана “рабочая” конфигурация атомов в ячейке размером 96.154 × 96.154 × 36.783 Å.
Временной шаг при всех молекулярно-динамических (МД) расчетах составлял 0.25 фс.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
При расчетах структурных и транспортных характеристик в системе выделялись три слоя: слой ScSZ ($ - \frac{c}{2} + 4.5{ {\AA}} < z < - 4.5{ {\AA}}$, c – ребро моделируемой ячейки в направлении z), граничный слой ($ - 4.5{ {\AA}} \leqslant z \leqslant 4.5{ {\AA}}$) и слой GDC ($4.5{ {\AA}} < z < \frac{c}{2} - $ $ - \;4.5{ {\AA}}$).
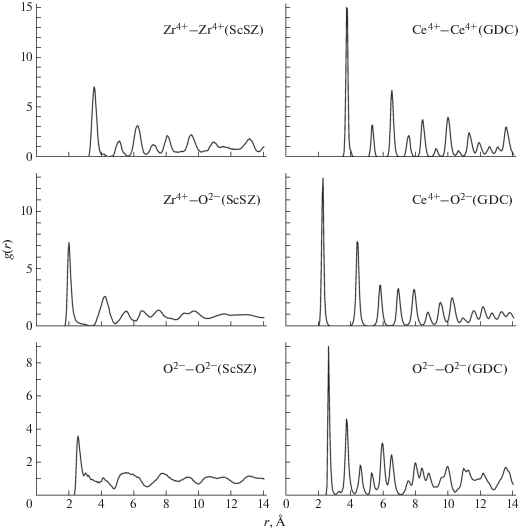
Информация о структурных характеристиках моделируемой системы получена путем расчета и последующего анализа радиальных парных корреляционных функций (РПКФ) gij(r). Для системы в состоянии равновесия при 1 K рассчитаны РПКФ и профили плотности ионов вдоль оси с (z), для чего был осуществлен дополнительный прогон в течение 100 пс. Результаты представлены на рис. 1.
Видно, что в модельной системе фаза ScSZ несколько более разупорядочена, чем фаза GDC, о чем свидетельствуют менее острые пики РПКФ для пар кислород–кислород. Эта разупорядоченность способствует диффузии ионов кислорода. Расстояния между максимумами РПКФ катион–катион и катион–анион, как и в [23], хорошо согласуются со значениями для соответствующих решеток флюоритового типа (практически идеальной в случае GDC и слегка искаженной разупорядочением в случае ScSZ), что приемлемо для выбранных модельных потенциалов.
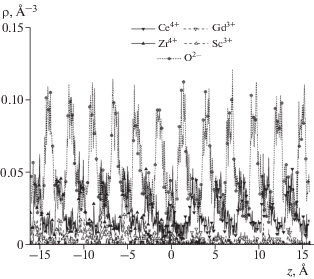
На рис. 2 можно видеть, что в результате отжига фаза ScSZ содержит незначительную примесь церия и гадолиния по всему объему слоя, в то время как в фазе GDC примесь циркония и скандия наблюдается лишь в приграничной области.
Рис. 2.
Профили средней плотности ионов вдоль оси с(z) в интервале $ - 16.1{ {\AA}} \leqslant z \leqslant 16.1{ {\AA}}$. Отрицательные значения z соответствуют слою ScSZ, положительные – слою GDC.
Систему, пришедшую в состояние равновесия при 1 K, нагревали до температур 1000, 1175, 1335, 1500, 1700, 2000 и 2500 K. При каждой температуре включали режим термализации, в ходе которого в течение 62.5 пс система уравновешивалась. Затем осуществляли прогон длительностью 500 пс, в ходе которого рассчитывали среднеквадратичные смещения ионов кислорода (термализацию и основной прогон осуществляли в анизотропном NpT-ансамбле с сохранением ортогональности ребер ячейки). Из этих данных рассчитывали коэффициенты диффузии ионов кислорода, вносящих основной вклад в ионную проводимость ScSZ и GDC.
На рис. 3 представлены рассчитанные коэффициенты диффузии ионов кислорода в направлении, перпендикулярном оси c (z), для слоя ScSZ, граничного слоя и слоя GDC, а также по всем направлениям для всей системы в целом.
Рис. 3.
Температурные зависимости расчетных коэффициентов диффузии ионов кислорода для трех слоев и для системы GDC/ScSZ в целом.
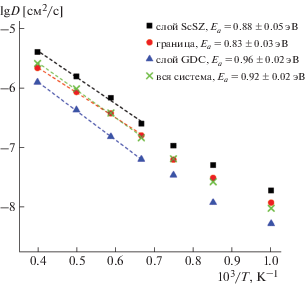
При расчете коэффициентов в отдельных слоях учитывались только ионы, остававшиеся внутри соответствующего слоя на всем протяжении 500-пикосекундного пробега. На рис. 3 также приведены значения энергии активации Ea (в температурном интервале 1500–2500 K), найденные из соотношения Аррениуса:
Рисунок 4 демонстрирует сравнение рассчитанных коэффициентов диффузии кислорода в отдельных слоях гетеросистемы c литературными данными, полученными как из прямых измерений коэффициентов (само)диффузии физическими методами, так и определенными из МД-расчетов.
Рис. 4.
Температурные зависимости коэффициентов диффузии ионов кислорода для слоев GDC (а)
( – МД-расчеты, Ce0.9Gd0.1O1.95, настоящая работа;
– МД-расчеты, Ce0.9Gd0.1O1.95, настоящая работа;  – эксперимент, монокристалл Ce0.69Gd0.31O2-δ [33];
– эксперимент, монокристалл Ce0.69Gd0.31O2-δ [33];  – эксперимент, керамика Ce0.9Gd0.1O2-δ [34];
– эксперимент, керамика Ce0.9Gd0.1O2-δ [34];  – МД-расчеты, Ce0.852Gd0.148O1.926 [35];
– МД-расчеты, Ce0.852Gd0.148O1.926 [35];  – МД-расчеты, Ce0.8Gd0.2O1.9, [36]) и ScSZ (б) (
– МД-расчеты, Ce0.8Gd0.2O1.9, [36]) и ScSZ (б) ( – МД-расчеты, Zr0.8Sc0.2O1.9, настоящая работа,
– МД-расчеты, Zr0.8Sc0.2O1.9, настоящая работа,  – МД-расчеты, Zr0.82Sc0.18O1.91, [37];
– МД-расчеты, Zr0.82Sc0.18O1.91, [37];  – эксперимент, керамика Zr0.818Sc0.182O2 – δ, [38]) в системе GDC/ScSZ в сравнении с литературными данными.
– эксперимент, керамика Zr0.818Sc0.182O2 – δ, [38]) в системе GDC/ScSZ в сравнении с литературными данными.
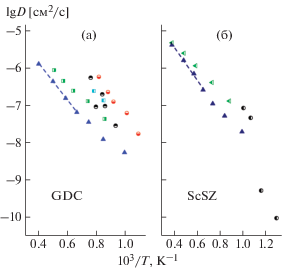
Рассчитанные значения диффузионных параметров в целом удовлетворительно согласуются с литературными данными с учетом того, что химические составы изученных материалов несколько отличаются друг от друга. Кроме того, следует учитывать, что в МД-расчетах при варьировании параметров потенциала, как отмечалось в [37], зависимость транспортных характеристик рассматриваемых модельных систем от состава может заметно меняться. При этом МД-моделирование системы Zr1 – xScxO2 – x/2 указывает на существование максимума на кривых D(x) при х = 0.12 [37, 39], хотя прямой эксперимент указывает на наличие максимума при х = 0.2 [38].
Кроме того, различия между расчетными и экспериментальными значениями в параметрах диффузии могут быть связаны с тем, что в реальных образцах сильно допированных твердых растворов (особенно со структурой флюорита [40]) образуются кластеры различного типа, которые играют роль ловушек кислородных вакансий. В этом случае потенциальный рельеф, связанный с анионным переносом, может существенно измениться [30, 41] и привести к изменениям транспортных характеристик.
В ряде экспериментальных работ для систем Ce1 – xGdxO2 – δ/ZrO2 [42] и ZrO2(Y2O3)/SrTiO3 [43] сообщалось о существенном (на несколько порядков) увеличении ионной проводимости приграничного слоя. Однако в предыдущих расчетных работах для систем CeO2 – δ/YSZ [32] и Ce1 ‒ xGdxO2 – δ/YSZ [23] не было обнаружено эффекта возрастания проводимости на границе двух слоев. Настоящее исследование также подтверждает (рис. 3) отсутствие в приграничной области – тонком граничном слое между пленками допированных оксидов церия и циркония – эффекта возрастания проводимости. Отметим, что толщина исследуемой модельной системы составляла чуть более 3 нм, что существенно меньше толщин реальных физических систем (десятки нанометров); возможно, поэтому в МД-расчетах проявляются размерные эффекты. Однако в [44] было аргументированно показано, что результаты экспериментальных работ [42, 43] должны быть поставлены под сомнение, поскольку наблюдавшийся в них эффект возрастания проводимости связан с некорректной интерпретацией полученных результатов. Результаты, полученные в настоящей работе, подтверждают высказанный тезис о том, что в изученных гетеросистемах не наблюдается значительного изменения (увеличения) кислород-ионной проводимости.
ЗАКЛЮЧЕНИЕ
Результаты компьютерного моделирования подтверждают возможность конструирования реалистической атомистической модели для GDC/ScSZ. Модельная система состоит из тонких слоев Zr0.8Sc0.2O1.9 и Ce0.9Gd0.1O1.95, которые сохраняют свою исходную кристаллическую структуру типа флюорита. Рассчитанные транспортные характеристики гетерогенной системы GDC/ScSZ в целом аналогичны ранее рассчитанным для системы GDC/YSZ. В рассмотренной модельной системе ионы кислорода в GDC менее подвижны, чем в ScSZ, в то время как в граничной области коэффициент диффузии принимает промежуточное значение, а энергия активации несколько ниже, чем внутри обеих граничащих фаз.
Работа выполнена при частичной финансовой поддержке Российского фонда фундаментальных исследований (проект № 17-03-00650).
Список литературы
Huijmans J.P.P., van Berkel F.P.F., Christie G.M. // J. Power Sources. 1998. V. 71. P. 107.
Steele B.C.H., Heinzel A. // Nature. 2001. V. 414. P. 345.
Takeguchi T., Kikuchi R., Yano T. et al. // Catal. Today. 2003. V. 84. P. 217.
Haile S.M. // Acta Mater. 2003. V. 51. P. 5981.
Rossmeisl J., Bessler W.G. // Solid State Ionics. 2008. V. 178. P. 1694.
Tarancon A., Burriel M., Santiso J. et al. // J. Mater. Chem. 2010. V. 20. P. 3799.
Chueh W.C., Hao Y., Jung W. et al. // Nat. Mater. 2012. V. 11. P. 155.
Marina O.A., Bagger C., Primdahl S. et al. // Solid State Ionics. 1999. V. 123. P. 199.
Wang S., Kobayshi T., Dokiya M. et al. // J. Electrochem. Soc. 2000. V. 147. P. 3606.
Faber J., Geoffroy C., Roux A. et al. // Appl. Phys. A. 1989. V. 49. P. 225.
Jiang S.P., Li J. // Solid Oxide Fuel Cells. Materials Properties and Performance / Eds. Fergus J.W. et al. Boca Raton; London; New York: CRC Press, 2009. P. 131.
Mai A., Haanappel V.A.C., Uhlenbruck S. et al. // Solid State Ionics. 2005. V. 176. P. 1341.
Sun C., Hui R., Roller J. // J. Solid State Electrochem. 2010. V. 14. P. 1125.
Matsui T., Li S., Muroyama H. et al. // Solid State Ionics. 2017. V. 300. P. 135.
Lee D., Lee I., Jeon Y. et al. // Solid State Ionics. 2005. V. 176. P. 1021.
Plonczak P., Joost M., Hjelm J. et al. // J. Power Sources. 2011. V. 196. P. 1156.
Uhlenbruck S., Jordan N., Sebold D. et al. // Thin Solid Films. 2007. V. 515. P. 4053.
Shiono M., Kobayashi K., Nguyen T.L. et al. // Solid State Ionics. 2004. V. 170. P. 1.
Somekawa T., Matsuzaki Y., Tachikawa Y. et al. // Solid State Ionics. 2015. V. 282. P. 1.
Wang F., Brito M.E., Yamaji K. et al. // Solid State Ionics. 2014. V. 262. P. 454.
Готлиб И.Ю., Иванов-Шиц А.К., Мурин И.В. // Тез. докл. Всерос. конф. с междунар. участием “Химия твердого тела и функциональные материалы-2018”, 21–27 мая 2018 г., Санкт-Петербург.
Иванов-Шиц А.К., Мазо Г.Н. // Кристаллография. 2018. Т. 63. № 1. С. 5.
Галин М.З., Иванов-Шиц А.К., Мазо Г.Н. // Кристаллография. 2018. Т. 63. № 1. С. 114.
Yashima M., Takizawa T. // J. Phys. Chem. C. 2010. V. 114. P. 2385.
Politova T.I., Irvine J.T.S. // Solid State Ionics. 2004. V. 168. P. 153.
Badwal S.P.S., Ciacchi F.T., Milosevic D. // Solid State Ionics. 2000. V. 136–137. P. 91.
Smith W., Todorov I.T., Leslie M. // Z. Kristallogr. 2005. B. 220. S. 563.
Computer Modelling in Inorganic Chemistry / Ed. Catlow C.R.A. London: Academic Press, 1997.
Chaplot S.L. // Phys. Rev. B. 1990. V. 42. P. 2149.
Miller S.P., Dunlap B.I., Fleischer A.S. // J. Fuel Cell Sci. Tech. 2015. V. 12. P. 021003.
Devanathan R., Thevuthasan S., Gale J.D. // Phys. Chem. Chem. Phys. 2009. V. 11. P. 5506.
Sayle T.X.T., Parker S.C., Sayle D.C. // J. Mater. Chem. 2006. V. 16. P. 1067.
Ruiz-Trejo E., Sirman J.D., Baikov Yu.M. et al. // Solid State Ionics. 1998. V. 113–115. P. 565.
Manning P.S., Sirman J.D., Kilner J.A. // Solid State Ionics. 1997. V. 93. P. 125.
Tarancón A., Morata A., Peiró F. et al. // Fuel Cells. 2011. V. 11. P. 26.
Huang C.W., Wei W.C.J., Chen C.S. et al. // J. Eur. Ceram. Soc. 2011. V. 31. P. 3159.
Yu Z.Q., Devanathan R., Jiang W. et al. // Solid State Ionics. 2010. V. 181. P. 367.
Sakai T., Hyodo J., Ogushi M. et al. // Solid State Ionics. 2017. V. 301. P. 156.
Devanathan R., Thevuthasan S., Gale J.D. // Phys. Chem. Chem. Phys. 2009. V. 11. P. 5506.
Иванов-Шиц А.К., Мурин И.В. Ионика твердого тела. Т. 2. СПб.: Изд-во СПбГУ, 2010.
Li Y., Hafskold B. // J. Phys.: Condens. Matter. 1995. V. 7. P. 1255.
Azad A., Marina O.A., Wang C.M. et al. // Appl. Phys. Lett. 2005. V. 86. P. 131906.
Garcia-Barriocanal J., Rivera-Calzada A., Varela M. et al. // Science. 2008. V. 321. P. 676.
Näfe H. // Ionics. 2018. V. 24. P. 763.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография