Кристаллография, 2022, T. 67, № 3, стр. 442-450
Микроскопический анализ поверхности кристаллов кислых солей сульфатов калия–аммония
Р. В. Гайнутдинов 1, А. Л. Толстихина 1, *, Е. В. Селезнева 1, И. П. Макарова 1
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
* E-mail: alla@crys.ras.ru
Поступила в редакцию 09.09.2021
После доработки 13.10.2021
Принята к публикации 15.10.2021
- EDN: FWQENV
- DOI: 10.31857/S0023476122030080
Аннотация
Методами электрической атомно-силовой микроскопии исследованы монокристаллы твердых растворов (K$_{{1--x}}$(NH4)x)3H(SO4)2 (x ≥ 0.57). При 296 K для образцов с разной концентрацией катионов K и NH4 измерены локальные вольт-амперные характеристики тригональных суперпротонных фаз в зависимости от ориентации оси с и установлена анизотропия проводимости. Показана степень зависимости проводящих свойств от состава. Прослежены и оценены временные изменения в морфологии, потенциале и производных емкости поверхности (001) (K0.43(NH4)0.57)3H(SO4)2 при выдержке образцов в воздушной среде в условиях постоянства влажности и температуры.
ВВЕДЕНИЕ
Настоящая работа продолжает исследования структуры и свойств новых кристаллов твердых растворов (K$_{{1--x}}$(NH4)x)3H(SO4)2, выращенных в многокомпонентной водно-солевой системе K2SO4–(NH4)2SO4–H2SO4–H2O [1–3]. Эти соединения принадлежат семейству кислых солей щелочных металлов с общей формулой MmHn(AO4)$_{{(m + n)/2}}$ ⋅ ⋅ yH2O (М = K, Rb, Cs, NH4; AO4 = SO4, SeO4, HAsO4, HPO4), проявляющих высокую протонную проводимость при температурах 300–500 K, благодаря чему считаются перспективными материалами для использования в различных электрохимических устройствах [4–7].
У выращенных кристаллов выявлен ряд особенностей структуры и транспортных свойств, связанных с изоморфным замещением катионов K и NH4. Впервые при комнатной температуре обнаружено формирование тригональной суперпротонной фазы в образцах (K0.43(NH4)0.57)3 H(SO4)2. Замещение аммония на калий привело к повышению симметрии координационного окружения катионов, образованию динамически разупорядоченной системы водородных связей и появлению высокой протонной проводимости [1]. По данным диэлектрической спектроскопии при комнатной температуре величина проводимости кристаллов вдоль оси c составила 10–5 См см–1, что соответствует проводимости исходных соединений K3H(SO4)2 и (NH4)3H(SO4)2 при высоких температурах [2]. При повышении температуры до 353 K проводимость смешанных кристаллов увеличилась на 2 порядка величины 7.42 × 10–3 См∙см–1 [2]. То есть кристаллы с замещением в катионной подрешетке (K$_{{1--x}}$(NH4)x)3 H(SO4)2 (x ≥ 0.57) показывают улучшенные транспортные свойства – высокую протонную проводимость в области более низких температур, что делает актуальным исследование их функциональных свойств.
Несмотря на неоспоримые достоинства устройств на основе кислых солей, ряд присущих им природных свойств, таких как гигроскопичность, твердофазные реакции при высоких температурах и для некоторых соединений узкий диапазон существования суперпротонной фазы, пока сдерживает их техническое использование [8–10]. Очевидно, что необходимы дополнительные усилия для усовершенствования составов соединений, улучшения их свойств и стабильности суперпротонных фаз. Сложность изучаемых объектов требует проведения фундаментальных исследований на монокристаллах, что позволит получить базовую информацию об атомной и реальной структуре, физических и химических свойствах и в итоге приведет к пониманию механизмов электрохимических процессов в объеме и на поверхности этих материалов, в том числе при использовании в качестве протонообменных мембран топливных элементов.
В работе рассмотрен ряд вопросов, связанных с устойчивостью поверхности кристаллов твердых растворов (K$_{{1--x}}$(NH4)x)3H(SO4)2 (x ≥ 0.57) (в исследуемых образцах аммоний превышает по количеству калий, но используется обозначение (K$_{{1--x}}$(NH4)x) для сохранения единообразия формул соединений в системе K2SO4–(NH4)2SO4–H2SO4–H2O) по отношению к воздействию окружающей воздушной среды. А именно, как влияет частичное изоморфное замещение катионов K и NH4 на стабильность и свойства протонных проводников, каким образом изменяется во времени поверхность кристалла при атмосферных условиях, близких к нормальным. На микроскопическом уровне исследовали локальную проводимость на постоянном токе в зависимости от состава и кристаллографической ориентации образцов. Использование простого способа получения атомно-гладкой и чистой поверхности путем раскалывания кристаллов по плоскостям спайности и перпендикулярно им, а также измерение локальных вольт-амперных характеристик (ВАХ) позволили получить прямые данные о токах утечки и проводимости монокристаллических образцов и проанализировать особенности соединений разного состава. Для структурной характеризации образцов и изучения поверхностных явлений на наноуровне был использован комплекс электрических методик атомно-силовой микроскопии (АСМ).
ЭКСПЕРИМЕНТАЛЬНЫЕ УСТАНОВКИ И МЕТОДИКИ ИЗМЕРЕНИЙ
Наиболее подходящими объектами для изучения физических свойств кристаллических водородсодержащих материалов, включая процессы на поверхности, считаются монокристаллические образцы. Для изучения влияния катионного замещения на свойства фаз (K$_{{1--x}}$(NH4)x)3H(SO4)2 были использованы монокристаллы с пластинчатым габитусом, выращенные в ИК РАН им. А.В. Шубникова методом управляемого снижения растворимости из водных растворов K3H(SO4)2 и (NH4)3H(SO4)2 с соотношением K+ : NH$_{4}^{ + }$ ∼ 3 : 7–1 : 9 при температурах 303–313 K. Полученные кристаллы твердых растворов обладают при комнатной температуре тригональной симметрией и высокой проводимостью, как и исходные фазы K3H(SO4)2 и (NH4)3H(SO4)2 при повышенных температурах – 458 K [10] и 355 K [11] соответственно. При 296 K кристаллы (K0.43(NH4)0.57)3 H(SO4)2, полученные из растворов с соотношением K+ : NH$_{4}^{ + }$ ∼ 3 : 7, имеют пр. гр. R$\bar {3}$, Z = 3, a = b = 5.7768(3), c = 22.0983(1) Å [1]. Кристаллы, выращенные из растворов с соотношением K+ : NH$_{4}^{ + }$ ∼ 2 : 8 и 1 : 9, по данным монокристаллического рентгеноструктурного анализа (РСА) являются изоструктурными (K0.43(NH4)0.57)3H(SO4)2 (параметры элементарной ячейки a = b = 5.8048(3), c = 22.2363(1) Å и a = b = 5.8364(4), c = 22.4006(1) Å соответственно) и различаются соотношением заселенности позиций K/N (x ≈ 0.68 и x ≈ 0.81 соответственно). Исследование их атомной структуры будет опубликовано в отдельной работе.
Подготовку и исследование поверхности образцов методом АСМ проводили на микроскопе NTEGRA Prima (NT-MDT Spectrum Instruments, Зеленоград) в условиях чистой зоны контрольно-измерительного комплекса “TRACKPORE ROOM-05” (класс чистоты 5 ИСО (100), точность поддержания температуры (Т) воздушной среды в чистой зоне в диапазоне 298 ± 5 ± 0.05 K, относительная влажность воздуха 35 ± 1%). Локальные ВАХ измеряли в диапазоне напряжений смещения от –4 до +4 В. Кремниевый кантилевер (HA_FM, балка B, Tipsnano, Эстония), покрытый Pt, имел следующие характеристики: резонансная частота f = 114 кГц, жесткость k = 6 Н/м, радиус закругления острия R < 35 нм. Рельеф поверхности образцов изучали в прерывисто-контактном режиме с использованием кантилеверов той же марки. Регистрацию локального пьезоотклика материала проводили в контактном режиме при приложении переменного электрического напряжения амплитудой 4 В и частоты 350 кГц к проводящему Pt-зонду.
Методом сканирующей микроскопии Кельвина (СМК) в бесконтактном режиме регистрировали распределение поверхностного потенциала на основе компенсационного принципа (постоянную компоненту поданного напряжения UDC подбирали таким образом, чтобы колебания кантилевера на частоте ɷ переменной компоненты напряжения отсутствовали). Измерения потенциала проводили в режиме амплитудной модуляции. К образцу прикладывали напряжение смещения переменного тока UAC = 3 В частоты 114 кГц. Для измерения поверхностной емкости применяли резонансную двухпроходную методику, в которой при первом проходе в процессе сканирования регистрируется рельеф, а при повторном, проводимом на постоянном расстоянии кантилевера от поверхности при поданном переменном напряжении U = UDC + UACsinɷt половине (ɷ/2) и трети (ɷ/3) резонансной частоты, измеряется амплитуда колебаний кантилевера на резонансной частоте [12–14]. Измерения емкостной силы на (ɷ/2) проводили при приложении переменного электрического поля с амплитудой 5 В и частотой 57 кГц, UDC = 0, а на (ɷ/3) – с амплитудой 10 В и частотой 38 кГц.
ЭКСПЕРИМЕНТАЛЬНЫЕ РЕЗУЛЬТАТЫ
Поверхность смешанных кристаллов и ее изменение во времени. Для АСМ-исследований из кристаллов (K$_{{1--x}}$(NH4)x)3H(SO4)2, обладающих спайностью по (001), выкалывали плоскопараллельные образцы. Наблюдения с помощью оптического поляризационного стереомикроскопа Nikon SMZ1270 показали, что поверхность образцов видоизменяется со временем. На рис. 1а показана свежая поверхность образцов (K0.43(NH4)0.57)3H(SO4)2 с ориентацией перпендикулярно оси с тригональной фазы. За время выдержки на воздухе t = 840 ч в контролируемых условиях (296 K, 35%) поверхность скола модифицируется, особенно в местах с неоднородным грубым рельефом (рис. 1б). Наблюдаемые в оптическом диапазоне изменения коррелируют с составом соединений: поверхность образцов с более низким содержанием аммония (х = 0.57) подвержена меньшей модификации (показывают большую устойчивость), чем с повышенным количеством (х = 0.81). По данным АСМ при сколе по спайности кристаллов с повышенным содержанием аммония образуется неоднородная шероховатая поверхность (001), которая достаточно быстро изменяется даже в условиях пониженной влажности воздуха. Изменения кристаллов, включая их поверхность, в условиях влажности нежелательны для возможных практических применений, что, например, отмечалось для исходной моноклинной фазы (NH4)3H(SO4)2 при изготовлении топливных элементов [15]. Поэтому было выполнено отдельное исследование процесса модификации поверхности (001) тригональных фаз (K$_{{1--x}}$(NH4)x)3H(SO4)2 при комнатной температуре и влажности воздуха 35%.
Рис. 1.
Микрофотография выколотой из монокристалла (K0.43(NH4)0.57)3H(SO4)2 плоскопараллельной пластины с ориентацией перпендикулярно тригональной оси с. Свежая (а) и трансформировавшаяся со временем (б) поверхность.

Для экспериментов отобрали кристалл с составом (K0.43(NH4)0.57)3H(SO4)2 с достаточно гладкой поверхностью скола (001) и применили комплекс электрических методик АСМ. Для суперпротонных кристаллов плоскость (001) рассматривается как основная с точки зрения транспорта протонов. Характерный ступенчатый нанорельеф поверхности свежего скола в виде ямок и отдельных выступов с устойчивыми параметрами по высоте (глубине) ∼0.7 нм, соответствующими величине 1/3c в элементарной ячейке, показан на рис. 2а. В конкретном случае прослеживается корреляция данных АСМ с параметрами слоистой структуры кристалла, найденными методом РСА (рис. 2б).
Рис. 2.
Нанорельеф поверхности (001) (а), атомная структура кристалла (K0.43(NH4)0.57)3H(SO4)2 (б), расположение катионов в структуре (в) и схематическое представление строения поверхности в виде ступенек высотой 1/3с, каждая из которых состоит из чередующихся молекулярных слоев …K2/N2…K1/N1, SО4–H–SО4…K2/N2… (г). Показаны тетраэдры SО4, соединенные водородными связями, и расположение атомов K и N (в группах NH4) (б, в).
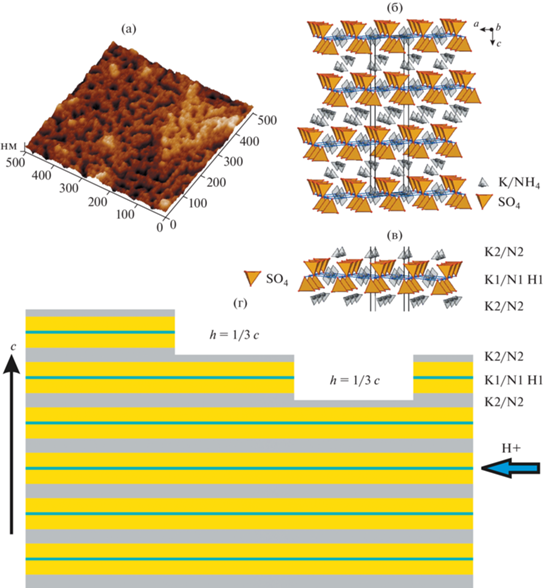
Рассмотрим особенности строения нанорельефа поверхности (001) (K0.43(NH4)0.57)3H(SO4)2 с помощью схемы, построенной на основе данных АСМ и структурного анализа (рис. 2). Если обратиться к деталям атомной структуры [1], то плоскую ступень высотой h = 1/3c можно представить в виде двойного слоя тетраэдров SO$_{4}^{{2 - }}$, вершины которых соединены водородными связями (рис. 2б), посреди этого слоя расположены катионы K1/N1, а выше и ниже – слои K2/N2 (рис. 2в). В позициях K1/N1 отношение K+ : NH$_{4}^{ + }$ = 5 : 1, а в позициях K2/N2 – 1 : 3, т.е. в слоях K2/N2 накапливается наибольшее количество аммония. Очевидно, что расщепление кристалла по плоскостям (001) с наименьшими энергетическими затратами будет происходить по слоям K2/N2, как связанным слабее в структуре (рис. 2г). Наличие отрицательных катионных вакансий, локализованных на террасах, и отрицательных зарядов двойных слоев сульфат-ионов на кромках ступеней будет определять вклад в поверхностный электростатический потенциал, который может быть детектирован на наномасштабах с помощью СМК. Здесь уместна аналогия с получением поверхностей (001) щелочно-галоидных кристаллов и кристаллов MgO путем раскола, который приводил к появлению заряженных дефектов в объеме и на поверхности [16]. В результате метод СМК фиксировал сдвиги напряжения в десятки вольт на свежих диэлектрических поверхностях [17, 18].
С помощью бесконтактных методов измерения потенциала и емкости изучены поверхность свежего скола образца (K0.43(NH4)0.57)3H(SO4)2 и ее изменение при выдержке на воздухе во времени при условиях, близких к нормальным (296 K, 35%). Заметим, что в сканирующей емкостной силовой микроскопии градиент емкости dC/dZ применяют для картирования вариации емкости (и статической диэлектрической проницаемости) или вариации толщины тонких диэлектрических пленок [12–14]. Дифференциальную емкость dC/dU используют для картирования постепенных изменений количества и местоположения накопленного заряда, которые могут изменяться в зависимости от напряжения, времени, температуры или других экспериментальных переменных [12, 13]. Корреляционные измерения локальных электрических характеристик дополняют друг друга и наряду с топографическими данными обеспечивают обнаружение отдельных составляющих гетерогенных материалов и дефектных зон с высокой чувствительностью, что было продемонстрировано для ряда полимеров [19, 20] и сегнетоэлектрического водородсодержащего кристалла с неоднородным распределением примеси [21].
На рис. 3а представлено характерное топографическое изображение участка свежей поверхности (001) размером 5 × 5 мкм2. После расщепления кристалла (K0.43(NH4)0.57)3H(SO4)2 образовался характерный нанорельеф в виде плоских террас, параллельных (001), с многочисленными мелкими выступами и ямками, с латеральными размерами от 40–250 нм и перепадами высот ∼1/3c. Для данного гладкого участка (размах высот – максимальный перепад высот Ry не превышает параметра с элементарной ячейки) величина локальной поверхностной контактной разности потенциалов (UCPD) составила UCPD = –114 мВ. Судя по данным измерений электрических характеристик – распределения локального потенциала UCPD (рис. 3б) и емкости (dC/dz, dC/dU), поверхность свежего скола отрицательно заряжена и энергетически однородна.
Рис. 3.
АСМ-изображения одного и того же участка поверхности (001) кристалла (K0.43(NH4)0.57)3H(SO4)2, полученной свежим сколом (а, б), и трансформировавшейся со временем (500 ч) (в). Топография (а, в), поверхностный потенциал (б), профиль сечения (г) вдоль линии (в).

В воздушной среде со временем начинают происходить изменения морфологии и зарядового состояния поверхности образцов (скорее всего в результате реакции ионов активных центров с адсорбированной H2O). После 24 ч сначала пропадают элементы 2D-рельефа, характерные для исходной свежей поверхности кристалла (заметно уменьшается количество выступов высотой 1/3c). Вместе с этим меняется знак потенциала с отрицательного на положительный и его величина UCPD = +5.8 мВ. После 430 ч рельеф изменяется коренным образом: появляется слой с порами с размерами отверстий в сотни нанометров (рис. 3в), вместе с этим значительно увеличивается величина потенциала UCPD = +84 мВ. Глубина отдельных пор, согласно профилю сечения на данном участке поверхности (рис. 3г), составляет ∼250 нм.
Для характеристики новообразовавшегося слоя и оценки размеров внутренних объемных дефектов рассмотрим серию изображений одного и того же участка поверхности с большей площадью (50 × 50 мкм2), а именно, топографическое (рис. 4а), потенциала (рис. 4б), производных емкости dC/dz (рис. 4в) и dC/dU (рис. 4г). Статистический анализ показывает, что шероховатость трансформировавшейся за 430 ч поверхности выросла почти в 40 раз (Ry = 398.4 нм, а Rq = 28.5 нм) по сравнению с исходной. На изображениях наблюдается большое количество пор с латеральными размерами и глубиной 300–800 и 50–300 нм соответственно. Местами поры выстраиваются в ряды и, объединяясь, образуют канавки. На основании измерения глубины пор можно сделать приближенные оценки толщины самого трансформировавшегося слоя – не менее 300 нм за 500 ч (примерная скорость роста слоя 10–2 нм/мин). Распределение поверхностного потенциала на изображении остается достаточно равномерным, несмотря на то что на отдельных глубоких порах видны всплески сигнала, связанные с вкладом рельефа (рис. 4б). Для данного участка поверхности UCPD = +84 мВ. Вне сомнения, образование слоя изменило зарядовое состояние и морфологию поверхности кристалла.
Рис. 4.
АСМ-изображения одного и того же участка поверхности (001) кристалла (K0.43(NH4)0.57)3H(SO4)2 размером 50 × 50 мкм2 при воздействии окружающей среды в течение 500 ч при 296 K: топография (а), потенциал (б), распределение дифференциальной емкости dC/dz (в), dC/dU (г).

Дополнительную информацию о дефектности поверхностного слоя кристалла дает сопоставление изображений поверхностного распределения производных емкости и потенциала (рис. 4). Вследствие высокой чувствительности метода к перепадам рельефа на обоих емкостных изображениях dC/dz и dC/dU поверхностного слоя с хорошим контрастом выявляются элементы топографии: граница ступени, поры и каналы (рис. 4в, 4г). Кроме этого, видны крупные светлые области в одних и тех же относительно ровных участках поверхности, не коррелирующие с рельефом (рис. 4в, 4г). Возможно, в конкретном случае емкостные методы обнаруживают скрытые внутренние неоднородности модифицировавшегося слоя. На это указывает сопоставление изображений поверхностного распределения емкости и потенциала.
Итак, при выдержке образца во времени в воздушной атмосфере (296 K, 35%) в отсутствие внешних температурных и электрических полей наблюдается изменение локальных электрических характеристик поверхности, что указывает на самопроизвольное протекание химического процесса на поверхности (001) кристаллических образцов (K0.43(NH4)0.57)3H(SO4)2. Характеристические стадии процесса во времени при неизменных внешних условиях: свежая наноструктурированная поверхность кристалла имеет отрицательный заряд, модифицированная – положительный. Образовавшийся на поверхности слой содержит микроскопические дефекты в виде сквозных пор и скрытых неоднородностей, что, по-видимому, связано с массопереносом на межфазовой границе. Добавим, что свойств поверхности, связанных с пьезо- и сегнетоэлектрической активностью, у образцов (K0.43(NH4)0.57)3H(SO4)2, полученных свежим сколом, выдержанных во времени или подвергнутых полировке, при комнатной температуре не обнаружено.
Локальная проводимость смешанных кристаллов. Для изучения зависимости электропроводности от состава х и ориентации образцов были измерены локальные ВАХ перпендикулярно (рис. 5а) и вдоль (рис. 5б) оси с при 296 K. Учитывая упомянутые выше процессы модификации поверхности, измерения выполнены на образцах со свежими сколами. На рис. 5 представлены графики зависимостей I(U) контакта зонд–образец для составов (K0.19(NH4)0.81)3H((SO4)2 и K0.43(NH4)0.57)3H(SO4)2, полученные при статичном положении зонда при подаче напряжения смещения от –4 до +4 В. Для повышения достоверности информации ВАХ усредняли по 25 кривым. Величины тока утечки (I) и локальной проводимости (σDC) приведены в табл. 1.
Рис. 5.
ВАХ образцов (K0.43(NH4)0.57)3H(SO4)2 (1) и (K0.19(NH4)0.81)3H((SO4)2 (2), зарегистрированные при 296 K вдоль (а) и перпендикулярно (б) тригональной оси с. Поверхность образцов получена свежим сколом.
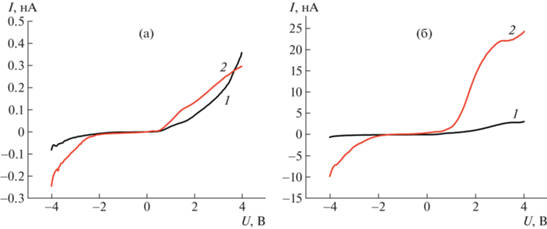
Таблица 1.
Электропроводность локальной области под кантилевером при подаче напряжения смещения 3 В
| x | Величина тока (I), нА | Толщина пластины, мм | Проводимость (σDC), См см–1 | |||
|---|---|---|---|---|---|---|
| ⊥ с | || с | ⊥ с | || с | ⊥ с | || с | |
| 0.57 | 1.86536 | 0.81103 | 1.27 | 0.27 | 7.95 × 10–4 | 3.02 × 10–4 |
| 0.81 | 13.63603 | 0.783 | 1.6 | 0.3 | 5.92 × 10–3 | 2.94 × 10–4 |
При измерении тока вдоль оси с (поперек двойных сульфатных слоев, рис. 2) электрические характеристики образцов с разным составом аналогичны: несимметричные ВАХ как у полупроводникового диода с очень маленькой проводимостью (при U = 3В ток утечки I ∼ 0.15–0.20 нА) (рис. 5а). Небольшое различие между ними проявляется в интервале приложенных напряжений смещения от 0 до +4 В, а именно, для состава x = = 0.81 характер зависимости I(U) ближе к омическому типу, тогда как для x = 0.57 – к экспоненциальному.
Анизотропия проводимости и различия между составами становятся более выраженными при измерении зависимости I(U) перпендикулярно оси с, т.е. вдоль сульфатных слоев и соединяющих их системы водородных связей (рис. 5б). Для образцов с бóльшим содержанием ионов аммония (х = 0.81) при U = 3 В величина тока больше почти в 7 раз, чем с меньшим (х = 0.57) (табл. 1). Так же как кристаллы (NH4)3H(SO4)2, образцы (K$_{{1--x}}$(NH4)x)3H(SO4)2 при комнатной температуре продемонстрировали высокий уровень анизотропии проводимости. Соотношения величин предэкспоненциальных коэффициентов уравнения Аррениуса в направлении кристаллографических осей а и с моноклинного (NH4)3H(SO4)2 различались примерно в 5 раз (5.3 × 108 и 1.1 × × 108 См см–1 K соответственно) при T < 413 K [22]. При приложении напряжения, превышающего 3 В, для состава х = 0.19 наблюдается смена механизма проводимости (рис. 5б), одной из причин которой могут быть необратимые процессы изменения структуры вещества в зоне контакта с Pt-зондом.
В целом механизм электропроводности образцов твердых растворов (K$_{{1--x}}$(NH4)x)3H(SO4)2 при комнатной температуре можно определить как структурно-чувствительный. Локальная проводимость образцов в направлении вдоль оси с одинаково невысокая, а в направлении, перпендикулярном с, увеличивается почти в 2 раза для х = = 0.57 и на порядок величины для х = 0.81. Анизотропия статической проводимости отражает слоистую структуру кристалла (K$_{{1--x}}$(NH4)x)3H(SO4)2, что наглядно показано на рис. 2. Разница в измеряемой величине локальной проводимости в плоскости (001) для тригональных фаз разного состава указывает на роль разной заселенности катионных позиций при переносе заряда.
ОБСУЖДЕНИЕ ЭКСПЕРИМЕНТАЛЬНЫХ РЕЗУЛЬТАТОВ
Микроскопический анализ показал, что свойства поверхностного слоя смешанных кристаллов (K$_{{1--x}}$(NH4)x)3H(SO4)2 меняются со временем. В связи с этим обратимся к литературным данным и обсудим роль адсорбции воды в трансформации поверхности. Изучение поверхности щелочно-галоидных кристаллов NaCl показало, что при относительной влажности менее 30% вода адсорбируется в основном на краях ступеней, при 35% образуется равномерный слой воды и наблюдается медленное развитие ступенек на поверхности, а при 73% ступенчатая структура становится нестабильной и размывается на поверхности соли [23]. Наблюдения за изменениями поверхности кристаллов (K0.43(NH4)0.57)3H(SO4)2 на воздухе показывают, что при относительной влажности 35% также происходит постепенное равномерное сглаживание ступенчатой структуры, сопровождающееся переходом от отрицательно заряженной поверхности к нейтральной, а затем положительно заряженной. В кристаллах (K0.20(NH4)0.80)3H(SO4)2 и K0.33(NH4)0.67)3H(SO4)2 элементы ступенчатого строения свежей поверхности (001), еще различимые на топографических изображениях при 30%-ной влажности воздуха, полностью исчезали при повышении влажности до 40% [3]. Кинетика процесса и скорость образования модифицированного слоя зависят от влажности атмосферы и долевого соотношения ионов калия и аммония. Можно предположить, что в данном случае при комнатной температуре имеет место химическая адсорбция слоя воды, которая вызывает перестройку структуры поверхности кристаллов кислых солей и способствует образованию модифицированного дефектного слоя, вероятно, многофазного. Важную роль в процессе переноса адсорбата играют поры и другие поверхностные неоднородности.
Реальная структура и механизмы изменения кристаллов (K$_{{1--x}}$(NH4)x)3H(SO4)2 нуждаются в дальнейшем исследовании. На данном этапе получена важная информация об анизотропии локальной проводимости, распределении поверхностного потенциала и емкости суперпротонных фаз, которая расширяет представления о функциональных свойствах кристаллов. В процессе выполнения работы предложен оригинальный подход к исследованию анизотропии проводимости, в котором проведение измерений осуществляется прямым методом на свежих поверхностях образцов различной кристаллографической ориентации.
ЗАКЛЮЧЕНИЕ
Для анализа поверхности суперпротонных кристаллов твердых растворов (K$_{{1--x}}$(NH4)x)3H(SO4)2 применен комплекс контактных и бесконтактных методов электрической АСМ. С помощью проводящей АСМ впервые обнаружена анизотропия локальной проводимости кристаллов (K$_{{1--x}}$(NH4)x)3H(SO4)2 при комнатной температуре. Показано, что проводимость образцов в направлении вдоль оси с близка по величине (∼3 × × 10–4 См см–1), а в направлении, перпендикулярном с, существенно увеличивается – почти в 2 раза для х = 0.57 и на порядок величины для х = 0.81.
Методы СМК и емкостной силовой микроскопии способны давать дополнительную информацию об изменениях поверхности, связанных с локальным накоплением заряда и химическими реакциями в суперпротонных кристаллах. Установлено, что наноструктурированная поверхность (001), образующаяся при свежем сколе кристалла (K0.43(NH4)0.57)3H(SO4)2, имеет отрицательный заряд. Адсорбция влаги приводит к формированию на поверхности пористого слоя толщиной в несколько сот нанометров, при этом изменяются знак и величина поверхностного потенциала.
Авторы выражают благодарность В.В. Долбининой за предоставленные для исследований образцы.
Работа выполнена при поддержке Министерства науки и высшего образования РФ в рамках выполнения работ по Государственному заданию ФНИЦ “Кристаллография и фотоника” РАН. Эксперименты проведены с использованием оборудования ЦКП ФНИЦ “Кристаллография и фотоника” при поддержке Минобрнауки.
Список литературы
Selezneva E.V., Makarova I.P., Malyshkina I.A. et al. // Acta Cryst. B. 2017. V. 73. P. 1105. https://doi.org/10.1107/S2052520617012847
Малышкина И.А., Селезнева Е.В., Макарова И.П., Гаврилова Н.Д. // Вестн. МГУ. Сер. 3. Физика. Астрономия. 2019. № 4. С. 52. https://doi.org/10.3103/S002713491904012X
Гайнутдинов Р.В., Толстихина А.Л., Селезнева Е.В., Макарова И.П. // ЖТФ. 2020. Т. 9. № 11. С. 1843. https://doi.org/10.21883/JTF.2020.11.49972.116-20
Баранов А.И. // Кристаллография. 2003. Т. 48. № 6. С. 1081.
Norby T. // Nature. 2001. V. 410. № 6831. P. 877.
Fitzgerald R. // Physics Today. 2001. V. 54. № 7. P. 22. https://doi.org/10.1063/1.1397388
Haile S.M., Boysen D.A., Chisholm C.R.I., Merle R.B. // Nature. 2001. V. 410. P. 910. https://doi.org/10.1038/35073536
Baranov A.I., Grebenev V.V., Khodan A.N. et al. // Solid State Ionics. 2005. V. 176. № 39–40. P. 2871. https://doi.org/10.1016/j.ssi.2005.09.018
Boysen D.A., Uda T., Chisholm C.R.I., Haile S.M. // Science. 2004. V. 303. № 5654. P. 68.
Макарова И.П., Черная Т.С., Филаретов А.А. и др. // Кристаллография. 2010. Т. 55. № 3. С. 429. https://doi.org/10.1134/S1063774510030065
Fukami T., Tobaru K., Kaneda K. et al. // J. Phys. Soc. Jpn. 1994. V. 63. P. 2829. https://doi.org/10.1143/JPSJ.63.2829
Kobayashi K., Yamada H., Matsushige K. // Appl. Phys. Lett. 2002. V. 81. P. 2629. https://doi.org/10.1063/1.1510582
Kimura K., Kobayashi K., Yamada H., Matsushige K. // Appl. Surf. Sci. 2003. V. 210. P. 93. https://doi.org/10.1016/S0169-4332(02)01486-1
Гайнутдинов Р.В., Толстихина А.Л., Лашкова А.К. и др. // ЖТФ. 2019. № 11. С. 1692. https://doi.org/10.1134/S1063784219110094
Merle R.B., Chisholm C.R.I., Boysen D.A., Haile S.M. // Energy Fuels. 2003. V. 17. P. 210. https://doi.org/10.1021/ef0201174
Barth C., Henry C.R. // Phys. Rev. Lett. 2007. V. 98. P. 136804. https://doi.org/10.1103/PhysRevLett.98.136804
Harris L.B., Fiasson J. // J. Phys. C. 1985. V. 18. P. 4845. https://doi.org/10.1088/0022-3719/18/25/005
Barth C., Foster A.S., Henry C.R., Shluger A.L. // Adv. Mater. 2011. V. 23. P. 477. https://doi.org/10.1002/adma.201002270
Magonov S., Alexander J. // Beilstein J. Nanotechnol. 2011. V. 2. P. 15. https://doi.org/10.3762/bjnano.2.2
Magonov S., Alexander J. // Microscopy and Microanalysis. 2011. V. 17. № 4. P. 587. https://doi.org/10.1017/S1431927611000122
Gainutdinov R.V., Belugina N.V., Lashkova A.K. et al. // Ferroelectrics. 2019. V. 541. № 1. P. 39. https://doi.org/10.1080/00150193.2019.1574640
Sohn Y.J., Sparta K.M., Meven M. et al. // Solid State Ionics. 2013. V. 252. P. 116. https://doi.org/10.1016/j.ssi.2013.06.011
Dai Q., Hu J., Salmeron M. // J. Phys. Chem. B 1997. V. 101. № 11. P. 1994. https://doi.org/10.1021/jp9625772
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография


