Кристаллография, 2022, T. 67, № 3, стр. 437-441
Электропроводность кристаллов LiNbO3 в условиях температурного воздействия в вакууме
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
* E-mail: nsorokin1@yandex.ru
Поступила в редакцию 24.04.2021
После доработки 21.06.2021
Принята к публикации 29.06.2021
- EDN: ALIWVD
- DOI: 10.31857/S0023476122030195
Аннотация
Методом импедансной спектроскопии изучена температурная зависимость статической электропроводности σdc(T) монокристалла LiNbO3 (пр. гр. R3c), ориентированного вдоль кристаллографической оси c. Измерения импеданса проводились в условиях температурного воздействия в вакууме в цикле нагрев−охлаждение. При нагреве получена зависимость σdc(T) с энергией активации Ea = = 1.22 эВ, обусловленная миграцией вакансий лития $V_{{{\text{Li}}}}^{'}$. При охлаждении кривая σdc(T) разбивается на три участка с энергиями активации 0.66, 0.915 и 0.285 эВ. После измерений в вакууме в объеме кристалла образуются центры окраски, содержащие вакансии кислорода $V_{{\text{O}}}^{{ \bullet \bullet }}$ и электроны. Тепловое воздействие в вакууме на кристалл LiNbO3 приводит к смене ионного механизма электропроводности на смешанный ионно-электронный механизм. При 673 K ионная проводимость при охлаждении равна 3.2 × 10–6 См/см и превышает σdc при нагреве в ∼4 раза. При 500 K электронная проводимость при охлаждении равна 4.3 × 10–7 См/см и превышает σdc при нагреве в ∼515 раз (экстраполяция).
ВВЕДЕНИЕ
Кристаллы ниобата лития обладают перспективными сегнетоэлектрическими и нелинейно-оптическими свойствами, относятся к важнейшим функциональным материалам электронной техники, интегральной оптики и нелинейной фотоники, являются эффективными преобразователями частоты лазерного излучения [1–4]. Сегнетоэлектрический переход в LiNbO3 из полярной (пр. гр. R3c) в параэлектрическую центросимметричную фазу (пр. гр. R3m) происходит незадолго до плавления (TC ≈ 1413 K и Tfus ≈ 1528 K [2]). Физические свойства кристаллов LiNbO3 в большой степени зависят от условий выращивания и технологических воздействий [5, 6]. Например, температура Кюри TC является неявной функцией концентрации дефектов и может изменяться в пределах 150 K.
Ниобат лития имеет ильменитоподобную кислородно-октаэдрическую структуру (пр. гр. R3c, Z = 6) [7, 8]. Параметры элементарной ячейки и плотность для конгруэнтного состава (48.45 мол. % Li2O и 51.55 мол. % Nb2O5) следующие: a = 5.150, c = 13.864 Å, ρ = 4.647 г/см3 [2, 9]. Катионы Li+ и Nb5+ окружены искаженными октаэдрами из анионов кислорода (координационное число (КЧ) 6). Октаэдры [LiO6] и [NbO6] соединяются ребрами и общими гранями, образуя пространственный каркас. Катионы Nb5+, находящиеся в центрах координационных октаэдров [NbO6], определяют дипольное упорядочение и сегнетоэлектрические свойства ниобата лития.
Кристаллохимический анализ указывает на возможность реализации Li+-ионного переноса в структуре сложного оксида LiNbO3. Ионы Li+ имеют единичный заряд и малую величину ионного радиуса, поэтому, как правило, обладают высокой подвижностью в кристаллических структурах химических веществ. Способствуют подвижности ионов Li+ в структуре ниобата лития и более слабые химические связи Li−O в координационных октаэдрах [LiO6] по сравнению со связями Nb−O в октаэдрах [NbO6] [7, 8]. По этим причинам именно расположенные в октаэдрах [LiO6] подвижные катионы Li+ являются ответственными за появление ионной проводимости в кристаллах LiNbO3.
Ниобат лития имеет склонность к проявлению нестехиометрии (отношение концентраций катионов [Li]/[Nb] < 1), поэтому выращенные кристаллы обладают высокой концентрацией собственных дефектов [2, 10]. Основными собственными дефектами являются вакансии лития $V_{{{\text{Li}}}}^{'}$ и кислорода $V_{{\text{O}}}^{{ \bullet \bullet }}$ (обозначение дефектов приведено в символах Крегера–Винка [11]). Также кристаллы LiNbO3 могут содержать значительные концентрации несобственных дефектов за счет примесей. Повышение концентрации вакансий $V_{{{\text{Li}}}}^{'}$ приводит к увеличению ионной проводимости, в то время как повышение концентрации вакансий $V_{{\text{O}}}^{{ \bullet \bullet }}$, образующих донорные центры, приводит к росту электронной проводимости n-типа.
Активно проводятся исследования электропроводности сегнетоэлектрических и нелинейно-оптических кристаллов LiNbO3 [12–23]. Однако приведенные в этих работах сведения о природе электропроводности, типе носителей заряда и механизме электропереноса противоречивы. Номинально чистые кристаллы LiNbO3 характеризуются высокой чувствительностью электрофизических свойств к способам получения, внешним воздействиям и степени нестехиометрии [Li]/[Nb] [4, 14, 20].
При комнатной температуре электропроводность ниобата лития невысока. Так, по данным [22] кристаллы LiNbO3 имеют ионную (Li+) проводимость σ ∼ 10–12 См/см при 373 К, что существенно ниже литий-ионной проводимости в катион-дефицитном твердом растворе Li3xLa1/3−xNbO3 со структурой перовскита [24]. Для Li3xLa$_{{1/3 - x}}$NbO3 проводимость σ = (1−5) × 10–5 См/см при 298 K и энергия активации ионного переноса Eσ = 0.3− 0.4 эВ (вакансии лития $V_{{{\text{Li}}}}^{'}$). Анизотропия электропроводности в кристаллах LiNbO3 практически отсутствует [17, 25].
В [12, 13, 26, 27] на температурной зависимости ионной электропроводности кристаллов LiNbO3 наблюдали скачок проводимости при T0 ≈ 760 К. В области температур ниже сегнетоэлектрического перехода (T < TC) ниобат лития не имеет других фазовых переходов [4, 28], поэтому скачок проводимости в [12, 13, 26] связали с ориентационным (торсионным) движением октаэдров [NbO6]. При этом ионы кислорода смещаются, увеличивая “окно проводимости” для миграции катионов Li+. Наличие вакансий $V_{{\text{O}}}^{{ \bullet \bullet }}$ и увеличение с ростом температуры тепловых колебаний ионов кислорода, находящихся на гранях полиэдров [LiO6], способствуют миграции катионов Li+.
Путем восстановительного (в том числе вакуумного) отжига кристаллы LiNbO3 можно перевести в полупроводниковое состояние [5, 19, 29–32]. В кристаллах, подвергнутых восстановительному отжигу, энергия активации электронного переноса равна 0.3 эВ (при 80−450 K) [19], что в несколько раз меньше энергии активации ионного переноса (0.7−1.2 эВ по данным [13, 14, 16–18]).
В работе представлены результаты измерений зависимости статической электропроводности σdc(T) в условиях температурного воздействия в вакууме и обсуждаются структурные механизмы электропереноса для конгруэнтно плавящегося кристалла LiNbO3 в цикле нагрев–охлаждение.
ЭКСПЕРИМЕНТ И ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В кондуктометрических экспериментах использовали монодоменные конгруэнтные кристаллы LiNbO3 [33], на которых ранее [5, 34] проводились измерения пироэлектрических свойств. Оптические монокристаллы конгруэнтного состава выращены из расплава методом Чохральского. Конгруэнтный состав ниобата лития является дефицитным по литию с отношением концентраций [Li]/[Nb] = 0.94 (дефицит по Li равен ∼6 мол. %). Параметры элементарной ячейки равны a = 5.150, c = 13.861 Å и c/a = 2.69 для гексагональной установки и хорошо совпадают с данными [2, 9].
Монокристаллический образец ориентирован вдоль кристаллографической оси c пр. гр. R3c. Он выполнен в виде цилиндра высотой 4.7 мм и диаметром 12 мм. На торцы образца нанесены металлические электроды в виде круга диаметром 5 мм. В качестве материала электродов использована серебряная паста (Leitsilber). Описание экспериментальной установки и методика электрофизических измерений даны в [35]. Относительная погрешность измерений σdc равна 5%.
Статическую электропроводность σdc определяли из спектров импеданса в диапазоне частот (5–5) × 105 Гц и сопротивлений 1–107 Ом (прибор Tesla BM-507). Температурные измерения импеданса выполнены в цикле нагрев–охлаждение от комнатной температуры до 818 K. Из-за низкой электропроводности кристаллов LiNbO3 значения σdc из спектров импеданса удалось определить только в температурных интервалах 665−818 K (нагрев) и 818−513 K (охлаждение).
Температурные зависимости электропроводности σ||c(T) кристалла LiNbO3 в цикле нагрев–охлаждение показаны на рис. 1. Кондуктометрические данные обрабатывали в соответствии с уравнением Аррениуса–Френкеля:
где σ0 – предэкспоненциальный множитель электропроводности и Eσ – энергия активации электропереноса. При нагреве на кривой σdc(T) никаких аномалий не обнаружено (участок I), параметры уравнения Френкеля–Аррениуса приведены в табл. 1. Значения σdc при 665 и 812 K равны 6.3 × × 10–7 и 2.7 × 10–5 См/см соответственно. Изменение величины электропроводности на участке I составляет ∼40 раз. Полученное значение энергии Eσ = 1.22 эВ хорошо совпадает с данными [14, 16, 17] для ионной электропроводности (1.16−1.25 эВ). Ионный перенос в кристаллах LiNbO3 происходит по вакансионному механизму [12, 15], в котором подвижными ионными дефектами являются вакансии $V_{{{\text{Li}}}}^{'}$. По данным 7Li-ядерного магнитного резонанса [16] диффузионное движение ионов Li+ в кристаллах LiNbO3 начинается при ∼700 K. При 800 K ионная проводимость кристалла LiNbO3 соответствует уровню проводимости одномерного (1D) ионного проводника Li2B4O7 [36].Рис. 1.
Температурные зависимости электропроводности кристалла LiNbO3 вдоль кристаллографической оси c в цикле нагрев–охлаждение: участок I – нагрев, участки II–IV – охлаждение.

Таблица 1.
Параметры участков температурной зависимости электропроводности кристалла LiNbO3 в цикле нагрев–охлаждение
| Режим | Участок кривой σdc(T) | Интервал температур, K |
Множитель σ0, СмK/см | Энергия Eσ, эВ |
|---|---|---|---|---|
| Нагрев | I | 665−812 | 8.2 × 105 | 1.22 |
| Охлаждение | II | 776−818 | 4.5 × 102 | 0.66 |
| III | 651−752 | 1.55 × 104 | 0.915 | |
| IV | 513.5−626 | 1.6 × 10–1 | 0.285 |
В структуре ниобата лития вдоль кристаллографической оси c располагаются цепочки октаэдров …[LiO6]–[NbO6]–[$V_{{{\text{Li}}}}^{'}$O6]…[LiO6]–[NbO6]–[$V_{{{\text{Li}}}}^{'}$O6]…, где $V_{{{\text{Li}}}}^{'}$ – вакантная позиции лития. Октаэдрические пустоты в кислородном каркасе на 1/3 заняты катионами Li+, на 1/3 – катионами Nb5+ и на 1/3 пустые. Колонки кислородных октаэдров вытянуты вдоль полярной оси c и имеют общие грани. Химические связи Nb−O являются преимущественно ковалентными, а связи Li−O – ионными (кулоновское взаимодействие). Ионный транспорт катионов Li+ осуществляется через грани полиэдров [LiO6]. Катионы Li+ внутри колонок октаэдров могут переходить из одного кислородного октаэдра в другой.
Для конгруэнтных кристаллов LiNbO3 ([Li]/[Nb] = 0.94) структурными исследованиями [37–41] доказано нахождение “нестехиометрических“ катионов Nb5+ в позициях Li+. Ионные радиусы катионов Li+ (0.76 Å для КЧ 6 [42]) и Nb5+ (0.64 Å) не сильно различаются. Собственные дефекты образуются путем замещения катионов Li+ на катионы Nb5+ в октаэдрических позициях:
Существование дефектов ${\text{Nb}}_{{{\text{Li}}}}^{{ \bullet \bullet \bullet \bullet }}$ и $V_{{{\text{Li}}}}^{'}$ лежит в основе всех моделей дефектной структуры ниобата (танталата) лития [2, 3, 10, 27, 37–41].
Отметим, что возникновение вакансий $V_{{{\text{Li}}}}^{'}$ является предпочтительным способом создания разупорядоченной подсистемы мобильных катионов проводимости в литийпроводящих кристаллических электролитах [43]. Появление вакансий $V_{{{\text{Li}}}}^{'}$ приводит к увеличению подвижности катионов Li+ без изменения пространственного расположения каналов проводимости. Взяв типичную для литийпроводящих твердых электролитов энергию миграции вакансий $V_{{{\text{Li}}}}^{'}$, равной Em ≈ 0.3 эВ, можно оценить энергию ассоциации дефектов ${\text{Nb}}_{{{\text{Li}}}}^{{ \bullet \bullet \bullet \bullet }}$ + 4$V_{{{\text{Li}}}}^{'}$:
При охлаждении поведение электропроводности кристалла LiNbO3 кардинально изменяется. Кривая σdc(T) разбивается на три области (участки II–IV на рис. 1), для которых параметры уравнения Френкеля–Аррениуса приведены в табл. 1. По величине Eσ можно предположить, что в областях II и III доминирует ионная составляющая проводимости. Этот вывод подтверждается линейной корреляцией (правило Майера–Нейдела [44]) между параметрами проводимости $\lg {{\sigma }_{0}}$ и Eσ для участков I–III: представленной на рис. 2 (коэффициент корреляции R2 = 0.999):
Рис. 2.
Корреляция между электрофизическими параметрами $\lg {{\sigma }_{0}}$ и Eσ для участков I–III ионной проводимости кристалла LiNbO3.
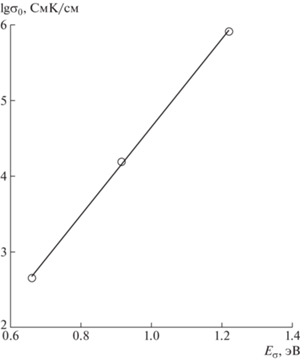
В [23] показано, что правило Майера–Нейдела выполняется для большой группы кислородно-октаэдрических сегнетоэлектриков, к которым относится и ниобат лития.
На кривой σdc(T) наблюдается скачок проводимости при T0 = 764 ± 12 K, разделяющий участки II и III. Эта аномалия проводимости хорошо совпадает со скачком проводимости при 760 K, обнаруженным в [13, 26]. Скачок проводимости при T0 ≈ 760 K соответствует порогу Таммана Tdiff (Tdiff – температура активации объемной диффузии) [45], ниже которого замораживаются диффузионные процессы в кристалле: Tdiff ≈ 0.52Tfus = = 794 K.
После кондуктометрических измерений в вакууме образец потемнел, что прямо указывает на образование в ходе проведения эксперимента стабильных центров окраски, содержащих вакансии кислорода $V_{{\text{O}}}^{{ \bullet \bullet }}$ и электроны [5, 31]. При измерениях кристалла LiNbO3 в вакууме протекает реакция:
При доминировании ионного переноса в кристалле LiNbO3 значение σdc при 665 K в режиме охлаждения равно 2.7 × 10–6 См/см, что превышает соответствующее значение σdc при нагреве в ∼4 раза. Улучшению ионного транспорта катионов Li+ может способствовать “искажение” полиэдров [LiO6] за счет образования вакансий $V_{{\text{O}}}^{{ \bullet \bullet }}$.
Энергия активации электропроводности (0.28 эВ) на участке IV значительно ниже, чем на участках I−III с ионной проводимостью. В этой низкотемпературной области доминирует электронная проводимость [19, 46]. Ширина запрещенной зоны в конгруэнтном кристалле LiNbO3 равна Eg = 3.7 эВ [23, 47], поэтому механизм электронной проводимости несобственный. Электронная проводимость чувствительна к появлению в кристалле LiNbO3 центров окраски. Таким образом, тепловое воздействие в вакууме приводит к появлению смешанной ионно-электронной проводимости в кристалле LiNbO3. При охлаждении электропроводность образца определяется как катионами Li+, так и электронами. Экстраполированные значения σdc при 500 K составляют 8.3 × 10–10 См/см (нагрев) и 4.3 × 10–7 См/см (охлаждение). Проводимость при охлаждении по отношению к нагреву возрастает в ∼515 раз.
ЗАКЛЮЧЕНИЕ
Обнаружена невоспроизводимость электрофизических данных для кристалла LiNbO3 в кондуктометрических измерениях, проведенных в вакууме в цикле нагрев–охлаждение. Проанализированы параметры электропереноса в разных температурных областях (участки I–IV на кривых σdc(T)). Тепловое воздействие в вакууме на кристалл LiNbO3 приводит к изменению характера электропроводности с ионного типа при нагреве на смешанный ионно-электронный тип при охлаждении. Это связано с тем фактом, что при температурном воздействии в вакууме в объеме кристалла LiNbO3 появляются электроны и вакансии $V_{{\text{O}}}^{{ \bullet \bullet }}$, часть электронов локализуется на вакансиях $V_{{\text{O}}}^{{ \bullet \bullet }}$, образуя центры окраски, приводящие к потере прозрачности кристалла.
Ионная проводимость (участки I–III) обусловлена миграцией по кристаллической решетке вакансий $V_{{{\text{Li}}}}^{ \bullet }$, которые образуются при выращивании из расплава конгруэнтных кристаллов LiNbO3. Центры окраски вносят возмущения в энергетическую структуру этих кристаллов. Это приводит к понижению энергетического рельефа для движения ионов Li+ по вакантным кристаллографическим позициям и, как следствие, к снижению энтальпии активации ионного транспорта на участках II и III. Низкотемпературная проводимость кристалла LiNbO3 на участке IV, по-видимому, обусловлена движением электронов.
Работа выполнена при поддержке Министерства науки и высшего образования в рамках выполнения работ по Государственному заданию ФНИЦ “Кристаллография и фотоника” РАН.
Список литературы
Jackson R.A., Szaller Z. // Crystals. 2020. V. 10. P. 780.
Volk T.R., Wohlecke M. Lithium niobate: defects, photorefraction and ferroelectric switching. Berlin: Springer, 2008. 247 p.
Сидоров Н.В., Волк Т.Р., Маврин Ю.Н., Калиников В.Т. Ниобат лития: дефекты, фоторефракция, колебательный спектр, поляритоны. М.: Наука, 2003. 255 с.
Кузьминов Ю.С. Электрооптические и нелинейнооптические кристаллы ниобата лития. М.: Наука, 1987. 264 с.
Шалдин Ю.В., Габриэлян В.Т., Матыясик С. // Кристаллография. 2008. Т. 53. № 5. С. 896.
Сидоров Н.В., Палатников М.Н., Габриэлян В.Т. и др. // Неорган. материалы. 2007. Т. 43. № 1. С. 66.
Nassau K., Levinstein H.J., Loiacono G.M. // J. Phys. Chem. Solids. 1966. V. 27. P. 983.
Abrachams S.C., Reddy J.M., Bernstein S.L. // J. Phys. Chem. Solids. 1966. V. 27. P. 997.
Lerner P., Legras C., Dumas J.P. // J. Cryst. Growth. 1968. V. 3–4. P. 231.
Schirmer O.F., Thiemann O., Wohlecke M. // J. Phys. Chem. Solids. 1991. V. 52. № 1. P. 185.
Kroger F.A. The chemistry of inperfect crystals. Amsterdam: North-Holland, 1964. 1039 p.
Palatnikov M.N., Yatsenko A.V., Sandler V.A. et al. // Solid State Ionics. 2020. V. 345. P. 115178. https://doi.org/10.1016/j.ssi.2019.11517
Палатников М.Н., Сандлер В.А., Сидоров Н.В., Макарова О.В. // ФТТ. 2019. Т. 61. № 7. С.1277.
El Bachiri A., Bennami F., Bousselamti M. // J. Asian Ceram. Soc. 2016. V. 4. P. 46.
Притуленко А.С., Яценко А.В., Евдокимов С.В. // Кристаллография. 2015. Т. 60. № 2. С. 293.
Heitjans P., Masoud M., Feldhoff A. // Faraday Discuss. 2007. V. 134. P. 67.
Niitsu H.T., Nagata N., Rodrigues A.C.M. // J. Appl. Phys. 2004. V. 95. № 6. P. 3116.
Bredikhin S., Scharner S., Klinger M. et al. // Solid State Ionics. 2000. V. 135. P. 737.
Ахмаддулин И.Ш., Голенищев-Кутузов В.А., Мигачев С.А. // ФТТ. 1998. Т. 40. № 7. С. 1307.
Габриелян В.Т., Касперович В.С., Климко С.А., Чарная Е.В. // ФТТ. 1996. Т. 38. № 6. С. 1884.
Блистанов А.А., Гераськин В.В., Степанова А.В. и др. // ФТТ. 1984. Т. 26. № 4. С. 1128.
Frauke H. // Phys. Status. Solidi. A. 1984. V. 83. P. 73.
Гуревич В.М. Электропроводность сегнетоэлектриков. М.: Изд-во комитета стандартов, 1969. 383 с.
Kawakami Y., Ikuta H., Wakihara M. // J. Solid State Electrochem. 1998. V. 2. P. 206.
Яценко А.В., Палатников М.Н., Сидоров Н.В. и др. // ФТТ. 2015. Т. 57. № 5. С. 932.
Палатников М.Н., Сандлер В.А., Сидоров Н.В., Макарова О.В. // Изв. СПбГТИ (ТУ). 2017. № 37. С. 75.
Яценко А.В., Палатников М.Н., Сидоров Н.В. // Кристаллография. 2019. Т. 64. № 1. С. 41.
Lines M.E., Glass A.M. Principles and application of ferroelectrics and related materials. Oxford: Clarendon Press, 1977. 680 p.
Jorgensen P.J., Bartlett R.W. // Phys. Chem. Solids. 1969. V. 30. № 12. P. 2639.
Bergmann G. // Solid State Commun. 1968. V. 6. P. 77.
Яценко А.В., Евдокимов С.В., Притуленко Д.Ю. и др. // ФТТ. 2012. Т. 54. № 11. С. 2098.
Bredikhin S., Scharner S., Klingler M. et al. // J. Appl. Phys. 2000. V. 88. P. 5687.
Баласанян Р.Н., Габриэлян В.Т., Коканян А.Т. // Кристаллография. 1990. Т. 35. № 6. С. 1545.
Шалдин Ю.В., Matyjasik S., Рабаданов М.Х. и др. // Докл. РАН. 2007. Т. 417. № 3. С. 328.
Иванов-Шиц А.К., Сорокин Н.И., Федоров П.П., Соболев Б.П. // ФТТ. 1983. Т. 25. № 6. С. 1748.
Sorokin N.I., Pisarevskii Yu.V., Lomonov V.A. // Crystallog. Rep. 2021. V. 66. № 6. P. 1051. https://doi.org/10.1134/S1063774521060377
Abrachams S.C., Marsh P. // Acta Cryst. B. 1986. V. 42. P. 61.
Iyi N., Kitamura K., Izumi F. et al. // J. Solid State Chem. 1992. V. 101. P. 340.
Zotov N., Boysen H., Frey F. et al. // J. Phys. Chem. Solids. 1994. V. 55. P. 145.
Blumel J., Born E., Metzger T. // J. Phys. Chem. Solids. 1994. V. 55. P. 589.
Leroux Ch., Nihoul G., Malovichenko G. et al. // J. Phys. Chem. Solids. 1998. V. 59. P. 311.
Shannon R.D. // Acta Cryst. A. 1976. V. 32. № 5. P. 751.
Иванов-Шиц А.К., Мурин И.В. Ионика твердого тела. СПб.: Изд-во СПб-ГУ. 2000. Т. 1. 616 с.
Meyer W., Neldel N. // Z. Techn. Phys. 1937. B. 18. S. 588.
Сорокин Н.И., Соболев Б.П. // Электрохимия. 2007. Т. 43. № 4. С. 420.
Esin A.A., Akhmatkhanov A.R., Shur V.Ya. // Ferroelectrics. 2016. V. 496. P. 102.
Сидоров Н.В., Палатников М.Н., Теплякова Н.А. и др. // Неорган. материалы. 2018. Т. 54. № 6. С. 611.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография


