Кристаллография, 2022, T. 67, № 3, стр. 392-398
Структура двух ацетиленовых производных салициловой кислоты
С. А. Найферт 1, Д. А. Жеребцов 1, *, К. Раджакумар 1, Д. А. Южакова 1, Д. В. Спиридонова 2, М. А. Полозов 1, А. А. Осипов 1, **, А. И. Луценко 1
1 Южно-Уральский государственный университет
Челябинск, Россия
2 Научный парк, Санкт-Петербургский государственный университет
Санкт-Петербург, Россия
* E-mail: zherebtsov_da@yahoo.com
** E-mail: darkforshine2015@mail.ru
Поступила в редакцию 29.08.2021
После доработки 05.10.2021
Принята к публикации 11.10.2021
- EDN: GXSDHZ
- DOI: 10.31857/S0023476122030146
Аннотация
Описан синтез метил-2-гидрокси-5-[(триметилсилил)этинил]бензоата и метил-2-гидрокси-5-этинилбензоата, представлены их кристаллографические данные. Особенность структуры обоих соединений – их слоистое строение, являющееся следствием плоской структуры молекул. Вместе с тем плоские молекулы не образуют стопочной упаковки. В метил-2-гидрокси-5-этинилбензоате молекулы в слое связаны между собой водородными связями, в том числе с участием терминального протона этинильной группы. Для обоих соединений приведены ИК-спектры и интерпретированы основные полосы поглощения. Приведен спектр фотолюминесценции метил-2-гидрокси-5-[(триметилсилил)этинил]бензоата: максимум эмиссии в твердом состоянии находится около 566 нм, а в растворе в хлороформе – 500 нм.
ВВЕДЕНИЕ
Салициловая кислота и ее производные широко применяются в медицине и аналитической химии. Ацетиленовые производные салициловой кислоты, такие как метил-2-гидрокси-5-[(триметилсилил)этинил]бензоат (1) и метил-2-гидрокси-5-этинилбензоат (2), были получены ранее [1], однако их структура до сих пор не была известна. Данные соединения являются важными прекурсорами для получения более сложных производных, например, 2 путем окислительной димеризации по реакции Гляйзера может быть преобразован в диметиловый эфир диацетилендисалициловой кислоты, перспективной жесткой линкерной молекулы для синтеза металлоорганических каркасов [2], ковалентных органических каркасов [3], а также графеновых нанолент [4]. В работе приводятся и обсуждаются структуры данных производных салициловой кислоты, а также их ИК-спектры и спектры фотолюминесценции 1.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез 5-иодсалициловой кислоты (2-гидрокси-5-иодобензойной кислоты). В круглодонную колбу объемом 250 мл поместили 14 г металлического йода (0.055 моль), 100 мл уксусной кислоты, затем добавили 7 г салициловой кислоты (0.05 моль). Через полчаса добавили 13.5 г (NH4)2S2O8 (0.06 моль), и нагревали смесь при 80°С в течение суток с обратным холодильником. После того как на верхних стенках колбы начал конденсироваться йод, добавили 8 мл ССl4 для смывания йода со стенок в раствор. Через 24 ч смесь охладили до комнатной температуры. Затем полученный раствор влили в 10%-й водный раствор Na2SO3 со льдом для того, чтобы нейтрализовать непрореагировавший йод и выделить целевой продукт, выпадающий в осадок. Раствор отфильтровали через воронку Бюхнера, а полученный осадок серого цвета высушили. Выход продукта составил 12.1 г (95%).
Синтез метилового эфира 5-иодсалициловой кислоты (5-иодметилсалицилата). В круглодонную колбу объемом 250 мл поместили 2-гидрокси-5-иодбензойную кислоту (10.5 г, 39.8 ммоль), 100 мл метанола и 5 мл концентрированного раствора H2SO4. Полученный раствор перемешивали на магнитной мешалке с кипячением в течение 24 ч. Затем смесь охладили до комнатной температуры и отогнали основную часть метанола на роторном испарителе. Далее неочищенную смесь смешали с СHCl3 и промыли водой. Органическую часть после испарения растворителя очистили методом колоночной хроматографии (элюент – гексан). Конечный продукт – твердое вещество белого цвета. Выход продукта составил 65%.
Cинтез метил-2-гидрокси-5-[(триметилсилил)этинил]бензоата (1). В двугорлую колбу объемом 250 мл поместили 5-иодометилсалицилат (4.00 г, 14.39 ммоль), Pd(PPh3)4 (0.16 г, 0.14 ммоль), триметилсилилацетилен (2.54 мл, 17.99 ммоль) и CuI (27 мг, 0.14 ммоль) с добавлением триэтиламина (5 мл) и тетрагидрофурана (30 мл). Смесь перемешивали при 40°C в течение 24 ч в инертной атмосфере (Ar). Полученный раствор промыли водой и экстрагировали хлороформом. После испарения органического растворителя образовалось желтовато-коричневое твердое вещество. Его очистку провели методом колоночной хроматографии (силикагель, элюент – гексан). При испарении гексана были получены кристаллы светло-коричневого цвета (1.1 г, 45%), пригодные для структурного анализа. 1Н ЯМР-спектроскопия подтвердила строение молекулы 1: 1H NMR (400 MГц, CDCl3) δ 10.88 (s, 1H), 7.97 (d, J = 2.1 Гц, 1H), 7.53 (dd, J = 8.6, 2.1 Гц, 1H), 6.91 (d, J = 8.6 Гц, 1H), 3.95 (s, 3H), 0.24 м.д. (s, 9H).
Синтез метил-2-гидрокси-5-этинилбензоата (2). В коническую колбу объемом 100 мл добавили 28 мл метилового спирта, K2CO3 (10 ммоль) и 1.1 г (4 ммоль) метил-2-гидрокси-5-[(триметилсилил)этинил]бензоата. Смесь перемешивали при комнатной температуре в течение 12 ч. Затем реакционный раствор отфильтровали и осадок промыли СHCl3. Полученную смесь промыли водой, экстрагировали СHCl3, органическую часть осушили с помощью Na2SO4. Раствор упарили, при этом удалось найти монокристаллы. Выход составил 0.48 г (61%). 1Н ЯМР-спектроскопия подтвердила строение молекулы 2: 1H NMR (400 MГц, CDCl3) δ 10.90 (s, 1H), 8.00 (d, J = 2.1 Гц, 1H), 7.55 (dd, J = = 8.6, 2.1 Гц, 1H), 6.94 (d, J = 8.6 Гц, 1H), 3.96 (s, 3H), 2.99 м.д. (s, 1H).
Рентгеноструктурное исследование образцов проведено с использованием монокристального дифрактометра Rigaku XtaLab Synergy-S с детектором HyPix-6000HE (CuKα, λ = 1.54184 Å). Температуру съемки 100 K поддерживали с помощью системы Oxford Cryostream 800. ИК-спектры получены на спектрометре Shimadzu IRAffinity-1S, в качестве матрицы использовали бромид калия. 1Н ЯМР-спектроскопия проведена на спектрометре Bruker Avance III 400 МГц.
Первичная обработка экспериментальных данных, поправка на поглощение, введенная при помощи алгоритма SCALE3 ABSPACK, выполнены в пакете программ CrysAlisPro [5]. Структуры соединений 1 и 2 решены с использованием программ Olex2 [6], SHELXT [7] и уточнены в анизотропном приближении смещений для всех атомов, кроме водорода с помощью программы SHELXL [8]. Атомы водорода помещали в геометрически рассчитанные положения и уточняли с использованием модели “наездника” (Uiso(H) = = nUeq(C), где n = 1.5 для CH3-групп, n = 1.2 для CH- и CH2-групп).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджский банк структурных данных (№ 2098429 для 1 и № 2098428 для 2; deposit@ccdc.cam.ac.uk; http:// www.ccdc.cam.ac.uk). Кристаллографические данные, параметры эксперимента и уточнения структур соединений 1 и 2 приведены в табл. 1 и 2.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры соединения 1
| Эмпирическая формула | C13H16O3Si |
|---|---|
| М, г/моль | 248.35 |
| Т, К | 100(2) |
| Сингония, пр. гр., Z | Триклинная, P$\bar {1}$, 2 |
| a, b, c, Å | 7.1105(3), 9.7128(3), 9.9672(2) |
| α, β, γ, град | 101.704(2), 92.679(3), 97.752(3) |
| V, Å3 | 665.94(4) |
| ρрасч, г/см3 | 1.239 |
| μ, мм–1 | 1.520 |
| F (000) | 264.0 |
| Размер кристалла, мм | 0.28 × 0.24 × 0.2 |
| Излучение; λ, Å | CuKα; 1.54184 |
| 2θ, град | 9.088–139.9 |
| Пределы h, k, l | –8 ≤ h ≤ 8, –10 ≤ k ≤ 11, –12 ≤ l ≤ 12 |
| Количество отражений: измеренных/независимых (N1), Rint, Rσ/с I ≥ 2σ(I) (N2) | 6988/2490, 0.0284, 0.0327/2259 |
| Количество параметров | 159 |
| R1/wR2 по N1 | 0.0387/0.0936 |
| R1/wR2 по N2 | 0.0355/0.0919 |
| S | 1.055 |
| Δρmin/Δρmax, э Å–3 | –0.24/0.37 |
Таблица 2.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры соединения 2
| Эмпирическая формула | C10H8O3 |
|---|---|
| М, г/моль | 176.16 |
| Т, К | 100(2) |
| Сингония, пр. гр., Z | Моноклинная, P21/c, 4 |
| a, b, c, Å | 9.1938(2), 12.7346(3), 7.14552(18) |
| β, град | 90, 95.436(2), 90 |
| V, Å3 | 832.82(4) |
| ρрасч, г/см3 | 1.405 |
| μ, мм–1 | 0.872 |
| F(000) | 368.0 |
| Размер кристалла, мм | 0.14 × 0.12 × 0.1 |
| Излучение; λ, Å | CuKα; 1.54184 |
| 2θ, град | 9.664–139.838 |
| Пределы h, k, l | –11 ≤ h ≤ 11, –15 ≤ k ≤ 15, –8 ≤ l ≤ 8 |
| Количество отражений: измеренных/независимых (N1), Rint, Rσ/с I ≥ 2σ(I) (N2) | 5560/1562, 0.0253, 0.0251/1412 |
| Количество параметров | 120 |
| R1/wR2 по N1 | 0.0367/0.0923 |
| R1/wR2 по N2 | 0.0338/0.0902 |
| S | 1.073 |
| Δρmin/Δρmax, э Å–3 | –0.20/0.19 |
Плоская форма молекул 1 обусловила их упаковку в слоистую структуру (рис. 1). Расстояние между слоями составляет ∼3.532(2) Å, что несколько больше, чем расстояние между слоями графена в графите (3.35 Å).
Рис. 1.
Проекция структуры соединения 1 на плоскости: а – bc, б – ac. Пунктирные линии обозначают водородные связи.

Водородные связи в 1 – только интрамолекулярные, между протоном гидроксогруппы и кислородом карбонильной группы. Их длина обусловлена геометрией молекулы и составляет 1.872(2) Å.
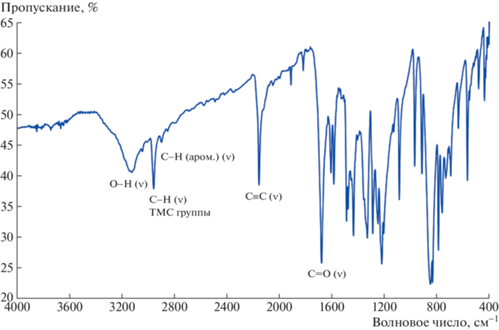
ИК-спектр соединения 1 (рис. 2) хорошо соответствует его структуре. В ИК-спектре отчетливо видна интенсивная полоса валентных колебаний С≡С-связей около 2156 см–1, полоса валентных колебаний С–Н-связей четырех метильных групп около 2957 см–1, широкая полоса валентных колебаний О–Н-связей гидроксогрупп около 3119 см–1, слабая полоса валентных колебаний С–Н-связей ароматического ядра около 2895 см–1, сильная полоса валентных колебаний С=О-связей карбонильных групп около 1682 см–1, многочисленные полосы колебаний других групп и связей между 400 и 1650 см–1.
Особенностью упаковки молекул 2 также является формирование слоистой структуры (рис. 3). Расстояние между слоями составляет ∼3.230(2) Å, что меньше, чем в 1 и в графите. Образование слоев становится возможным благодаря плоской жесткой структуре молекул.
Рис. 3.
Структура соединения 2: а – проекция на плоскость ас, б – произвольная проекция. Пунктирные линии обозначают водородные связи.

Доминирующим фактором формирования слоев является образование сетки водородных связей. Наиболее прочные водородные связи – интрамолекулярные связи между протоном гидроксогруппы и кислородом карбонильной группы. Ее длина обусловлена геометрией молекулы 2, однако по сравнению с 1 она увеличена и составляет 1.878(2) Å. Удлинение этой связи можно объяснить участием как протона, так и карбонильного кислорода в образовании водородных связей с другими атомами. Связывание соседних молекул между собой происходит за счет формирования водородных связей между протоном этинильной группы и атомом кислорода той же карбонильной группы. В этом случае длина связи составляет 2.296(2) Å. Именно эти сравнительно короткие связи формируют цепочки молекул, а цепочки формируют слои. Кратчайший О···Н-контакт между цепочками молекул составляет 2.619(2) Å, что можно интерпретировать как слабую водородную связь.
Снятие триметилсилильной группы в 2 приводит к появлению в ИК-спектре валентных колебаний (Н–С≡С) протона при тройной связи около 3260 см–1 (рис. 4). Интересной особенностью спектра является практически полное исчезновение полосы валентных колебаний С≡С-связи, что может быть обусловлено ее малой полярностью после удаления электродонорной триметилсилильной группы. Снятие триметилсилильной группы выразилось и в резком снижении интенсивности полосы С–Н метильных групп около 3002 см–1. Полоса поглощения ОН-группы около 3142 см–1 осталась уширенной. Полоса валентных колебаний С=О-связей карбонильных групп – около 1676 см–1.
Несмотря на то что оба соединения бесцветны, при возбуждении УФ-источником с длиной волны 369 нм, они способны флуоресцировать в голубой области (рис. 5). Максимум эмиссии соединения 1 в твердом состоянии находится около 566 нм, а в растворе в хлороформе – около 500 нм.
ЗАКЛЮЧЕНИЕ
Успешно проведен синтез метил-2-гидрокси-5-[(триметилсилил)этинил]бензоата и метил-2-гидрокси-5-этинилбензоата. Отмечены особенности формирования их структур: слоистая упаковка плоских молекул и сетка водородных связей в метил-2-гидрокси-5-этинилбензоате. Образование слоев в структуре не характерно для такого родственного соединения, как их прекурсор 2-гидрокси-5-йодбензоат [9], образующий стопки молекул, связанные галогенными связями йод–кислород.
Работа выполнена при финансовой поддержке Российского научного фонда (проект № 21-73-20019). Исследование 1H ЯМР выполнено в Научном парке СПбГУ “Магнитно-резонансные методы исследования”, а дифракционные исследования – в Научном парке СПбГУ “Рентгенодифракционные методы исследования”. ИК-спектры получены в научно-образовательном центре Нанотехнологий ЮУрГУ.
Список литературы
Takalo H., Kankare J., Haenninen E. // Acta Chem. Scand. B. 1988. V. 42 (7). P. 448.
Gomez-Gualdron D.A., Gutov O.V., Krungleviciute V. et al. // Chem. Mater. 2014. V. 26. P. 5632. https://doi.org/10.1021/cm502304e
Huang N., Wang P., Jiang D. // Nat. Rev. Mater. 2016. V. 1. Article 16068. https://doi.org/10.1038/natrevmats.2016.68
Li Y.L., Zee C.-T., Lin J.B. et al. // J. Am. Chem. Soc. 2020. V. 142 (42). P. 18093. https://doi.org/10.1021/jacs.0c07657
CrysAlisPro 1.171.41.103a (Rigaku Oxford Diffraction, 2021).
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339. https://doi.org/10.1107/S0021889808042726
Sheldrick G.M. // Acta Cryst. A. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053273314026370
Sheldrick G.M. // Acta Cryst. C. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053229614024218
CCDC №1403121. Y. Wang, R.M. Strongin, F.R. Fronczek. (2015) Private Communication.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография