Мембраны и мембранные технологии, 2022, T. 12, № 4, стр. 235-244
Экспериментальное определение влияния температуры на газотранспортные характеристики полимерных газоразделительных волокон на основе полисульфона
К. А. Смородин a, А. А. Атласкин a, Д. М. Зарубин a, А. Н. Петухов a, С. С. Крючков a, А. Н. Петухова a, М. Е. Атласкина a, *, А. Н. Степакова a, А. Н. Марков a, И. В. Воротынцев a
a Российский химико-технологический университет им. Д.И. Менделеева
125047 Москва, Миусская пл., 9, Россия
* E-mail: atlaskin@muctr.ru
Поступила в редакцию 11.01.2022
После доработки 01.04.2022
Принята к публикации 08.04.2022
- EDN: IBQUSO
- DOI: 10.31857/S2218117222040095
Аннотация
Проведено исследование влияния температуры в широком диапазоне (от 258.15 до 293.15 К) на газотранспортные характеристики полимерных газоразделительных асимметричных волокон на основе полисульфона для компонентов бинарной газовой смеси CO2/N2 различного состава. В рамках работы были определены значения коэффициентов проницаемости, диффузии и растворимости чистых газов в интересующем диапазоне температур, а также значения коэффициента проницаемости компонентов бинарной газовой смеси CO2/N2 с привлечением ГХ анализа потока пермеата. В данной работе было продемонстрировано: процесс разделения проходит наиболее эффективно при комнатной температуре в случае низкого содержания диоксида углерода (до 15 мол. %) в бинарной смеси. Экспериментально было показано, что в остальном диапазоне концентраций CO2 процесс разделения смеси наиболее эффективен при пониженной температуре (273.15 К). Дальнейшее снижение температуры не делает процесс разделения смеси более эффективным во всём рассмотренном диапазоне концентраций диоксида углерода.
ВВЕДЕНИЕ
Постепенное изменение климата стало общемировой проблемой в связи с быстрым ростом концентрации CO2 в атмосфере. В связи с изменением климата [1] была разработана стратегия CCS (carbon capture and storage). Этот подход подразумевает поиск технологических решений способствующих снижению выбросов диоксида углерода [2, 3], потому что увеличение выбросов CO2 может привести к закислению океана [4, 5] повышению уровня моря дополняя глобальное потепление. Одним из направлений этой стратегии является улавливание диоксида углерода из стационарных источников, генерирующих газовые выбросы с высоким содержанием CO2 (например, дымовых газов ТЭЦ).
Существует множество технологий для улавливания CO2 из газовых смесей: химическая абсорбция, адсорбция [6, 7], и мембранная технология [8]. Улавливание CO2 из дымовых газов ТЭЦ с помощью химической абсорбции водными растворами аминоспиртов, на сегодняшней день, является общемировой практикой [9–11]. Но несмотря на распространенность подхода и высокую эффективность выделения диоксида углерода даже с низким содержанием целевого компонента [12], данный подход имеет ряд серьезных недостатков [10, 13]: высокие энергозатраты, коррозию оборудования, высокие капитальные и операционные затраты, разложение и испарение абсорбента, что в свою очередь может привести к загрязнению окружающей среды. В работах было описано, что в случае применения аминной абсорбции возможно подорожание электроэнергии производимой ТЭЦ на 50–90% поскольку абсорбционная система потребляет 30–50% электроэнергии для регенерации сорбента и извлечения СО2 [14–17].
В связи с вышесказанным, постепенно растет интерес к применению мембранных технологий [18–20] в задачах выделения CO2 из природного газа и дымовых газов ТЭЦ. Изначально не было единого мнения о преимуществах мембранных методов над традиционными методами разделения газов [21]. Но исследования указывают на то, что сегодня метод мембранного газоразделения является наиболее перспективной альтернативой традиционным методам в силу своих преимуществ [22–25]: энергоэффективность, экологичность, масштабируемость, возможность “настройки” процесса разделения путем подбора мембран и конфигураций разделительных аппаратов. Поэтому мембранное газоразделение интенсивно интегрируется в реальный сектор экономики [22, 26]. Поскольку интерес к данному методу газоразделения активно растет, исследовательские группы [27, 28] сосредоточили свои интересы в двух основных областях: разработка новых конфигураций мембранных аппаратов [29–31] и создание новых материалов для газоразделительных процессов [32–34].
Сегодня достаточно широк выбор материалов половолоконных мембран для различных задач [35–38], нередко половолоконные мембранные модули создают на основе полисульфона [39–43], также проводятся исследования в области модификации [44–48] его структуры для получения лучших газотранспортных характеристик в тех или иных задачах. Перечень задач в которых используются газоразделительные мембраны достаточно широк, и они могут сильно различаться по условиям (давление, температура), необходим подбор материалов с известными и подходящими свойствами для наиболее эффективного выделения целевого компонента. Изменение температуры процесса газоразделения [49] может привести к специфическим явлениям, таким как пластификация [50] мембраны, что может снизить эффективность выделения целевого компонента. Для решения этой задачи постоянно проводятся исследования влияния температур на газотранспортные характеристики полимерных мембран различными научными группами [50–55].
Для того, чтобы наиболее эффективно использовать полимерные газоразделительные мембраны в различных задачах, необходимо понимать их поведение в специфических условиях, например при пониженных температурах. Одной из таких технологий, где процесс мембранного газоразделения реализуется при низких температурах является мембранно-газогидратная кристаллизация [56], другим примером применения мембран в условиях низких температур является гибридный процесс на основе ректификации и мембранного газоразделения [57].
Целью настоящей работы является исследование влияния температуры в широком диапазоне (от 258.15 до 293.15 К) на газотранспортные характеристики полимерных газоразделительных волокон на основе полисульфона в процессе разделения бинарной газовой смеси с различным соотношением концентраций компонентов питающей смеси СO2/N2.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование влияния температуры на газотранспортные характеристики газоразделительных полых волокон на основе полисульфона была проведена как для индивидуальных газов, так и для бинарной газовой смеси. В настоящей работе были использованы чистые газы He (99.9999 об. %), N2 (99.9995 об. %), CO2 (99.99 об. %) приобретенные в НИИ КМ (Россия, Москва). Бинарная газовая смесь готовилась методом динамического смешения потоков, непосредственно в экспериментальной установке.
Исследование газотранспортных характеристик проводилось для коммерчески доступных газоразделительных мембран, приобретенных у Hangzhou Kelin Aier Qiyuan Equipment Co., Ltd. (Ханчжоу, Китай). Исследуемые мембраны представляют собой полые волокна с анизотропной структурой на основе полисульфона с внутренним селективным слоем толщиной 45–50 нм. Для определения толщины селективного слоя, из приобретенного мембранного модуля было извлечено 20 волокон. После были сделаны СЭМ-микрофотографии двух срезов каждого исследуемого волокна. Из полученных значений толщины было определено среднее. Микрофотографии поперечного сечения полых волокон представлены на рис. 1.
Определение газотранспортных свойств мембраны проводилось с использованием специально разработанной экспериментальной установки для определения газотранспортных характеристик полимерных мембран сопряженной с масс-спектрометром. Кроме того, было выполнено определение коэффициента проницаемости компонентов бинарных газовых смесей с различным соотношением концентраций CO2/N2.
Определение проницаемости чистых газов при различных температурных режимах
Тестирование половолоконных мембран проводились на экспериментальной установке, сопряженной с масс-спектрометром [58] при разных температурах – 293.15, 273.15 и 258.15 К. Принципиальная схема такой установки приведена на рис. 2. Газораспределительная система включает в себя 3 регулятора расхода газа (Bronkhorst FG-201CV) для подачи в установку индивидуальных газов, которые могут использоваться по отдельности или в виде газовой смеси, полученной методом динамического смешения потоков в камере смешения. Два других регулятора расхода газа (Bronkhorst F201CV и Bronkhorst F201CM) используются для подачи в систему гелия и аргона. Гелий используется для продувки газораспределительной системы между экспериментами, а аргон в качестве внутреннего стандарта для масс-спектрометра. Четырехпортовый двухпозиционный кран соединяет полость высокого давления мембранного модуля с камерой смешения или линией подачи гелия. Также, полость высокого давления модуля соединена с регулятором давления газа “до себя” (Bronkhorst P702CM) для поддержания постоянного давления газа в мембранном модуле. Полость низкого давления мембранного модуля соединена с вакуумным постом, состоящим из мембранного и турбомолекулярного вакуумных насосов (Pfeiffer Hi-Cube ECO 300), обеспечивающим разряжение в подмембранном пространстве. Определение давление в полости низкого давления осуществляется с помощью преобразователя давления (Pfeiffer MPT200), а диафрагменный клапан с электромагнитным актуатором (Pfeiffer DVC 025 PX) служит для отсечения вакуумного оборудования от газораспределительной системы в случае повреждения мембраны и резкого роста давления. Вакуумный пост далее соединяется с камерой масс-спектрометра (Pfeiffer PrismaPro QMG 250 M2), вакуум в которой обеспечивается вторым постом (Pfeiffer Hi-Cube 80 Eco), а его уровень определяется с помощью второго преобразователя давления той же модели. Важно отметить, что мембранный модуль, камера смешения, а также газовые магистрали, соединяющие эти компоненты были помещены в криостат. Охлаждение системы до температур 273.15 и 258.15 К осуществлялось путем помещения модуля в жидкость и последующее ее охлаждение холодильной машиной производства HRZ004-L1 (SMC Corporation).
Рис. 2.
Принципиальная схема установки для определения газотранспортных характеристик мембраны в сопряжении с масс-спектрометром.
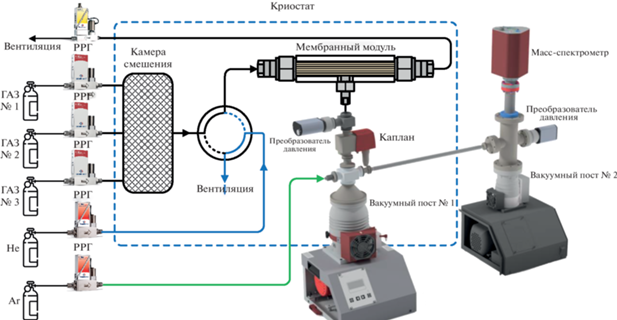
Экспериментальная процедура включает в себя следующие этапы. До начала эксперимента мембранный модуль продувается постоянным потоком гелия (50–150 см3 мин–1), в то время как в камеру смешения подаются требуемые газы (общий объемный расход составляет 200 см3 мин–1). В вакуумную часть газораспределительной системы подается аргон (4 см3 мин–1). Концентрация посторонних газов, которые требуется удалить с помощью продувки мембранного модуля гелием, определяется по масс-спектру, формирующемуся в реальном времени с задержкой обновления показаний 1 мс. После того, как примеси были удалены из системы, двухпозиционный кран переключается в положение, соединяющее камеру смешения с полостью высокого давления мембранного модуля (время переключения крана составляет 8 мс). В таком режиме работы системы осуществляется сбор показаний контрольно-измерительных приборов. Величина давления газа в полости высокого давления модуля и объемные расходы газов регистрируются с помощью программного обеспечения FlowPlot, давление в полости низкого давления модуля и камере масс-спектрометра регистрируется с помощью программного обеспечения PV TurboViewer, а запись масс-спектра осуществляется в программном обеспечении PV MassSpec. Таким образом, осуществляется сбор всех экспериментальных данных для определения коэффициентов проницаемости, диффузии и расчета коэффициента сорбции. Коэффициент проницаемости мембраны рассчитывается согласно формуле:
где Ji – объемный поток компонента i в пермеате, см3 мин–1; l – толщина мембраны, см; Δp – разница парциальных давлений газа через мембрану, см рт. ст.; A – площадь мембраны, см2.Программное обеспечение масс-спектрометра позволяет преобразовывать сигнал по каждому определяемому компоненту в величину его парциального давления. Таким образом, объемный расход пермеата можно определить по формуле:
где JAr – объемный расход аргона, см3 мин–1; pi – парциальное давление компонента i в пермеате, см рт. ст.; pAr – парциальное давление аргона в пермеате, см рт. ст.Коэффициенты диффузии для чистых газов рассчитывались по формуле:
где θ – время задержки, мс; θ0 – инструментальное время задержки, мс. Инструментальное время задержки было определено с помощью замены половолоконной мембраны на фторопластовый капилляр с отверстием, выполненным иглой от микрошприца.Коэффициент сорбции чистых газов рассчитывался по формуле:
где P – коэффициент проницаемости, D – коэффициент диффузии.Определение проницаемости компонентов газовой смеси
Газораспределительная система экспериментальной установки изготовлена из труб с внешним диаметром 1/4″, выполненных из нержавеющей стали марки S316 (Hy-Lok, Корея). В качестве контрольно-измерительных приборов были использованы: три редуктора (установлены на линии подачи чистых газов) 072S-0050C-1S-5 (Drastar LTD, Корея), один преобразователь давления PT 5000 (в полости низкого давления мембранного модуля) (A-flow, Франция), три регулятора расхода газа (на линиях подачи чистых газов) El-Flow Prestige FG-201CV и регулятор давления газа (на линии ретентата) El-Press P-702CM (Bronkhorst, Нидерланды). Эффективная площадь мембраны, доступная для газопроницаемости, составляет 1.6 см2. Аналитическое обеспечение для определения состава газовой смеси представлено газохроматографическим комплексом на базе Хромос ГХ-1000 (Хромос, Россия). Газовый хроматограф оборудован проточными детекторами по теплопроводности.
Процедура проведения эксперимента включает в себя следующие этапы. Смесь, приготавливаемая в реальном времени методом динамического смешения потоков, величина который задается с помощью регуляторов расхода газа непрерывно подается из камеры смешения в систему с постоянным потоком под давлением, поддерживаемым регулятором давления газа. Измерение давления в полости низкого давления осуществляется с помощью преобразователя давления, с точностью 0.05% от полного диапазона. Проникшие через мембрану компоненты газовой смеси удаляются из полости низкого давления потоком гелия, контролируемым регулятором расхода газа. При этом в качестве газа носителя хроматографа используется гелий из того же баллона. Величина потока ретентата регулируется комбинацией приборов: регуляторы расхода газа на входе в модуль и регулятор давления газа на линии ретентата. Перепад давления в течение всего эксперимента поддерживался равным 790 кПа. Система была термостатирована, охлаждение до температур 293.15, 273.15 и 258.15 К было реализовано путем погружения мембранного модуля в жидкость охлаждаемую холодильной машиной производства “SMC Corporation” (Япония): HRZ004-L1.
Для анализа состава потока пермеата он вводится в кран-дозатор газового хроматографа, а затем попадает в вытяжку. Разделение компонентов пробы происходит на хроматографической колонке Haysep R в изотермических условиях. Анализ пробы осуществлялся при помощи детектора по теплопроводности. Условия проведения хроматографического анализа показаны в табл. 1. Принципиальная схема прибора показана на рис. 3.
Таблица 1.
Условия проведения хроматографического анализа
| Компонент ГХ | Характеристика |
|---|---|
| Детекторы | ДТП 120°C, 111mA |
| Хроматографические колонки | Haysep R, 80/100 mesh, 4 м × 3 мм, нержавеющая сталь |
| Температура колонок | 120°C |
| Дозирующие петли | 1 см3, 120°C |
| Газ носитель | He 99.9999 об. %, 20 см3/мин |
Рис. 3.
Принципиальная схема экспериментальной установки для определения коэффициента проницаемости компонентов газовой смеси.
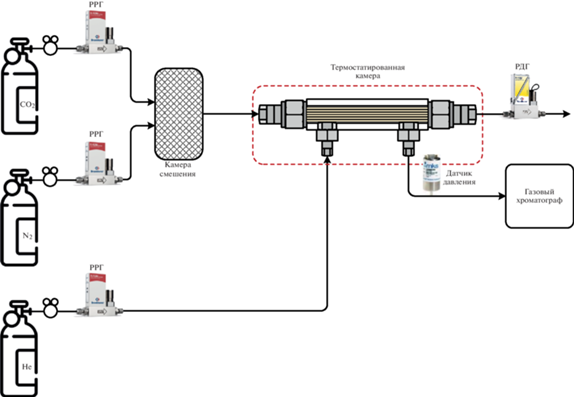
Для расчета коэффициента проницаемости была использована следующая формула (3):
где ${{P}_{A}}$ – коэффициент проницаемости компонента А, см3 см см–2 с–1 см рт. ст.–1, $x_{A}^{P}$ – доля компонента A в потоке пермеата, J – поток гелия, см3 с–1, $l$ – толщина селективного слоя мембраны, $x_{{{\text{He}}}}^{p}$ – доля гелия в потоке пермеата, $\Delta p$ – разница парциальных давлений компонента A через мембрану, см рт. ст.Селективность для пар газов CO2/N2 была рассчитана по формуле:
где PA – коэффициент проницаемости компонента А, PБ – коэффициент проницаемости компонента Б.РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В результате определения газотранспортных характеристик половолоконной мембраны из полисульфона для чистых газов (диоксид углерода и азот) в зависимости от температуры были экспериментально установлены значения коэффициентов проницаемости (P, Баррер) и диффузии (D, м2 с–1), на основании которых были рассчитаны коэффициент растворимости (S, моль Па–1 м–3) и идеальная селективность (α(CO2/N2)). Все определенные величины представлены в табл. 2.
Таблица 2.
Газотранспортные характеристики половолоконной мембраны из полисульфона, полученные при различных температурах
| Газ | P, Баррер | D × 1012, м2 с–1 | S × 103, моль Па–1 м–3 | α(CO2/N2) |
|---|---|---|---|---|
| 293.15 К | ||||
| CO2 | 8.6 | 2.2 | 1.3 | 16 |
| N2 | 0.54 | 2.1 | 0.09 | |
| 273.15 К | ||||
| CO2 | 6.4 | 1.5 | 1.4 | 17 |
| N2 | 0.38 | 1.5 | 0.09 | |
| 258.15 К | ||||
| CO2 | 5.4 | 1.2 | 1.5 | 19 |
| N2 | 0.3 | 1.1 | 0.09 | |
Из представленных результатов видно, что по мере снижения температуры наблюдается значительное уменьшение значения коэффициента проницаемости мембраны для обоих чистых газов. Таким образом, определенное при T = 293.15 K значение коэффициента проницаемости мембраны для диоксида углерода составляет 8.6 Баррер, при T = 273.15 K его величина снижается на 25.6% и составляет 6.4 Баррер, а при T = 258.15 K наблюдается снижение на 37.2% от первоначального значения и опускается до значения 5.4 Баррер. При этом, в случае изучения массопереноса азота через образец той же мембраны наблюдается аналогичная тенденция, однако уменьшение значения коэффициента проницаемости носит более резкий характер, а именно, при T = 293.15 K значение коэффициента проницаемости по азоту составляет 0.54 Баррер, при T = 273.15 K наблюдается снижение этой величины на 29.6% (0.38 Баррер), а при T = 258.15 K значение коэффициента проницаемости составляет 0.3 Баррер (снижение на 44% относительно первоначальной величины). Таким образом, наблюдается рост величины идеальной селективности мембраны с 16 до 17 при понижении температуры с 293.15 до 273.15 K и дальнейшее более значительное увеличение этого показателя до 19 при дальнейшем снижении температуры до 258.15 K. Из всего изученного температурного диапазона сравнению с литературными данными подлежат значения коэффициента проницаемости, полученные при Т = 293.15 K так как большинство работ ограничивается изучением газотранспортных характеристик при 298.15 и 308.15 К. К. Корос и Пиннау в своем исследовании [58] сообщают о том, что коэффициент проницаемости для азота составляет 0.171 Баррер при перепаде давления в 3.5 атм., а в работе Макхэтти и Короса [59] коэффициенты проницаемости по диоксиду углерода и азоту составляют 5.6 и 0.25 Баррер, соответственно. В этой работе измерения проводили при перепаде давления в 10 атмосфер и температуре 308.15 К. В работе [60] исследовались плоские симметричные мембраны. Измерения проводились при перепаде давления около 6 атмосфер и температуре 298.15 К, коэффициенты проницаемости для CO2 и N2 равны 6.07 и 0.179 Баррер соответственно. Расхождение полученных и литературных значений коэффициентов проницаемости может быть объяснено точностью определения толщины селективного слоя, используемой при расчете газотранспортных характеристик и/или неравномерностью селективного слоя. В работе [61] представлены коэффициенты проницаемости для чистого полисульфона: 4.9 и 0.2 Баррер для CO2 и N2, соответственно при перепаде давления 10 атмосфер и температуре равной 308.15 К. Исследование [62] также содержит экспериментально определенные значения газотранспортных характеристик для симметричной мембраны на основе полисульфона, полученные при перепаде давления в 2 атмосферы и температуре 303.15 К, которые равны 6.1 и 0.8 Баррер для CO2 и N2 соответственно.
Для объяснения полученной зависимости были определенны значения коэффициентов диффузии и растворимости мембраны для этих чистых газов.
Из результатов видно, что величина коэффициента диффузии снижается по мере уменьшения температуры, при этом, эта тенденция наблюдается для обоих исследуемых газов. Таким образом, для случая массопереноса диоксида углерода через полое волокно из полисульфона значения коэффициента диффузии равны 2.2 × 10–12, 1.5 × 10–12 и 1.2 × 10–12 м2 с–1 при температурах 293.15, 273.15 и 258.15 К, а уменьшение составило около 32 и 45%, соответственно. При исследовании массопереноса азота через образец такой же мембраны были получены следующие значения коэффициента диффузии: 2.1 × 10–12, 1.45 × 10–12 и 1.12 × 10–12 м2 с–1 при температурах 293.15, 273.15 и 258.15 К, а уменьшение составило порядка 31 и 47% соответственно. Во всем рассмотренном интервале температур значение коэффициентов диффузии полого волокна из полисульфона для диоксида углерода и азота близки, что обусловлено величиной кинетического диаметра молекул этих газов (3.30 и 3.64 Å). При этом, снижение величины коэффициента диффузии для обоих чистых газов так же близко, что, вероятнее всего, связано со снижением подвижности молекул газа в свободном объеме полимера. В случае сравнения полученных значений коэффициентов диффузии с литературными данными (также, как и в предыдущем случае только для Т = 293.15 К) обнаруживается довольно хорошее соответствие ранее представленным значениям: при Т = 298.15 К и перепаде давления 10 атм. для CO2 и N2 значения этого параметра составили 2 × 10–12 и 1.2 × 10–12 м2 с–1 [59]. Однако в работе [61], где исследования газотранспортных характеристик полисульфона проводилось при Т = 308.15 К и перепаде давления 10 атм., значение коэффициента диффузии для CO2 составило 1.84 × 10–12 м2 с–1.
С помощью экспериментально определенных значений коэффициентов проницаемости и диффузии были рассчитаны значения растворимости диоксида углерода и азота и изучаемом образце половолоконной мембраны из полисульфона. В отличии от коэффициента диффузии, по мере уменьшения температуры от 293.15 до 258.15 К наблюдается рост значения коэффициента растворимости. В случае диоксида углерода, величины коэффициента растворимости были равны 1.3 × × 10–3, 1.4 × 10–3 и 1.5 × 10–3 моль Па–1 м–3 при температурах 293.15, 273.15 и 258.15 К, соответственно, а рост составил около 8 и 15% соответственно. Рассчитанное значение коэффициента растворимости азота в полисульфоновой мембране, во-первых, как минимум в 14 раз ниже того же параметра, определенного для диоксида углерода, а во-вторых, во всем диапазоне температур не наблюдается изменение этого параметра. Таким образом, значение коэффициента растворимости для азота равно 9 × 10–5 моль Па–1 м–3 во всем рассмотренном диапазоне температур. Таким образом видно, что снижение коэффициента проницаемости, характерное для обоих газов, вызвано снижением значения коэффициента диффузии молекул газа в свободном объеме исследуемого полимера, при этом разная “скорость” снижения этого значения обусловлена изменением коэффициента растворимости этих газов в мембране. Как было отмечено выше, снижение коэффициента диффузии при понижении температуры приблизительно одинаково для обоих газов (32 и 45% для диоксида углерода; 31 и 47% для азота), в то время как для диоксида углерода наблюдается рост коэффициента растворимости при понижении температуры, а в случае азота практические не наблюдается изменение того же параметра.
Следующим этапом настоящего исследования было экспериментальное определение зависимости величин коэффициента проницаемости половолоконной мембраны из полисульфона для компонентов бинарной газовой смеси от концентрации диоксида углерода при различных температурах. Результаты представлены на рис. 4, 5. Рис. 6 иллюстрирует зависимость селективности этой мембраны от концентрации диоксида углерода в бинарной газовой смеси при тех же температурах. Для наглядности на рис. 4 и 5, также, представлены значения коэффициента проницаемости этой мембраны для чистых газов (закрашенные маркеры).
Рис. 4.
Зависимость коэффициента проницаемости CO2 от его концентрации в питающей смеси при различных температурах. Закрашенные маркеры – значения, полученные для чистого диоксида углерода.
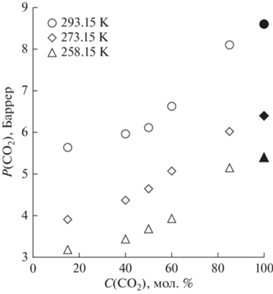
Рис. 5.
Зависимость коэффициента проницаемости N2 от концентрации CO2 в питающей смеси при различных температурах. Закрашенные маркеры – значения, полученные для чистого азота.
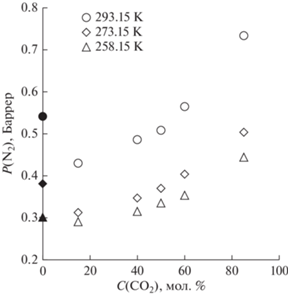
Рис. 6.
Зависимость селективности мембраны для бинарной газовой смеси CO2/N2 от концентрации CO2 в питающей смеси при разных температурных режимах.
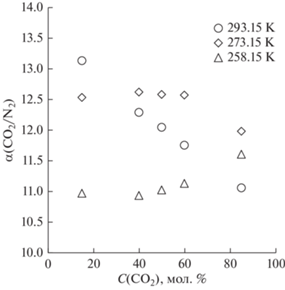
Как видно из представленных диаграмм, для обоих компонентов газовой смеси наблюдается одинаковая тенденция, выраженная в росте значения коэффициента проницаемости мембраны как для диоксида углерода, так и для азота во всем рассмотренном диапазоне концентраций CO2 в бинарной смеси. При этом, по мере снижения температуры, происходит снижение значений коэффициента проницаемости обоих компонентов, что хорошо согласуется с результатами, полученными для аналогичного исследования на чистых газах. При этом рост значения коэффициента проницаемости мембраны для диоксида углерода, наблюдаемый при увеличении его концентрации в смеси, менее значительный, чем изменение того же параметра для азота при температуре 293.15 К. В результате наблюдается снижение значения эффективной селективности мембраны во всем диапазоне концентраций CO2 в смеси. В случае проведения эксперимента при температуре равной 273.15 К, темп роста значений коэффициента проницаемости мембраны для обоих компонентов остается одинаковым в диапазоне концентраций CO2 от 15 до 60 мол. %, что обеспечивает постоянство значения эффективной селективности мембраны на уровне 12.5. При увеличении концентрации диоксида углерода до 85 мол. % наблюдается больший рост значения коэффициента проницаемости азота, чем того же параметра для диоксида углерода, что снижает значение эффективной селективности до 12. При температуре 258.15 К наблюдается противоположная тенденция. Темп роста значения коэффициента проницаемости мембраны по диоксиду углерода превышает рост того же параметра для азота, что в результате, выражается в увеличении значения эффективной селективности этой мембраны во всем рассмотренном диапазоне концентраций диоксида углерода в газовой смеси. К сожалению, сравнение определенных в настоящей работе значений газотранспортных характеристик, полученных при низких температурах, с литературными данными не представляется возможным ввиду отсутствия подобных исследований для полисульфона. В результате анализа литературных данных не было обнаружено работ, посвященных низкотемпературному массопереносу через полисульфон, и большинство работ ограничивается изучением газотранспортных характеристик при 298.15 и 308.15 К.
ЗАКЛЮЧЕНИЕ
Представленные результаты обеспечивают понимание поведения половолоконной мембраны, изготовленной из полисульфона в процессе разделении бинарной газовой смеси (CO2/N2) в широком диапазоне концентраций диоксида углерода при различных температурах (в том числе низких). Наглядно продемонстрировано преимущество проведения процесса при комнатной температуре в случае низкого содержания диоксида углерода (до 15 мол. %), также показано, что в остальном диапазоне концентраций диоксида углерода процесс целесообразно проводить при пониженной температуре (273.15 К). При этом дальнейшее понижение температуры не приводит к повышению эффективности процесса разделения такой смеси во всем рассмотренном диапазоне концентраций диоксида углерода.
Список литературы
Melillo J.M., McGuire A.D., Kicklighter D.W. // Nature. 1993. V. 363. P. 234–240.
Brovkin V., Sitch S., Von Bloh W. // Global Change Biology. 2004. V. 10. I.8. P. 1253–1266.
Song C. // Catalysis Today. 2006. V. 115. I. 1–4. P. 2–32.
Fontela M., Velo A., Gilcoto M. // Science of the Total Environment. 2021. V. 779. P. 146570
Magi M., Murai S. // Energy Procedia. 2011. V. 4. P. 4005–4011.
Petukhov A., Atlaskin A., Sergeeva M. // Taylor & Francis. 2021. P. 1–16.
Herri J.M., Bochemoua A., Kwaterski M. // Oil & Gas Science and Technology – Revue d’IFP Energies nouvelles. Technip. 2014. V. 69. № 5. P. 947–968.
Sifat N.S., Haseli Y. // Energies. 2019. V. 12. I. 21. P. 4143.
Yamada H. // Polymer J. 2021. V. 53. P. 93–102.
Rao A.B., Rubin E.S. // Environmental Science and Technology. 2002. V. 36. I. 20. P. 4467–4475.
Rochelle G.T. // Science. 2009. V. 325. I. 5948. P. 1652–1654.
Hasan M.M.F., Baliban R.C., Elia J.A. // Industrial and Engineering Chemistry Research. 2012. V. 51. I. 48. P. 15 665–15 682.
Zhang X, Sighn B., He X. // International J. Greenhouse Gas Control. 2014. V. 27. P. 289–298.
Stuart Haszeldine R. // Science. 2009. V. 325. P. 1647–1652.
Fout T., Zoelle A., Keairns D. // Taylor & Francis, National Energy Technology Laboratory (NETL). 2015. P. 1281–1288.
Figueroa J.D., Fout T., Plasynski S. // International J. Greenhouse Gas Control. 2008. V. 2. I. 1. P. 9–20.
Rubin E.S., Davison J.E., Herzog H.J. // International J. Greenhouse Gas Control. 2015. V. 40. P. 378–400.
Alent’ev A.Y., Volkov A.V., Vorotyntsev I.V. // Membranes and Membrane Technologies. Pleiades J. 2021. V. 3. № 5. P. 255–273.
Novitskii E.G., Bazhenov S.D., Volkov A. // Petroleum Chemistry. 2021. V. 61. № 4. P. 407–423.
Atlaskin A.A., Trubyanov M.M., Yanbikov N.R. // J. Membrane Science. 2019. V. 572. P. 92–101.
Khalilpour R., Mumford K., Zhai H. // J. Cleaner Production. 2015. V. 103. P. 286–300.
Sanders D.F., Smith Z.P., Guo R. // Polymer. 2013. V. 54. I. 18. P. 4729–4761.
Skorek-Osikowska A., Kotowicz J., Janusz-Szymańska K. // Energy and Fuels. 2012. V. 26. I. 11. P. 6509–6517.
Belaissaoui B., Favre E. // Oil and Gas Science and Technology. 2014. V. 69. I. 6. P. 1005–1020.
Merkel T.C., Lin H., Wei X., Baker R. // J. Membrane Science. 2010. V. 359. I. 1–2. P. 126–129.
Apel P.Y., Bobreshova O.V., Volkov A.V. // Membranes and Membrane Technologies. 2019. V. 1. I. 2. P. 45–63.
Leamon G., Allinson G., Wiley D.E. // Greenhouse Gas Control Technologies. 2005. V. 45. I. 8. P. 2546–2552.
Wang L., Corriou J.P., Castel C. // J. Membrane Science. 2011. V. 383. I. 1–2. P. 170–188.
Dai Z., Noble R.D., Gin D.L. // J. Membrane Science. 2016. V. 497. P. 1–20.
He X., Hägg M.B. // Membranes. 2012. V. I. 4. P. 706–726.
Hussain A., Farrukh S., Minhas F.T. // Energy and Fuels. 2015. V. 29. I. 10. P. 6664–6669.
Venna S.R., Carreon M.A. // Chemical Engineering Science. 2015. V. 124. P. 3–19.
Vinh-Thang H., Kaliaguine S. // Chemical Reviews. 2013. V. 113. I. 7. P. 4980–5028.
Brinkmann T., Lillepärg J., Notzke H. // Engineering. 2017. V. 3 I. 4. P. 485–493.
Esposito E., Clarizia G., Bernardo P. // Chemical Engineering and Processing: Process Intensification. 2015. V. 94. P. 53–61.
Li L., Ma G., Pan Z. // Membranes. 2020. V. 10. № 12. P. 1–20.
Chen X.Y., Kaliaguine S., Rodrigue D. Polymer hollow fiber membranes for gas separation: A comparison between three commercial resins // AIP Conference Proceedings. 2019.
Chen H.Z., Thong Z. Li P. // International J. Hydrogen Energy. 2014. V. 39. I. 10. P. 5043–5053.
Anokhina T., Raeva A., Makaev S. // Membranes. Multidisciplinary Digital Publishing Institute, 2021. V. 11. I. 6. P. 396.
Min K.J., Lee W. G., Kang S.W. // Macromolecular Research. 2017. V. 25. I. 4. P. 352–356.
Lim J.H., Lee C.S., Kim H.E. // Membrane J. 2015. V. 25. I. 3. P. 99–106.
Ismail A.F., Shilton S.J. // J. Membrane Science. 1998. V. 139. I. 2. P. 285–286.
Bernardo P., Tasselli F., Clarizia G. // Chemical Engineering Transactions. 2019. V. 74. № April 2018. P. 775–780.
Zahri K., Wong K.C., Goh P.S. // RSC Advances. 2016. V. 6. № 92. P. 89130–89139.
Liu L., Chakma A., Feng X. // Chemical Engineering J. 2004. V. 105. I. 1–2. P. 43–51.
Jiang L. // J. Nanomaterials. 2021. P. 1–10.
Chong K.C., Lai S.O., Lau J.W. // Aerosol and Air Quality Research. 2017. V. 17. I. 11. P. 2735–2742.
Bhardwaj V., Macintosh A., Sharpe I.D. // Annals of the N.Y. Academy of Sciences. 2003. V. 984. I. 1. P. 318–328.
Acharya N.K., Yadav P.K., Vijay Y.K. // Indian J. Pure and Applied Physics. 2004. V. 42. P. 179–181.
Duthie X., Kentish S., Powell C. // J. Membrane Science. 2007. V. 294. I. 1–2. P. 40–49.
Ahmad F., Lau K.K., Shariff A.M. // J. Membrane Science. 2013. V. 430. P. 44–55.
Stevens K.A., Moon J.D., Borjigin H. // J. Membrane Science. 2020. V. 593. P. 117427.
Nedeljkovic D. // Polymers. 2021. V. 13. I. 13. P. 2053.
Lasseuguette E., Malpass-Evans R., Carta MAriolino // Membranes. 2018. V. 8 I. 4. P. 13255.
Zhmakin V.V., Teplyakov V.V. // Petroleum Chemistry 2016 56:4. Springer, 2016. V. 56. № 4. P. 335–343.
Sergeeva M.S., Mokhnachev N.A., Shablykin D.N. // J. Natural Gas Science and Engineering. 2021. V. 86. № 103 740.
Trubyanov M.M., Shablykin D.N., Mokhnachev N.A. // Separation and Purification Technology. 2020. V. 241. № 116 678.
Fraga S., Monteleone M., Lanč M. // J. Membrane Science. 2018. V. 561. P. 39–58.
Pinnau I., Koros W.J. // J. Applied Polymer Science. 1991. V. 43. I. 8. P. 1491–1502.
McHattie J.S., Koros W.J., Paul D.R. // Polymer. 1991. V. 32. I. 5. P. 840–850.
Rezac M.E., Le Roux J.D., Chen H. // J. Membrane Science. 1994. V. 90. I. 3. P. 213–229.
Barbari T.A., Koros W.J., Paul D.R. // J. Membrane Science. 1989. V. 42. P. 69–86.
Orme C.J., Stone M.L., Benson M.T. // Separation Science and Technology. 2003. V. 38. I. 12–13. P. 3225–3238.
Дополнительные материалы отсутствуют.
Инструменты
Мембраны и мембранные технологии



