Российские нанотехнологии, 2021, T. 16, № 2, стр. 208-214
ЭФФЕКТИВНЫЕ ГИДРИДООБРАЗУЮЩИЕ МАТЕРИАЛЫ НА ОСНОВЕ LANI5 ДЛЯ СИСТЕМ АККУМУЛИРОВАНИЯ ЭНЕРГИИ
А. Н. Казаков 1, *, В. И. Борзенко 1, Д. О. Дуников 1, 2, И. А. Романов 1, Д. В. Блинов 1, 2
1 Объединенный институт высоких температур РАН
Москва, Россия
2 Национальный исследовательский университет МЭИ
Москва, Россия
* E-mail: h2lab@mail.ru
Поступила в редакцию 10.06.2020
После доработки 21.09.2020
Принята к публикации 21.09.2020
Аннотация
Переход от традиционных энергоносителей к возобновляемым, энерго- и ресурсосберегающим технологиям производства энергии поднимает ряд задач, среди которых одними из ключевых являются разработка и создание эффективных систем аккумулирования энергии. Одним из наиболее перспективных промежуточных энергоносителей является водород за счет высокой удельной теплоты сгорания и экологичности, однако существуют трудности в хранении. Гидридообразующие материалы (LaNi5, TiFe, TiCr2, Mg2Ni и другие) обладают рядом преимуществ в качестве материалов для хранения водорода: высокая объемная плотность хранения, безопасность благодаря образованию гидридной твердой фазы, селективность поглощения водрода и др. Представлены результаты экспериментальных исследований новых гидридообразующих материалов на основе LaNi5 и систем аккумулирования энергии на их основе.
ВВЕДЕНИЕ
В последние годы наблюдается устойчивый рост установленной мощности возобновляемых источников энергии (ВИЭ). В 2019 г. установленная мощность ВИЭ выросла более чем на 200 ГВт. Ввод мощностей солнечной энергетики увеличился на 12% в 2019 г. до рекордных 115 ГВт. В ветроэнергетическом секторе рост мощностей составил 19% до 650 ГВт по всему миру [1]. Сокращение потребления традиционных углеводородных энергоносителей, разработка и внедрение энергосберегающих технологий, увеличение производства электроэнергии на основе ВИЭ способствуют улучшению экологической ситуации в мире, рациональному использованию энергетических ресурсов и децентрализации энергоснабжения.
Неравномерный характер режимов работы ветровых и солнечных энергоустановок требует создания систем аккумулирования энергии, которые будут удовлетворять нуждам потребителей в соответствии с необходимым графиком нагрузки. Одним из перспективных путей решения этой задачи является использование водородных систем аккумулирования [2–5], преимущество которых заключается в возможности длительного хранения энергии без потерь, что недостижимо для химических источников тока, а также в высокой плотности хранения энергии и малых капитальных затратах по сравнению с гидро- и пневмоаккумулирующими системами. Водород производится электролизом воды за счет электроэнергии от ВИЭ, аккумулируется в системе хранения и используется для производства электроэнергии по необходимому потребителю графику в низкотемпературных топливных элементах или других энергоустановках (например, дизель-генераторах) [2, 6]. Еще одним перспективным направлением является производство водорода биологическими методами из доступного сырья местных ресурсов биомассы [7–9].
Среди разрабатываемых новых технологий очистки и хранения водорода для автономной энергетики экономически приемлемыми и безопасными могут стать устройства и системы, основанные на использовании обратимых металлогидридов (МГ) – интерметаллических соединений (ИМС), способных избирательно и обратимо поглощать водород [10, 11]. Избирательность поглощения водорода, возможность гибко контролировать термодинамические свойства интерметаллических сплавов с помощью вариации их состава позволяют использовать их не только для хранения, но и для высокоэффективной очистки водорода, создания термохимических тепловых насосов и водородных компрессоров.
Хранение водорода МГ основано на способности металлов и ИМС обратимо поглощать и хранить атомарный водород в межатомных пустотах кристаллической решетки. Реакцию водорода с металлом или ИМС можно схематически представить в виде уравнения
(1)
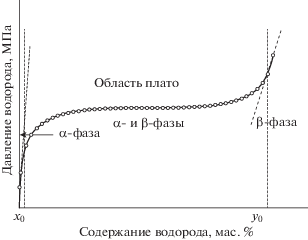
$M + {\text{\;}}\frac{x}{2}{{{\text{H}}}_{2}}{\text{\;}} \leftrightarrow M{{{\text{H}}}_{x}} + {\text{\;}}\Delta {\text{H,}}$Типичную изотерму реакции металла с водородом можно разделить на три области по мере роста давления водорода [12]: растворение водорода в металле (α-фаза); сосуществование насыщенного раствора водорода в металле и гидрида (α+β фазы); растворение водорода в гидриде (β-фаза) (рис. 1). В двухфазной области существует “плато” изотермы, где давление меняется незначительно, и в первом приближении можно считать, что поглощение или выделение водорода происходит при постоянных температуре и давлении. Это свойство удобно для практического применения в устройствах хранения водорода. Если давление на входе в МГ-реактор выше равновесного давления, соответствующего температуре водородпоглощающего материала, то водород будет абсорбироваться с выделением тепла, если ниже, то будет десорбироваться с поглощением тепла.
Обратимые гидриды ИМС являются перспективными материалами для аккумулирования водорода особенно в стационарных применениях в интеграции с топливными элементами, которые можно представить общей формулой AmBnHx, где A – металл, образующий стабильный бинарный гидрид (La, Ce, Mm, Ti, Zr, V, Mg), а металл B в обычных условиях с водородом не взаимодействует (обычно переходный металл, например Fe, Co, Ni, V, Mn, Cr и т.д.). В зависимости от стехиометрического соотношения металла А к металлу В выделяют несколько основных типов ИМС: AB5, AB2, AB3–3.5, AB, A2B, а также твердые растворы внедрения на основе Ti и V.
Наиболее перспективными ИМС являются сплавы АВ5-типа благодаря ряду преимуществ: возможность варьирования рабочих характеристик в умеренных условиях при температурах 273–373 К и давлениях 0–1.0 МПа за счет изменения состава, легкость активации, устойчивость к небольшим количествам примесей водяного пара и кислорода в водороде, легкость восстановления свойств после отравления поверхности газами CO, H2S [13].
Использование МГ-систем в хранении водорода, получаемого из ВИЭ (солнечная, ветровая и биоэнергетика), делает необходимыми разработку и исследование новых гидридобразующих ИМС с требуемыми равновесными давлениями, циклической стабильностью и устойчивостью к газовым примесям.
В настоящей работе представлены результаты экспериментальных исследований новых гидридообразующих ИМС АВ5-типа для систем очистки и хранения водорода и их использования в разработанных в ОИВТ РАН демонстрационных установках.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Серия лабораторных образцов АВ5-типа на основе LaNi5 с частичным замещением La на Ce, Ni на Fe, Mn, Al, Sn и другие металлы была приготовлена плавлением исходных стехиометрических навесок чистых металлов в электродуговой печи в аргоновой атмосфере. Для достижения гомогенности состава каждый образец переплавляли не менее 3 раз. Чистота исходных металлов составляла не менее 99.5%.
Фазовый состав и параметры кристаллической решетки приготовленных ИМС определяли с помощью рентгенофазового анализа с использованием дифрактометра D8 Advance (Bruker) с CuKα-излучением. Обработку дифрактограмм проводили в программных средах Jana2006 и Crystal Impact Match с использованием дифракционных баз данных JCPDS PDF-2.
Водородсорбционные свойства сплавов исследовали с помощью газовой PCT (давление–концентрация–температура) установки типа Сивертса [14]. Корольки сплавов загружали в термостатируемый реактор. Перед началом измерений все образцы были активированы в вакууме при 300°C в течение 60 мин. Затем выполнили активацию – три цикла полной абсорбции–десорбции, после которых проводили измерения. Сорбцию и десорбцию водорода проводили в интервале температур 295–333 К и давлений 0.001–5 МПа.
Исследования перспективных композиций ИМС для учебно-демонстрационной установки “H2Biopower” и систем хранения водорода проводили на комплексном стенде 12-04 ОИВТ РАН.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
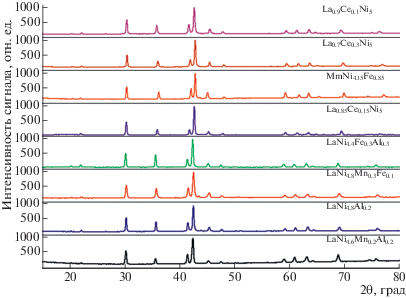
Структурные и водородсорбционные свойства ИМС АВ5-типа. Рентгенофазовый анализ показал высокую гомогенность всех исследуемых образцов (рис. 2). Полученные спектры хорошо описываются теоретически рассчитанными. Положения линий совпадают с расчетными и отсутствуют пики (интенсивность которых превышала бы интенсивность фона), принадлежащие другим фазам. Рентгенограммы подтверждают, что структуры полученных соединений принадлежат структурному типу CaCu5.
РСТ-изотермы десорбции водорода при комнатной температуре представлены на рис. 3. Частичное замещение Ni на Al, Mn, Fe значительно снижает равновесное давление водорода по сравнению с исходным LaNi5. Большие атомы Al, Mn, Fe относительно атомов Ni увеличивают параметры кристаллической элементарной ячейки, что приводит к увеличению межатомных пустот в кристаллической структуре. Наибольшая обратимая емкость 1.2 мас. % Н2 измерена для LaNi4.8Al0.2, но давление равновесия водорода слишком высокое для использования при очистке водорода, получаемого биологическим путем. Сплавы LaNi4.8Fe0.3Mn0.1 и LaNi4.4Fe0.3Al0.3 демонстрируют необходимые свойства в условиях окружающей среды.
Рис. 3.
РСТ-изотермы десорбции водорода ИМС АВ5-типа при 295 К: низкие (а) и высокие (б) равновесные давления.
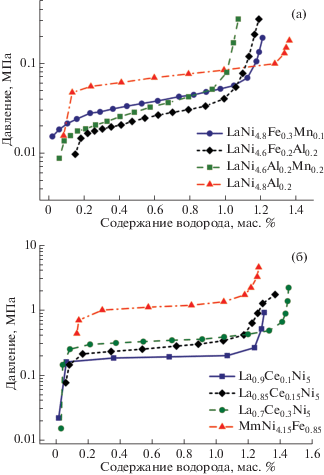
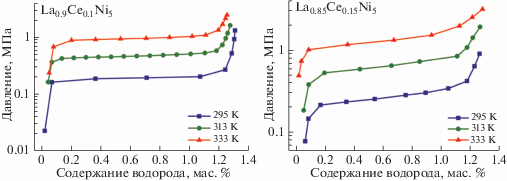
С другой стороны, частичное замещение La на Ce или использование смеси редкоземельных металлов (мишметалл Mm) увеличивает равновесное давление водорода. Этот эффект появляется из-за уменьшения объема кристаллической ячейки для Се-замещенных сплавов. Особое поведение сплавов, замещенных Се, связывают с промежуточным валентным состоянием Се (Се3+, Се4+) [15]. Сплавы La0.9Ce0.1Ni5 и La0.85Ce0.15Ni5 обладают подходящими равновесными давлениями и емкостями по водороду для использования в системах длительного хранения водорода, получаемого путем электролиза с использованием энергии ВИЭ.
Водородсорбционные и термодинамические свойства исследованных образцов приведены в табл. 1. Образцы ИМС с низкими равновесными давлениями обладают высокой стабильностью гидридов, что увеличивает циклическую стабильность при их использовании в системах очистки водорода. Для образцов с высокими равновесными давлениями характерны более высокие обратимые емкости по водороду, что позволит оптимизировать массогабаритные характеристики систем хранения водорода.
Таблица 1.
Водородсорбционные и термодинамические свойства сплавов АВ5-типа
| Состав ИМС | Pдес 295 К, МПа | Cобр 295, мас. % Н2 | ΔHдес, кДж/моль | ΔSдес, Дж/(моль К) |
|---|---|---|---|---|
| Сплавы с низким равновесным давлением | ||||
| LaNi4.8Fe0.3Mn0.1 | 0.049 | 1.0 | –36.8 | 119.7 |
| LaNi4.6Al0.2Mn0.2 | 0.033 | 0.9 | –35.0 | 107.2 |
| LaNi4.8Al0.2 | 0.074 | 1.2 | –35.5 | 116.9 |
| LaNi4.4Fe0.3Al0.3 | 0.024 | 1.1 | –36.1 | 110.4 |
| Сплавы с высоким равновесным давлением | ||||
| La0.9Ce0.1Ni5 | 0.19 | 1.1 | –31.2 | 112.1 |
| La0.85Ce0.15Ni5 | 0.27 | 1.15 | –33.2 | 121.6 |
| La0.7Ce0.3Ni5 | 0.36 | 1.3 | –33.1 | 123.0 |
| La0.36Ce0.64Ni4.15Fe0.85 | 1.18 | 1.1 | –28.3 | 115.8 |
В активированном состоянии МГ-сплавы превращаются в мелкодисперсный порошок. Типичное распределение частиц по размерам и изображение активированного порошка, полученное с помощью сканирующего электронного микроскопа (СЭМ), представлены на рис. 4. Характерный размер частиц 10–30 мкм, что снижает эффективную теплопроводность МГ-засыпок и тем самым ухудшает тепломассоперенос в объеме реакторов хранения [16]. Интенсификацию тепломассопереноса достигали добавлением охлаждающих контуров [17–19], пеноматериалов с высокой теплопроводностью [20–22], созданием композитных компактов с углеродными материалами [23–25]. Разработка оптимальных конструкций МГ-реакторов для практического применения является очень сложной из-за широкого выбора материалов, различной геометрии реактора, площади поверхности теплообмена и степени интенсификации теплопереноса. Все указанные выше параметры должны быть оптимизированы в соответствии требованиями для МГ-системы, включая общую массу системы и рабочие условия.
Рис. 4.
Распределение частиц по размерам и СЭМ-изображение активированного металлогидридного порошка.

Разработка металлогидридных систем очистки и хранения водорода. Разделение и очистка водорода с использованием МГ основаны на их способности к высокоселективному поглощению водорода из различных газовых смесей. МГ-технология разделения водорода может быть перспективным решением для малых энергоустановок на основе водорода, получаемого биологическим путем. Малые потоки газов, низкие давление и содержание водорода делают неприменимыми методы короткоцикловой адсорбции [26, 27], криогенной дистилляции, мембранных технологий [28–33]. Тогда как МГ-технологии позволяют извлекать водород из различных газовых смесей (аммиачные смеси, риформинговый газ, биогаз) с высокой эффективностью [17, 34–37].
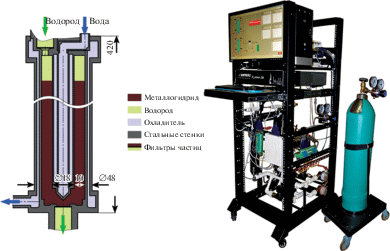
Для разделения и очистки водорода была разработана конструкция проточного МГ-реактора с двумя теплообменными контурами, которая показала свою эффективность [38]. Сплавы LaNi4.8Fe0.3Mn0.1 и LaNi4.4Fe0.3Al0.3 были отобраны для дальнейших исследований по очистке водорода из различных водородных смесей в реакторах проточного типа РХО-8 с номинальной емкостью 110 нл Н2, которые вмонтированы в демонстрационную энергоустановку “H2Biopower” (рис. 5). При разделении газовой смеси водород–диоксид углерода (40: 60%) моделирующего состава биоводорода эффективность извлечения водорода сплавом LaNi4.8Fe0.3Mn0.1 достигает свыше 80% при использовании практически всего полезного объема реактора при входном расходе газовой смеси 5 нл/мин (рис. 6). Эффективность разделения водород-метановых газовых смесей с объемной долей водорода не более 10% сплавом LaNi4.4Fe0.3Al0.3 достигает 70% при использовании 90% полезного объема реактора. Более высокие значения коэффициента извлечения водорода и использования полезного объема реактора для сплава LaNi4.4Fe0.3Al0.3 достигнуты за счет оптимизации состава и увеличения проницаемости МГ-засыпки в реакторе.
Системы долговременного хранения водорода РХ-1 (рис. 7) номинальными объемом 10 с использованием сплавов La0.9Ce0.1Ni5 и La0.85Ce0.15Ni5 отличаются эффективностью и безопасностью (рис. 8). Водородпоглощающие материалы могут обеспечить выходное давление водорода 0.15–0.2 МПа при комнатных условиях, достаточное для работы топливных элементов с твердополимерными мембранами. Данные системы могут быть перспективны в качестве резервных источников энергии. Повышение выходного давления до 0.9–1.1 МПа достигается использованием в качестве теплоносителя горячей воды.
ВЫВОДЫ
Системы хранения водорода на основе обратимых металлогидридных материалов демонстрируют свою перспективность для интеграции с быстро растущими технологиями производства возобновляемой энергии. Интерметаллические соединения АВ5-типа обладают такими преимуществами, как легкая активация, стойкость к примесным газам, высокая объемная плотность водорода в твердофазном состоянии и разнообразие составов для удовлетворения требований для практического применения в различных областях.
Структурные, водородсорбционные и термодинамические свойства новых интерметаллическихсоединений на основе LaNi5, замещенного Ce, Al, Mn, Fe, исследованы для определения перспективных композиций. Обратимые водородные емкости достигают 1.1–1.3 мас. %, а равновесные давления водорода находятся в широком диапазоне от 0.02 до 1.18 МПа для исследуемых сплавов. Ряд сплавов LaNi4.8Fe0.3Mn0.1, LaNi4.4Fe0.3Al0.3, La0.9Ce0.1Ni5 и La0.85Ce0.15Ni5 масштабирован для применения в пилотных энергоустановках и системах хранения водорода с общей загрузкой водородпоглощающего материала от 1 до 80 кг.
Эффективность очистки водорода сплавами низкого давления в проточном реакторе РХО-8 достигает 70–80% для различных водородсодержащих газовых смесей.
Сплавы высокого давления La0.9Ce0.1Ni5 и La0.85Ce0.15Ni5, применяемые в системах хранения РХ-1, при нормальных условиях могут обеспечить долговременное хранение водорода в безопасном твердофазном состоянии до 10 нм3 Н2.
Список литературы
REN21, RENEWABLES 2020 Global Status Report. Paris. 2020.
Zoulias E.I., Lymberopoulos N. // Hydrogen-based autonomous power systems: techno-economic analysis of the integration of hydrogen in autonomous power systems. Springer, 2008.
Hydrogen and Fuel Cells: Fundamentals, Technologies and Applications. Weinheim, Germany: WILEY-VCH Verlag GmbH. 2010. 877.
Малышенко С.П. // Российский химический журнал. 2005. Т. XLI. С. 112.
да Роза А. Возобновляемые источники энергии. Физико-технические основы: учебное пособие. М.: Издательский дом МЭИ, 2010. 704 с.
Tzamalis G., Zoulias E.I, Stamatakis E. et al. // Renewable Energy. 2011. V. 36 (1). P. 118. https://doi.org/10.1016/j.renene.2010.06.006
Kim D.-H., Kim S.-H., Kim K.-Y., Shin H.-S. // Int. J. Hydrogen Energy. 2010. V. 35 (4). P. 1590. https://doi.org/10.1016/j.ijhydene.2009.12.041
La Licata B., Sagnelli F., Boulanger A. et al. // Int. J. Hydrogen Energy. 2011. V. 36 (13). P. 7861. https://doi.org/10.1016/j.ijhydene.2011.01.096
Morra S., Arizzi M., Allegra P. et al. // Int. J. Hydrogen Energy. 2014. V. 39 (17). P. 9018. https://doi.org/10.1016/j.ijhydene.2014.04.009
Малышенко С.П., Назарова О.В. // Аккумулирование водорода. Атомно-водородная энергетика и технология. 1988. Вып. 8. С. 155.
Verbetsky V.N., Malyshenko S.P., Mitrokhin S.V. et al. // Int. J. Hydrogen Energy. 1998. V. 23 (12). P. 1165. https://doi.org/10.1016/s0360-3199(98)00006-8
Колачев Б.А., Шалин Р.Е., Ильин А.А. Сплавы-накопители водорода. М.: Металлургия, 1995. 384 с.
Sandrock G. // J. Alloys Compd. 1999. V. 293–295. P. 877. https://doi.org/10.1016/s0925-8388(99)00384-9
Malyshenko S.P., Mitrokhin S.V., Romanov I.A. // J. Alloys Compd. 2015. V. 645. Suppl. 1. P. S84. https://doi.org/10.1016/j.jallcom.2014.12.273
Senoh H., Takeichi N., Takeshita H.T. et al. // Mater. Sci. Eng. B. 2004. V. 108 (1–2). P. 96. https://doi.org/10.1016/j.mseb.2003.10.055
Borzenko V., Dunikov D., Malyshenko S. // High Temp. 2011. V. 49 (2). P. 249. https://doi.org/10.1134/s0018151x11010019
Dunikov D., Borzenko V., Blinov D. et al. // Int. J. Hydrogen Energy. 2016. V. 41 (46). P. 21787. https://doi.org/10.1016/j.ijhydene.2016.08.190
Malyshenko S.P., Borzenko V.I., Dunikov D.O., Nazarova O.V. // Therm. Eng. 2012. V. 59 (6). P. 468. https://doi.org/10.1134/S0040601512060055
Dunikov D., Borzenko V., Malyshenko S. // Int. J. Hydrogen Energy. 2012. V. 37. P. 13843. https://doi.org/10.1016/j.ijhydene.2012.04.078
Supper W., Groll M., Mayer U. // J. Less-Common Met. 1984. V. 104 (2). P. 279. https://doi.org/10.1016/0022-5088(84)90412-0
Groll M. // Heat Recovery Systems CHP. 1993. V. 13 (4). P. 341. https://doi.org/10.1016/0890-4332(93)90059-5
Isselhorst A., Groll M. // J. Alloys Compd. 1995. V. 231 (1–2). P. 888. https://doi.org/10.1016/0925-8388(95)01777-1
Ron M., Gruen D., Mendelsohn M., Sheet I. // J. Less-Common Met. 1980. V. 74 (2). P. 445. https://doi.org/10.1016/0022-5088(80)90183-6
Klein H.-P., Groll M. // Int. J. Hydrogen Energy. 2004. V. 29 (14). P. 1503. https://doi.org/10.1016/j.ijhydene.2004.01.017
Rodríguez Sánchez A., Klein H.-P., Groll M. // Int. J. Hydrogen Energy. 2003. V. 28 (5). P. 515. https://doi.org/10.1016/S0360-3199(02)00057-5
Zhu X., Shi Y., Li S., Cai N. // Int. J. Hydrogen Energy. 2018. V. 43 (29). P. 13305. https://doi.org/10.1016/j.ijhydene.2018.05.030
Delgado J.A., Águeda V.I., Uguina M.A. et al. // Chem. Eng. J. 2017. V. 326. P. 117. https://doi.org/10.1016/j.cej.2017.05.144
Mohamad I.N., Rohani R., Mastar M.S. et al. // Int. J. Hydrogen Energy. 2016. V. 41 (7). P. 4474. https://doi.org/10.1016/j.ijhydene.2015.08.002
Bernardo P., Jansen J.C. // Compendium of Hydrogen Energy. Oxford: Woodhead Publishing, 2015. P. 419. https://doi.org/10.1016/B978-1-78242-361-4.00014-5
Bakonyi P., Nemestóthy N., Bélafi-Bakó K. // Int. J. Hydrogen Energy. 2013. V. 38 (23). P. 9673. https://doi.org/10.1016/j.ijhydene.2013.05.158
Koroglu E.O., Ozdemir O.K., Ozkaya B., Demir A. // Int. J. Hydrogen Energy. 2019. V. 44 (32). P. 17297. https://doi.org/10.1016/j.ijhydene.2019.01.291
Chesnokov V.V., Chichkan A.S., Parmon V.N. // Nanotechnologies in Russia. 2017. V. 12 (3). P. 165. https://doi.org/10.1134/S1995078017020057
Volkov V.V., McHedlishvili B.V., Roldugin V.I. et al. // Nanotechnologies in Russia. 2008. V. 3 (11). P. 656. https://doi.org/10.1134/S1995078008110025
Au M., Chen C., Ye Z. et al. // Int. J. Hydrogen Energy. 1996. V. 21 (1). P. 33. https://doi.org/10.1016/0360-3199(95)00044-e
Miura S., Fujisawa A., Tomekawa S. et al. // J. Alloys Compd. 2013. V. 580. Suppl. 1(0). P. S414. https://doi.org/10.1016/j.jallcom.2013.03.154
Miura S. // 19th World Hydrogen Energy Conference 2012.
Dunikov D., Blinov D. // Int. J. Hydrogen Energy. 2020. V. 45 (16). P. 9914. https://doi.org/10.1016/j.ijhydene.2020.01.201
Blinov D.V., Borzenko V.I., Dunikov D.O., Kazakov A.N. // J. Phys. Conf. Ser. 2018. V. 1128. P. 012120 https://doi.org/10.1088/1742-6596/1128/1/012120
Дополнительные материалы отсутствуют.
Инструменты
Российские нанотехнологии