Нефтехимия, 2019, T. 59, № 2, стр. 222-226
Синтез и свойства новых неионогенных поверхностно-активных веществ на основе эпихлоргидрина, нафтеновых спиртов и ортофосфорной кислоты
Р. Н. Будагова 1, *, С. Б. Зейналов 1, Г. Х. Ходжаев 2
1 Институт катализа и неорганической химии им. академика М. Нагиева, НАН Азербайджана
Баку, Азербайджан
2 Азербайджанский государственный университет нефти и промышленности
Баку, Азербайджан
* E-mail: rahila.budaqova@mail.ru
Поступила в редакцию 31.05.2017
После доработки 15.10.2018
Принята к публикации 13.09.2018
Аннотация
Выбран оптимальный режим процесса хлороксипропилирования нафтеновых спиртов. Методами ГЖХ, ЯМР1Н и ИК-спектроскопии структура и состав синтезированных олигомеров с различной средней степенью хлороксипропилирования и продуктов их модификации с помощью Н3РО4 установлены. Синтезированные соединения были испытаны как поверхностно-активные вещества. Определены физико-химические показатели и исследована поверхностная активность. Выявлена способность этих продуктов замедлять испарение бензина при хранении.
Соединения, проявляющие высокую поверхностную активность (ПАВ), находят широкое применение в промышленности, в том числе нефтеперерабатывающей и нефтедобывающей, проявляют дифильные свойства, входят в состав нефтесобирающих и диспергирующих реагентов. Наибольшее распространение получили водорастворимые ПАВ, которые делятся на неионогенные (НПАВ) и ионогенные. Растворимость НПАВ в воде связана с наличием в молекуле полярной оксиалкильной цепи. Для проявления высоких поверхностно-активных свойств, гидрофильная оксиалкиленовая цепь должна быть сбалансирована длинной алкильной группой. Меняя гидрофобную часть в молекуле олигомеров, можно получать ПАВ с различными свойствами, поскольку от соотношения баланса между гидрофильной и гидрофобной группами зависят поверхностная активность и растворимость ПАВ.
Наиболее эффективными среди используемых ПАВ являются такие неионогенные ПАВ, как эфиры полиэтиленгликолей, получаемые взаимодействием этиленоксида с протонодонорными органическими соединениями: алкилфенолами, алифатическими спиртами, карбоновыми кислотами и аминами [1–5].
Изучено оксипропилирование нафтеновых спиртов, полученных из бутилнафтенатов [6]. Реакцию проводили при температуре 145–180°С и мольном соотношении спирт : пропиленоксид = 1 : 4. Полученные соединения обладают смачивающей способностью, высокими индексом вязкости и температурой вспышки, низкой температурой застывания.
Исследованы свойства продуктов взаимодействия низкомолекулярных нафтеновых спиртов: циклопентанола, циклогексанола и циклогексилкарбинола с пропиленоксидом [7]. При мольном соотношении исходных реагентов, равном 1 : 4, 1 : 6 и температуре 130–140°С в присутствии едкого натрия получены эфиры с различной степенью оксипропилирования, обладающие качествами синтетических масел.
Ранее нами была также исследована кинетика, механизм и закономерности распределения состава продуктов реакции взаимодействия этиленоксида и пропиленоксида с нафтеновыми спиртами [8–10]. Реакцией взаимодействия эпихлоргидрина (ЭХГ) с нафтеновыми спиртами были получены моно- и дихлороксипроизводные нафтеновых спиртов с дальнейшим их дегидрохлорированием до эпоксиэфиров [11].
Продолжая исследования в этом направлении, нами была проведена реакция хлороксипропилирования нафтеновых спиртов, содержащих как гидрофобные (алициклический радикал), так и гидрофильные (гидроксильная группа) фрагменты, и являющихся удобными исходными объектами для получения на их основе реагентов, проявляющих высокие нефтесобирающие и диспергирующие свойства.
В качестве исходных реагентов для получения неионогенных ПАВ использовали эпихлоргидрин и нафтеновые спирты: транс-циклогександиол-1.2, циклогексанол и метилциклогексанол.
Представляется, что наличие в структуре ЭХГ двух реакционноспособных групп – эпоксидной и СН2Сl-группы, способствует его реакции взаимодействия с различными классами органических соединений с образованием многофункциональных соединений и дает возможность проведения новых синтезов с целью получения неионогенных ПАВ [12].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Нафтеновые спирты: транс-циклогександиол-1,2, циклогексанол, метилциклогексанол – реактивы “ос. ч.” – продукты окисления нафтеновых углеводородов (циклогексена, циклогексана и метилциклогексана), выделяемых из нефтей. Эпихлоргидрин – промышленный продукт с чистотой 99.98% завода “Оргсинтез” (г. Сумгаит, Азербайджан). Гидроксид натрия – реактив марки “ ч. д. а.” фирмы “Chemapol”. Ортофосфорная кислота – 86.4%-ный реактив марки “ч”.
Реакцию хлороксипропилирования нафтеновых спиртов проводили при избытке ЭХГ в автоклаве, снабженном регулируемой системой обогрева при 140°С в течение 10–12 ч. В качестве катализатора использовали гидроксид натрия в этаноле в количестве 0.5–1 мол. % от спиртов. Предварительно нафтеновые спирты обезвоживали кипячением над оксидом кальция и перегоняли.
Непрореагировавшийся в реакции ЭХГ удаляли путем нагревания целевого продукта при умеренной температуре до образования массы постоянного состава. Далее гравиметрическим методом определяли конверсию ЭХГ и рассчитывали среднюю молекулярную массу синтезированных олигомеров.
Модификацию хлороксипропилированных эфиров (ХОПЭ) нафтеновых спиртов проводили в стеклянном реакторе с помощью ортофосфорной кислоты при мольном соотношении 1 : 1, комнатной температуре 18–20°С и постоянном перемешивании до получения целевого продукта густой массы.
Структура и состав синтезированных олигомеров с различной средней степенью хлороксипропилирования были установлены методами ЯМР1 Н и ИК-спектроскопии.
ИК-спектры сняты на спектрометре “Specord M-80”. Спектры ЯМР1 Н снимали в растворе ССl4 с внешним эталоном гексаметилендисилоксаном (ГМДС) на спектрометре “Tesla” марки “ВS-487 С”, а химические сдвиги были зафиксированы в σ-шкале [13, 14].
Содержание спиртов и продуктов их хлороксипропилирования в реакционной смеси определяли методом ГЖХ. Использовали хроматограф “Цвет-4” с пламенно-ионизационным детектором. Колонку длиной 3000 мм и диаметром 3 мм заполняли хроматон N-AW-ДМСS, на который наносили Апиезон L (15%); газ-носитель – гелий. Точность определения концентраций спиртов составляла 5%.
Поверхностную активность водных растворов исследовали методом сталагмометрии. Гидрофильно-липофильный баланс (ГЛБ) рассчитывали по системе, приведенной в [3]. Коэффициент преломления ($n_{D}^{{20}}$) измеряли с помощью рефрактометра марки “ИРФ-22”, а коэффициент экстинкции (ε) 0.5%-ных по массе водных растворов – прибо-ром марки “АОМ-102”. Плотность (ρ) определяли с помощью пикнометра по известной методике [15].
Способность синтезированных соединений замедлять испарение бензина проводили по методике [4, 16]. Для этого в градуированные стеклянные стаканы наливали по 100 мл товарного бензина марки АИ-92. В первый стакан добавляли 5%-ный по массе водный раствор испытуемого реагента, во второй – 100%-ный неразбавленный реагент, а в третий стакан – чистый бензин. За изменением уровня бензина наблюдали по градуированной шкале. Эффект замедления испарения бензина при хранении рассчитывали по следующей формуле:
где V0 – обьем испарившегося бензина в холостом опыте, V – объем испарившегося бензина из стакана с реагентом.РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
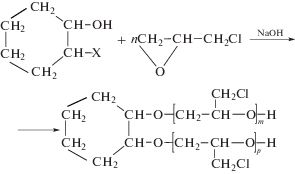
При катализе алкоголятом спирта или щелочью последовательно-параллельная реакция хлороксипропилирования нафтеновых спиртов протекает по следующей схеме:
где Х = Н, –СН3, –ОН; n = m + p – число группы эпоксидного происхождения (средняя степень хлороксипропилирования).Хлороксипропилированием в автоклаве нафтеновых спиртов, получаемых из нефтей, в присутствии 0.5–1%-ного раствора щелочи в этаноле при температуре 140°С были получены эфиры с различным количеством присоединенных молей ЭХГ, с увеличением молекулярной массы которых улучшается смачивающаяся и диспергирующая способность.
Исходное мольное соотношение реагентов – спирт: ЭХГ варьировали в широком интервале (1 : 1)–(1 : 60). Продукты реакции представляют собой маслянистые жидкости с цветом, изменяющимся от светло-желтого до красно-коричневого. При взаимодействии нафтеновых спиртов с ЭХГ при мольном соотношении исходных реагентов 1 : 1 конверсия ЭХГ составляет 100%, “n” равняется 1. При мольном соотношении реагентов 1 : 5 конверсия ЭХГ составляет соответственно для транс-циклогександиола-1,2, циклогексанола и метилциклогексанола 87.4, 88.3 и 86.2%, “n” равняется 4.5, 4.3, 4.2 соответственно для каждого спирта. Коэффициенты рефракции при 18–19°С равны 1.479, 1.455, 1.460; ГЛБ равны –15.62, –13.7, –12.18 соответственно для каждого спирта.
Результаты исследования реакции хлороксипропилирования нафтеновых спиртов и некоторые физико-химические показатели целевых продуктов ре приведены в табл. 1.
Таблица 1.
Физико-химические характеристики продуктов реакции хлороксипропилирования транс-циклогександиола, циклогексанола и метилциклогексанола
| Мольное соотношение исходных компонентов спирт : ЭХГ | Конверсия ЭХГ, % |
Средняя степень хлорокси- пропилирования | $n_{D}^{{20}}$ (Т, °С) |
ρ4 (Т, °С), г/см3 | ε, л моль см–1 |
ГЛБ |
|---|---|---|---|---|---|---|
| 1 : 1 | ∼100.0 | 1.0 | 1.4760 | 1.220 | – | 5.84 |
| 1.4500 (18) | 1.117 (18) | 4.96 | ||||
| 1.4525 | 1.110 | 4.84 | ||||
| 1 : 5 | 87.4 | 4.5 | 1.4790 | 1.295 | – | –15.62 |
| 88.3 | 4.3 | 1.4550 (19) | 1.180 (19) | –13.70 | ||
| 86.2 | 4.2 | 1.4600 | 1.175 | –12.18 | ||
| 1 : 10 | 97. 6 | 6.8 | 1.4820 | 1.320 | 53.25 | –40.76 |
| 93.5 | 8.7 | 1.4610 (27) | 1.210 (21) | –35.14 | ||
| 91.9 | 8.9 | 1.4650 | 1.192 | –33.25 | ||
| 1 : 15 | 92.4 | 15.8 | 1.4690 | 1.250 | 72.33 | –76.19 |
| 95.6 | 18.6 | 1.4485 (22) | 1.206 (22) | –63.33 | ||
| 94.3 | 17.5 | 1.4460 | 1.182 | –60.93 | ||
| 1 : 30 | 95.5 | 29.4 | 1.4560 | 1.128 | 128.45 | –151.27 |
| 97.8 | 33.3 | 1.4430 (23) | 1.086 (23) | –127.77 | ||
| 96.5 | 32.8 | 1.4410 | 1.024 | –119.43 | ||
| 1 : 45 | 93.2 | 39.9 | 1.4500 | 1.245 | – | –200.62 |
| 94.1 | 42.5 | 1.4410 (22) | 1.164 (22) | –181.10 | ||
| 93.8 | 41.4 | 1.4380 | 1.143 | –162.22 | ||
| 1 : 60 | 90.1 | 50.5 | 1.4470 | 1.202 | – | –265.69 |
| 93.6 | 55.6 | 1.4360 (20) | 1.125 (20) | –241.10 | ||
| 92.4 | 53.4 | 1.4350 | 1.106 | –240.86 |
Как видно из табл. 1, у эфиров со средней степенью хлороксипропилирования 8.9, 18.6 и 32.8 определены коэффициенты экстинкции, которые равны соответственно 53.25, 72.33, 128.45 л (моль см) для каждого спирта соответственно.
Было выявлено, что по мере протекания реакции хлороксипропилирования нафтеновых спиртов с увеличением мольного количества ЭХГ повышается способность превращения ЭХГ, средняя степень хлороксипропилирования (n) и значения коэффициентов экстинкции (ε), а рассчитанные значения ГЛБ конечных продуктов снижаются, т.е. увеличиваются гидрофобные свойства ХОПЭ спиртов.
Максимальное превращение ЭХГ наблюдается при эквимолярном соотношении исходных реагентов.
С увеличением числа звеньев ЭХГ, присоединившихся к спиртам, при мольном соотношении от 1 : 1 до 1 : 10 значения показателя преломления и плотности возрастают. Увеличение числа групп эпоксидного происхождения в ХОПЭ спиртов при мольном соотношении исходных реагентов от 1 : 15 до 1 : 60 приводит к снижению значений коэффициента преломления и плотности. Такой неоднозначный характер изменения указанных показателей с удлинением гетероцепи можно связать с конформационными переходами олигомерной молекулы. Причем показатели преломления и плотности у ХОПЭ одноатомных нафтеновых спиртов – циклогексанола и метилциклогексанола ниже, чем у эфиров двухатомного спирта – транс-циклогександиола-1,2.
В ЯМР 1Н-спектре ХОПЭ нафтеновых спиртов со средней степенью хлорокси-пропилирования п = 1 в области 3.8 м.д. наблюдаются химические сдвиги протонов хлорметиленовой группы ‒СН2Сl; протоны метиленовых групп, связанные в эфирном фрагменте, имеют сдвиги ~3.56 и 3.50 м.д., протоны, находящиеся по соседству с –ОН-группой имеют химические сдвиги ~3.30 м.д.
Независимым методом, исходя из интегральных интенсивностей сигналов протонов –СН3- и ОСН2-групп, была определена степень хлороксипропилирования.
В ИК-спектре ХОПЭ нафтеновых спиртов со средней степенью хлороксипропилирования “n” = = 4.52 присутствует широкая полоса валентных колебаний связи –ОН-группы при 3100–3700 см–1, полоса валентных колебаний связей С–Н в СН3-, СН2- и СН-группах 2840–3040 см–1, полосы деформационных колебаний связей С–Н в СН3-, СН2- и СН-группах 1280–1460 см–1; полосы асимметричных и симметричных валентных колеба-ний связей С–О в эфирной группе 1260–1085 см–1, полоса валентных колебаний связи СО в составе фрагмента С–ОН 1057 см–1, а при 963 см–1 полоса внеплоскостных деформационных колебаний группы С–Н гетероцепи и полоса валентных колебаний связи С–Сl 758–760 см–1 .
Сталагмометрическим методом определяли значения поверхностного натяжения водных растворов с различной концентрацией хлороксипропилированных производных нафтеновых спиртов на границе с керосином. Концентрация этих растворов изменяется в интервале 0.025–10.00%.
Результаты экспериментов и некоторые физико-химические характеристики целевых продуктов и их модификаторов приведены в табл. 2.
Таблица 2.
Поверхностное натяжение хлороксипропилированного транс-циклогександиола-1.2 (ХОПЦЛ) и его модификаторов на границе керосин−вода.
| Средняя степень хлорокси-пропилирования |
Поверхностное натяжение на границе керосин−вода, мН/м | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Т, °С | концентрация ХОПЦЛ, мас. % | |||||||||
| 0.025 | 0.05 | 0.1 | 0.5 | 1.0 | 3.0 | 5 | 7.0 | 10.0 | ||
| 1.0 | 27 | 49.6 | 47.1 | 43.2 | 40.6 | 39.4 | 31.8 | 30.9 | 30.0 | – |
| 2.37 | 19 | 48.7 | 45.4 | 43.3 | 39.9 | 40.2 | 40.3 | 40.0 | 41.4 | – |
| 4.86 | 25 | 44.7 | 41.9 | 31.6 | 22.5 | 21.9 | 18.6 | 15.0 | 13.5 | 9.0 |
| 15.08 | 23 | 30.4 | 27.7 | 22.1 | 21.7 | 19.2 | 15.4 | 11.1 | 10.8 | 12.5 |
| 29.4 | 26 | 46.7 | 45.4 | 45.0 | 43.2 | 36.6 | 31.4 | 15.4 | 19.3 | 17.6 |
| 39.9 | 21 | 40.3 | 38.6 | 37.4 | 32.8 | 30.3 | 27.9 | 24.1 | 22.2 | 19.9 |
| 50.5 | 18 | 38.5 | 31.9 | 28.2 | 29.7 | 28.8 | 23.6 | 19.3 | 17.0 | 15.5 |
| Модификаторы ХОПЦЛ, содержащие фосфатную группу | ||||||||||
| 4.56 | 26 | 42.0 | 35.4 | 37.4 | 27.7 | 26.3 | 19.9 | 18.3 | 14.5 | 9.3 |
| 8.32 | 20 | 27.3 | 28.0 | 22.5 | 21.3 | 15.9 | 12.4 | 11.2 | 9.6 | 8.9 |
| 14.23 | 23 | 38.2 | 38.6 | 38.0 | 29.2 | 19.0 | 18.5 | 16.6 | 14.2 | 12.6 |
| 26.04 | 24 | 39.0 | 39.1 | 38.0 | 35.5 | 32.8 | 27.4 | 20.6 | 18.3 | 14.7 |
| 30.12 | 24 | 39.9 | 39.9 | 38.6 | 36.3 | 35.7 | 33.7 | 19.9 | 19.0 | 15.8 |
Таким образом, по мере превращения ЭХГ в хлороксипропилированные фраг-менты цепи липофильные свойства синтезированных ПАВ повышаются, т.е. ухудшается их водорастворимость, на что указывает ГЛБ (табл. 1).
Как видно в интервале “n”, равном 2.73–15.08 наблюдается наиболее высокая поверхностная активность, которая снижает значения поверхностного натяжения в сравнении с водой на границе с керосином. Далее наблюдается относительная стабильность.
С целью придания гидрофильных свойств синтезированных олигомерных ПАВ на основе ЭХГ и нафтеновых спиртов с различной длиной цепи они были фосфатированы орто-фосфорной кислотой Н3РО4.
В результате модификации ХОПЭ спиртов (с различными средними степенями хлороксипропилирования) с помощью ортофосфорной кислоты Н3РО4 были получены модифицированные олигоэфиры, физико-химические характеристики, которых приведены в табл. 3.
Таблица 3.
Физико-химические характеристики ХОПЭ спиртов, модифициро ванных с помощью Н3РО4
| Средняя степень хлорокси- пропилирования |
$n_{D}^{{20}}$ | ρ4, при комнат. температуре | ε, л моль–1 см–1 | Кислотное число, мг КОН/г |
|---|---|---|---|---|
| 4.56 | 1.4590 | 1.504 | 26.44 | 645.3 |
| 8.32 | 1.4638 | 1.516 | 93.28 | 634.7 |
| 14.23 | 1.4770 | 1.543 | 141.35 | 710.6 |
| 26.04 | 1.4680 | 1.546 | 286.99 | 648.4 |
| 30.12 | 1.4687 | 1.545 | – | 705.9 |
Фосфатирование ХОПЭ спиртов со средней степенью хлороксипропилирования 4.56 и 14.23 несколько снижает поверхностную активность. Введение фосфатной группы в цепь при “n” равном 8.32 и 26.04 незначительно улучшает поверхностную активность ХОПЭ спиртов.
Полученные олигоэфиры представляют собой вязкие текучие жидкости. Увеличение вязкости связано с введением сильнополярной фосфатной группы в олигомерную цепь, способствующей усилению сил межмолекулярного взаимодействия и водородной связи.
По мере протекания реакции фосфатирования запах исходного олигомера исчезает, реакционная масса становится вязкой, окраска изменяется от желтого до темно-коричневого, частично растворяется в воде. Гидрофилизация хлороксипропилированных эфиров нафтеновых спиртов с помощью Н3РО4 приводит к высокой нефтесобирающей способности.
ЗАКЛЮЧЕНИЕ
Синтезированные ХОПЭ нафтеновых спиртов и продукты их модификации с помощью Н3РО4 проявляют высокий эффект замедления испарения бензина при его хранении и могут быть использованы как неионогенные ПАВ в нефтедобывающей промышленности. Установлено, что с увеличением мольного количества ЭХГ повышается способность превращения ЭХГ и степень хлороксипропилирования, а также значения коэффициентов экстинкции. При этом степень хлороксипропилирования понижается в ряду транс-циклогександиол-1,2, 4-метилциклогексанол, циклогексанол, что, видимо, связано co стерическими особенностями используемых нафтеновых спиртов.
Список литературы
Шенфельд Н.А. // Поверхностно-активные вещества на основе оксида этилена. М.: Химия, 1982. 749 с.
Плетнев М.Ю. // Журн. Химическая промышленность. 2000. № 1. С. 48.
Ланге К.Р. // Поверхностно-активные вещества. Синтез, свойства, анализ, применение. С.-Петербург: Профессия. 2005. 240 с.
Коршак А.А. // Современные средства сокращения потерь бензина от испарения. М.: Сервис, 2001. 142 с.
Наметкин Н.С., Егорова Г.М., Хамаев В.Х. // Нафтеновые кислоты и продукты их химической переработки. М.: Химия, 1982. 111 с.
Наметкин Н.С., Егорова Г.М., Хамаев В.Х. // Нефтехимия. 1967. Т. 7. № 3. С. 402.
Хамаев В.Х., Мазатова А.К., Пустовит И.И., Биккулов А.З. // Нефтехимия. 1978. № 8. С. 202
Зейналов С.Б., Гуськов А.К., Щвец В.Ф. // Азерб. хим. журн. 1988. № 2. С. 13.
Будагова Р.Н., Зейналов С.Б., Ходжаев Г.Х. // Журн. химическая промышленность сегодня. 2016. № 1. С. 48.
Зейналов С.Б. // Эфиры алициклического ряда. Баку: Изд-во “Элм”, 2003. 188 с.
Будагова Р.Н., Зейналов С.Б., Садыхова Г.К. // Эпокси- и краун-эфиры. Германия: изд-во Lap-Lambert, 2017. 86 с.
Зейналов С.Б., Кязимова Т.И., Шарифова С.К. // Эпихлоргидрин. Баку: Изд-во “Элм”, 2000. 188 с.
Гюнтер Х.А. // Введение в курс спектроскопии ЯМР. М.: 1984. 92 с.
Тарасевич Б.Н. // ИК-спектры основных классов органических соединений. М.: МГУ, 2012. 55 с.
Куренков В.А. // Практикум по химии и физике полимеров. М.: Химия, 1990. 304 с.
Гумбатов Г.Г., Дашдиев Р.А. // Химические реагенты, применяемые при добыче, подготовке нефти и газа. Баку: Изд-во “Элм”, 1999. 376 с.
Дополнительные материалы отсутствуют.