Нефтехимия, 2019, T. 59, № 2, стр. 152-158
Изомеризация н-гексана на нанодисперсных катализаторах, нанесенных на кислотно-активированный монтмориллонит в Nа-форме
Л. С. Джумабаева 1, 2, *, Н. А. Закарина 1, **, В. Ф. Третьяков 3, Г. Ж. Елигбаева 2, Д. А. Жумадуллаев 1, Т. Б. Егорова 4
1 АО “Институт топлива, катализа и электрохимии им. Д.В. Сокольского”
Алматы, Казахстан
2 Казахский национальный исследовательский технический университет им. К.И. Сатпаева
Алматы, Казахстан
3 Российский технологический университет МИРЭА
Москва, Россия
4 Московский государственный университет имени М.В. Ломоносова
Москва, Россия
* E-mail: djumabaevals@mail.ru
** E-mail: nelly_zakarina@rambler.ru
Поступила в редакцию 23.05.2018
После доработки 15.10.2018
Принята к публикации 17.09.2018
Аннотация
Катализаторы Pd-золь/NaHММ были испытаны в реакции изомеризации н-гексана. Увеличение содержания Pd с 0.1 до 0.35% приводит к повышению активности катализаторов. Селективность по С6+-изомерам, остается стабильной и достаточно высокой – 94.6–98.0% на катализаторах c содержанием Pd 0.1 и 0.35% соответственно. Максимальная конверсия н-гексана на 0.35%-ном Pd-катализаторе составляет 52.6% при температуре 400°С, добавление морденита ведет к незначительному снижению конверсии до 50.9%. На 0.1%-ном Pd-катализаторе максимальная конверсия составляет 45.0% при 400°С, а на катализаторе, модифицированном морденитом – 50.4%. Максимальный выход изомерных гексанов на бесцеолитных 0.35 и 0.1%-ных Pd-катализаторах составляет 44.9 и 39.3% соответственно. На морденитсодержащем 0.35%-ном Pd/NaHММ + НМ-катализаторе выход С6-изомеров составляет 44.3%, а на низкопроцентном 0.1%-ном Pd/NaHММ + НМ-катализаторе выход С6-изомеров – 43.0%. Количество продуктов гидрокрекинга не превышает 0.7%. Размер частиц Pd-золей, определен на просвечивающем электронном микроскопе высокого разрешения (ПЭМВР) марки JEM 2100 и составляет 3.5–5 нм. Методом энергодисперсионной рентгенофлуоресцентной спектроскопии определен элементный состав Рd–Z/NaHMM-катализаторов с различным содержанием палладия и модифицированных морденитом.
Материалы на основе природных силикатов используются в качестве эффективных и относительно дешевых сорбентов и носителей катализаторов [1]. Наиболее известными представителями слоистых силикатов являются бентонитовые глины, которые обладают адсорбционными и ионообменными свойствами [2, 3]. Основным компонентом бентонитовых глин является монтмориллонит, имеющий слоистую структуру с расширяющейся решеткой. Благодаря особенностям строения каркаса кристаллической структуры монтмориллонита, высокой удельной поверхности и объема пор, а также высокой катионообменной емкости – от 60 до 150 мЭкв/100 г [4, 5], открываются возможности создания на его основе новых сорбентов, носителей катализаторов для различных процессов [4]. Кроме того, способность монтмориллонита набухать в воде и полярных жидкостях с проникновением жидкости между пакетами и их раздвижением [6–8] открывает возможность активирования монтмориллонитовых глин и их модифицирования, что направлено на увеличение пористости и удельной поверхности, повышение ионнобменных свойств и создание новых активных центров [9].
Известно, что кислотная обработка глин приводит к увеличению удельной поверхности, а основная часть щелочных и щелочноземельных катионов, при этом, заменяется протоном кислоты [10]. Результаты исследования образцов методом низкотемпературной адсорбции азота показали рост удельной поверхности и незначительное увеличение диаметра пор после кислотной обработки [11]. Промышленное производство кислотно активированных монтмориллонитов на основе природных глин Баварии, США, Алжира осуществляется крупными фирмами [12–14].
Анализ литературы по свойствам металлических наночастиц показал, что наночастицы палладия, нанесенные на различные носители, проявили высокую каталитическую активность в реакциях гидрирования, окисления, изомеризации и др. [15, 16].
В данной работе были использованы гидрозоли палладия с размером частиц 3.5–5.0 нм, которые синтезировали при восстановлении водородом водных растворов полигидроксокомплексов Pd, полученных путем взаимодействия растворов PdCl2 с молибдатом Na при кипячении [17].
Цель работы заключалась в изучении текстурных свойств и дисперсности Pd-катализаторов, представляющих собой Pd-золи, нанесенные на активированный монтмориллонит Nа-формы и испытании полученных катализаторов в реакции изомеризации н-гексана, в зависимости от содержания активного металла и введения морденита.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Монтмориллонитовую глину Таганского месторождения (ММ) подвергали кислотной активации путем кипячения в 20%-ном растворе H2SO4 в течение 6 ч с последующим отмыванием от ионов ${\text{SO}}_{4}^{{2 - }}$. Полученную Н-форму Таганского ММ формовали, сушили сначала при комнатной температуре, затем при 150°С и далее подвергали прокаливанию при 500°С [18, 19].
Н-форма ММ служила носителем для Pd-катализаторов.
Катализаторы готовили методом пропитки носителя водными растворами Pd-золей; методика приготовления описана в работе [20]. Pd-катализаторы после пропитки, восстанавливали в токе водорода при температуре 250–400°С. Содержание металла в образцах составило 0.1 и 0.35 мас. %.
Текстурные характеристики образцов определяли методом БЭТ по низкотемпературной адсорбции азота на приборе ACCUSORB. Элементный анализ композитов проводили с помощью энергодисперсионной рентгенофлуоресцентной спектроскопии на энергодисперсионной системе микроанализа INCA–Energy 450, установленной на сканирующий электронный микроскоп JSM6610LV, JOEL, Япония. Исследование образцов просвечивающей электронной микроскопией высокого разрешения (ПЭМВР) проведено на приборе JEM 2100 (JEOL) с рабочей энергией электронов 200 кэВ.
Активность образцов в изомеризации н-гексана исследовали в проточном реакторе в среде водорода при варьировании температуры процесса в интервале 250–400°С.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
По данным работы [21], в которой была изучена реакция изомеризации н-гексана на палладиевых катализаторах, нанесенных на SO4/ZrO2/Al2O3, в зависимости от концентраций Pd было показано, что оптимальное содержание Pd, обеспечивающее максимальную изомеризующую активность находится в интервале 0.3–0.75 мас. %.
Серии опытов, проведенные нами, позволяют сделать вывод, что наиболее оптимальная концентрация гидрирующего металла (Pd-золь) составляет 0.35 мас. %. Данные по выходу продуктов гидроизомеризации н-гексана на Pd-катализаторах с различным содержанием Pd (01 и 0.35%) и модифицированных морденитом (НМ) приведены в табл. 1. н-Гексан изомеризуется на изученных катализаторах с образованием моно- и ди-замещенных изогексанов: 2-метилпентана (2МП); 2,2-диметилбутана (2,2ДМБ) и небольших количеств изобутана, изопентана – 2-метилбутана (2МБ) и изогептанов – 2,2-диметилпентана (2,2 ДМП); 2,4-диметилпентана (2,4ДМП); 2,2,3-триметилбутана (2,2,3ТМБ); 3,3-диметилпентана (3,3ДМП); 2-метилгексана (2МГ); 3-метилгексана (3МГ); 3-этилпентана (3ЭП).
Таблица 1.
Изомеризация н-гексана на Pd-золь/NаHММ-композитном катализаторе c различным содержанием Pd и модифицированных морденитом (НМ)
| Катализатор | Т, °С | α, % | ${{{\text{S}}}_{{{{{\text{C}}}_{6}}}}}$, % | ${{{\text{S}}}_{{{{{\text{C}}}_{{4 + }}}}}}$, % | Выход продуктов реакции, мас. % | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| С1–С4 | изо-Б | 2-МБ | 2,2ДМБ | 2МП | сумма С7 | |||||
| 0.1% Pd | 250 | 5.0 | 74.0 | 98.0 | – | – | 0.1 | 2.4 | 1.7 | 1.3 |
| 300 | 16.0 | 76.0 | 97.0 | – | – | 0.4 | 7.0 | 4.9 | 3.3 | |
| 350 | 41.0 | 90.0 | 99.0 | – | – | 0.5 | 20.8 | 15.8 | 3.5 | |
| 400 | 45.0 | 88.0 | 96.0 | 0.2 | 0.3 | 1.5 | 22.0 | 17.2 | 3.3 | |
| 0.1% Pd + HM | 250 | 13.0 | 80.5 | 98.2 | – | – | 0.23 | 6.3 | 4.15 | 2.3 |
| 300 | 42.2 | 91.0 | 97.8 | 0.08 | 0.18 | 0.67 | 20.8 | 17.6 | 2.8 | |
| 350 | 48.9 | 88.0 | 94.8 | 0.53 | 0.76 | 1.25 | 23.8 | 19.2 | 3.3 | |
| 400 | 50.4 | 83.3 | 95.2 | 0.67 | 0.72 | 1.0 | 22.7 | 19.2 | 6.0 | |
| 0.35% Pd | 250 | 4.8 | 74.2 | 96.7 | – | – | 0.16 | 1.9 | 1.6 | 1.0 |
| 300 | 29.4 | 73.5 | 94.9 | – | – | 1.5 | 13.0 | 8.7 | 6.3 | |
| 350 | 46.2 | 83.8 | 95.5 | 0.2 | 0.23 | 1.6 | 20.5 | 18.0 | 5.4 | |
| 400 | 52.6 | 85.4 | 96.7 | 0.2 | 0.35 | 1.2 | 25.2 | 19.7 | 5.9 | |
| 0.35% Pd + HM | 250 | 13.0 | 45.9 | 97.3 | – | – | 0.35 | 3.5 | 2.4 | 6.7 |
| 300 | 28.7 | 91.7 | 97.7 | – | 0.22 | 0.45 | 16.0 | 10.2 | 1.7 | |
| 350 | 44.9 | 91.7 | 97.0 | 0.23 | 0.35 | 0.76 | 22.7 | 18.5 | 2.4 | |
| 400 | 50.9 | 87.1 | 96.6 | 0.45 | 0.43 | 0.84 | 25.0 | 19.3 | 4.8 | |
Как видно из табл. 1, снижение количества Pd в катализаторе до 0.1% приводит к незначительному снижению изомеризующей активности катализатора. С повышением температуры на обоих ка-тализаторах наблюдается рост конверсии н-гексана, сопровождающийся увеличением выхода С4+-изомеров. Так, конверсия н-гексана при 400°С на 0.35 и 0.1% Pd составляет 52.6 и 45.0% соответственно.
Добавление морденита в 0.1%-ный Рd способствует увеличению конверсии н-гексана при всех температурах, а также выхода дизамещенных С6-изомеров. Так, на бесцеолитном 0.1%-ном Pd-контакте выход 2,2-ДМБ составляет 7.0% при 300°С, а на том же катализаторе, модифицированном морденитом, –20.8%. Максимальный выход 2,2-ДМБ наблюдается при температуре 350°С на 0.1%-ном Pd-контакте + НМ и составляет 23.8%. Кроме того, найдено 19.2% 2МП. При этом выход продуктов гидрокрекинга не превышает 0.7%.
При содержании палладия 0.35%, максимальный выход 2,2-ДМБ составляет 25.2%, а 2МП – 19.7% (400°С). При добавлении морденита выход 2,2-ДМБ снижается незначительно и составляет 25.0%, а 2МП при этой же температуре –19.3%. Выход продуктов гидрокрекинга не превышает 0.4%.
Для наглядности на рис. 1 приведена зависимость выходa изогексанов и С4+ от температуры процесса изомеризации н-гексана на катализаторах с различным содержанием Pd и с добавлением морденита.
Рис. 1.
Зависимость выходa изогексанов и C4+-изомеров из н-гексана от температуры на катализаторах: 0.1%-ный Pd/NаHММ (а); 0.1%-ный Pd/NаHММ + HM (б); 0.35%-ный Pd/NаHММ (в); 0.35%-ный Pd/NаHММ + HM (г).
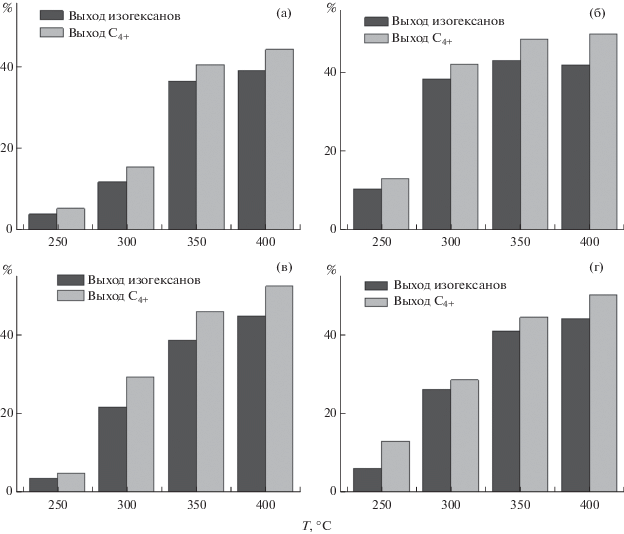
Как видно из рис. 1, выход изогексанов и всех образующихся изомеров, начиная с изобутана (изо-С4+), растет с повышением температуры.
Если провести сопоставление результатов на изученных катализаторах, то можно видеть, что максимальная конверсия н-гексана (52.6%) наблюдается на 0.35%-ном Pd-катализаторе при 400°С. По выходу всех изомеров самые высокие результаты были получены также на 0.35%-ном Pd-катализаторе (52.37%), за ним следует 0.35%-ный Pd + НМ (50.37%), затем 0.1%-ный Pd + НМ (49.62%) и 0.1%-ный Pd (44.3%).
Элементный анализ катализаторов проводили с помощью энергодисперсионной-рентгенофлуросцентной спектроскопии на энергодисперсионной системе микроанализа INCA – Energy 450, установленной на сканирующий электронный микроскоп JSM6610LV, JOEL, Япония.
Как видно из табл. 2, после кислотной активации значительно снижается содержание кальция и натрия в монтмориллоните (NaНММ). Количество магния снижается в катализаторах, модифицированных морденитом. По данным элементного анализа найдены несколько завышенные количества палладия по сравнению с введенным методом пропитки. Так, количество палладия по данным анализа составляет 0.5–0.17% по сравнению с расчетным количеством 0.1%.
Таблица 2.
Элементный состав исходного, активированного монтмориллонита и Рd–Z/NaHMM-катализаторов c различным содержанием Pd и модифицированных морденитом (НМ)
| Образец | Содержание основных компонентов, % | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| C | О | Na | Mg | Al | Si | Cl | S | Ca | Fe | Pd | |
| NaММ | – | 53.21 | 1.49 | 2.33 | 12.90 | 28.51 | 0.44 | – | 0.64 | 0.48 | – |
| NaНММ | – | 57.92 | 0.04 | 1.71 | 11.49 | 28.53 | – | – | – | 0.31 | – |
| NaHMM + НМ | – | 57.60 | 0.08 | 1.15 | 12.99 | 27.78 | – | – | 0.11 | 0.28 | |
| 0.1% Pd-золь/ NaHMM | 10.31 | 48.88 | 0.08 | 1.37 | 12.60 | 26.06 | – | 0.04 | 0.08 | 0.33 | 0.25 |
| 0.1% Pd-золь/NaHMM + НМ | 9.44 | 48.39 | 0.10 | 0.98 | 12.07 | 28.40 | – | 0.07 | 0.07 | 0.31 | 0.17 |
| 0.35% Pd-золь/ NaHMM | 10.86 | 47.83 | 0.10 | 1.34 | 12.54 | 26.42 | – | 0.06 | 0.06 | 0.37 | 0.41 |
| 0.35% Pd-золь/NaHMM + НМ | 9.59 | 48.88 | 0.16 | 0.98 | 11.46 | 28.03 | – | 0.08 | 0.06 | 0.26 | 0.51 |
Некоторые физико-химические характеристики палладиевых катализаторов на основе активированного монтмориллонита приведены в табл. 3.
Таблица 3.
Удельная поверхность и эффективный объем пор и их распределение для Pd–Z/NaHММ
| Образец | S, м2/г | Общий объем пор, см3/г | R, Å | Относительное количество, % | |
|---|---|---|---|---|---|
| микропоры 0–20 Å | мезопоры, 20–80 Å |
||||
| NaMM | 48.2 | 0.478 | 12.0–60.0 | 17.0 | 83.0 |
| NaHMM | 245.1 | 0.468 | 15.0–80.0 | 12.9 | 87.1 |
| 0.35% Pd-золь/NaHMM | 116.7 | 0.110 | 10.0–70.0 | 37.0 | 62.9 |
| 0.1% Pd-золь/NaHMM | 131.3 | 0.118 | 10.0–70.0 | 43.5 | 56.4 |
| 0.35% Pd-золь/NaHMM + HM | 140.3 | 0.118 | 10.0–70.0 | 40.6 | 59.4 |
| 0.1% Pd-золь/NaHMM + HM | 155.6 | 0.134 | 10.0–70.0 | 46.8 | 53.1 |
Активирование глины приводит к росту удельной поверхности от 48.2 до 245.1 м2/г (табл. 3). Нанесение палладия на активированный ММ приводит к снижению удельной поверхности и общего объема пор. Чем выше концентрация наносимого палладия, тем в большей степени уменьшается удельная поверхность катализатора. При введении 0.1% Pd удельная поверхность на бесцеолитном образце снижается от 245.1 до 131.3 м2/г. Общий объем пор уменьшается от 0.468 до 0.118 см3/г. С ростом содержания Pd до 0.35% удельная поверхность и общий объем пор продолжает уменьшаться.
Модифицирование морденитом приводит к повышению удельной поверхности с 116.7 до 140.3 м2/г, общий объем пор меняется незначительно. С добавлением морденита наблюдается незначительное снижение количеств мезопор и соответственно рост содержания микропор на 0.35%-ном Pd-контакте. Такая же закономерность наблюдается на 0.1%-ном Pd-катализаторе.
Таким образом, введение в катализатор морденита приводит к изменению текстурных характеристик Pd-катализаторов. Наблюдается корреляция между количеством мезопор и активностью 0.35%-ного Pd катализатора. При температуре 400оС конверсия н-гексана составляет 52.6%, а количество мезопор 62.9%, добавление морденита ведет к снижению мезопор до 59.4%, изомеризующая активность падает до 50.9%.
Влияние кислотных центров также необходимо учитывать в реакции изомеризации. Так, из табл. 4 видно, что с увеличением количества палладия с 0.1 до 0.35% наблюдается повышение общего количества кислых центров с 101.72 до 147.71 на бесцеолитных катализаторах, и с 149.15 до 183.51 – на морденит содержащих катализаторах. Содержание средних и сильных кислотных центров на этих катализаторах также растет с добавлением морденита. Такое распределение кислотных центров способствует росту изомеризующей активности Pd-катализаторов.
Таблица 4.
Кислотные свойства бесцеолитных и морденитсодержащих 0.1 и 0.35%-ных Pd–Z/NaHMM-катализаторов
| Образец | Содержание к. ц. | Кислотные центры | |||
|---|---|---|---|---|---|
| слабые <200°С |
средние 200–300°С | сильные >300°С | общая кислотность | ||
| 0.1% Pd золь/ NaHMM | % | 50.35 | 43.4 | 6.23 | 100 |
| мкмоль NH3/г | 51.21 | 44.14 | 6.33 | 101.72 | |
| 0.1% Pd золь/ NaHMM + HM | % | 39.6 | 47.01 | 13.61 | 100 |
| мкмоль NH3/г | 58.7 | 70.11 | 20.30 | 149.15 | |
| 0.35% Pd золь/ NaHMM | % | 47.68 | 44.1 | 8.20 | 100 |
| мкмоль NH3/г | 70.42 | 65.15 | 7.68 | 147.71 | |
| 0.35% Pd золь/ NaHMM + HM | % | 44.7 | 44.38 | 10.88 | 100 |
| мкмоль NH3/г | 82.02 | 81.44 | 19.96 | 183.51 | |
Для проведения ПЭМ подготовку образцов проводили диспергированием в растворе этанола, после чего полученную суспензию помещали на полимерную микродырчатую подложку, закрепленную на медной решетке. Результаты исследования, проведенные ПЭМ ВР поверхности катализатора, представлены на рис. 2 для двух разных полей (а, б) образца 0.35%-ного Pd-золь /NaHMM + НМ.
На снимках ПЭМ образца 0.35%-ного Pd-золь/ NaHMM + НМ, обнаружено дисперсное распределение частиц Pd. Размер частиц Pd колеблется в пределах 3.5–5.0 нм. Метод синтеза гидрозолей палладия, полученных при восстановлении водородом растворов полигидроксокомплексов Pd, обеспечивает получение устойчивых золей со средним размером металлических частиц палладия, равным до 4.5–5.0 нм, который мало меняется при нанесении на активированную глину.
Параллельно исследования проводились в сканирующем режиме с приставкой рентгеновского энергодисперсионного микроанализа (EDX analyzer), где было подтверждено наличие Pd на медной решетке, что иллюстрирует рис. 3.
По проделанной работе можно сделать вывод о перспективности Pd-золей, нанесенных на кислотно активированный монтмориллонит Na-формы, в процессе гидроконверсии н-гексана с получением высокооктановых изомеров.
Авторы благодарят сотрудника лаборатории физико-химических методов исследования за анализ образцов методом БЭТ старшего научного сотрудника, АО ИТКЭ им. Д.В. Сокольского, PhD Е. Нурмаканова.
Работа выполнена в рамках Программы целевого финансирования Министерства образования и науки Республики Казахстан “Создание основ производства продуктов нефти- и газопереработки на базе отечественных каталитических технологий” 2018–2020 гг.
Список литературы
Батталова Ш. Б. Физико-химические основы получения и применения катализаторов и адсорбентов из бентонитов. Алма-Ата: Наука, 1986. 168 с.
Грим Р. Минералогия и практическое использование глин. М.: Мир,1967. 512 с.
Травкина О.С., Куватова Р.З., Павлова И.Н., Ахмед Канаан Рамадан, Ахметов А.Ф., Кутепов Б.И. // Нефтехимия. 2015. Т 55. № 5. С. 826.
Везенцев А.И., Воловичева Н.А. // Сорбционные и хроматографические процессы. 2007. Т. 7. №. 4. С. 639.
Мерабишвили М.С. Бентонитовые глины. М.: Госгеодтехиздат, 1962. 128 с.
Assifaoui A., Huault L., Maissiat C., Roullier-Gall C., Jeandet P., Hirschinger J., Raya J., Jaber M., Lambert J., Cayot P., Gougeon R.D // RSC Adv. 2014. V. 4. P. 61096.
Арипов Э.А., Агзамходжаев А.А. // Активные центры монтмориллонита и хемосорбция. Ташкент: ФАН, 1983. 164 с.
Shibata M., Matsushima R., Tomita Y., Maeda Y., Kobayashi K. // Applied Clay Science. 2009. V. 42. № 3–4. P. 519.
Трофимова Ф.А., Лыгина Т.З., Наумкина Н.Н, Гревцев В.А., Пермяков Е.Н., Сучкова Г.Г., Аухадеев Ф.Л. // Сборник статей по материалам конференции “Структура и динамика молекулярных систем”, 2006. Ч. 2. С. 301.
Финевич В.П., Аллерт Н.А., Карпова Т.Р, Дуплякин В.К. // Рос. хим. журн. (Ж. Рос. хим. об-ва им. Д.И. Менделеева). 2007. Т. LI. № 4. С. 69.
Карнаухов А.П. / Адсорбция. Текстура дисперсных и пористых материалов. Новосибирк: Наука, 1999. 470 с.
Hart M.P., Brown D.D. J. Mol. Catal. A. 2004. V. 212. P. 315.
Moronta A., Luengo J., Ramirez Y., Quinonez J., Conzalez E., Sanchez J. // Appl. Clay Sci. 2005. V. 29. P. 117.
Harrad D., Chambellan A., Lavelley J.C. // Catal. Let. 1998. V. 54. P. 227.
Zhang H., Yang Y., Wei Dai, Lu S., Yu H., JI Y. // Chinese J. of Chem. Engineering. 2014. V. 22. № 5. P. 516.
Advanced Catalysts and Nanostructured Materials. Modern Synthetic Methods / Ed. Moser W.R. N.Y.: Acad. Press, 1996.
Максимов Г.М., Зайковский В.И., Матвеев К.И., Лихолобов В.А. // Кинетика и катализ. 2000. Т. 41. № 6. С. 925.
Ханхасаева С.Ц., Дашинамжилова Э.Ц., Рампилова В.В. // Вестник Бурятского гос. ун-та. 2011. № 3. С. 134.
Закарина Н.А., Акурпекова А.К. // Вестник НАН Республики Казахстан. 2017. № 1. С. 59.
Закарина Н.А., Акурпекова А.К., Джумабаева Л.С., Жумадуллаев Д.А. // Доклады Национальной академии наук Республики Казахстан. 2017. № 5. С. 83.
Смоликов М.Д., Джикия О.В., Казанцев К.В., Киреева Т.В., Белый А.С. // Катализ в нефтеперерабатывающей промышленности. 2018. Т. 18. № 3. C. 48.
Дополнительные материалы отсутствуют.




