Нефтехимия, 2020, T. 60, № 4, стр. 476-482
Ионные жидкости как экстрагенты серосодержащих соединений дизельного топлива
Н. С. Коботаева 1, *, Т. С. Скороходова 1
1 Институт химии нефти СО РАН
634055 Томск, Россия
* E-mail: nat@ipc.tsc.ru
Поступила в редакцию 14.10.2019
После доработки 16.11.2019
Принята к публикации 11.03.2020
Аннотация
Рассмотрена возможность удаления серосодержащих соединений из дизельного топлива (ДТ) экстракцией при использовании в качестве экстрагентов ионных жидкостей (ИЖ) на основе 1,3-дибутилимидазолий бромида и 1-бутил-3-октилимидазолий бромида и солей переходных металлов (бромидов и трифторацетатов Cu, Co, Ni, Mn). Показано, что использование экстракционных систем, содержащих ИЖ и соли металлов, увеличивает степень удаления серосодержащих соединений из дизельного топлива. Высказано предположение, что соли металлов, обладающие электроноакцепторными свойствами, обеспечивают дополнительное комплексообразование с сернистыми соединениями углеводородного сырья, что и влечет за собой увеличение экстракционной емкости экстрагента.
За последние годы по мере истощения крупнейших месторождений легкого и малосернистого углеводородного сырья значительно возросла доля добываемых и перерабатываемых тяжелых высокосернистых нефтей и газовых конденсатов в общей добыче нефти Российской Федерации. Присутствие гетероатомных компонентов в нефтяном сырье значительно осложняет технологию переработки сырья, снижаются срок действия и селективность катализаторов, ухудшаются эксплуатационные характеристики получаемых продуктов. Существенная часть компонентов сжигается в составе топлив, в результате в атмосферу выбрасываются оксиды серы, азота, металлов, что наносит непоправимый вред окружающей среде. Особое внимание уделяется содержанию серы и полициклических ароматических углеводородов (УВ) в нефтяных фракциях, что связано с большой токсичностью продуктов сгорания. Высокие показатели содержания серы в российской нефти также являются основной причиной снижения ее конкурентоспособности на рынке сырья [1–3]. В связи с переходом нефтеперерабатывающей промышленности России на выпуск топлив, отвечающих европейским стандартам, необходимо усовершенствование процессов нефтепереработки, позволяющих получать экологически чистые ДТ, отвечающие современным и перспективным требованиям [2]. Основным направлением очистки УВ от примесей серы является процесс гидроочистки на твердофазных катализаторах.
Главные недостатки этого процесса – повышенная чувствительность катализаторов к металлам и гетероатомным соединения нефтей, большой расход водорода, высокое давление и высокое остаточное содержание тиофенов. Поэтому для каталитических установок малой и средней мощности рассматриваемая технология является не совсем рентабельной, что служит одной из причин для развития альтернативных технологий очистки углеводородного сырья.
Одними из перспективных методов облагораживания ДТ являются экстракционные процессы, позволяющие значительно снизить содержание серы и полиароматических УВ в топливе.
Преимуществом процессов экстракции является возможность их осуществления при атмосферном давлении и невысоких температурах, отсутствие необходимости использования катализатора, адсорбентов и водорода, что позволяет избежать образования углеродистых отложений и изменения углеводородного состава исходного сырья.
Эффективность экстракционной десульфуризации (ЭД) зависит от выбора растворителя, химической активности удаляемых компонентов и других факторов, включающих экологических аспекты и токсикологические ограничения. В большинстве исследований для ЭД используют высокополярные органические растворители, такие как ацетонитрил (АН), N,N-диметилформамид (ДМФА) [4–6], N-метилпирролидона (N-МП) [7–9], этиленгликоль [10]. В работе [11] исследован ряд апротонных и протонодонорных полярных растворителей и экстракционных систем, включая неполярный растворитель (гексан), в качестве экстрагентов удаления серосодержащих соединений (СС) из дизельной фракции высокосернистой южно-узбекской нефти и показано, что эффективное обессеривание фракции достигается при использовании экстракционной системы фенол–вода–гексан.
Можно отметить процесс GT-DeSulf SM, который является примером технологии экстракционной сероочистки. Этот процесс позволяет отделять сероорганические соединения и ароматические УВ из крекинговых дистиллятов с использованием смеси растворителей [12].
Наряду с технологиями экстракционных процессов, связанных с использованием традиционных растворителей, в настоящее время происходит стремительное развитие научных исследований и технологических разработок в области “зеленой химии”. Одним из важных направлений “зеленой химии” является замена традиционных растворителей. Перспективным представляется использование ИЖ. Интерес к ИЖ обусловлен, в основном, их экологическими характеристиками (не горючи, термически устойчивы, обладают низкой токсичностью, могут использоваться повторно), благодаря которым они рассматриваются в качестве альтернативы традиционным летучим органическим растворителям. ИЖ представляют собой соединения, состоящие из ионов и находящиеся в жидком состоянии при комнатной температуре. Как правило, ИЖ состоят из объемного, несимметричного органического катиона и слабо координирующего неорганического или органического аниона. Пожалуй, самым важным и привлекательным свойством ИЖ является возможность управления физическими и химическими свойствами ИЖ путем подбора структуры катиона и аниона.
Наиболее распространенными являются ИЖ на основе катионов имидазолия, пиридиния, пирролидиния, тетраалкиламмония. ИЖ активно используются в нефтехимии в качестве экстракционных систем для удаления сернистых соединений из различных видов моторных топлив [13–22].
Для улучшения экстракционной способности ИЖ создают экстракционные системы на основе ИЖ и солей металлов. Предполагается, что соли переходных металлов, входящие в состав ИЖ, обеспечивают дополнительное комплексообразование с сернистыми соединениями, находящимися в очищаемом углеводородном сырье, что влечет за собой увеличение экстракционной емкости.
Особенно эффективны ИЖ, которые содержат ионы Cu(I) и Ag(I), ввиду их значительной склонности к образованию π-комплексов с тиофеновыми производными [23, 24]. Так, например, в работе [24] показано, что ИЖ на основе имидазола и CuCl имеют хорошую десульфирующую способность, однако экстракцию проводят при достаточно высокой температуре (80°С).
В патенте [25] в качестве экстрагентов для удаления сернистых соединений из модельной смеси с содержанием общей серы 500 ррм рассмотрен ряд ИЖ на основе органического аниона – алкил имидазолия с различными заместителями и неорганического аниона хлорид а железа (FeCl4 ). Степень удаления общей серы ИЖ на основе этой смеси составляет 99%.
В работе [26] для десульфуризации сернистых соединений модельного жидкого топлива, содержащего дибензтиофен и коммерческого ДТ, использовали ряд ИЖ на основе 1-бутил-3- метилимидазолия (BMIm) с различными анионами – Br, Cl, OH, HSO4, BF4 и различными солями металлов – FeCl3, CuCl2, CoCl2, ZnCl2, MoCl2, MnCl2. Из коммерческого ДТ сера извлекалась с выходом 90%.
Процесс удаления СС из газойля при комнатной температуре в присутствии модифицированной ИЖ ([Bmim]Cl Fе0) рассмотрен в работе [27]. Максимум экстракционной эффективности достигается при одностадийной экстракции со степенью удаления 83.6%.
В настоящей работе проведено исследование процесса удаления СС из ДТ экстракцией ИЖ на основе алкилимидазола (1,3-дибутилимидазолиябромида, 1,3-дибутил-2-метилимидазолия бромида и 1-бутил-3-октилимидазолиябромида) и солей переходных металлов (бромидов итрийфторацетатов меди, кобальта, никеля и марганца).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве объектов исследования использовали прямогонную дизельную фракцию Омского НПЗ с пределами выкипания 200–360°С (ГОСТ 2177_99) с содержанием общей серы 0.349 мас. %. Групповой состав СС дизельной фракции представлен в табл. 1.
Таблица 1.
Групповой состав сернистых соединений прямогонной дизельной фракции
| Сернистые соединения: | Содержание серы, мас. % |
|---|---|
| Сульфиды | 0.4 |
| Тиофены | 0.86 |
| в том числе | |
| бензотиофен (БТ) и его гомологи | 0.61 |
| дибензотофен (ДБТ) и его гомологи | 0.25 |
В работе использованы ИЖ на основе имидазола и 2-метилимидазола – 1,3-дибутилимидазолий бромид (1,3диБImBr), 1,3-дибутил-2-метилимидазолий бромид (1,3диБ2MImBr) и 1-бутил-3-октилимдазолий бромид (1Б3ОImBr), синтезированные по методике, описанной в [25].
Синтез металлосодержащих ИЖ проводили в 2 этапа:
– синтез 1,3-дибутилимидазолия бромида (1-бутил-3-октилимидазолия бромида);
– взаимодействие 1,3-дибутилимидазолия бромида (1-бутил-3-октилимидазолия бромида) с солями металлов (CuBr2, NiBr2, CoBr2 , Cu(ТФА)2, Co(ТФА)2, Mn(ТФА)2).
Этап 1. В трехгорлую колбу, снабженную термометром, механической мешалкой и капельной воронкой вносили 37.0 см3 (0.3 моль) 1-бутил-имидазола. При температуре 65–70°С добавляли по каплям 36 см3 (0.34 моль) 1-бромбутана. После добавления всего количества 1-бромбутана смесь перемешивали 4 ч при температуре не более 70°С. Сушили продукт при температуре 75°С и 1 мм рт. ст. Продукт представляет собой светло-желтую вязкую жидкость. Выход 97.7% от теоретического.
Структуру полученных соединений подтверждали методом элементного анализа и ИК-спектроскопии. ИК-спектры регистрировали на ИК-Фурье-спектрометре Nicolet 5700 в матрице KBr в области частот 400–4000 см–1 с разрешением 4 см–1. Основные полосы в ИК-спектре ИЖ: 3217–3064 см–1 полосы колебания ароматической системы; 3021–2801 см–1 – полосы колебания алифатических групп; 3435 см–1 – полоса колебания воды; 1022 и 754 см–1– 1,3-замещение.
Этап 2. В реактор с магнитной мешалкой приливают 5 см3 ИЖ – 1,3ВImВr и добавляют при непрерывном перемешивании в течение 30 мин и температуре 25°С 0.05 г соли (CuBr2(безв.), NiBr2, CoBr2) или 0.1 г ((ТФА)2Cu(безв.), (ТФА)2Co(безв.), (ТФА)2Mn(безв.)).
Безводные соли – СuBr2, NiBr2, CoBr2 получены по методикам, описанным в [28], а трифторацетаты металлов (Co(ТФА)2, Мn(ТФА)2, Сu(ТФА)2 ) – по методикам для синтеза ацетатов металлов, описанным в работе [29].
Содержание серы в исходной и очищенной дизельных фракциях определяли методом сжигания в лампе по ГОСТ 19121-73.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для создания экстракционной системы (ЭС) “соль металла–ИЖ” растворяли безводные соли бромидов (Сu, Co, Ni) и трифторацетатов (ТФА) металлов (Co, Мп, Сu) в ИЖ. Критериями выбора ИЖ как основного компонента экстракционной системы являются температура плавления (ниже 50°С) и растворимость в УВ (менее 1%). Кроме этого, ИЖ должна хорошо растворять соли металлов. С учетом этих критериев были выбраны ИЖ на основе замещенного катиона имидазолия, а именно – 1,3-дибутилимидазолий бромид, 1,3-бутил-2-метилимидазолий бромид и 1-бутил-3-октилимидазолий бромид. ИЖ с более длинными алкильными заместителями в положении 3 имидазольного кольца обладают недостаточной растворяющей способностью относительно солей металлов.
ИЖ на основе имидазола можно отнести к координирующим полярным растворителям, таким как, например, ДМФА или ДМСО, т.к. они, также как и традиционные растворители имеют неподеленную электронную пару на атомах азота имидазольного кольца.
В работах [30, 31] показано, что ЭС на основе координирующих полярных растворителей (ДМФА и ДМСО) и солей переходных металлов обладают более высокой экстракционной способностью относительно СС моторных топлив, чем органические растворители без солей металлов. Авторы работ предполагают, что соли металлов, обладающие электроноакцепторными свойствами, обеспечивает дополнительное комплексообразование с СС, находящимися в очищаемом углеводородном сырье, что и влечет за собой увеличение экстракционной емкости экстрагента. В работе [31] наряду с бромидами и хлоридами переходных металлов рассмотрены трифторацетаты переходных металлов, обладающие более сильными электроноакцепторными свойствами, чем галогениды металлов.
В данной работе изучалась экстракционная десульфуризация СС ДТ экстракционными системами на основе имидазолсодержащих ИЖ и галогенидов и трифторацетатов переходных металлов.
При добавлении солей металлов к ИЖ на основе имидазола меняются их физико-химические свойства, такие как плотность, вязкость, электропроводность и многие другие [32], что может повлечь за собой и изменение экстракционной способности ИЖ.
Для нахождения оптимальной концентрации солей металлов в ИЖ рассмотрено влияние концентрации соли металла на эффективность удаления СС из ДТ (табл. 2).
Таблица 2.
Зависимость степени удаления сернистых соединений из дизельных топлив от концентрации соли металла в ионных жидкостях
| Экстракционная система | Степень удаления сернистых соединений из дизельного топлива, мас. % |
|---|---|
| 1,3диБImБ/0.5CuBr2 | 0.12 |
| 1,3диБImБ/0.6CuBr2 | 0.085 |
| 1,3диБImБ/0.7CuBr2 | 0.08 |
| 1,3диБImБ/1.0CuBr2 | 0.12 |
| 1,3диБImБ/1.2CuBr2 | 0.14 |
| 1,3диБImБ/1.5CuBr2 | 0.14 |
| 1,3диБImБ/0.5Cu(ТФА)2 | 0.1 |
| 1,3диБImБ/0.7Cu(ТФА)2 | 0.8 |
| 1,3диБImБ/1.0Cи(ТФА)2 | 0.06 |
| 1,3диБImБ/1.5Cu(ТФА)2 | 0.08 |
Как видно из табл. 2, степень десульфуризации увеличивается с увеличением количества молей соли металла в ИЖ и начинает снижаться, когда мольное соотношение превышает величину 0.7 для CuBr2 и 1.0 для Cu(ТФА)2. Эту закономерность можно объяснить, учитывая результаты исследований, приведенные в работе [32]. Высокая плотность, вязкость и электропроводность ИЖ без солей металлов связана с образованием некоторой упорядоченной структуры (ионные пары, ассоциаты) в молекуле ИЖ. Введение малых добавок солей металлов приводит к распаду ассоциатов, возрастанию удельной электропроводности и снижению вязкости; при дальнейшем же увеличении концентрации соли происходит связывание Br-аниона в крупный малоподвижный металлсодержащий комплексный ион.
Время и температуру экстракции подбирали экспериментально. На рис. 1 показано влияние температуры экстракции на степень удаления СС из ДТ на примере ЭС – 1,3диБImBr и 1,3диБImBrCuBr2.
Рис. 1.
Влияние температуры на степень удаления сернистых соединений из дизельных топлив на примере различных экстракционных систем: (а) 1 – 1,3диБImBr, 2 – 1,3диБImBrCuBr2; (б) 1 – 1Б3ОImBr, 2 – 1Б3ОImBrCо(ТФА).
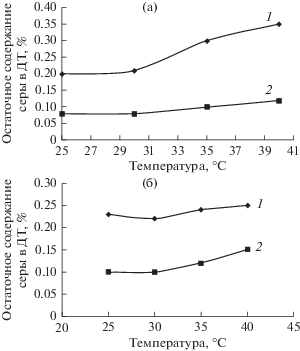
При увеличение температуры экстракции от 25 до 30°С степень удаления СС из ДТ не меняется, дальнейшее увеличение температуры влечет за собой снижение степени удаления СС. Исходя из этого, экстракцию СС ИЖ проводили при 25–30°С.
На рис. 2 на примере ЭC – 1,3-дибутилимидазолия бромида и 1-бутил-3-октилимидазолия бромида с солями Cu(ТФА)2 и СuBr2 показана зависимость остаточного содержания СС ДТ от времени экстракции.
Рис. 2.
Зависимость остаточного содержания сернистых соединений в дизельных топливах от времени экстракции при использовании в качестве экстракционных систем: (а) 1 – 1,3-диБImBr и 2 – 1,3-диБImBr-Сu(ТФА)2; (б) 1 – 1Б3ОImBr и 2 – 1Б3ОImBr-СuBr2..

Для ЭС на основе металлосодержащих ИЖ минимальное количество СС в ДТ остается при проведении процесса экстракции в течение 10 мин, дальнейшее увеличение времени экстракции не приводит к положительным результатам. Для ИЖ без солей металлов время экстракции для достижения минимального эффекта больше и составляет примерно 30–35 мин. Данный результат косвенно указывает на увеличение экстракционной емкости экстрагента при добавлении солей металлов – контактного времени 10 мин достаточно для достижения равновесия.
Далее рассмотрено влияние металла-комплексообразователя ИЖ на эффективность экстракции СС из ДТ.
Данные по остаточному содержанию СС в прямогонной дизельной фракции с пределами выкипания 200–360°С (ГОСТ 2177_99) после экстракции ЭС на основе хлоридов и трифторацетатов металлов и ИЖ – 1,3диБImBr, 1,3ди Б2МImBr и 1Б3ОImBr, представлены на рис. 3–5.
Рис. 3.
Зависимость остаточного содержания серы в дизельном топливе от вида используемой экстракционной системы (1,3диБImBr–соли металлов). Время экстракции – 10 мин, T = 25°C.
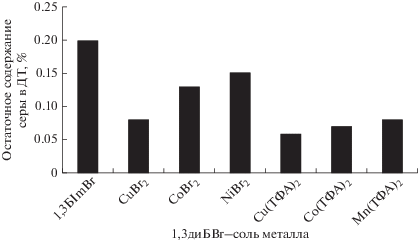
Рис. 4.
Зависимость остаточного содержания серы в дизельном топливе от вида используемой экстракционной системы (1,3диБ2МImBr–соли металлов). Время экстракции – 10 мин, T = 25°C.

Рис. 5.
Зависимость остаточного содержания серы в дизельном топливе от вида используемой экстракционной системы (1Б3ОImBr–соли металлов). Время экстракции – 10 мин, T = 25°C.

Гистограммы показывают влияние соли металла в составе экстракционной системы на остаточное содержание серы в ДТ.
Согласно данным, представленным на гистограммах, экстракция СС дизельного топлива ИЖ без солей металлов позволяет снизить содержание общей серы с 0.34 до 0.2–0.14 мас. %. Добавление солей металлов к ИЖ значительно улучшает коэффициент обессеривания, причем большая степень обессеривания достигается при использовании трифторацетатов металлов, но только с ИЖ на основе бутилимидазола. С ИЖ на основе 1Б3ОImBr и трифторацетатов металлов такого эффекта не наблюдается. Минимальное остаточное содержание серы достигает 0.06–0.05 мас. %. Можно предположить, что происходит комплексообразование между СС ДТ и солями металлов, присутствующими в составе ИЖ, т.е. идет комплексообразование при участии неподеленной пары электронов на атомах серы органических СС ДТ и незанятых орбиталей иона переходного металла. В присутствие ИЖ без соли металла может быть только π–π-взаимодействие между насыщенными связями органических СС ДТ и имидазольного кольца ИЖ.
ЗАКЛЮЧЕНИЕ
Проведен процесс экстракции СС ДТ ионными жидкостями на основе 1,3-дибутилимидазолиябромида и 1-бутил-3-октилимидазолий бромида и бромидов и трифторацетатов переходных металлов (Cu, Co, Ni).
Рассмотрено влияние температуры, времени экстракции и концентрации металла-комплексообразователя на степень удаления СС из ДТ и показано, что использование металлосодержацих ИЖ для экстракции позволяет значительно снизить содержание серы в ДТ (до 85 мас. %). Вероятно, присутствие солей металлов составе ИЖ, имеющих свободные молекулярные орбитали, приводит к комплексообразованию с СС ДТ, имеющими неподеленную электронную пару на атомах серы.
Список литературы
Ахметов С.А. Технология глубокой переработки нефти и газа. Уфа: Гилем, 2002. 669 с.
Ляпина Н.К. Химия и физикохимия сераорганических соединений нефтяных дистиллятов. М.: Наука, 1984. 120 с.
Харлампиди Х.Э., Мустафин Х.В., Чиркунов Э.В. // Вестник Казанского технологического университета. 1998. № 1. С. 76.
Wan Mokhtar W., Abu Bakar W., Rusmidah A. // J. of the Taiwan Institute of Chemical Engineers. 2014. V. 35. P. 314.
Сафаров Б.Ж., Шамсиева М.Б., Нормуродов Б.Р. // Молодой ученый. 2014. № 9. С. 200.
Сайфидинов Б.М. Автореферат дисс. на соискание к.х.н. С.-Петербургский гос. технологический институт. 2012. 18 с.
Колбин В.А., Дезорцев С.В., Теляшев Э.Г., Креймер М.Л., Ахметов А.Ф. // Башкирский химический журнал. 2016. Т. 23. № 1. С. 3.
Пыхалова Н.В., Аппазов А.Ю., Баламедова У.А. // Нефтепереработка и нефтехимия. 2012. №4. С. 12.
Смолянинов И.В., Кузьмин В.В., Джувалякова Н.С. // Геология, география и глобальная энергия. 2014. Т. 54. № 3. С. 126.
Kianpour E., Azizian S. // Fuel. 2014. V. 137. P. 36.
Гайле А.А., Сомов В.Е. Процессы разделения и очистки продуктов переработки нефти и газа. Учебное пособие. Изд: С.-Петербург. 2012. 396 с.
Gentry J., Khanmamedov T., Wytcherley R.W. // Chemistry and Technology of Fuels and Oils. 2002. V. 38. № 3. P. 150.
Anisimov A.V., Tarakanova A.V. // Russian J. of General Chemistry. 2009. V. 79. № 6. P. 1264.
Асланов Л.А., Анисимов А.В. // Нефтехимия. 2004. Т. 44. № 2. С. 83.
Zhao D., Wang Y., Duan E. // Molecules. 2009. V. 14. P. 4351.
Bösmann A., Datsevich L., Jess A., Lauter A., Schmitz C., Wasserscheid P. // Chem. Communications (Cambridge). 2001. V. 23. P. 2494.
Zhang S.G., Zhang Z.C. // Green Chemistry. 2002. V. 4. № 4. P. 376.
Zhang S.G., Zhang Q.L., Zhang Z.C. // Industrial & Engineering Chemistry Research. 2004. V. 43. № 2. P. 614.
Esser J., Wasserscheid P., Jess A. // Green Chemistry. 2004. V. 6. P. 316.
Nie Y., Li C.X., Wang Z.H. // Industrial & Engineering Chemistry Research. 2007. V. 46. № 15. P. 5108.
Wang J.L., Zhao D.S., Zhou E.P., Dong Z. // J. Fuel. Chem. Technol. 2007. V. 35. № 3. P. 293.
Gao H.S., Li Y.G., Liu Q.F., Li W.L., Liu H.Z. // Industrial & Engineering Chemistry Research. 2008. V. 47. № 21. P. 8384.
Hernandez A.J., Yang R.T. // Ind. Eng. Chem. Res. 2003. V. 42. P. 123.
Huang C. Chen B., Zhang J., Liu Z., Li Y. // J. Energy and Fuels. 2004. V. 18. P. 1862.
Likhanova N.V., Palou R.M., Santiago J.F.P. // Patent US № 8821716. 26.05.2009 г.
Ren T.-J., Zhang J., Hua Y.-H., Li J.-P., Liu M.-S., Zhao D.-Z. // Chinese Chemical Letters. 2015. V. 26. P. 1169.
Salwa M.I., Morsy, and Seham A. Shaban // Int. J. Curr. Microbiol. App. Sci. 2014. V. 3. № 1. P. 167.
Карякин Ю.В., Ангелов И.И. Чистые химические вещества. М.: Химия, 1974. 407с.
Глазунова Т.Ю. Дис. ... на соискание к.х.н. 2005. МГУ. Москва. 220 с.
Савинова И.А., Мин Р.С., Плюснин А.Н. // Сибирский химический журнал. 1992. № 1. С. 8.
Kobotaeva N., Skorohodova T., Andrienko O., Marakina E., Sachkov V. // Appl. Sci. 2018. V. 8. № 8. P. 1259.
Гришина Е.П., Раменская Л.М. // Известия вузов. Химия и хим. технология. 2016. Т. 59. № 6. С. 89.
Дополнительные материалы отсутствуют.


