Неорганические материалы, 2019, T. 55, № 10, стр. 1108-1115
Стеклование жидкости и замороженная деформация стекол
Д. С. Сандитов 1, 2, *, С. С. Бадмаев 1
1 Бурятский государственный университет
670000 Улан-Удэ, ул. Смолина, 24 а, Россия
2 Институт физического материаловедения СО Российской академии наук
670047 Улан-Удэ, ул. Сахьяновой, 6, Россия
* E-mail: sanditov@bsu.ru
Поступила в редакцию 11.10.2018
После доработки 04.04.2019
Принята к публикации 16.04.2019
Аннотация
Развивается представление, что у аморфных веществ в окрестности температуры стеклования происходят обратимые конфигурационные структурные изменения, сопровождающиеся локальным расширением и сжатием (делокализацией атомов). Они по природе аналогичны конфигурационным изменениям структуры стекол при их обратимой замороженной деформации и при ее термостимулированной релаксации.
ВВЕДЕНИЕ
Природа структурных изменений при переходах жидкость $ \rightleftarrows $ стекло остается не совсем ясной (см., например, [1–6]).
В данной статье с привлечением модели делокализованных атомов [2, 7, 8] проводится сравнение размягчения стекла с обратимой замороженной деформацией стеклообразных твердых тел, что позволяет получить определенную информацию о процессе стеклования. Наряду с этим обсуждается один из возможных вариантов перехода жидкость–стекло, основанный на выключении пускового механизма текучести – делокализации атома.
СТЕКЛОВАНИЕ ЖИДКОСТИ КАК СЛЕДСТВИЕ ЗАМОРАЖИВАНИЯ ПРОЦЕССА ДЕЛОКАЛИЗАЦИИ АТОМА
В силикатных стеклах делокализация атома представляет собой предельное смещение мостикового атома кислорода в Si–O–Si, связанное с локальной низкоактивационной деформацией кремнекислородной сетки из валентных связей [7, 8].
Полагаем, что делокализация атома – предельное смещение мостикового атома – служит необходимым условием реализации элементарного акта процесса вязкого течения неорганического стекла (например, переключения валентной связи [5]). Без делокализации атома (“пускового механизма” текучести) невозможно вязкое течение. Поэтому замораживание процесса делокализации активного атома в области стеклования приводит к прекращению вязкого течения и к переходу расплава в стеклообразное состояние.
Этот момент наступает тогда, когда энергия тепловых колебаний решетки, отнесенная к атому, становится равной или меньше энергии делокализации атома: $({i \mathord{\left/ {\vphantom {i 2}} \right. \kern-0em} 2})kT \leqslant \Delta {{\varepsilon }_{e}},$ что приводит к следующему условию перехода жидкость–стекло:
где $i$ – число степеней свободы кинетической единицы, ответственной за стеклование, Tg – температура перехода. Энергия делокализации атома тесно связана с упругой деформацией связи между атомами и равна работе предельного смещения атома, совершаемой против внутреннего давления pi, обусловленного силами межатомного (межмолекулярного) притяжения. Здесь Δve – элементарный флуктуационный объем, необходимый для смещения атома (объем делокализации атома) [2, 7].Как и следовало ожидать, в соответствии с критерием (1) энергия $\Delta {{\varepsilon }_{e}},$ определенная независимым способом (R – газовая постоянная)
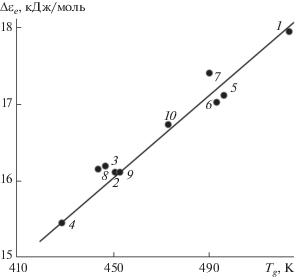
для натриевосиликатных стекол линейно зависит от температуры стеклования Tg (рис. 1). Здесь D – эмпирический параметр уравнения Енкеля [9, 10] успешно описывающего температурную зависимость вязкости ${\eta }(T)$ стеклообразующих жидкостей в широком интервале температур. У сульфатно-фосфатных стекол NaPO3–MSO4 (M = Li, Na, K) [11, 12] между энергией делокализации атома Δεe и температурой стеклования Tg также наблюдается линейная корреляция (рис. 2). Величина Δεe рассчитана по формуле (табл. 1) где с – эмпирическая постоянная в уравнении Брэдбури–Шишкина [13, 14] которое описывает зависимость η(T) в области стеклования.Рис. 1.
Корреляция между энергией делокализации атома Δεe и температурой стеклования Tg натриевосиликатных стекол Na2O–SiO2: $\Delta {{\varepsilon }_{e}} = RD$, где R – газовая постоянная, D – эмпирический параметр уравнения Енкеля для вязкости (5); cодержание Na2O, мол. %: 15 (1), 20 (2), 25 (3), 30 (4), 35 (5).
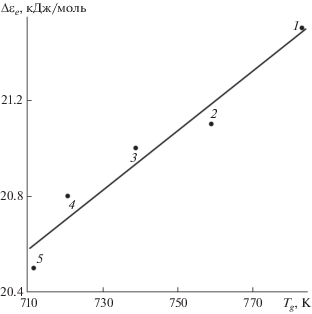
Таблица 1.
Свойства сульфатно-фосфатных стекол NaPO3–MSO4 (M = Li, Na, K) и параметры модели делокализованных атомов (использованы данные [11, 12])
| № | Стекло | Tg, K | E, МПа | ${\mu }$ | a | c, K | fg | $\Delta {{\varepsilon }_{e}}$, ${\text{кДж/моль}}$ | Δve, ${{{\AA}}^{3}}$ |
${{p}_{i}}$, $\frac{{{\text{кгс}}}}{{{\text{м}}{{{\text{м}}}^{{\text{2}}}}}}$ | HV, МПа |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| (9) | (4) | |||||||||||
| 1 | NaPO3 | 523 | 36 100 | 0.294 | 0.99 | 2160 | 0.016 | 17.9 | 17.9 | 16 | 195 | 1750 |
| 2 | 0.9NaPO3–0.1Li2SO4 | 451 | 41 400 | 0.300 | 0.97 | 1940 | 0.014 | 16.0 | 16.1 | 13 | 206 | 2000 |
| 3 | 0.8NaPO3–0.2Li2SO4 | 447 | 42 100 | 0.303 | 0.95 | 1950 | 0.013 | 16.1 | 16.2 | 14 | 205 | 2000 |
| 4 | 0.7NaPO3–0.3Li2SO4 | 429 | 42 300 | 0.034 | 0.95 | 1860 | 0.014 | 15.2 | 15.4 | 11 | 212 | 2150 |
| 5 | 0.9NaPO3–0.1Na2SO4 | 496 | 37 300 | 0.299 | 0.97 | 2060 | 0.016 | 17.0 | 17.1 | 14 | 207 | 1950 |
| 6 | 0.8NaPO3–0.2Na2SO4 | 493 | 35 500 | 0.292 | 0.96 | 2050 | 0.016 | 16.9 | 17.0 | 15 | 191 | 1900 |
| 7 | 0.7NaPO3–0.3Na2SO4 | 490 | 35 400 | 0.288 | 0.95 | 2095 | 0.015 | 17.1 | 17.4 | 16 | 172 | 1800 |
| 8 | 0.9NaPO3–0.1K2SO4 | 444 | 33 800 | 0.316 | 0.95 | 1945 | 0.013 | 16.0 | 16.1 | 16 | 175 | 2100 |
| 9 | 0.8NaPO3–0.2K2SO4 | 453 | 33 500 | 0.316 | 0.96 | 1940 | 0.014 | 16.0 | 16.1 | 15 | 185 | 2050 |
| 10 | 0.7NaPO3–0.3K2SO4 | 473 | 33 400 | 0.313 | 0.99 | 2015 | 0.014 | 16.8 | 16.7 | 16 | 180 | 2000 |
При выводе уравнений вязкости (3) и (5) в рамках модели делокализованных атомов и активационной теории вязкости величины RD и Rc приобретают смысл энергии делокализации атома Δεe [2, 15]:
(6)
${\eta } = {{{\eta }}_{0}}\exp \left\{ {\frac{{\Delta {{F}_{\infty }}}}{{kT}} + \frac{{\Delta {{v}_{e}}}}{v}\left[ {\exp \left( {\frac{{\Delta {{{\varepsilon }}_{e}}}}{{kT}}} \right) - 1} \right]} \right\},$(7)
${\eta } = {{{\eta }}_{0}}\exp \left[ {\left( {\frac{v}{{\Delta {{v}_{e}}}}} \right)\exp \left( {\frac{{\Delta {{\varepsilon }_{e}}}}{{kT}}} \right)} \right].$В результате делокализации (тепловых смещений) атомов в жидкостях и аморфных твердых телах возникает флуктуационный объем Δ${{V}_{e}}$ = = NeΔve, где Ne – число делокализованных атомов. У неорганических стекол, металлических аморфных сплавов, аморфных органических полимеров и низкомолекулярных органических стекол доля флуктуационного объема fg, замороженная при температуре стеклования Tg, слабо зависит от природы стекол (табл. 2)
(8)
${{f}_{g}} = {{\left( {\frac{{\Delta {{V}_{e}}}}{V}} \right)}_{{T = {{T}_{g}}}}} \approx 0.025 - 0.030.$Таблица 2.
Параметры уравнения ВЛФ C1, C2 и доля флуктуационного объема fg, замороженная при температуре стеклования Tg [2, 7, 8]
| Аморфное вещество | Tg, К | C1 | C2, К | fg | ln(1/ fg) | Δεe, кДж/моль |
|---|---|---|---|---|---|---|
| Натриевосиликатные стекла Na2O–SiO2 | ||||||
| Na2O, мол. % | ||||||
| 15 | 782 | 36 | 430 | 0.028 | 3.6 | 23 |
| 20 | 759 | 36 | 390 | 0.028 | 3.6 | 23 |
| 25 | 739 | 35 | 355 | 0.028 | 3.6 | 22 |
| 30 | 721 | 35 | 322 | 0.028 | 3.6 | 22 |
| 33 | 712 | 35 | 304 | 0.028 | 3.6 | 21 |
| 35 | 705 | 35 | 291 | 0.028 | 3.6 | 21 |
| Металлические стекла (аморфные сплавы) | ||||||
| Pd40Ni40P20 | 602 | 39 | 93 | 0.026 | 3.6 | 18 |
| Pt60Ni15P25 | 500 | 37 | 95 | 0.027 | 3.6 | 15 |
| Pd77.5Cu6Si16.5 | 653 | 38 | 100 | 0.026 | 3.6 | 19 |
| Fe80P13C7 | 736 | 38 | 120 | 0.026 | 3.6 | 22 |
| Аморфные органические полимеры и селен | ||||||
| Поливинилацетат | 305 | 36 | 47 | 0.028 | 3.6 | 9 |
| Натуральный каучук | 300 | 38 | 54 | 0.026 | 3.6 | 9 |
| Метакрилат этиловый | 335 | 40 | 65 | 0.025 | 3.6 | 10 |
| Селен | 303 | 32 | 58 | 0.031 | 3.5 | 9 |
| Низкомолекулярные органические стекла | ||||||
| Пропанол | 98 | 41 | 25 | 0.024 | 3.7 | 3 |
| Пропиленгликоль | 160 | 44 | 40 | 0.023 | 3.8 | 5 |
| Глицерин | 185 | 42 | 53 | 0.024 | 3.7 | 6 |
У стекол одного типа она практически постоянна. Например, у натриевосиликатных стекол: fg ≈ ≈ const = 0.028 (табл. 2). Величина fg определяется по данным о вязкости в области стеклования [7, 8]. У сульфатно-фосфатных стекол значения fg меняются также в небольших пределах (fg ≈ const), однако они заметно ниже, чем у силикатных стекол (табл. 1). Доля флуктуационного объема fg входит в формулы модели делокализованных атомов (см., например, (9)).
При размягчении стекла появляются состояния, не характерные для стеклообразных твердых тел [16, 17]. Было развито представление о том, что выше Tg в стеклообразующих жидкостях существует возбужденное состояние, отличающееся от основного состояния небольшим избытком энергии [17]. Исходя из подобных работ предполагаем, что вязкое течение расплавов неорганических стекол выше Tg реализуется за счет возбужденных делокализованных мостиковых атомов с энергией возбуждения $\Delta {{\varepsilon }_{e}}$. У щелочносиликатных стекол эта энергия составляет (табл. 2)
(9)
$\Delta {{\varepsilon }_{e}} \approx R{{T}_{g}}\ln (1/{{f}_{g}}) \approx {{20}^{{}}}{\text{кДж}}{\text{/}}{\text{моль}}{\text{.}}$При охлаждении стеклообразующего расплава относительное число делокализованных атомов (Ne/N), ответственных за вязкое течение выше Tg, в интервале стеклования уменьшается до ничтожно малого значения, порядка 3%
что равносильно их замораживанию (N – число атомов). При T = Tg замораживается процесс делокализации атома (переход активной частицы из основного состояния в возбужденное). В процессе размягчения стекла при нагревании постепенно размораживается процесс делокализации атома и количество делокализованных атомов возрастает от малых значений в замороженном состоянии до концентрации (Ne/N), соответствующей жидкому состоянию.“ПЛАСТИЧНОСТЬ” СТЕКЛА И ДЕЛОКАЛИЗАЦИЯ АТОМА
Эффект пластичности неорганических стекол впервые обнаружили Бриджмен и Саймон [18] и позже детально изучили другие исследователи [19, 20]. Опыты показали, что стекла могут “пластически” уплотняться как при одноосном, так и при всестороннем сжатии, если механическое напряжение (давление) превышает некоторый порог σy, который для силикатных стекол при 20°С составляет около
Однако примечательно то обстоятельство, что при нагревании ниже температуры стеклования и вблизи Tg данная деформация релаксирует до исчезновения. Следовательно, она оказывается замороженной обратимой деформацией (см. [3]). Тем не менее, следуя многим авторам, будем пользоваться термином “пластическая”, а величину σy назовем пределом текучести (“пластичности”).
Аналогичная замороженная обратимая деформация (по ранней терминологии – вынужденноэластическая деформация [21]) наблюдается у аморфных органических полимеров [22, 23]. У массивных металлических стекол недавно обнаружены замороженная деформация и ее термостимулированная релаксация [24], основные закономерности которых фактически такие же, как и у стеклообразных органических полимеров и неорганических стекол.
Скорость процессов уплотнения и термостимулированного разуплотнения стекол зависит от температуры экспоненциально [18, 19, 23]. Энергия активации этих процессов у щелочносиликатных стекол составляет около: Δu ≈ 20 кДж/моль.
Таким образом, замороженная обратимая деформация стекол оказывается низкоактивационным релаксационным процессом.
“Пластичность” хрупких неорганических стекол удобно изучать измерением микротвердости. При вдавливании алмазной пирамидки Виккерса и других заостренных инденторов в силикатное стекло при 20°С образуется “пластическая” лунка – микроотпечаток (рис. 3). При этом микротвердость по Виккерсу HV у силикатных, германатных и ряда других неорганических стекол совпадает с пределом текучести HV ≈ σy, выше которого наблюдается “пластическая” деформация [3, 25].
Рис. 3.
Микроотпечатки Виккерса на листовом силикатном стекле: a – при t = 20°C; б, в – виды в интерференционном микроскопе после нагрева соответственно при t = 100 и 450°C в течение 10 мин; P = 1.50 Н, tg = 620°C.

Как и следовало ожидать, при нагревании ниже и вблизи Tg микроотпечаток уменьшается и постепенно исчезает – залечивается (рис. 3). Энергия активации этого процесса у силикатных стекол составляет ∼20 кДж/моль [3].
Представление о том, что элементарный акт замороженной деформации стекол сводится к делокализации атома (кинетической единицы), находится в удовлетворительном согласии с экспериментальными данными: расчеты предела текучести и энергии активации этой деформации согласуются с экспериментом [3, 25]. Энергия активации “пластической” деформации силикатных стекол Δu ≈ 20 кДж/моль совпадает с энергией делокализации атома в них Δu ≈ $\Delta {{\varepsilon }_{e}}$.
Предел текучести σy имеет смысл напряжения, необходимого для критического смещения (делокализации) кинетической единицы. По величине σy совпадает с внутренним давлением
против которого совершается работа делокализации атома. Принимая во внимание равенство σy = pi и соотношение для энергии делокализации атома Δεe (9), приходим к следующей связи между пределом текучести σy и температурой размягчения (температурой стеклования) TgКак отмечалось выше, в качестве кинетических единиц, способных к делокализации, в неорганических стеклах выступают мостиковые “шарнирные” атомы типа мостикового атома кислорода в Si–O–Si. Поэтому объем делокализации атома Δve у стекол одного класса фактически одинаков: Δve ≈ const [2, 7, 8].
В соответствии с формулой (12) при fg ≈ const и ΔVe ≈ const для стекол одного типа должна наблюдаться линейная корреляция между величинами σy и Tg, а также между HV и Tg. В самом деле, у аморфных полимеров между σy и Tg обнаруживается линейная корреляция (рис. 4) [3, 25, 26]. Как видно из рис. 5 и 6, микротвердость (предел текучести) ряда стекол также линейно зависит от температуры стеклования Tg [3, 27].
Рис. 4.
Линейная корреляция между пределом текучести σy и температурой стеклования Tg аморфных полимеров: 1 – политетрафторэтилен, 2 – полиэтилен, 3 – полипропилен, 4 – полиамид, 5 – полиэтилентерефталат, 6 – поливинилхлорид, 7 – поликарбонат, 8 – полиарилатсульфон, 9 – полисульфон, 10 – полиарилат.
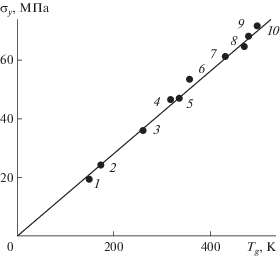
Рис. 5.
Корреляция между микротвердостью HV и температурой стеклования силикатных стекол: 1 – свинцовосиликатное, 2 – щелочносиликатные, 3 – алюмосиликатные, 4 – кварцевое.
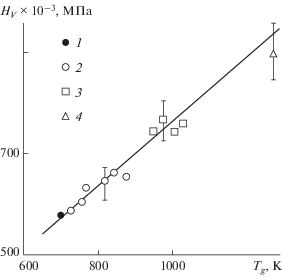
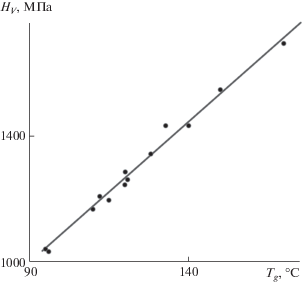
Рис. 6.
Линейная корреляция между HV и Tg для бескислородных халькогенидных стекол системы мышьяк–теллур–алюминий при различных содержаниях компонентов [27].
Таким образом, данный подход дает один из вариантов объяснения наличия линейной корреляции между пределом текучести и температурой размягчения стекол.
Скорость термостимулированного восстановления “пластически” деформированных стеклообразных полимеров vrel как функция температуры и давления подчиняется следующей экспоненциальной зависимости [23]:
Для эпоксидного сеточного аморфного полимера получено значение активационного объема данного релаксационного процесса, равное [23]В модели делокализованных атомов скорость термостимулированного восстановления исходного недеформированного состояния стекла (13) определяется скоростью изменения числа делокализованных атомов в данном процессе
откуда зависимость (13) выводится из уравнения модели для относительного числа делокализованных атомов [7](15)
$\frac{{{{N}_{e}}}}{N} = \exp \left( { - \frac{{\Delta {{\varepsilon }_{e}} + p\Delta {{v}_{e}}}}{{kT}}} \right).$Активационный объем Δvy получает следующую трактовку: Δvy = Δve. У сетчатых эпоксидных полимеров типа модифицированной эпоксидной смолы ЭД-16 значения объема делокализации атома Δve, рассчитанные по формуле модели [7, 8]:
(16)
$\Delta {{v}_{е}} = \frac{{3(1 - 2{\mu })k{{T}_{g}}}}{{{{f}_{g}}E}} \approx 45 - 74\,{{{\AA}}^{3}},$Процессу “делокализации атома” в стеклообразных органических полимерах соответствует предельное смещение небольшого участка основной цепи макромолекулы (группы атомов в соединительном звене) [7, 8].
СТРУКТУРНЫЕ ИЗМЕНЕНИЯ ВБЛИЗИ ТЕМПЕРАТУРЫ СТЕКЛОВАНИЯ ЖИДКОСТЕЙ
Анализ изменения энтропии, объема и свободной энергии при стекловании жидкости привел Кауцмана [29] к заключению, что при переходе через Tg замораживаются внутренние степени свободы кинетических единиц. Последние, скорее всего, являются конфигурационными степенями свободы, ибо только конфигурационные степени свободы (а не поступательные и вращательные) могут вносить вклад в потенциальную энергию системы [16]. А в стекле замораживается избыток потенциальной энергии и энтропии.
Делокализация атома обусловлена перегруппировкой соседних частиц и отражает локальное конфигурационное структурное изменение. При термостимулировании стекла (при нагреве до Tg) процесс делокализации атома размораживается и атом возвращается в равновесное положение. При этом вблизи точки стеклования происходят обратимые конфигурационные структурные изменения, реализуемые при небольших смещениях атома или структурных групп (кинетических единиц).
Такие же обратимые конфигурационные изменения структуры происходят при замороженной обратимой деформации стекол, а также при ее термостимулированной релаксации. Это положение подтверждается линейной корреляцией между температурой размягчения (температурой стеклования) Tg и пределом текучести σy, выше которого наблюдается “пластическая” деформация стекол (рис. 4–6). Размягчение стекла при нагревании в области Tg и его “пластическая” деформация под действием механического напряжения σ > σy при 20°С характеризуются общим молекулярным механизмом – делокализацией атома, связанной с локальным конфигурационным структурным изменением.
Таким образом, сравнение размягчения стекла с обратимой замороженной деформацией стеклообразных твердых тел подтверждает предположение о том, что в окрестности температуры стеклования происходят обратимые конфигурационные структурные изменения, связанные со смещением (делокализацией) атомов из равновесных положений.
В связи с этим отметим модель Беленького [30], с помощью которой показано, что в металлических стеклах в окрестности температуры стеклования происходят структурные превращения, состоящие в обратимом перераспределении структурных единиц, характеризуемых локальной дилатацией (расширением и сжатием). Этот вывод можно отнести и к другим стеклующимся системам, ибо основные закономерности процесса стеклования в качественном отношении оказываются одинаковыми для всех аморфных веществ независимо от их природы: для аморфных органических полимеров, неорганических стекол, металлических аморфных сплавов, водных растворов, халькогенидов и т.д. (см. [2, 3]), что, в частности, подтверждается наличием в области стеклования универсальных уравнений и правил: правила Симхи – Бойера, уравнения Бартенева–Ритланда, правила “двух третей”, уравнения Вильямса–Ландела–Ферри и др. (см. [3]).
При обсуждении природы перехода жидкость–стекло, в частности, обсуждая структурные изменения в области стеклования, необходимо иметь ввиду, что величина Tg не является константой (как температура кристаллизации), на нее оказывает влияние температурно-временной режим, например, быстрота изменения температуры в процессе охлаждения стеклообразующих жидкостей.
В связи с зависимостью температуры стеклования Tg от скорости охлаждения расплава рядом исследователей в дилатометрии стекол было предложено пользоваться понятием о стандартной скорости охлаждения
принятой в технологии стекла (см., например, [31, 32]). Ввиду относительно слабой (полулогарифмической) зависимости Tg(q) небольшие отклонения q от стандартного значения особо не сказываются на величине Tg, за редкими исключениями. При изменении q в 10 раз температура стеклования смещается лишь на малую величину ΔT ≈ 0.03Tg [31, 32]. Обычно полагают, что подавляющее большинство данных о Tg относится к стандартной скорости охлаждения (нагревания). Для других значений q данных мало.Влияние различных факторов, в первую очередь температурно-временных режимов, на значения температуры стеклования подробно обсуждается в работе Мазурина [33]. Рекомендованы наиболее рациональные условия измерений температур стеклования. В дилатометрах, например, рекомендуется скорость нагревания, равная 5 K/мин (близкая к стандартному значению). Как следует из анализа Мазурина, широко распространенное представление, что для всех стекол температура стеклования соответствует температуре, при которой вязкость стекла равна 1013 Пз, не оправдывается. “В то же время для большинства исследованных до сих пор стекол значения Tg (полученные в условиях, близких к стандартным) соответствуют температурам, при которых вязкость находится в пределах от 1012 до 1013 Пз” [33].
ЗАКЛЮЧЕНИЕ
Из модели делокализованных атомов вытекает линейная корреляция между температурой стеклования жидкости Tg и пределом текучести – механическим напряжением σy, выше которого при 20°С наблюдается замороженная обратимая деформация стекол, что подтверждается экспериментальными данными. Отсюда можно предположить, что в окрестности температуры Tg происходят такие же обратимые конфигурационные изменения структуры, которые наблюдаются при замороженной обратимой деформации стекол. Размягчение стекла при нагревании в области T = Tg и обратимая замороженная деформация стекла под действием механического напряжения при 20°С определяются одним и тем же молекулярным механизмом, а именно делокализацией атома – его предельным смещением из равновесного положения, которое связано с локальным конфигурационным изменением структуры.
Развито представление о том, что делокализация атома – предельное смещение активного атома – служит необходимым условием реализации элементарного акта вязкого течения стекол и их расплавов. Поэтому замораживание процесса делокализации атома (“пускового механизма” текучести) в области стеклования приводит к прекращению вязкого течения и к переходу расплава в стеклообразное состояние. Этот момент наступает тогда, когда энергия тепловых колебаний решетки, отнесенная к атому, становится равной или меньше энергии делокализации атома. Отсюда следует определенный критерий стеклования.
Список литературы
Тропин Т.В., Шмельцер Ю.В.П., Аксенов В.Л. Современные аспекты кинетической теории стеклования // Успехи физ. наук. 2016. Т. 186. № 1. С. 47–73.
Sanditov D.S., Ojovan M.I. On Relaxation Nature of Glass Transition in Amorphous Materials // Physica B. 2017. V. 523. P. 96–113.
Сандитов Д.С., Бартенев Г.М. Физические свойства неупорядоченных структур. Новосибирск: Наука, 1982. 259 с.
Ростиашвили В.Г., Иржак В.И., Розенберг Б.А. Стеклование полимеров. Л.: Химия, 1987. 192 с.
Мюллер Р.Л. Химические особенности полимерных стеклообразующих веществ и природа стеклообразования // Стеклообразное состояние. Тр. III Всесоюз. совещ. М.–Л.: Изд-во АН СССР, 1959. С. 61–71.
Мазурин О.В. Стеклование. Л.: Наука, 1986. 158 с.
Сандитов Д.С. Модель делокализованных атомов в физике стеклообразного состояния // ЖЭТФ. 2012. Т. 142. Вып. 1(7). С. 123–137.
Сандитов Д.С., Бадмаев С.С. Делокализация атома в стеклах и их расплавах // Физика и химия стекла. 2015. Т. 40. № 5. С. 621–630.
Jenckel E. Zur temperaturabhängigkeit der Viskosität Von Schmelzen // Z. Physik. Chem. 1939. B. 184. № 1. S. 309–319.
Meerlender G. Die erweiterte Jenckel-Gleichung, eine leistungsfähige Viskositäts – temperature – formel. I, II // Rheol. Acta. 1967. V. 6. № 4. S. 309–377.
Мамошин В.Л. Структурные особенности и свойства неупорядоченных конденсированных систем на основе сульфатов и полифосфатов: Автореф. дис. … докт. хим. наук. Свердловск: УПИ им. С.М. Кирова, 1990. 40 с.
Сандитов Д.С., Мамошин В.Л., Архипов В.Г. Применение теории свободного объема к сульфатно-фосфатным стеклам и их расплавам // Физика и химия стекла. 1993. Т. 19. № 4. С. 593–601.
Bradbury D., Mark M., Kleinschmidt R.V. Viscosity and density of lubricating oils from 0 to 150000 Psig and 32 to 425 F // Trans. Am. Soc. Mech. Eng. 1951. V. 73. № 5. P. 667–676.
Шишкин Н.И. Зависимость кинетических свойств жидкостей и стекол от температуры, давления и объема // Журн. техн. физики. 1956. Т. 26. Вып. 7. С. 1461–1473.
Сандитов Д.С. Модель вязкого течения стеклообразующих жидкостей и стекол // ДАН. 2013. Т. 451. № 6. С. 650–654.
Немилов С.В. Развитие представлений о характере внутренних изменений систем при переходе стекло-жидкость // Физика и химия стекла. 1980. Т. 6. № 3. С. 257–268.
Leidecker H.W., Simmons J.H., Litovitz J.H., Macedo P.B. Degenerate Excited State in the Structure of B2O3 // J. Chem. Phys. 1971. V. 55. № 5. P. 2028–2031.
Bridgman P.W., Simon I. Effects of Very High Pressures on Glass // J. Appl. Phys. 1953. V. 24. P. 405–413.
Mackenzie J.D. High-Pressure Effects on Oxide Glasses. II Subsequent Heat Treatment // J. Am. Ceram. Soc. 1963. V. 46. P. 470–476.
Шишкин Н.И. Стеклование жидкостей и полимеров под давлением. V. Образование уплотненных стекол // ФТТ. 1960. Т.2. С. 350–357.
Лазуркин Ю.С., Фогельсон Р.Л. О природе больших деформаций высокомолекулярных веществ в стеклообразном состоянии // Журн. техн. физики. 1954. Т. 21. С. 267–279.
Олейник Э.Ф., Руднев С.Н., Саламатина О.Б., Котелянский М.И. Механизм неупругой деформации в твердых полимерах: твердотельные и жидкоподобные процессы // Высокомолек. соединения. Сер. А. 2008. Т. 50. № 5. С. 773–788.
Магафуров И.Ш., Тополкараев В.А., Маркарян Р.Е., Олейник Э.Ф. Восстановление размеров деформированных полимерных стекол под давлением // Высокомолек. соединения. Сер. Б. 1991. Т. 32. № 2. С. 147–150.
Чах К., Ляхов С.А., Хоник В.А. Обратимая вязкоупругая деформация массивного металлического стекла // Деформация и разрушение материалов. 2006. № 8. С. 22–25.
Сандитов Д.С., Сангадиев С.Ш., Сандитов Б.Д. Пластичность и вязкость стеклообразных материалов // Деформация и разрушение материалов. 2013. № 3. С. 2–7.
Козлов Г.В., Сандитов Д.С. Ангармонические эффекты и физико-механические свойства полимеров. Новосибирск: Наука, 1994. 261 с.
Дунаев А.А., Борисова З.У., Михайлов М.Д., Братов А.В. Синтез и свойства стекол системы мышьяк–теллур–алюминий // Физика и химия стекла. 1980. Т. 6. № 2. С. 174–178.
Филянов Е.М. Активационные параметры пластической деформации и структура стеклообразных сетчатых полимеров // Высокомолек. соединения. Сер. А. 1987. Т. 29. № 5. С. 975–982.
Kauzmann N. The Nature of the Glassy State and the Behavior of Liquids at Low Temperatures // Chem. Rev. 1948. № 2. P. 219–256.
Беленький А.Я. Обратимые структурные изменения в аморфных металлических сплавах вблизи точки стеклования // Журн. физ. химии. 1983. Т. 57. № 4. С. 950–953.
Бартенев Г.М. Строение и механические свойства неорганических стекол. М.: Стройиздат, 1966. 216 с.
Бартенев Г.М., Лукьянов И.А. Зависимость температуры стеклования аморфных веществ от скорости нагревания и связь температуры стеклования с энергией активации // Журн. физ. химии. 1955. Т. 29. № 8. С. 1486–1498.
Мазурин О.В. Проблемы обеспечения совместимости значений температур стеклования, публикуемых в мировой литературе // Физика и химия стекла. 2007. Т. 33. № 1. С. 34–55.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы