Неорганические материалы, 2019, T. 55, № 9, стр. 969-974
Синтез и свойства наноразмерных пленок, сформированных термооксидированием MnO2/InP под воздействием Mn3(PO4)2
И. Я. Миттова 1, *, Б. В. Сладкопевцев 1, А. А. Самсонов 1, Е. В. Томина 1, С. Ю. Андреенко 1, П. В. Костенко 1
1 Воронежский государственный университет
394018 Воронеж, Университетская пл., 1, Россия
* E-mail: imittova@mail.ru
Поступила в редакцию 14.02.2019
После доработки 10.04.2019
Принята к публикации 12.04.2019
Аннотация
При термическом оксидировании InP положительный эффект совместного воздействия нанесенных на его поверхность слоев MnO2 и вводимого через газовую фазу Mn3(PO4)2 состоит в увеличении темпа прироста толщины пленок, быстром химическом связывании индия с блокированием его диффузии в пленку и интенсификации процессов фосфатообразования, что приводит к формированию наноразмерных диэлектрических пленок, удельное сопротивление которых достигает 1010 Ом см.
ВВЕДЕНИЕ
Фосфид индия, как и арсенид галлия, характеризуется энергетическими параметрами монокристаллической фазы, очень близкими к параметрам монокристаллического кремния, что дает возможность изготавливать на его основе гибридные приборы интегральной электроники. На полупроводниках АIIIВV также возможно создание гетероструктур, используемых для преобразования солнечной энергии в электрическую [1, 2]. Одним из факторов, ограничивающих применение InP в современном материаловедении, микроэлектронике и вообще в электронных технологиях, является сложность формирования на этом материале наноразмерных диэлектрических и полупроводниковых пленок с воспроизводимыми стабильными характеристиками технологичными и экономичными способами.
На арсениде галлия искомый результат был достигнут нанесением на поверхность полупроводника методом магнетронного распыления наноразмерного слоя MnO2 c последующим термооксидированием сформированной гетероструктуры [3]. Результатом явились диэлектрические пленки с удельным сопротивлением порядка 1010 Ом см и электрической прочностью (5–8) × 106 В/см [4]. Для InP также показано, что MnO2 эффективно увеличивает рост пленок, обусловливает их регулярную структуру на наноуровне и отсутствие омической проводимости, свойственной собственным оксидам [5]. Однако диэлектрические пленки с приемлемыми технологическими характеристиками не получены. Это объясняется различием в стадиях собственного оксидирования GaAs и InP: в первом случае выделяющийся As концентрируется на внутренней границе раздела [6] и нанесенный MnO2 как хемостимулятор переводит его в окисленное состояние, что резко улучшает качество пленок. Во втором случае (InP) отсутствие омической проводимости под влиянием MnO2 объясняется доокислением индия, ликвидирующим омическую проводимость в пленках [5], однако, по всей видимости, избежать заметного испарения оксидов фосфора и сопутствующего порообразования не удается. Представляется целесообразным компенсировать потерю фосфат-анионов в процессе термооксидирования добавлением модификатора состава и структуры пленок. Ясно, что фосфат-анионы имеет смысл вводить в систему в сочетании с катионом, уже давшим положительные результаты по воздействию на скорость роста и свойства пленок. Помимо отмеченного положительного воздействия оксидов марганца на процессы термооксидирования бинарных полупроводников [4, 5], появляется все больше публикаций, касающихся роли марганца в модификации свойств самых различных наноматериалов [7–9].
Цель данной работы – синтез диэлектрических пленок термооксидированием MnO2/InP под воздействием Mn3(PO4)2, вводимого через газовую фазу, и установление влияния состава сформированных оксидных пленок на их электрофизические свойства.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве подложек использовали полированные пластины InP ФИЭ-1А (100), легированного оловом, с концентрацией основных носителей заряда при 300 K не менее 5 × 1016 см–3, собственным n-типом проводимости, предварительно обработанные травителем состава H2SO4 (ХЧ ГОСТ-4204-77, 92.80%-ная) : Н2О2 (ОСЧ ТУ 6-02-570-750, 56%-ная) : Н2О = 2 : 1 : 1 в течение 10 мин и многократно промытые в бидистиллированной воде. Образцы MnO2/InP синтезировали методом магнетронного распыления мишени из оксида марганца (чистота 99.8%) в аргоновой атмосфере на установке Angstrom engineering CoVap II, режим напыления полностью аналогичен описанному в [5].
Синтез фосфата марганца(II) проводили по методике [10] с использованием: MnCl2 ∙ 4H2O (“ч. д. а.”), ГОСТ 612-67; (NH4)2HPO4 (“ч. д. а.”), ГОСТ 3771-64. Методом рентгенофазового анализа (ДРОН-3) подтверждено образование осадка целевого продукта.
Навеску Mn3(PO4)2 (m = 0.3 г) помещали в цилиндрический кварцевый контейнер (до отметки на этом контейнере), крышкой которого служил образец MnO2/InP, рабочая сторона которого находилась на фиксированном расстоянии (10 мм) от поверхности фосфата. Образцы термооксидировали в печи резистивного нагрева (МТП-2М-50-500) в потоке кислорода (объемная скорость 30 л/ч) при температурах 450, 475, 500, 530 и 550°С. Через каждые 10 мин образец извлекали из реактора и определяли толщину образовавшейся оксидной пленки методом лазерной эллипсометрии (ЛЭ, ЛЭФ-754, HeNe-лазер с длиной волны излучения 632.8 нм). После этого термооксидирование продолжали при обновленной навеске модификатора. Максимальное время оксидирования составляло 60 мин. Метод спектральной эллипсометрии (СЭ, “Эллипс-1891”, диапазон длин волн 250–1100 нм) был выбран для подтверждения адекватности применения однослойной модели или корректировки результатов ЛЭ [11].
Фазовый, химический и элементный составы пленок определяли методами РФА, инфракрасной спектроскопии (ИКС, ИК-Фурье-спектрометр Vertex 70) и локального рентгеноспектрального микроанализа (ЛРСМА, JEOL-6510LV с системой энергодисперсионного микроанализа Bruker соответственно). Для определения удельного сопротивления ρ (Ом см) использовали универсальный мультиметр Agilent 344 10A, на поверхность образцов предварительно в вакууме магнетронно напыляли алюминиевые контакты площадью 5 × 10–3 см2. В процессе измерения ρ сразу учитывалась толщина сформированной пленки, поэтому дополнительных пересчетов к размерности (Ом см) не требовалось.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Кинетические изотермы в двойных логарифмических координатах процесса термооксидирования гетероструктур MnO2/InP при введении в реакционную зону Mn3(PO4)2 через газовую фазу (MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$) представлены на рис. 1. Рассчитанные по рассмотренному в [4, 5] уравнению величины показателя n (табл. 1) отвечают интервалу 0.11–0.15; nср, равное 0.13, значительно меньше 0.5, что реализуется в случае твердофазного процесса, лимитируемого диффузией в твердой фазе. Величина эффективной энергии активации (ЭЭА), равная 110 кДж/моль (табл. 1), также типична для реакции твердое–твердое без каталитического эффекта [12], однако дополнительное использование в процессе Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ привело к снижению величины ЭЭА до 110 кДж/моль по сравнению с ~180 кДж/моль для MnO2/InP без его добавления [5].
Рис. 1.
Кинетические изотермы в двойных логарифмических координатах процесса термооксидирования MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ (а) и аррениусовская зависимость усредненной константы скорости процесса lnkср = f(103/RT) (б).
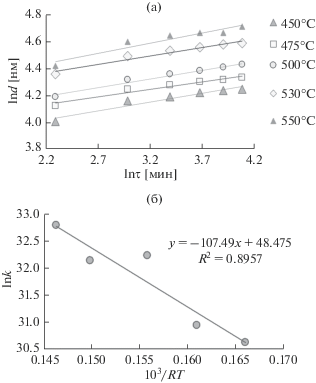
Таблица 1.
Кинетические параметры процесса термооксидирования MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}},$ рассчитанные по степенному уравнению d = (kτ)n
| Параметры оксидирования | n ± Δn, нм1/n/мин | |
|---|---|---|
| t, °C | ln kср | |
| 450 | 30.621 | 0.12 ± 0.0049 |
| 475 | 30.943 | 0.11 ± 0.0059 |
| 500 | 32.131 | 0.13 ± 0.0064 |
| 530 | 32.221 | 0.13 ± 0.0074 |
| 550 | 32.769 | 0.15 ± 0.0078 |
| ncp | 0.13 ± 0.0059 | |
На рис. 2 представлены кривые относительного увеличения толщины пленок, выращенных термооксидированием MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}},$ относительно эталонов – собственного термооксидирования InP и MnO2/InP [5], рассчитанные по формулам
Рис. 2.
Зависимости относительного увеличения темпа роста оксидной пленки от времени термического оксидирования образцов MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ при различных температурах в сравнении с эталоном InP (а); в сравнении с MnO2/InP (б).
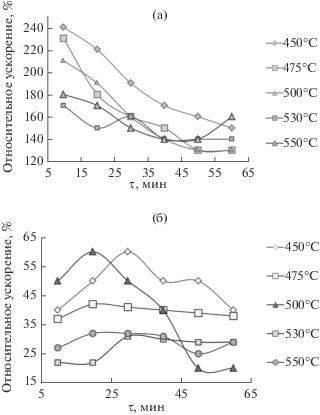
Для синтезированных образцов во всем исследованном температурно-временном диапазоне относительное увеличение толщины пленки составляет 1.5–2 раза (150–200%) по сравнению с оксидированием InP, а в сравнении с оксидированием MnO2/InP – от 30 до 40% на начальном этапе процесса (в первые 20 мин, рис. 2б).
Формируемые наноразмерные оксидные пленки являются слабопоглощающими, в пользу чего свидетельствуют отсутствие неокисленного индия в них (рис. 3) и хорошая сходимость спектров эллипсометрических параметров Ψ и Δ, полученных экспериментально и рассчитанных по модели Коши (рис. 3). В их состав входят оксиды MnO2 и In2O3, а также фосфаты In(PO3)3, InPO4, In2(P2O7), Mn2P2O7, Mn3(PO4)2 (РФА, табл. 2, идентификацию фаз осуществляли по [13]). Данные ИКС для образцов MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ коррелируют с данными РФА и свидетельствуют о разнообразии соединений – различных фосфатов индия и марганца, образующихся в результате термооксидирования. ИК-спектр поглощения образца, сформированного в режиме 450°С, 60 мин, в качестве примера представлен на рис. 4 (расшифровка ИК-спектров проведена на основе [14]).
Рис. 3.
Спектры эллипсометрических параметров ψ (1, 2) и ∆ (3, 4) для образца, полученного оксидированием MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ (500°С, 60 мин) (2, 3 – измеренные, 1, 4 – рассчитанные по модели Коши).
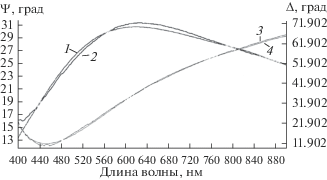
Таблица 2.
Идентифицированные фазы при термооксидировании MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ при различных температурах в течение 60 мин
| t, °C | dhkl | Фаза |
|---|---|---|
| 450 | 9.4523 | In(PO3)3 |
| 7.6641, 3.5589 | Mn2P2O7 | |
| 4.43 | InPO4 | |
| 4.4193, 8.1265 | Mn3(PO4)2 | |
| 475 | 9.4524 | In(PO3)3 |
| 6.919 | MnO2 | |
| 6.9315 | Mn2P2O7 | |
| 3.5498, 3.5396 | Mn3(PO4)2 | |
| 500 | 2.3870 | In2O3 |
| 7.264 | In2(P2O7) | |
| 3.5713, 8.1265, 3.5686 | Mn3(PO4)2 | |
| 7.6641, 7.2131 | Mn2P2O7 | |
| 2.382 | InPO4 | |
| 550 | 10.3757, 3.5498, 2.3695, 2.375, 8.1265, 3.5396, 2.3871 | Mn3(PO4)2 |
| 7.2131, 3.5589, 2.3774 | Mn2P2O7 | |
| 2.3701 | InPO4 | |
| 2.387 | In2O3 |
Рис. 4.
ИК-спектр поглощения образца MnO2/InP + + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ после термооксидирования при 450°С в течение 60 мин.
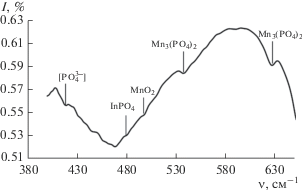
Во всех полученных спектрах присутствуют полосы поглощения [${\text{PO}}_{4}^{{3 - }}$] (ν = 414.67621, 414.67621, 416.60493 см–1). Для образца MnO2/InP + + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ при температуре 450°С сформированная пленка состоит из In(PO3)3, MnO2, InPO4, Mn3(PO4)2, [${\text{PO}}_{4}^{{3 - }}$]. При 500°С состав сформированной пленки – In(PO3)3, Mn2P2O7, MnO, Mn2O3, Mn3(PO4), MnPO4, [${\text{PO}}_{4}^{{3 - }}$], а при 550°С – In(PO3)3, Mn3(PO4)2, [${\text{PO}}_{4}^{{3 - }}$], InPO4. Отметим, что при 450 и 500°С в пленках присутствуют различные оксиды марганца, 1а при 550°С оксиды марганца полностью расходуются с образованием целого ряда фосфатов, т.е. с ростом температуры активизируются процессы фосфатообразования.
Повышенное содержание фосфора фиксируется и методом ЛРСМА, показавшим, что для отвечающих одинаковому режиму оксидирования (530°С, 60 мин) образцов MnO2/InP и MnO2/InP + + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ во втором случае содержание фосфора больше, что коррелирует с данными ИКС и РФА.
Введение Mn2(PO4)3 в реакционную зону при термооксидировании MnO2/InP приводит к росту удельного сопротивления пленок как в сравнении с собственными пленками на InP, обладающими омической проводимостью, так и с оксидированными образцами MnO2/InP (табл. 3). При 500°С ρ максимально, порядок величины составляет 1010 Ом см, что позволяет считать пленки диэлектрическими и, вообще говоря, является значительным достижением. При 550°С ρ несколько уменьшается, что связано с деструкцией оксидно-фосфатных пленок.
Таблица 3.
Электрофизические свойства образцов, полученных термооксидированием MnO2/InP и MnO2/InP + Mn3$\left( {{\text{P}}{{{\text{O}}}_{4}}} \right)_{2}^{{({\text{г}})}}$ при различных температурах в течение 60 мин
| Образец | t, °C | ρ, Ом см |
|---|---|---|
| MnO2/InP | 450 | 2.3 × 108 |
| 475 | 2.9 × 108 | |
| 500 | 4.2 × 108 | |
| 530 | 5.9 × 108 | |
| 550 | 6.3 × 108 | |
| MnO2/InP + ${\text{M}}{{{\text{n}}}_{{\text{2}}}}{\text{(P}}{{{\text{O}}}_{{\text{4}}}})_{3}^{{({\text{г}})}}$ | 450 | 2.1 × 109 |
| 475 | 3.2 × 109 | |
| 500 | 1.5 × 1010 | |
| 530 | 8.3 × 109 | |
| 550 | 4.8 × 108 |
ЗАКЛЮЧЕНИЕ
Модифицирование поверхности InP магнетронно нанесенными наноразмерными слоями хемостимулятора MnO2 и введение в реакционную зону Mn3(PO4)2 через газовую фазу приводит к заметному снижению ЭЭА (от ~180 кДж/моль при термооксидировании InP и MnO2/InP до 110 кДж/моль) и способствует увеличению темпа роста пленок по сравнению как с собственным оксидированием InP, так и с термооксидированием MnO2/InP.
По данным СЭ, синтезированные пленки являются слабопоглощающими в интервале длин волн 450–900 нм (k не превышает 0.1), при 500 и 550°С недоокисленный индий в них отсутствует.
Благодаря развитым процессам фосфатообразования (In(PO3)3, InPO4, In2(P2O7), Mn2P2O7, Mn3(PO4)2) предложенным методом удалось синтезировать наноразмерные пленки с удельным сопротивлением 109–1010 Ом см, максимальное значение – 1010 Ом см (500°С), что указывает на их диэлектрическую природу и отличает от полупроводниковых, выращенных без введения фосфата марганца [5].
Список литературы
Fundamentals of III-V Semiconductor MOSFETs / Ed. Oktyabrsky S., Ye P.D. N.Y.: Springer, 2010. 445 p.
Васильев М.Г., Васильев А.М., Шелякин А.А. Разработка мощного полупроводникового лазера на основе зарощенных гетероструктур InP/GaInAsP с полосой модуляции до 10 ГГц // Неорган. материалы. 2010. Т. 46. № 9. С. 1128–1133.
Миттова И.Я., Сладкопевцев Б.В., Третьяков Н.Н., Кострюков В.Ф., Самсонов А.А., Томина Е.В. Способ создания наноразмерных диэлектрических пленок на поверхности GaAs с использованием магнетронно сформированного слоя диоксида марганца: Пат. RU 2677266 МПК H01L 21/316, B82 1/00 Москва, 2019.
Миттова И.Я., Сладкопевцев Б.В., Томина Е.В., Самсонов А.А., Третьяков Н.Н., Пономаренко С.В. Синтез диэлектрических пленок термооксидированием MnO2/GaAs // Неорган. материалы. 2018. Т. 54. № 11. С. 1149–1156. https://doi.org/10.1134/S0002337X18110106
Третьяков Н.Н., Миттова И.Я., Сладкопевцев Б.В., Самсонов А.А., Андреенко С.Ю. Влияние магнетронно напыленного слоя MnO2 на кинетику термооксидирования InP, состав и морфологию синтезированных пленок // Неорган. материалы. 2017. Т. 53. № 1. С. 41–48. https://doi.org/10.7868/S0002337X17010171
Thurmond C.D., Schwartz G.P., Kammlott G.W., Schwartz B. GaAs Oxidation and the Ga–As–O Equilibrium Phase Diagram // J. Electrochem. Soc. 1980. V. 127. № 6. P. 1366–1371. https://doi.org/10.1149/1.2129900
Маренкин С.Ф., Кочура А.В., Федорченко И.В., Изотов А.Д., Васильев М.Г., Трухан В.М., Шёлковая Т.В., Новодворский О.А., Желудкевич А.Л. Ферромагнетизм сплавов InSb с Mn // Неорган. материалы. 2016. Т. 52. № 3. С. 309–314. https://doi.org/10.7868/S0002337X16030118
Агафонов А.В., Иванов В.К. Золь–гель материалы – перспективные наполнители электрореологических жидкостей // Сб. тез. Пятой междунар. конф. стран СНГ “Золь–гель синтез и исследование неорганических соединений, гибридных функциональных материалов и дисперсных систем”. 2018. С. 28–29.
Пашкова О.Н., Изотов А.Д., Лобанов Н.Н., Саныгин В.П., Филатов А.В. Синтез и магнитные свойства твердых растворов In1 – xGaxSb(Mn) // Журн. неорган. химии. 2017. Т. 62. № 1. С. 97–101. https://doi.org/10.7868/S0044457X17010147
Неорганическая химия: в 3-х т. / Под ред. Третьякова Ю.Д. Т. 3. Химия переходных элементов. Кн. 1. Академия, 2007. 352 с.
Миттова И.Я., Швец В.А., Томина Е.В., Самсонов А.А., Сладкопевцев Б.В., Третьяков Н.Н. Определение толщины и оптических постоянных наноразмерных пленок, выращенных термооксидированием InP с магнетронно нанесенными слоями хемостимуляторов V2O5, V2O5 + PbO, NiO + PbO // Неорган. материалы. 2013. Т. 49. № 10. С. 1037. https://doi.org/10.7868/S0002337X13100072
Миттова И.Я. Влияние физико-химической природы хемостимулятора, способа и метода его введения в систему на механизм термооксидирования GaAs и InP // Неорган. материалы. 2014. Т. 50. № 9. С. 948–955. https://doi.org/10.7868/S0002337X14090097
Diffraction Data. Catalog v.2.4, International Centre for Diffraction Data. http://www.icdd.com/translation/rus/ pdf2.htm
Атлас ИК-спектров фосфатов / Под ред. Мельниковой Р.Я. М.: Наука, 1985. 235 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы


