Неорганические материалы, 2019, T. 55, № 9, стр. 984-988
Механизм фазовых превращений при гидротермальной обработке γ-Al2O3, Al(OH)3 в бемит (AlOOH)
Г. П. Панасюк 1, *, И. В. Козерожец 1, Е. А. Семенов 1, М. Н. Данчевская 2, Л. А. Азарова 1, В. Н. Белан 1
1 Институт общей и неорганической химии им. Н.С. Курнакова Российской академии наук
119991 Москва, Ленинский пр., 31, Россия
2 Московский государственный университет им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
* E-mail: panasyuk@igic.ras.ru
Поступила в редакцию 18.02.2019
После доработки 19.04.2019
Принята к публикации 22.04.2019
Аннотация
Предложен механизм, позволяющий описать фазовые превращения при гидротермальной обработке микронных и наноразмерных порошков γ-Al2O3 и Al(OH)3. Идентифицированы этапы превращения. Выявлена роль воды с низким значением теплоты испарения в процессе гидротермальной обработки.
ВВЕДЕНИЕ
Бемит (AlOOH) широко применяется в современной технике и производстве: в качестве наполнителя, в производстве катализаторов и антипиренов, в качестве сорбента для извлечения ценных металлов из сточных вод промышленных предприятий благодаря высокой сорбционной емкости и др. [1–7]. В настоящее время в промышленности получают бемит гидротермальной обработкой различных прекурсоров. При этом в ходе гидротермальной обработки может быть получен как наноразмерный порошок бемита, так и частицы микронного размера.
Исследованию механизма, описывающего фазовые превращения при гидротермальной обработке γ-Al2O3 и Al(OH)3 (гидраргиллита), посвящено большое число работ. Автор [8] выдвигает теорию перерастворения при гидротермальной обработке прекурсора, однако она не позволяет описать процесс гидротермальной обработки γ-Al2O3 и Al(OH)3 в воде, так как их растворимость в воде ничтожно мала. В работе [3] рассмотрен механизм образования бемита при гидротермальной обработке гидраргиллита. Высказано предположение, что данный механизм является твердофазным, идентифицированы этапы процесса, но не предлагается единая модель, описывающая весь процесс, и отсутствует обоснование зависимости размера синтезированных частиц бемита от исходного прекурсора и условий обработки.
Настоящая работа посвящена изучению механизма, позволяющего описать фазовые превращения при гидротермальной обработке в различных средах микронных и наноразмерных порошков γ-Al2O3 и Al(OH)3 (гидраргиллита).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовался наноразмерный порошок γ-Al2O3, синтезированный по технологии, описанной в работе [9]. Гидротермальная обработка γ-Al2O3 проводилась в автоклавах объемом 18 см3 в тефлоновом вкладыше в 1.5%-ном растворе НСl. Герметизированные автоклавы помещались в разогретую электрическую печь и выдерживались на воздухе при постоянной температуре в течение разного времени. После охлаждения и разгерметизации автоклавов образцы извлекали из контейнеров, промывали дистиллированной водой, высушивали при 100°С и исследовали различными методами: сканирующая электронная микроскопия (СЭМ) на приборе SCAN-S2, просвечивающая электронная микроскопия (ПЭМ) на приборе Jem-1001, РФА на дифрактометре Bruker D8 Advance, ДСК на термоанализаторе SDT Q600.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На основании данных [10–14] и результатов исследований, проводимых при гидротермальной обработке наноразмерного порошка γ-Al2O3 в 1.5%-ном растворе НСl, был предложен механизм, позволяющий описать фазовые превращения.
Согласно разработанному механизму, процесс трансформации системы прекурсор–гидротермальный раствор в различных средах можно подразделить на 4 этапа.
1. Поведение гидротермального раствора на поверхности частицы прекурсора. Микронные частицы γ-Al2O3 и гидраргиллита (Al(ОН)3), так же как и наноразмерные частицы, являются поликристаллическими [10–14] и состоят из мелких кристаллитов с размером 1–5 нм (рис. 1 и 2).
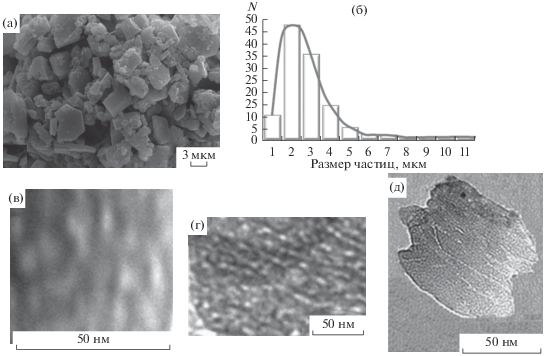
Рис. 1.
СЭМ-изображение (а), кривая распределения по размерам частиц гидраргиллита без диспергирования (б) и ПЭМ-изображения (в–д) частиц гидраргиллита после диспергирования [3].
При выполнении условия Гиббса–Смита, когда поверхностная энергия границы зерна больше поверхностного натяжения на границе твердое/жидкость, проникновение гидротермального раствора между кристаллитами с образованием тонкой жидкой пленки термодинамически выгодно. Согласно [15, 16], максимальное значение поверхностного натяжения на границе твердое/жидкость при 20°С составляет 218.58 мДж/м2, а поверхностная энергия границы зерна для γ-Аl2O3 – 747 мДж/м2, следовательно, при гидротермальной обработке прекурсора, независимо от размера частиц, возникает капиллярный эффект, гидротермальный раствор проникает внутрь поликристалла и образует тонкую жидкую пленку между кристаллитами. С уменьшением толщины жидкой пленки до предельного размера решающую роль приобретает расклинивающее давление, которое приводит к распаду частиц прекурсора на более мелкие кристаллиты.
Cвязь между кристаллитами в частицах прекурсора микронного размера более сильная, чем между кристаллитами в наноразмерных частицах за счет большего числа связей Аl–O–Al. В наноразмерных частицах превалирует водородная связь, что приводит к более высокой реакционной способности наноразмерного порошка γ-Al2O3. Так, по данным РФА, наноразмерный порошок бемита был получен при гидротермальной обработке наноразмерного порошка γ-Al2O3 в 1.5%-ном растворе НСl при температуре 80°С в течение 3 суток. Гидротермальная обработка микронного порошка γ-Al2O3 в тех же условиях не позволяет получить бемит.
2. Диффузия воды в объем частиц прекурсора, взаимодействие воды с алюмокислородным скелетом частиц и образование воды с низким значением теплоты испарения. С образованием тонкой жидкой пленки в объеме частиц прекурсора происходит диффузия воды, что приводит к образованию в объеме частиц воды с теплотой испарения значительно ниже табличных значений.
В работах [10, 13] представлены результаты исследования методом ДСК процесса превращения при гидротермальной обработке микронного гидраргиллита и γ-Al2O3 в бемит. Значения тепловых эффектов испарения воды из микронных частиц двухфазной системы (прекурсор–образующийся бемит) значительно ниже табличного значения теплоты испарения воды (40.62 кДж/моль Н2О): 27.5 кДж/моль Н2О (γ-Al2O3, обработанный в 1.5%-ном растворе NаОН при 200°С, р = 1.6 МПа, τ = 1 ч); 6.5 кДж/моль Н2О (γ-Al2O3, обработанный в 1.5%-ном растворе НСl при 200°С, р = 1.6 МПа, τ = 5 ч).
Значения тепловых эффектов испарения воды из двухфазной системы наноразмерных порошков (γ-Al2O3–образующийся AlOOH) также значительно ниже табличного значения теплоты испарения воды: 8 кДж/моль Н2О (при 150°С, τ = 8 ч); 16 кДж/моль Н2О (τ = 12 ч); 22 кДж/моль Н2О (τ = 16 ч).
Низкие значения тепловых эффектов испарения воды характерны как для микронных, так и для наноразмерных прекурсоров, что, по-видимому, определяется локализацией воды в структуре обрабатываемого материала и указывает на взаимодействие воды с алюмокислородным скелетом частиц, а также на активную роль воды с низким значением теплоты испарения в процессе гидротермальной обработки исходных прекурсоров.
Значения 6.5, 8, 16, 22 и 27.5 кДж/моль Н2О позволяют на основе данных [17] высказать предположение, что вода в структуре обрабатываемого материала присутствует в виде димеров и тримеров.
3. Перемещение кристаллитов в объеме исходной частицы прекурсора и переход к термодинамически более устойчивой форме будущей частицы бемита. Согласно данным [10, 13], на начальных этапах гидротермальной обработки частиц прекурсора микронного размера при 200°С в воде, в 1.5%-ном растворе НСl и в 1.5%-ном растворе NaOH, по данным СЭМ, в объеме частиц отчетливо фиксируется образование изометрического, пластинчатого или игольчатого габитуса, характерного для будущей частицы бемита, но результаты РФА не фиксируют фазу бемита. При увеличении времени гидротермальной обработки формируются частицы бемита микронного размера, обладающие разным габитусом: в воде – изометрическим, в 1.5%-ном растворе НСl – игольчатым, в 1.5%-ном растворе NaOH – пластинчатым (рис. 3).
Рис. 3.
СЭМ-изображения бемита, полученного при гидротермальной обработке гидраргиллита при 200°С в воде (а), в 1.5%-ном растворе НСl (б) и в 1.5%-ном растворе NaOH (в).

При гидротермальной обработке наноразмерного порошка γ-Al2O3 (рис. 2) при 150°С в течение 24 ч в воде и в 1.5%-ном растворе NaOH, согласно данным РФА и СЭМ, формируются наноразмерные частицы бемита без изменения размера и габитуса исходной частицы γ-Al2O3. При гидротермальной обработке наноразмерного порошка γ-Al2O3 при 150°С в 1.5%-ном растворе НСl в течение 96 ч формируются наноразмерные волокна шириной 20 нм и длиной 3 мкм (рис. 4).
Рис. 4.
ПЭМ-изображения бемита, полученного при гидротермальной обработке наноразмерного порошка γ-Al2O3 при 150°С в воде (а), в 1.5%-ном растворе NaOH (б) и в 1.5%-ном растворе НСl (в).

Таким образом, согласно представленным микрофотографиям, форма частиц бемита определяется значением рН гидротермального раствора. В кислой среде подвижность кристаллитов бемита выше, чем в нейтральной и щелочной, что определяет образование волокон.
4. Формирование структуры бемита. Согласно данным термического анализа процесса превращения при гидротермальной обработке микронного гидраргиллита и γ-Al2O3 в бемит [10, 13], на различных ее этапах значения тепловых эффектов дегидратации бемита с образованием γ-Al2O3 различаются и значительно ниже табличного значения (26.1 кДж/моль AlOOH): 10.2 кДж/моль АlОOH (гидраргиллит, обработанный при 200°С в воде в течение 1 ч, р = 1.6 МПа); 13.5 кДж/моль АlОOH (γ-Al2O3, обработанный в 1.5%-ном растворе НСl при 200°С, р = 1.6 МПа, τ = 5 ч); 21.4 кДж/моль АlОOH (γ-Al2O3, обработанный в 1.5%-ном растворе NаОН при 200°С, р = 1.6 МПа, τ = 1 ч).
Результаты термического анализа процесса образования наноразмерного порошка бемита при гидротермальной обработке наноразмерного порошка γ-Al2O3 в 1.5%-ном растворе НСl при 150°С на начальных этапах (4–48 ч) обработки показали, что при наличии смеси фаз прекурсора и бемита значения теплового эффекта дегидратации наноразмерного бемита с образованием γ‑Al2O3 также ниже теоретически рассчитанного и составляют 3.8 кДж/моль АlОOH (τ = 4 ч), 6.2 кДж/моль АlОOH (τ = 8 ч), 9.4 кДж/моль АlОOH (τ = 12 ч), 10.6 кДж/моль АlОOH (τ = 16 ч), 11.7 кДж/моль АlОOH (τ = 24 ч), 14.5 кДж/моль АlОOH (τ = 48 ч), 19.4 кДж/моль АlОOH (τ = 96 ч).
Значения тепловых эффектов дегидратации бемита до завершения процесса гидротермальной обработки независимо от размера частиц коррелируют с высокими значениями удельной поверхности (200 м2/г) и указывают на несовершенство структуры бемита. При увеличении времени гидротермальной обработки значения тепловых эффектов дегидратации бемита увеличиваются, а значения удельной поверхности падают (60 м2/г), что указывает на формирование более совершенной структуры бемита.
Для наноразмерных порошков бемита характерно понижение значения теплового эффекта превращения АlООН → γ-Al2O3 (19.4 кДж/моль AlOOH) по сравнению с микронными частицами (26 кДж/моль AlOOH), которое составляет 7 кДж/моль АlООН, что объясняется в основном размером частиц синтезированного бемита (АlООН).
ЗАКЛЮЧЕНИЕ
Механизм превращения при гидротермальной обработке γ-Al2O3 и Al(OH)3 в AlOOH является твердофазным и не зависит от размера частиц прекурсора. Значение энтальпии испарения воды не зависит от размера частиц прекурсора и значительно ниже табличного, что указывает на активную роль воды с низким значением теплоты испарения на начальных этапах гидротермальной обработки прекурсора. Величины тепловых эффектов дегидратации бемита до завершения процесса гидротермальной обработки не зависят от размера частиц и значительно ниже табличного значения, что связано с несовершенством структуры бемита.
Список литературы
Криворучко О.П., Жужгов А.В., Болотов В.А., Танашев Ю.Ю., Молина И.Ю., Пармон В.Н. Новый подход к синтезу бемита (γ-ALOOH) путем воздействия СВЧ-излучения на гиббсит: кинетика твердофазных превращений и диэлектрические свойства // Катализ в промышленности. 2014. № 2. С. 7–16.
Svarovskaya N.V., Bakina O.V., Glazkova E.A., Fomenko A.N., Lerner M.I. Glass and Cellulose Acetate Fibers-Supported Boehmite Nanosheets for Bacteria Adsorption // Prog. Natural Sci.-Mater. Int. 2017. V. 27. № 2. P. 268–274.
Panasyuk G.P., Belan V.N., Voroshilov I.L., Kozerozhets I.V. Hydrargillite → Boehmite Transformation // Inorg. Mater. 2010. V. 46. № 7. P. 747–753.
Alinejad B., Mahmoodi K., Ahmadi K. A New Route to Mass Production of Metal Hydroxide/Oxide Hydroxide Nanoparticles // Mater. Chem. Phys. 2009. V. 118. № 2–3. P. 473–476.
Даниленко Н.Б., Савельев Г.Г., Яворовский Н.А., Юрмазова Т.А., Галанов А.И., Балухтин П.В. Изучение состава и кинетики образования продуктов эрозии металлической загрузки электроразрядного реактора // Журн. прикл. химии. 2005. Т. 75. № 9. С. 1463–1468.
Глазкова Е.А., Бакина О.В., Домашенко В.В., Ложкомоев А.С., Сваровская Н.Б., Лернер М.И. Гидролиз нанопорошков алюмонитридной композиции // Нанотехника. 2010. Т. 8. № 4. С. 51–55.
Панасюк Г.П., Семенов Е.А., Козерожец И.В., Азарова Л.А., Ворошилов И.Л., Белан В.Н., Першиков С.А. Способ получения наполнителей для строительных материалов: Патент № 2625388 по заявке № 2015133561. Б.И. № 20.
Tsuchida T. Hydrothermal Synthesis of Submicrometer Crystals of Boehmite // J. Eur. Ceram. Soc. 2000. V. 20. № 11. P. 1759–1764.
Panasyuk G.P., Kozerozhets I.V., Semenov E.A., Azarova L.A., Belan V.N., Danchevskaya M.N. A New Method for Producing a Nanosized γ-Al2O3 Powder // J. Inorg. Chem. 2018. V. 63. № 10. P. 1303–1308. https://doi.org/10.1134/S0036023618100157
Panasyuk G.P., Kozerozhet I.V., Voroshilov I.L., Belan V.N., Semenov E.A., Luchkov I.V. The Thermodynamic Properties and Role of Water Contained in Dispersed Oxides in Precursor-Boehmite Conversion, Based on the Example of Aluminum Hydroxide and Oxide under Hydrothermal Conditions in Different Environments // J. Phys. Chem. A. 2015. V. 89. № 4. P. 592–597.
Панасюк Г.П., Ворошилов И.Л., Белан В.Н., Козерожец И.В. Получение наноразмерного порошка альфа-оксида алюминия // Хим. технология. 2011. № 4. С. 227–231.
Панасюк Г.П., Азарова Л.А., Белан В.Н., Семенов Е.А., Данчевская М.Н., Ворошилов И.Л., Козерожец И.В., Першиков С.А., Харатян С.Ю. Методы получения оксида алюминия высокой степени чистоты для выращивания кристаллов лейкосапфира (обзор) // Хим. технология. 2017. № 9. С. 393–400.
Панасюк Г.П., Белан В.Н., Ворошилов И.Л., Козерожец И.В., Лучков И.В., Кондаков Д.Ф., Демина Л.И. Исследование процесса перехода гидраргиллита и γ-оксида алюминия в бемит в различных гидротермальных средах // Хим. технология. 2012. № 6. С. 321–328.
Панасюк Г.П., Лучков И.В., Козерожец И.В., Шаба-лин Д.Г., Белан В.Н. Влияние предварительной термической обработки и легирования кобальтом гидраргиллита на кинетику перехода гидраргиллит–корунд в сверхкритическом водном флюиде // Неорган. материалы. 2013. Т. 49. № 9. С. 966–970.
Козерожец И.В. Разработка метода получения и исследование субмикронных и наноразмерных частиц оксидов алюминия с низким содержанием примесей: Дис. … к.х.н. М., 2011. 128 с.
Стромберг А.Г. Физическая химия. М.: Высш. школа, 2001.
Суходуб Л.Ф., Тележенко Ю.В., Шелковский В.С., Лисняк Ю.В. Энтальпия малых кластеров воды. Харьков: Физ.-техн. ин-т низких температур АН УССР, 1984. 26 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы



