Неорганические материалы, 2020, T. 56, № 10, стр. 1081-1087
Синтез, структура и термодинамические свойства апатитов Pb10 – xPrx(GeO4)2 + x(VO4)4 – x (x = 0, 1, 2, 3) в области 350–1050 К
Л. Т. Денисова 1, *, Ю. Ф. Каргин 2, Е. О. Голубева 1, Г. М. Зеер 3, А. К. Абкарян 3, В. М. Денисов 1
1 Институт цветных металлов и материаловедения Сибирского федерального университета
660041 Красноярск, Свободный пр., 79, Россия
2 Институт металлургии и материаловедения им. А.А. Байкова Российской академии наук
119334 Москва, Ленинский пр., 49, Россия
3 Политехнический институт Сибирского федерального университета
660041 Красноярск, Свободный пр., 79, Россия
* E-mail: ldenisova@sfu-kras.ru
Поступила в редакцию 17.04.2020
После доработки 28.05.2020
Принята к публикации 04.06.2020
Аннотация
Апатиты Pb10– xPrx(GeO4)2+x(VO4)4– x (x = 0, 1, 2, 3) синтезированы методом твердофазных реакций при последовательном обжиге на воздухе стехиометрических смесей исходных оксидов (PbO, Pr2O3, GeO2 и V2O5) в интервале температур 773–1073 K. Терморентгенографическим методом определены зависимости параметров элементарной ячейки от температуры и рассчитаны коэффициенты линейного и объемного термического расширения Pb7Pr3(GeO4)5(VO4). Методом дифференциальной сканирующей калориметрии в интервале температур 350–1050 K измерена теплоемкость синтезированных соединений со структурой апатита Pb10– xPrx(GeO4)2 +x(VO4)4 –x (x = 0, 1, 2, 3). Установлено, что на зависимостях cp = f(T) образцов с х = 1, 2 и 3 имеются экстремумы (в частности, при x = 3 с максимумами при 701, 917 и 1018 K), обусловленные фазовыми переходами. По экспериментальным значениям теплоемкости полученных зависимостей Cp = f(T) рассчитаны термодинамические функции синтезированных апатитов.
ВВЕДЕНИЕ
Апатитоподобные соединения с общей формулой M10(ZO4)6X2 (M = Ca, Ba, Pb, РЗЭ и др.; Z = = V, Ge, Si и др.; X = F, Cl, OH, O, вакансия) привлекают внимание исследователей наличием свойств прикладного характера [1–7]. Важным свойством соединений со структурой апатита является возможность замещения одних структурных единиц другими [8–10]. Согласно [2], замещение свинца в Pb5(GeO4)4(VO4)2 РЗЭ позволяет получить соединения Pb10 –xRx(GeO4)2 +x(VO4)4 –x (R = РЗЭ, x = 0–3). Свойства ванадатогерманатов свинца, особенно теплофизические, мало исследованы. Ранее получены данные по высокотемпературной теплоемкости Pb10– xLax(GeO4)2 +x(VO4)4 –x (x = 0, 1, 2, 3) [11] и Pb8Nd2(GeO4)4(VO4)2 [12].
Целью настоящей работы является синтез, терморентгенографическое исследование и измерение высокотемпературной теплоемкости соединений со структурой апатита Pb10 –xPrx(GeO4)2 +x(VO4)4– x (x = 0, 1, 2, 3).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве исходных компонентов для синтеза использовали PbO и V2O5 (“ос. ч.”), GeO2 – 99.999%; Pr2O3 получен из Pr6O11 (Alfa Aesar (99.996%)) подобно [13]. Образцы апатитов Pb10– xPrx(GeO4)2 + x(VO4)4– x (x = 0, 1, 2, 3) синтезировали твердофазным методом. Для этого стехиометрические смеси предварительно прокаленных исходных оксидов перетирали в агатовой ступке и прессовали в таблетки без добавления связующего. Обжиг таблеток проводили на воздухе при 773, 873 и 973 K (по 10 ч на каждой ступени) и 1073 K (100 ч). Для обеспечения полноты твердофазного взаимодействия компонентов через каждые 10 ч проводили измельчение спека и повторное прессование.
Фазовый состав полученных образцов контролировали с использованием дифрактометра X´Pert Pro MPD (PANalytical, Нидерланды, CuKα-излучение). Регистрацию дифрактограмм выполняли высокоскоростным детектором PIXcel в интервале 2θ = 8°–108° с шагом 0.013°. Параметры решетки определены путем полнопрофильного уточнения методом минимизации производной разности [14]. Эксперименты при высоких температурах проводили на дифрактометре D8 ADVANCE фирмы Bruker с использованием высокотемпературной камеры HTK 16 (Anton Paar).
Элементный анализ выполнен на растровом электронном микроскопе JSM 7000F (JEOL, Япония) с применением рентгеновского энергодисперсионного спектрометра INCA Penta FETx3 (OXFORD Instruments, Англия).
Теплоемкость апатитов Pb10 – xPrx(GeO4)2 + x(VO4)4– x (x = 0, 1, 2, 3) измеряли методом дифференциальной сканирующей калориметрии на приборе STA 449 C Jupiter (NETZSCH, Германия). Полученные экспериментальные результаты обрабатывали с помощью программного обеспечения NETZSCH Proteus Thermal Analysis и Sigma Plot 12 (Systat Software Inc., США). Погрешность измерений теплоемкости не превышала 2%. Методика экспериментов описана ранее [15]. Кривые ДТА снимали на этом же приборе, только использовали разные специальные держатели.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
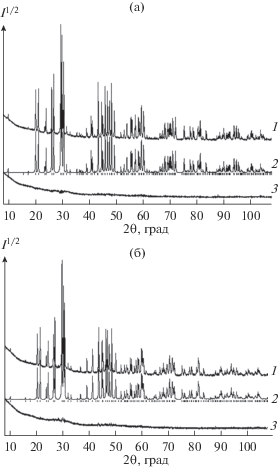
Структура апатита Pb10(GeO4)2(VO4)4 исследована разными авторами [2, 16–18], а подобные сведения для Pb8Pr2(GeO4)4(VO4)2 приведены в работе [19]. Поэтому на рис. 1 показаны данные рентгенофазового анализа только для однофазных образцов Pb9Pr(GeO4)3(VO4)3 и Pb7Pr3(GeO4)5(VO4), для которых сведения о структуре в литературе отсутствуют.
Рис. 1.
Дифрактограммы Pb9Pr(GeO4)3(VO4)3 (а) и Pb7Pr3(GeO4)5(VO4) (б) при комнатной температуре: экспериментальный (1), расчетный (2) и разностный (3) профили рентгенограмм после уточнения методом минимизации производной разности (штрихи указывают расчетные положение рефлексов).
Параметры элементарных ячеек синтезированных апатитов (пр. гр. P63/m) в сравнении с данными других авторов приведены в табл. 1. Можно отметить, что наблюдается их удовлетворительное согласие.
Таблица 1.
Параметры элементарных ячеек Pb10– xPrx(GeO4)2 +x(VO4)4 –x
| a, Å | c, Å | V, Å3 | d, г/см3 | Источник |
|---|---|---|---|---|
| Pb10(GeO4)2(VO4)4 | ||||
| 10.099(3) | 7.4000(20) | [2] | ||
| 10.0876(2) | 7.3927(1) | 651.49(2) | 7.15 | [11] |
| 10.089 | 7.393 | 7.15 | [15] | |
| 10.097(3) | 7.396(2) | [16] | ||
| 10.099(3) | 7.400(2) | [17] | ||
| Pb9Pr(GeO4)3(VO4)3 | ||||
| 10.0917(1) | 7.3653(2) | 649.60 | 7.05 | Настоящая работа |
| Pb8Pr2(GeO4)4(VO4)2 | ||||
| 10.0970(3) 10.0947(8) |
7.3351(2) 7.371(7) |
647.63(4) 645.72 |
6.96 6.98 |
Настоящая работа [18] |
| Pb7Pr3(GeO4)5(VO4) | ||||
| 10.0948(3) | 7.2837(3) | 642.80(4) | 6.90 | Настоящая работа |
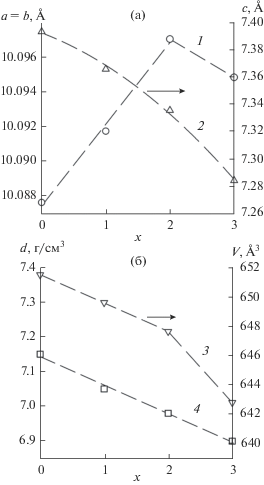
На рис. 2 показано влияние состава апатитов Pb10 –xPrx(GeO4)2 +x(VO4)4– x на параметры их элементарной ячейки. Из рис. 2 и данных табл. 1 видно, что значения a, c, V, d изменяются по мере замещения свинца празеодимом. Согласно [19], при замещении атома свинца на атом празеодима атомы последнего располагаются в основном в позиции Pb(1), хотя эффективный заряд Pr3+ больше, чем Pb2+. В структуре гидроксиапатита кальция при большем заряде у замещающего иона он преимущественно заселяет меньшую по размерам позицию Ca(2) [20].
Рис. 2.
Влияние состава апатитов Pb10– xPrx(GeO4)2 +x-(VO4)4– x на параметры их элементарной ячейки и плотность: a = b (1), c (2), V (3), d (4).
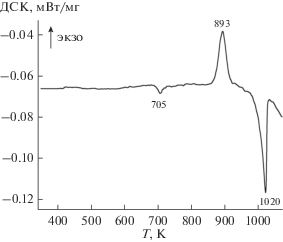
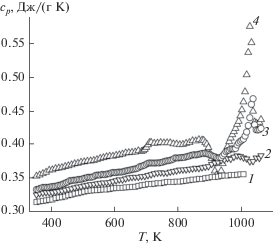
На рис. 3 приведены зависимости теплоемкости фаз со структурой апатита Pb10 –xPrx(GeO4)2 +x(VO4)4 –x (x = 0, 1, 2, 3) в интервале температур 300–1050 К. Для того, чтобы не учитывать различие молярных масс, приведены значения удельной теплоемкости. На рис. 3 видно, что замещение свинца празеодимом приводит к увеличению cp. Кроме того, на зависимостях cp = f(T) соединений, отвечающих х = 1, 2 и 3, имеются экстремумы (в частности, для фазы с x = 3 максимумы при 701, 917 и 1018 K). Подобные экстремумы на температурной зависимости теплоемкости могут наблюдаться при фазовых переходах, в области сегнетоэлектрических и ферромагнитных переходов и изменении атомной упорядоченности [21].
Рис. 3.
Влияние температуры на удельную теплоемкость Pb10– xPrx(GeO4)2 +x(VO4)4– x с x = 0 (1), 1 (2), 2 (3), 3 (4) (значения cp для Pb7Pr3(GeO4)5(VO4) смещены на +0.02 Дж/(г K) относительно Pb8Pr2(GeO4)3(VO4)2).
Для выяснения возможных причин появления максимумов на зависимостях cp = f(T) проведен дифференциальный термический анализ (ДТА) апатита состава Pb7Pr3(GeO4)5(VO4). Полученные результаты показаны на рис. 4: видно, что температуры экстремумов на кривой ДТА практически совпадают с таковыми на кривой cp = f(T) этого соединения. Отметим, что на кривой нагревания Pb7Pr3(GeO4)5(VO4) имеются два эндотермических и один экзотермический эффект (рис. 4). При этом на кривой охлаждения образца обратные эффекты не наблюдаются (изменение массы образцов также не регистрируется). Ранее аналогичное поведение было отмечено для апатита Pb4.8Bi1.6Na3.6(PO4)6, у которого на кривой ДТА при нагревании фиксируются два эндотермических эффекта – при 865 и 955 K, а при охлаждении наблюдается только один очень слабый эффект при 950 K [22]. В то же время изменение параметров элементарной ячейки (a и c) в зависимости от температуры происходит скачком (имеется разрыв) в области 838 K (при 865 и 955 K изменений нет – значения a и c с ростом температуры от 845 до 950 K закономерно увеличиваются по линейному закону).
Известно, что некоторые соединения семейства апатитов характеризуются наличием полиморфизма [3, 22–24], в частности свинецсодержащие [3, 22]. Исследование электропроводности апатитов Pb8– xGdxNa2(VO4)6Ox/2 [8] и Pb8– xSmxNa2(VO4)6Ox/2 [9] показало, что на зависимостях lgσ = f(1/T) имеется ряд изломов (в изученном интервале температур полученные данные не описываются одним уравнением). По-видимому, это может быть связано с полиморфными превращениями. В [24] замечено, что имеется тип полиморфизма, характеризующийся скачкообразным изменением некоторых физико-химические свойств, сопровождающимся тепловым эффектом, однако структура при этом не меняется. Можно предположить, что аналогичное поведение наблюдается и в нашем случае. Заметим, что имеется еще один тип полиморфного превращения, когда координационное число и тип упаковки сохраняются, но меняется мотив расположения атомов одного из элементов [24]. В [22] показано, что при нагревании Pb4.8Bi1.6Na3.6(PO4)6 наблюдаются два изменения, отнесенные к переходам порядок–беспорядок. При этом один был приписан переходу катионов с позиции M(2) в центр туннеля.
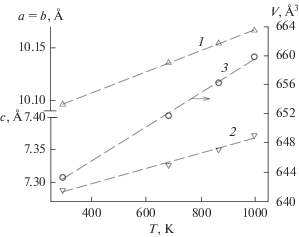
Учитывая сказанное выше, провели исследование апатита Pb7Pr3(GeO4)5(VO4) методом высокотемпературной рентгенографии при температурах 688, 870 и 1000 K. Линейный характер изменения параметров элементарной ячейки с ростом температуры свидетельствует об отсутствии фазовых переходов в данном апатите (рис. 5). Полученные данные могут быть описаны линейными уравнениями
(1)
$a = \left( {10.0650 \pm 0.0008} \right) + \left( {10.07 \pm 0.10} \right) \times {{10}^{{--5}}}T,$(2)
$c = \left( {7.2494 \pm 0.0074} \right) + \left( {11.83 \pm 0.97} \right) \times {{10}^{{--5}}}T,$Рис. 5.
Влияние температуры на параметры элементарной ячейки Pb7Pr3(GeO4)5(VO4): a = b (1), c (2), V (3).
Коэффициенты корреляции для уравнений (1)–(3) равны соответственно 0.9999, 0.9934 и 0.9989. С использованием этих результатов определены коэффициенты термического расширения по соотношению [18]
(4)
${{\alpha }_{L}} = \frac{1}{L}\left( {{{{\text{d}}L} \mathord{\left/ {\vphantom {{{\text{d}}L} {{\text{d}}T}}} \right. \kern-0em} {{\text{d}}T}}} \right),$Проведенное методом локального рентгеноспектрального анализа определение содержания химических элементов в Pb10 –xPrx(GeO4)2 +x(VO4)4 –x для x = 1, 3 показало их равномерное распределение по поверхности исследованных образцов. Результаты элементного анализа (использовано по три разных образца, в каждом из них измерения проведены в пяти различных точках) свидетельствуют об удовлетворительном согласии экспериментальных и теоретических значений (табл. 2). Некоторое различие в этих данных может быть связано с неоднородностью рельефа поверхности поликристаллических образцов.
Таблица 2.
Результаты элементного анализа Pb10– xPrx(GeO4)2 +x(VO4)4– x (x = 1, 3): числитель – расчет, знаменатель – эксперимент
| x | Pb | Pr | Ge | V | O |
|---|---|---|---|---|---|
| 1 | $\frac{{22.5}}{{21.8 \pm 2.1}}$ | $\frac{{2.5}}{{2.2 \pm 0.3}}$ | $\frac{{7.5}}{{8.6 \pm 0.4}}$ | $\frac{{7.5}}{{7.0 \pm 0.6}}$ | $\frac{{60}}{{60.2 \pm 3.3}}$ |
| 3 | $\frac{{17.5}}{{16.1 \pm 1.6}}$ | $\frac{{7.5}}{{6.8 \pm 0.7}}$ | $\frac{{12.5}}{{12.9 \pm 0.5}}$ | $\frac{{2.5}}{{2.3 \pm 0.2}}$ | $\frac{{60}}{{61.8 \pm 2.9}}$ |
Для соединений Pb9Pr(GeO4)3(VO4)3 (348–953 K), Pb8Pr2(GeO4)4(VO4)2 (348–868 K) и Pb7Pr3(GeO4)5(VO4) (348–873 K, без учета фазового перехода в интервале 678–798 K) молярные теплоемкости в зависимости от температуры могут быть описаны уравнением Майера–Келли, т.е.
Pb9Pr(GeO4)3(VO4)3:
(5)
$\begin{gathered} {{C}_{p}} = \left( {818.4 \pm 5.12} \right) + \left( {224.6 \pm 5.28} \right) \times {{10}^{{--3}}}T-- \\ - \,\,\left( {1.54 \pm 0.50} \right) \times {{10}^{5}}{{T}^{{--2}}}, \\ \end{gathered} $Pb8Pr2(GeO4)4(VO4)2:
(6)
$\begin{gathered} {{C}_{p}} = \left( {805.2 \pm 5.12} \right) + \left( {279.3 \pm 5.80} \right) \times {{10}^{{--3}}}T-- \\ - \,\,\left( {0.59 \pm 0.05} \right) \times {{10}^{5}}{{T}^{{--2}}}, \\ \end{gathered} $Pb7Pr3(GeO4)5(VO4):
(7)
$\begin{gathered} {{C}_{p}} = \left( {874.4 \pm 4.53} \right) + \left( {187.6 \pm 5.30} \right) \times {{10}^{{--3}}}T-- \\ - \,\,\left( {62.0 \pm 4.22} \right) \times {{10}^{5}}{{T}^{{--2}}}. \\ \end{gathered} $Коэффициенты корреляции для уравнений (5)–(7) равны соответственно 0.9960, 0.9975 и 0.9989. С использованием значений Cp, полученных по уравнениям (5)–(7), рассчитаны термодинамические свойства соответствующих соединений со структурой апатита (табл. 3).
Таблица 3.
Термодинамические свойства Pb10 –xPrx(GeO4)2 +x(VO4)4 –x
| T, K | Cp, Дж/(моль K) |
H°(T) – H°(350 K), кДж/моль |
S°(T) – S°(350 K), Дж/(моль) |
–(ΔG°/Т)*, Дж/(моль K) |
|---|---|---|---|---|
| Pb9Pr(GeO4)3(VO4)3 | ||||
| 350 | 896.9 | – | – | – |
| 400 | 908.1 | 45.13 | 120.5 | 7.68 |
| 450 | 919.4 | 90.81 | 228.1 | 26.30 |
| 500 | 930.6 | 137.1 | 325.6 | 51.43 |
| 550 | 941.8 | 183.8 | 414.8 | 80.46 |
| 600 | 953.1 | 231.2 | 497.2 | 111.8 |
| 650 | 964.3 | 279.2 | 573.9 | 144.4 |
| 700 | 975.5 | 327.7 | 645.8 | 177.7 |
| 750 | 986.8 | 376.7 | 713.5 | 211.2 |
| 800 | 998.0 | 426.4 | 777.5 | 244.6 |
| 850 | 1009 | 476.5 | 838.4 | 277.8 |
| 900 | 1020 | 597.3 | 896.4 | 310.5 |
| Pb8Pr2(GeO4)4(VO4)2 | ||||
| 350 | 902.5 | – | – | – |
| 400 | 916.5 | 45.48 | 121.4 | 7.74 |
| 450 | 930.6 | 91.65 | 230.2 | 26.52 |
| 500 | 944.6 | 138.5 | 328.9 | 51.90 |
| 550 | 958.6 | 186.1 | 419.7 | 81.26 |
| 600 | 972.6 | 243.4 | 503.7 | 113.0 |
| 650 | 986.6 | 283.4 | 581.0 | 146.1 |
| 700 | 1000 | 333.1 | 655.7 | 179.9 |
| 750 | 1015 | 383.4 | 725.2 | 213.9 |
| 800 | 1028 | 434.5 | 791.1 | 248.0 |
| 850 | 1043 | 486.3 | 853.9 | 281.8 |
| Pb7Pr3(GeO4)5(VO4) | ||||
| 350 | 889.4 | – | – | – |
| 400 | 910.6 | 45.02 | 120.2 | 7.65 |
| 450 | 928.2 | 91.00 | 228.5 | 26.27 |
| 500 | 943.4 | 137.8 | 327.1 | 51.50 |
| 550 | 957.0 | 185.3 | 417.7 | 80.72 |
| 600 | 969.7 | 233.5 | 501.5 | 112.3 |
| 650 | 981.6 | 282.9 | 579.6 | 145.3 |
| 800 | 1015 | 432.0 | 786.8 | 246.7 |
| 850 | 1025 | 483.0 | 848.6 | 280.3 |
ЗАКЛЮЧЕНИЕ
Твердофазным синтезом получены апатиты Pb10 – xPrx(GeO4)2 + x(VO4)4 – x (x = 0, 1, 2, 3). При помощи высокотемпературной рентгенографии установлен линейный характер зависимости параметров элементарной ячейки от температуры и рассчитаны коэффициенты линейного и объемного термического расширения Pb7Pr3(GeO4)5(VO4).
Методом дифференциальной сканирующей калориметрии в области температур 350–1050 К исследована теплоемкость синтезированных ванадатогерманатов свинца-празеодима. Установлено, что на кривых cp = f(T) образцов Pb10 – xPrx(GeO4)2 + x(VO4)4 – x при х = 1, 2, 3 имеются экстремумы. Для апатитов Pb9Pr(GeO4)3(VO4)3, Pb8Pr2(GeO4)4(VO4)2 и Pb7Pr3(GeO4)5(VO4) рассчитаны термодинамические свойства.
Список литературы
Каназава Т. Неорганические фосфатные материалы. Киев: Наук. думка, 1998. 298 с.
Журавлев В.Д., Великодный Ю.А. Ванадатогерманаты свинца-лантана и стронция-лантана со структурой апатита и оксоапатита // Журн. неорган. химии. 2009. Т. 54. № 10. С. 1626–1627.
Черноруков Н.Г., Князев А.В., Буланов Е.Н. Фазовые переходы и тепловое расширение некоторых соединений со структурой апатита // Неорган. материалы. 2011. Т. 47. № 2. С. 215–220.
Каржавин В.К. Термодинамические величины химических элементов и соединений. Примеры их практического применения. Апатиты: Изд-во Кольск. научн. центра РАН, 2011. 160 с.
Grossin D., Rollin-Martinet S., Estournis C. et al. Biomimetric Apatite Sintered at very Low Temperature by Spark Plasma Sintering: Physic-Chemistry and Microstructure Aspects // Acta Biomater. 2010. V. 6. № 2. P. 577–585.
Chakroun-Ouadhour E., Ternane R., Ben Hassen-Chehimi D. et al. Synthesis, Characterization and Electrical Properties of a Lead Sodium Vanadate Apatite // Mater. Res. Bull. 2008. V. 43. P. 2451–2456. https://doi.org/10.1016/j.materresbull.2007.07.030
Zhang J., Liang H., Yu R. et al. Luminescence of Ce3+ – activated Chalcogenide Apatites Ca10(PO4)6Y (Y = S, Se) // Mater. Chem. Phys. 2009. V. 114. № 1. P. 242–246.
Игнатов А.В., Саванкова Т.М., Дидоренко Е.Г. и др. Изоморфное замещение в системе Pb(8– x)GdxNa2(VO4)6O(x/2) // Вестн. Дон. нац. ун-та. Сер. А. Естеств. науки. 2014. № 1. С. 152–154.
Savankova T.M., Akselrud L.G., Ardanova L.I. et al. Synthesis, Crystal Structure Refinement, and Electrical Conductivity of Pb(8– x)Na2Smx(VO4)6O(x/2) // J. Chem. 2014. P. 1–7. https://doi.org/10.1155/2014/263548
Pasero M., Kampf A.R., Ferraris C. et al. Nomenclature of the Apatite Supergroup Minerals // Eur. J. Mineral. 2010. V. 22. P. 163–179. https://doi.org/10.1127/0935-1221/2010/0022-2022
Денисова Л.Т., Каргин Ю.Ф., Голубева Е.О. и др. Теплоемкость апатитов Pb10 –xLax(GeO4)2 +x(VO4)4 –x (x = 0, 1, 2, 3) в области 320–1000 K // Неорган. материалы. 2019. Т. 55. № 2. С. 182–186. https://doi.org/10.1134/S0002337X19020027
Денисова Л.Т., Каргин Ю.Ф., Белоусова Н.В. и др. Синтез и исследование высокотемпературной теплоемкости Pb8La2(GeO4)4(VO4)2 и Pb8Nd2(GeO4)4(VO4)2 со структурой апатита // Неорган. материалы. 2018. Т. 54. № 2. С. 177–180. https://doi.org/0.7868/S0002337X18020094
Денисова Л.Т., Каргин Ю.Ф., Чумилина Л.Г. и др. Синтез и теплоемкость Pr2CuO4 в области 364–1064 K // Неорган. материалы. 2014. Т. 50. № 12. С. 1324–1327. https://doi.org/10.7868/S0002337X14120057
Solovyov L.A. Full-Profile Refinement by Derivative Difference Minimization // J. Appl. Crystallogr. 2004. V. 37. P. 743–749 .https://doi.org/10.1107/S0021889804015638
Денисов В.М., Денисова Л.Т., Иртюго Л.А., Биронт В.С. Теплофизические свойства монокристаллов Bi4Ge3O12 // ФТТ. 2010. Т. 52. № 7. С. 1274–1277.
Yano T., Nabeta Y., Watanabe A. A New Crystal Pb5(GeO4)(VO4)2 for Acousto-optic Device Applications // Appl. Phys. Lett. 1971. V. 18. № 12. P. 570–571. https://doi.org/10.1063/1.1653544
Иванов С.А., Заводник В.Е. Особенности кристаллической структуры Pb5GeV2O12 // Кристаллография. 1989. Т. 34. № 4. С. 824–828.
Иванов А. Уточнение кристаллической структуры Pb5(GeO4)(VO4)2 по профилю порошковых рентгенограмм // Журн. структур. химии. 1990. Т. 31. № 4. С. 80–84.
Яблочкова Н.В. Синтез и уточнение кристаллической структуры Pb8Pr2(GeO4)4(VO4)2 // Журн. неорган. химии. 2013. Т. 58. № 7. С. 871–874. https://doi.org/10.7868/S0044457X1307026X
Get’man E.I., Yablochkova N.V., Loboda S.N. et al. Isomorphous Substitution of Europium for Strontium in the Structure of Synthetic Hidroxovanadate // J. Solid State Chem. 2008. V. 181. P. 2386–2392. https://doi.org/10.1016/j.jssc.2008.06.003
Шаскольская М.П. Кристаллография. М.: Высш. школа, 1984. 376 с.
Hamdi B., Feki H.El., Salah A. B. et al. Ionic Conductivity and Phase Transition in Pb4.8Bi1.6Na3.6(PO4)6, a Apatite-type Compound // Solid State Ionics. 2006. V. 177. № 17–18. P. 1413–1420. https://doi.org/10.1016/j.ssi.2006.06.031
Zhang F.X., Lang M., Zhang J.M. et al. Phase Transition and Abnormal Compressibility of Lanthanide Silicate with the Apatite Structure // Phys. Rev. B. 2012. V. 85. P. 214116-1–214116-6. https://doi.org/10.1103/PhysRevB.85.214116
Азимов Ш.Ю., Исматов А.А., Федоров Н.Ф. Апатиты и их редкоземельные аналоги. Ташкент: ФАН, 1990. 116 с.
Новикова С.И. Тепловое расширение твердых тел. М.: Наука, 1974. 294 с.
Филатов С.К. Высокотемпературная кристаллохимия. Л.: Недра, 1990. 288 с.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы