Неорганические материалы, 2020, T. 56, № 7, стр. 788-795
Влияние метода синтеза слоистых двойных гидроксидов на их фазовый состав и магнетизм
О. В. Нестройная 1, И. Г. Рыльцова 1, М. Н. Япрынцев 1, О. Е. Лебедева 1, *
1 Белгородский государственный национальный исследовательский университет
308015 Белгород, ул. Победы, 85, Россия
* E-mail: OLebedeva@bsu.edu.ru
Поступила в редакцию 26.08.2019
После доработки 19.12.2019
Принята к публикации 23.01.2020
Аннотация
Ряд тетраметаллических слоистых двойных гидроксидов, содержащих магний и кобальт в положениях двухзарядных катионов в структуре бруситоподобных слоев, а алюминий и железо – в положениях трехзарядных катионов, синтезировали с использованием трех различных методов: соосаждения, микроволнового и гидротермального синтезов. В качестве осадителя использован раствор гидроксида натрия. Показано, что при синтезе любым из указанных методов формируются хорошо окристаллизованный гидроталькитоподобный слоистый гидроксид и примесная фаза. Сделано заключение, что именно примесная фаза обусловливает магнетизм образцов. Наиболее вероятно, этой фазой является шпинель СoFe2O4.
ВВЕДЕНИЕ
Слоистые двойные гидроксиды (СДГ) или гидроталькитоподобные соединения – это основные соли со специфической слоистой структурой. Общая формула данного класса соединений – ${{\left[ {{\text{M}}_{{1 - x}}^{{2 + }}{\text{M}}_{x}^{{3 + }}{{{({\text{OH}})}}_{2}}} \right]}^{{х + }}}[{{({{{\text{A}}}^{{n - }}})}_{{x{\text{/}}n}}} \cdot m{{{\text{H}}}_{{\text{2}}}}{\text{O}}],$ где М2+ и М3+ – ионы металлов, находящиеся в октаэдрических позициях бруситоподобных слоев, Аn– – анионы, которые компенсируют положительный заряд бруситоподобных слоев [1, 2]. Особенности структуры гидроталькитоподобных соединений и разнообразие катионов, которые могут входить в их состав, обеспечивают специфические ионообменные [3], сорбционные [4, 5], электрические [6] и каталитические [7, 8] свойства СДГ и продуктов их термической деструкции. Привлекает внимание возможность получения СДГ, обладающих магнитными свойствами. Такой эффект наблюдается при одновременном введении в систему катионов железа и кобальта [9].
Ранее методом соосаждения при переменном рН был синтезирован ряд MgCo/AlFe-СДГ в карбонатной форме [10]. Было установлено, что только образцы с высоким содержанием железа и кобальта обладают магнитными свойствами, что, вероятнее всего, обусловлено присутствием примесной фазы. Полученные материалы, являющиеся, по сути дела, композитными, предложено использовать в качестве магнитных сорбентов [11].
Необходимость введения больших количеств железа и кобальта в состав материалов для получения магнитных образцов отрицательно влияет на кристалличность гидроталькитоподобной фазы.
Настоящее исследование направлено на выбор метода и оптимизацию условий синтеза образцов MgCo/AlFe-СДГ, обладающих магнетизмом при комнатной температуре, при возможно более низком содержании железа и кобальта.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве источников катионов металлов использовали следующие соли: Mg(NO3)2 ∙ 6H2O, Co(NO3)2 ∙ 6H2O, Al(NO3)3 ∙ 9(H2O), Fe(NО3)3 ∙ 9H2O. Все реактивы были квалификации “ч. д. а.”.
Синтез мультиметаллических СДГ состава (Mg1 – xCox)6(Al1 – yFey)2NO3 ∙ mH2O был осуществлен тремя методами: соосаждением при переменном рН, гидротермальным методом и микроволновым методом. Степень замещения магния на кобальт (x) и алюминия на железо (y) варьировали в пределах 10–50 ат. %.
Соосаждение осуществляли путем добавления раствора гидроксида натрия к раствору, содержащему необходимые количества солей. Общая концентрация ионов металлов в исходной реакционной смеси составляла 1 М, а отношение молярной концентрации двухзарядных ионов к концентрации трехзарядных [М2+]/[М3+] равнялось 3. В процессе синтеза рН смеси доводили до значения 9–10. Полученные осадки подвергали старению под маточным раствором в течение суток при комнатной температуре и двух суток при 98°С. Гидротермальный синтез СДГ проводили в автоклаве Autoclave Engineers Parker при температуре 140°С и давлении 250–304 кПа в течение 2 суток. Для проведения синтеза под действием микроволнового излучения использовался реактор MARS-6 с временем воздействия микроволнового излучения 10 мин и мощностью 700 Вт. Соотношение компонентов в реакционной смеси и значение рН в случае гидротермального и микроволнового методов синтеза были идентичны описанным выше в методике синтеза соосаждением. В дальнейшем для образцов, полученных методами соосаждения, гидротермальным и микроволновым соответственно используются обозначения MgCoX/AlFeY-с, MgCoX/AlFeY-ht и MgCoX/AlFeY-mw, где Х, Y –атомные доли кобальта и железа (в %) среди двух- и трехвалентных металлов, задаваемые при синтезе. Продукты осаждения, полученные всеми тремя методами, отделяли от маточного раствора, образцы промывали дистиллированной водой и высушивали при 120°С.
Рентгенофазовый анализа (РФА) осуществляли на дифрактометре Rigaku (CuKα-излучение) с шагом сканирования по 2θ 0.02°. Изучение морфологии синтезированных СДГ проводили методом просвечивающей электронной микроскопии (ПЭМ) на микроскопе JEOL JEM-2100 при рабочем напряжении 200 кВ. Также структуру образцов изучали с использованием дифракции электронов в выбранной области. Элементный состав образцов определяли с использованием растрового электронного микроскопа FEI Quanta 200 3D, оснащенного энергодисперсионным спектрометром (ЭДС) рентгеновского излучения фирмы EDAX при рабочем напряжении 30 кВ. ИК-спектры синтезированных образцов регистрировали с использованием ИК-фурье-спектрометра Shimadzu IR Prestige 21. Регистрацию осуществляли для смеси образцов с бромидом калия. Способность образцов притягиваться магнитом оценивали с использованием магнита в виде параллелепипеда 49 × 8 × 4 мм, сделанного из сплава Nd–Fe–B.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В предыдущих исследованиях [10] при синтезе железокобальтсодержащих СДГ в карбонатной форме в качестве раствора-осадителя нами использовалась смесь гидроксида и карбоната натрия. Последующие эксперименты показали, что осаждение только раствором гидроксида натрия приводит к проявлению магнитных свойств при введении в образцы заметно меньших количеств железа и кобальта. В настоящем исследовании использовали в качестве осадителя гидроксид натрия. В результате преобладающим анионом в образцах СДГ стал нитрат, хотя присутствие карбонатов, источником которых является диоксид углерода из воздуха, также нельзя исключить.
Наличие азота в образцах подтверждается результатами локального рентгеноспектрального анализа (рис. 1). Содержание углерода (в виде карбонатов), возможно, ниже чувствительности метода. В ЭДС-спектрах детектируются все металлы, вводимые при синтезе. Сигналы посторонних элементов отсутствуют. В табл. 1 представлены атомные доли катионов металлов, рассчитанные по данным локального рентгеноспектрального анализа. Из соотношения М2+/М3+ следует, что в среднем в образцах, полученных соосаждением, содержание двухзарядных катионов больше, чем в образцах, полученных двумя другими методами. Относительно меньшее количество двухзарядных катионов фиксируется в образцах, полученных микроволновым синтезом.
Рис. 1.
Результаты локального рентгеноспектрального анализа, полученные с использованием ЭДС, для образцов, синтезированных различными способами: a – MgCo40/AlFe40-с, б – MgCo40/AlFe40-ht, в – MgCo40/AlFe40-mw.
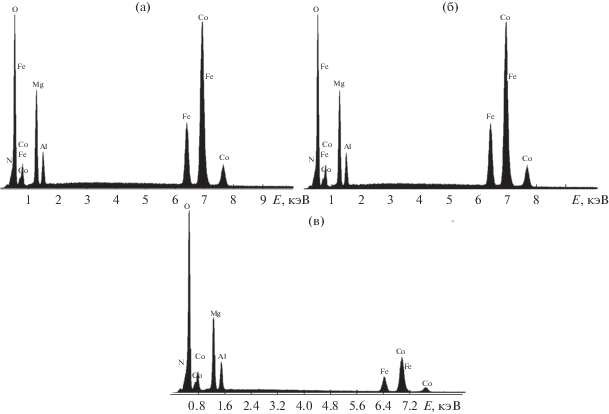
Таблица 1.
Атомные доли катионов металлов и параметры кристаллической решетки фазы СДГ
| Образец | Атомные доли катионов* | M2+/M3+ | c, Å | a, Å | |||
|---|---|---|---|---|---|---|---|
| Mg2+ | Co2+ | Al3+ | Fe3+ | ||||
| MgCo10/AlFe10-c | 0.682 | 0.096 | 0.191 | 0.031 | 3.50 | 23.88 | 3.09 |
| MgCo20/AlFe20-c | 0.604 | 0.173 | 0.172 | 0.052 | 3.48 | 24.14 | 3.09 |
| MgCo30/AlFe30-c | 0.512 | 0.258 | 0.145 | 0.085 | 3.35 | 23.84 | 3.09 |
| MgCo40/AlFe40-c | 0.435 | 0.338 | 0.117 | 0.109 | 3.41 | 24.00 | 3.10 |
| MgCo50/AlFe50-c | 0.382 | 0.388 | 0.101 | 0.128 | 3.36 | 23.93 | 3.12 |
| MgCo10/AlFe10-ht | 0.672 | 0.091 | 0.203 | 0.035 | 3.22 | 23.88 | 3.03 |
| MgCo20/AlFe20-ht | 0.595 | 0.168 | 0.186 | 0.051 | 3.21 | 23.97 | 3.09 |
| MgCo30/AlFe30-ht | 0.524 | 0.225 | 0.172 | 0.079 | 2.97 | 23.93 | 3.09 |
| MgCo40/AlFe40-ht | 0.447 | 0.306 | 0.139 | 0.109 | 3.04 | 24.02 | 3.10 |
| MgCo50/AlFe50-ht | 0.366 | 0.382 | 0.126 | 0.127 | 2.97 | 23.94 | 3.12 |
| MgCo10/AlFe10-mw | 0.633 | 0.102 | 0.228 | 0.037 | 2.78 | 23.30 | 3.07 |
| MgCo20/AlFe20-mw | 0.572 | 0.187 | 0.179 | 0.062 | 3.14 | 24.53 | 3.10 |
| MgCo30/AlFe30-mw | 0.486 | 0.264 | 0.161 | 0.089 | 3.00 | 23.83 | 3.08 |
| MgCo40/AlFe40-mw | 0.449 | 0.295 | 0.147 | 0.108 | 2.92 | 23.49 | 3.10 |
| MgCo50/AlFe50-mw | 0.345 | 0.400 | 0.116 | 0.138 | 2.93 | 23.48 | 3.07 |
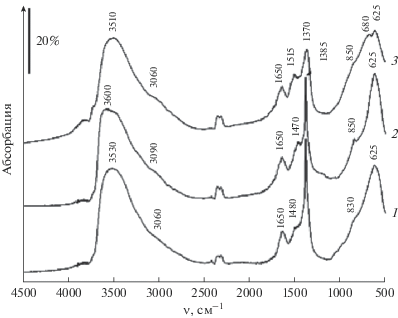
ИК-спектры всех образцов имеют вид, типичный для гидроталькитоподобных соединений (рис. 2), и подтверждают наличие нитрат-анионов в составе синтезированных материалов. В спектрах наблюдается расщепленная полоса в интервале 1370–1515 см–1. Интенсивный пик 1384 см–1 обычно относят к антисимметричным валентным колебаниям нитрат-анионов. Появление плеча 1470–1515 см–1 может быть обусловлено снижением симметрии некоторых нитрат-анионов oт D3h до С2ν, т.е. от “свободных” до монодентатных и/или бидентатных [12]. Согласно литературным данным, в области ниже 1000 см–1 проявляются как полосы, отвечающие деформационным колебаниям нитрат-анионов, так и полосы, относящиеся к колебаниям металл-кислород [12–14]. Полосу низкой интенсивности в области 2250–2375 см–1 обычно относят к атмосферному СО2.
Рис. 2.
ИК-спектры образцов, синтезированных различными способами: 1 – MgCo40/AlFe40-с, 2 – MgCo40/AlFe40-ht, 3 – MgCo40/AlFe40-mw.
Рентгеновские дифрактограммы образцов, полученных различными методами, приведены на рис. 3–5. Во всех случаях фаза СДГ преобладает – на всех дифрактограммах присутствуют семь рефлексов: 003, 006, 009/012, 015, 018, 110 и 113. Наиболее интенсивные и узкие рефлексы наблюдаются на дифрактограммах образцов СДГ, синтезированных в гидротермальных условиях (рис. 4), что свидетельствует о высокой степени кристалличности образцов. Методом Ритвельда были рассчитаны параметры кристаллической решетки СДГ (табл. 1). Параметр с коррелирует с величиной межслоевого расстояния. Расстояния между соседними катионами в бруситоподобном слое характеризуются параметром а [1, 15, 16]. Ожидалось, что введение в структуру бруситоподобных слоев более крупных по сравнению с магнием и алюминием катионов кобальта и железа должно приводить к увеличению параметра а. Действительно, такая тенденция прослеживается в сериях СДГ, синтезированных соосаждением и гидротермальным способом (табл. 1): с ростом содержания железа и кобальта увеличивается значение а.
Рис. 3.
Рентгеновские порошковые дифрактограммы образцов, синтезированных соосаждением: 1 – MgCo10/AlFe10, 2 – MgCo20/AlFe20, 3 – MgCo30/AlFe30, 4 – MgCo40/AlFe40, 5 – MgCo50/AlFe50.
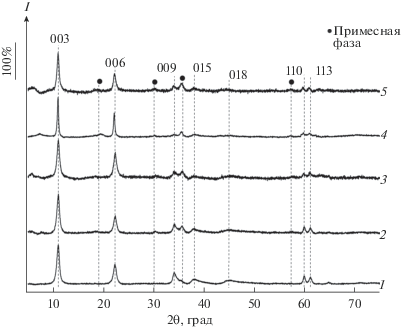
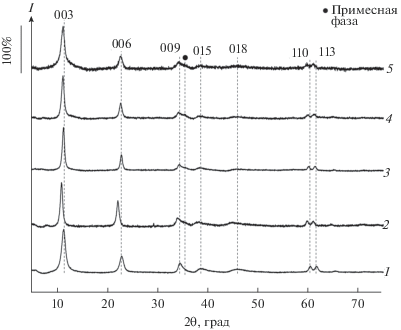
Рис. 4.
Рентгеновские порошковые дифрактограммы образцов, полученных гидротермальным синтезом: 1 – MgCo10/AlFe10, 2 – MgCo20/AlFe20, 3 – MgCo30/AlFe30, 4 – MgCo40/AlFe40, 5 – MgCo50/AlFe50.
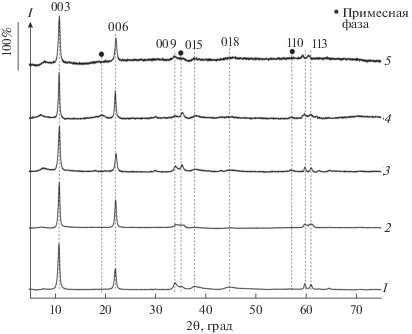
Рис. 5.
Рентгеновские порошковые дифрактограммы образцов, полученных микроволновым синтезом: 1 – MgCo10/AlFe10, 2 – MgCo20/AlFe20, 3 – MgCo30/AlFe30, 4 – MgCo40/AlFe40, 5 – MgCo50/AlFe50.
Все синтезированные образцы за исключением MgCo10/AlFe10-mw легко агломерируют под воздействием внешнего магнитного поля и способны притягиваться к магниту. В литературе существуют два противоположных мнения о природе ферромагнетизма кобальт-железных СДГ. В работе [9] показано, что ферромагнетизм при комнатной температуре наблюдался только для образцов, содержащих более 50 ат. % кобальта и железа в позициях двух- и трехзарядных катионов соответственно. Авторы объясняют ферромагнетизм полученных СДГ сосуществованием ферромагнитных взаимодействий Co2+–O2––Co2+ и антиферромагнитных взаимодействий Co2+–O2––Fe3+ и Fe3+–O2––Fe3+. Однако авторы [17] опровергают это заключение, полагая, что магнетизм при комнатной температуре в подобных системах может быть обусловлен присутствием примесей аморфных фаз, таких как ферригидрит (FeOOH) или наночастицы оксидов железа (маггемита и магнетита), которые могут не детектироваться с помощью РФА.
Результаты настоящего исследования согласуются с мнением авторов [17]. Большинство синтезированных нами образцов не являются однофазными продуктами. На дифрактограммах образцов присутствуют рефлексы примесной фазы, и есть основания полагать, что магнитные свойства обусловлены ее наличием. Действительно, рефлексы примесной фазы наименее выражены на дифрактограммах образцов, полученных микроволновым синтезом, и синтезированный этим методом образец с низким содержанием железа и кобальта магнитом не притягивается.
Вопрос о природе фазы, придающей образцам магнитные свойства, является дискуссионным. Сравнение дифрактограмм синтезированных образцов cо стандартными данными позволяет предположить, что примесная фаза представляет собой СoFe2O4 (PDF2 00-001-1121). Структура шпинели с отражениями 111, 220, 311 и 511 достаточно отчетливо идентифицирована на дифрактограммах образцов, полученных методом соосаждения. В пользу образования шпинели свидетельствует также тот факт, что трехметаллические СДГ, содержащие только железо или только кобальт, не магнитны.
Известно, что шпинель CoFe2O4 демонстрирует ферромагнитное поведение при комнатной температуре [18]. Формирование подобных структур в условиях синтеза, описанных в данной работе, возможно. Так, авторы [19] сообщают, что при соосаждении раствором гидроксида натрия из водных растворов хлоридов Co(II) и Fe(III), взятых в мольном соотношении 1 : 2, при 80°С возможно образование CoFe2O4. В работе [18] описан синтез наночастиц шпинели CoFe2O4 гидротермальным методом при различных температурах от 90 до 180°С с использованием ацетата кобальта(II) и хлорида железа(III) в качестве источников катионов металлов и гидроксида калия в качестве осадителя.
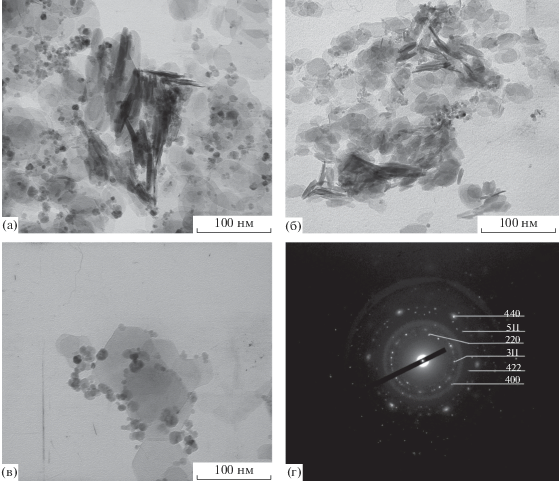
Морфологию синтезированных в настоящей работе образцов оценивали методом ПЭМ. Для образцов, полученных всеми тремя методами, удалось зафиксировать агрегаты пластинчатых частиц, в том числе и гексагональной формы, характерные для СДГ (рис. 6). Наряду с ними наблюдаются кристаллы иной формы. Дифракционная картина выделенной области этой примесной фазы для образца MgCo40/AlFe40-ht представлена на рис. 6г. Дифракционные кольца были проиндексированы как 220, 311, 400, 422, 511 и 440, что соответствует кубической гранецентрированной решетке шпинели и согласуется с данными РФА. По всей вероятности, осаждение смесью гидроксида и карбоната натрия, практиковавшееся нами в предыдущих исследованиях [10], в меньшей степени способствует формированию шпинельной фазы из-за осаждения основных карбонатов железа и кобальта. Отказ от введения в систему карбонатов в настоящей работе привел к формированию магнитной фазы при более низких содержаниях железа и кобальта.
ЗАКЛЮЧЕНИЕ
Синтез материалов, содержащих MgCo/AlFe-СДГ, возможен как соосаждением, так и гидротермальным или микроволновым методами. При использовании в качестве осадителя гидроксида натрия появление у образцов магнитных свойств происходит при более низком содержании железа и кобальта, чем это наблюдалось при гидроксидно-карбонатном осаждении. Магнитные свойства синтезированных материалов, вероятно, обусловлены присутствием примесной фазы шпинели СoFe2O4. При одинаковых составах реакционной смеси относительно меньшее количество шпинельной фазы образуется в ходе микроволнового синтеза. Хорошо окристаллизованная фаза СДГ в нитратной форме образуется при использовании всех трех методов синтеза.
Список литературы
Cavani F., Trifirò F., Vaccari A. Hydrotalcite-Type Anionic Clays: Preparation, Properties And Applications// Catal. Today. 1991. V. 11. P. 173–301. https://doi.org/10.1016/0920-5861(91)80068-K
Третьяков Ю.Д., Елисеев А.А., Лукашин А.В. Синтез функциональных нанокомпозитов на основе твердофазных нанореакторов // Успехи химии. 2004. Т. 73. № 9. С. 974–998.
Rives V., Arco M., Martín C. Intercalation of Drugs in Layered Double Hydroxides and Their Controlled Release: A Review // Appl. Clay Sci. 2014. V. 88–89. P. 239–269. https://doi.org/10.1016/j.clay.2013.12.002
Liang X., Zang Y., Xu Y., Tan X., Hou W., Wang L., Sun Y. Sorption of metal Cations on Layered Double Hydroxides // Colloids Surf., A. 2013. V. 433. P. 122–131. https://doi.org/10.1016/j.colsurfa.2013.05.006
Goha K.-H., Lima T.-T., Dong Z. Application of Layered Double Hydroxides for Removal of oxyanions: A Review // Water Res. 2008. V. 42. P. 1343–1368. https://doi.org/10.1016/j.watres.2007.10.043
Wang W., Zhang N., Shi Z., Ye Z., Gao Q., Zhi M., Hong Z. Preparation of Ni-Al Layered Double Hydroxide Hollow Microspheres for Supercapacitor Electrode // Chem. Eng. J. 2018. V. 338. P. 55–61. https://doi.org/10.1016/j.cej.2018.01.024
Fan G., Li F., Evans D.G., Duan X. Catalytic Applications of Layered Double Hydroxides: Recent Advances and Perspectives // Chem. Soc. Rev. 2014. V. 43. P. 7040–7066. https://doi.org/10.1039/C4CS00160E
Tanasoi S., Mitran G., Tanchoux N., Cacciaguerra T., Fajula F., Sandulescu I., Tichit D., Marcua I.-C. Transition Metal-containing Mixed Oxides Catalysts Derived from LDH Precursors for Short-Chain Hydrocarbons Oxidation // Appl. Catal., A. 2011. V. 395. P. 78–86. https://doi.org/10.1016/j.apcata.2011.01.028
Li Q., Xing L., Lu X., Li N., Mingxiang X. Magnetic Properties of Mg/Co(II)–Al/Fe(III) Layered Double Hydroxides // Inorg. Chem. Commun. 2015. V. 52. P. 46–49. https://doi.org/10.1016/j.inoche.2014.12.014
Рыльцова И.Г., Нестройная О.В., Лебедева О.Е., Воронцова О.А., Косова Н.И., Курзина И.А. Синтез и изучение новых слоистых двойных гидроксидов магния-кобальта-железа со структурой гидроталькита // Журн. неорган. химии. 2014. Т. 59. № 12. С. 1652–1659. https://doi.org/10.7868/S0044457X14120216
Рыльцова И.Г., Тарасенко Е.А., Нестройная О.В., Лебедева О.Е. Сорбционные свойства MgCo/AlFe слоистых двойных гидроксидов // Сорбционные и хроматографические процессы. 2019. Т. 19. № 3. С. 305– 314. https://doi.org/10.17308/sorpchrom.2019.19/747
Xu Z.P., Zeng H.C. Decomposition Pathways of Hydrotalcite-like Compounds Mg1 – xAlx(OH)2(NO3)x· nH2O as a Continuous Function of Nitrate Anions // Chem. Mater. 2001. V. 13. № 12. P. 4564–4572. https://doi.org/10.1021/cm010347g
Seftel E.M., Popovici E., Mertens M., Cool P., Vansant E.F. Infrared and Raman Spectroscopic Study of Sn-containing Zn/Al-Layered Double Hydroxides// J. Optoelectron. Adv. Mater. 2008. V. 10. P. 3477–3481.
Kloprogge J.T., Wharton D., Hickey L., Frost R.L. Infrared and Raman Study of Interlayer Anions ${\text{CO}}_{3}^{{2 - }},$ ${\text{NO}}_{3}^{ - },$ ${\text{SO}}_{4}^{{2 - }}$ and ${\text{CIO}}_{4}^{ - }$ in Mg/Al-Hydrotalcite // Am. Mineral. 2002. V. 87. P. 623–629. https://doi.org/10.2138/am-2002-5-604
Evans D.G., Slade R.C.T. Structural Aspects of Layered Double Hydroxides // Layered Double Hydroxides. Structure and Bonding / Eds. Duan X., Evans D.G. V. 119. Berlin, Heidelberg: Springer, 2005. P. 1–87. https://doi.org/10.1007/430_005
Rozov K.B., Berner U., Kulik D.A., Diamond L.W. Solubility and Thermodynamic Properties of Carbonate-bearing Hydrotalcite–pyroaurite Solid Solutions with a 3 : 1 Mg/(Al + Fe) Mole Ratio // Clays Clay Miner. 2011. V. 59. № 3. P. 215–232. https://doi.org/10.1346/CCMN.2011.0590301
Abellen G., Carrasco J., Coronado E. Room Temperature Magnetism in Layered Double Hydroxides due to Magnetic Nanoparticles // Inorg. Chem. 2013. V. 52. № 14. P. 7828–7830. https://doi.org/10.1021/ic400883k
Liu W., Chan Y., Cai J., Leung C., Mak C., Wong K., Zhang F., Wu X., Qi X.D. Understanding the Formation of Ultrafine Spinel CoFe2O4 Nanoplatelets and Their Magnetic Properties // J. Appl. Phys. 2012. V. 112. P. 104306. https://doi.org/10.1063/1.4765033
Roy P., Manjura H.S., Liba S.I., Choudhury S. Investigation of Various Magnetic Features of Spinel Type Cobalt Ferrite (CoFe2O4) Nanoparticles Tuned by Annealing Temperature // AIP Advances. 2018. V. 8. P. 105124. https://doi.org/10.1063/1.5040890
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы