Неорганические материалы, 2021, T. 57, № 12, стр. 1373-1379
Высокотемпературный синтез материалов в системе Cr–Mo–Al–C
В. А. Горшков 1, *, Д. Ю. Ковалев 1, О. Д. Боярченко 1, А. Е. Сычев 1
1 Институт структурной макрокинетики и проблем материаловедения им. А.Г. Мержанова
Российской академии наук (ИСМАН)
142432 Московская область, Черноголовка, ул. Академика Осипьяна, 8, Россия
* E-mail: gorsh@ism.ac.ru
Поступила в редакцию 21.05.2021
После доработки 02.08.2021
Принята к публикации 20.08.2021
Аннотация
Исследован высокотемпературный синтез литых композиционных материалов в системе Cr–Mo–Al–C. Впервые методом самораспространяющегося высокотемпературного синтеза в режиме горения из порошковой смеси Cr2O3 + MoO3 + Al + C получены материалы на основе фазы (Cr1 –xMox)2AlC. Синтез проводили в реакторе объемом 3 дм3 при давлении аргона 5 МПа. Показано, что соотношение исходных реагентов оказывает влияние на фазовый состав и структуру продуктов. Синтезированные материалы содержат фазы переменного состава (Cr1 –xMox)2AlC и (MoxCr1 –x)3Al2C, а также вторичные фазы карбидов и интерметаллидов хрома и молибдена. Полученные продукты охарактеризованы методами рентгеновской дифракции и электронной микроскопии.
ВВЕДЕНИЕ
Большой интерес вызывают соединения переходных металлов с алюминием и углеродом, особенно Mn + 1AlСn (M – переходный металл), относящиеся к семейству MAX-фаз [1]. Они имеют слоистую кристаллическую структуру с гексагональной плотной упаковкой P63/mmc, в которой карбидные блоки [Мn + 1Cn] разделены монослоями атомов Al. Интерес к MAX-фазам обусловлен физико-химическими свойствами, связанными с особенностями кристаллической структуры. Материалы на их основе обладают свойствами, объединяющими достоинства металлов и керамики: низким удельным весом, высокой прочностью, низким коэффициентом теплового расширения, устойчивостью к окислению и термическому удару [2]. В семействе MAX-фаз благодаря устойчивости в окислительной среде обращает на себя внимание фаза Cr2AlC [3–5]. Основными способами ее получения являются синтез из элементов методом горячего прессования (HIP), плазменно-искровое спекание (SPS) [6–10].
Изоморфное замещение в соединениях Mn + 1AlСn атомов переходного металла M близким по Периодической системе элементом ведет к изменению физико-химических свойств, что важно при создании функциональных материалов на основе четверных и более соединений со структурой МАХ-фазы. Известна возможность легирования Cr2AlC d-металлами 4-го периода Периодической системы элементов. Синтезирован ряд соединений на основе Cr2AlC при замещении части атомов Cr атомами Ti, Mn, V, Fe. В системе Cr–V–Al–C методом горячего прессования и спекания были получены фазы (Cr1 –xVx)2AlC в широком интервале составов [11–13]. В работе [14] методом микроволнового нагрева и спекания было проведено легирование Cr2AlC марганцем и железом. МАХ-фазы (Cr2/3Ti1/3)3AlC2 и (Cr5/8Ti3/8)4AlC3 и ряд твердых растворов (Cr1 – xTix)2AlC (x = 0.05–0.2) синтезированы методом горячего прессования порошков элементов при 1500°С в течение 1 ч под давлением 30 МПа в протоке аргона [15, 16]. Вместе с тем представляет интерес легирование Cr2AlC d-металлами других периодов, в частности Mo. МАХ-фаз, где в качестве элемента M выступает Mo, не существует. Из тройных фаз в системе Mo–Al–C известна Mo3Al2C – сверхпроводник с температурой перехода ~9 K, которую получали методом дугового плавления при давлении ~10 ГПа [17, 18].
Перспективным методом получения MAX-фаз является самораспространяющийся высокотемпературный синтез (СВС), практически не требующий затрат электроэнергии и обладающий достаточной производительностью [19, 20]. Методом СВС получены МАХ-фазы Ti2AlC, Ti3AlC2, Ti3SiC2 [21–23]. Авторы использовали исходные смеси, состоящие из порошков титана, алюминия, углерода и кремния. Другой подход – СВС-металлургия – заключается в использовании исходных смесей, состоящих из оксидов металлов, алюминия и углерода. Температура горения таких смесей превышает температуру плавления исходных реагентов и продуктов. В результате материал в процессе синтеза переходит в жидкое состояние с последующим фазоразделением и формированием слитка. Этот подход был ранее реализован при получении литых материалов на основе МАХ-фаз Cr2AlC [24, 25], V2AlC [26] и (V,Cr)AlC [27].
Целью настоящей работы является установление возможности получения методом СВС новых материалов на основе системы Cr–Mo–Al–C из порошковых смесей оксидов хрома(III), молибдена(VI) с алюминием и углеродом.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В экспериментах использовали порошки оксида хрома(III) и молибдена(VI) квалификации “ч. д. а.”, алюминий (АСД-1) и графит (ПГ). Для расчета состава шихты использовали следующую суммарную химическую реакцию в расчете на получение МАХ-фазы (Cr1 –nMon)2AlC для значений n = 0, 0.4, 0.5, 0.6 и 1.
(1)
$\begin{gathered} \left( {1--n} \right){\text{C}}{{{\text{r}}}_{{\text{2}}}}{{{\text{O}}}_{3}} + 2n{\text{Mo}}{{{\text{O}}}_{3}} + \left( {3 + 2n} \right){\text{Al}} + {\text{C}} = \\ = \,\,{{\left( {{\text{C}}{{{\text{r}}}_{{1--n}}}{\text{M}}{{{\text{o}}}_{n}}} \right)}_{2}}{\text{AlC}} + \left( {1 + n} \right){\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{О}}}_{{\text{3}}}}. \\ \end{gathered} $Перед смешиванием порошки выдерживали в сушильном шкафу СНОЛ в течение 3 ч при температуре 60°С. Шихту готовили перемешиванием вручную в фарфоровой ступке. Реакционную смесь насыпной плотности и массой 20 г помещали в кварцевый тигель диаметром 20 и высотой 50 мм. Синтезы проводили в СВС-реакторе объемом 3 дм3 в среде Ar при начальном давлении 5 МПа по методике, описанной в [24, 25]. Скорость горений Uг определяли по видеозаписи процесса, измеряя время прохождения волны горения по высоте образца. Для оценки параметров синтеза использовали величины η1 – выход продукта в слиток и η2 – потеря массы за счет разлета реагентов при горении:
Синтезированные материалы исследовали методами рентгеновской дифракции на дифрактометре ДРОН-3 (излучение CuKα, графитовый монохроматор на вторичном пучке) и электронной микроскопии на автоэмиссионном сканирующем электронном микроскопе сверхвысокого разрешения Zeiss Ultra plus на базе Ultra 55 с системой микроанализа INCA Energy 350 XT (Oxford Instruments). Рентгенофазовый анализ (РФА) проводился в программе Crystallographica Search-Match [28] с использованием базы дифракционных данных ICDD PDF2 [29]. Количественный РФА проводился методом Ритвельда в пакете программ PDWin “Буревестник” [30]. В качестве исходной модели для уточнения использовались структурные данные идентифицированных фаз, приведенные в Crystallography Open Database [31] и Materials Project [32]. Уточнялись профильные параметры рефлексов, фон, параметры элементарной ячейки и содержание фаз. Взвешенный (Rwp) фактор расхождения для всех образцов находился в интервале 8–12%. Для прецизионного определения параметров элементарной ячейки применялся метод внутреннего эталона, в качестве которого использовался Si (NIST SRM 640b).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При горении смеси 1 (табл. 1), не содержащей MoO3, после воспламенения на расстоянии 10–12 мм от инициирующей спирали наблюдались остановка фронта и затухание горения. Реакция является слабоэкзотермичной и распространяется в волновом режиме только при добавке в смесь высококалорийных реагентов [25].
Таблица 1.
Составы исходных смесей и параметры синтеза
| Смесь | n | Uг, см/с | η1, % | η2, % |
|---|---|---|---|---|
| 1 | 0 | 0 | – | – |
| 2 | 0.4 | 0.8 | 50 | 1.2 |
| 3 | 0.5 | 1.2 | 53 | 2.0 |
| 4 | 0.6 | 1.7 | 55 | 2.3 |
| 5 | 1 | 3.5 | 35 | 16 |
Горение смеси 5 происходило в нестационарном режиме с нелинейным фронтом и сильным выбросом материала из тигля. Реакция MoO3 + Al является высокоэкзотермичной. Скорость горения данной смеси равна 3.5 см/с. Из-за больших потерь массы (η2 = 16%) выход целевого продукта в слиток составлял η1 = 35% (табл. 1).
Смеси с различным соотношением компонентов в реакции (1) способны к горению при n > 0.2. Однако полное разделение на оксидную (Al2O3) и “металлическую” (Cr–Mo–Al–C) части происходило только в интервале n = 0.4–0.6. Смеси 2, 3 и 4 горят в стационарном режиме с практически плоским фронтом волны реакции и небольшим (менее 3%) выбросом материала из тигля. В процессе горения продукты синтеза плавятся и из-за различного удельного веса под действием гравитации разделяются на два слоя. После охлаждения слои легко отделяются друг от друга. При этом выход целевого продукта составляет от 50 до 55%.
РФА “металлических” слитков, полученных при горении смесей 2–4, показал, что в результате синтеза образуется многофазный материал (табл. 2). Максимальный выход МАХ-фазы (84 мас. %) был получен для смеси 2, содержащей минимальное количество MoO3. В этом случае дифрактограмма продукта (рис. 1а) указывает на преимущественное содержание МАХ-фазы, что подтверждается характером излома (рис. 1б) и слоистой ламинатной микроструктурой (рис. 1в, 1г).
Таблица 2.
Фазовый состав слитков, мас. %
| Смесь | 2 | 3 | 4 | 5 |
|---|---|---|---|---|
| n | 0.4 | 0.5 | 0.6 | 1 |
| x | 0.36 | 0.37 | 0.45 | 1 |
| (Cr1 –хMoх)2AlC (P63/mmc) | 84 | 69 | 8 | 0 |
| (MoхCr1 –х)3Al2C (P4132) | 0 | 0 | 92 | 71 |
| Al8Cr5 $\left( {I{{\bar {4}3}}m} \right)$ | 15 | 22 | 0 | 0 |
| Mo3Al (Pm3n) | <1 | <1 | 0 | 19 |
| Mo3Al8 (C2/m) | 0 | 0 | 0 | 6 |
| Mo2C (Pbcn) | 1 | 0 | 0 | 0 |
| MoC (P63/mmc) | 0 | 9 | <1 | 4 |
Между зернами МАХ-фазы слоистой ламинатной формы располагаются области интерметаллида Al8Cr5, содержание которого составляет 15 мас. %. Отмечается существенное смещение дифракционных рефлексов МАХ-фазы относительно углового положения рефлексов Cr2AlC (PDF2, card#000-65-3492). Сдвиг линий происходит в сторону меньших углов, что указывает на увеличение параметров элементарной ячейки. Принимая во внимание больший атомный радиус молибдена по сравнению с хромом, можно полагать, что в результате синтеза образовалась легированная молибденом МАХ-фаза (Cr1 – хMoх)2AlC. Действительно, энергодисперсионный анализ (ЭДА) областей с характерной для МАХ-фаз слоистой структурой показал, что доля атомов молибдена составляет х ~ 0.36, что меньше заложенного расчетного состава n = 0.4. Кроме того, данные СЭМ показывают неравномерное распределение Cr и Mo. В зернах МАХ-фазы наблюдаются области светло-серого цвета, обогащенные Mo, и более темные области, обедненные Mo. Продукт содержит небольшое количество фазы Mo2C, причем карбидные зерна округлой формы располагаются в областях зерен МАХ-фазы, обогащенных молибденом.
В продукте, полученном при горении смеси 3, содержание МАХ-фазы (Cr1 –хMoх)2AlC снижается до 69 мас. %, а количество примесных фаз Al8Cr5 и MoC увеличивается (табл. 2). Дифракционные рефлексы МАХ-фазы, как и в случае МАХ-фазы, синтезированной при горении смеси 2, смещены относительно углового положения рефлексов Cr2AlC (рис. 2а). Микроструктура слитка также характеризуется слоистыми ламинатными зернами (Cr1 –хMoх)2AlC, разделенными интерметаллидной прослойкой (рис. 2б). ЭДА зерен МАХ-фазы показывает, что доля атомов молибдена составляет х ~ 0.37, что ниже заложенного расчетного состава n = 0.5. Микроструктура зерен (Cr1 – хMoх)2AlC свидетельствует о концентрационной неоднородности распределения Cr и Mo. Содержание карбида молибдена заметно увеличилось по сравнению с составом 2 (табл. 2), причем карбидные зерна также располагаются в областях зерен МАХ-фазы, обогащенных Mo (рис. 2в, 2г).
С увеличением доли MoO3 (смесь 4) количество (Cr1 –хMoх)2AlC в продукте уменьшается до 8 мас. %, а основной фазой слитка является (Mo, Cr)3Al2C (табл. 2). ЭДА показал, что доля атомов Mo в элементарной ячейке МАХ-фазы (Cr1 – хMoх)2AlC достигает х ~ 0.45 (рис. 3).
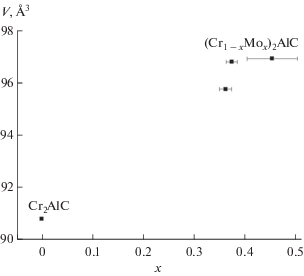
Очевидно, что полученная при горении смесей 2–4 МАХ-фаза является твердым раствором (MoхCr1 – х)3Al2C с изоморфным замещением структурных позиций атомов Cr атомами Mo. Данный вывод подтверждается также результатами прецизионного определения параметров элементарной ячейки МАХ-фазы (табл. 3). Во-первых, метрика ячейки существенно увеличивается по сравнению с фазой Cr2AlC и, во-вторых, наблюдается явная тенденция увеличения параметров ячейки (Cr1 – хMoх)3Al2C с увеличением содержания MoO3 в реакционной смеси (рис. 4).
При идентификации фазового состава продукта горения смеси 4 оказалось, что рефлексы основной фазы существенно сдвинуты от углового положения рефлексов соединения Mo3Al2C (PDF2, card#000-65-3346). Эта фаза имеет кубическую кристаллическую структуру типа β-Mn и является сверхпроводником с температурой перехода ~9 K [33]. Смещение рефлексов происходит в сторону бóльших углов относительно Mo3Al2C, что указывает на уменьшение метрики его элементарной ячейки. Учитывая меньший атомный радиус хрома по сравнению с молибденом, можно полагать, что в результате синтеза образовалась легированная хромом фаза (MoxCr1 –x)3Al2C. ЭДА областей, содержащих эту фазу, показал, что происходит замещение около половины атомов Mo атомами Cr, т.е. х ~ 0.5, а ее параметр элементарной ячейки оказался существенно ниже, чем у Mo3Al2C. Вместе с тем, параметр ячейки фазы Mo3Al2C, полученной при горении смеси 5, в которой не было Cr2O3, соответствует параметру ячейки Mo3Al2C по данным PDF2 (табл. 4).
ЗАКЛЮЧЕНИЕ
Методом СВС из смеси порошков оксидов хрома(III), молибдена(VI) с алюминием и углеродом получены литые материалы, основу которых составляют четверные соединения: (Cr1 –хMoх)2AlC и (MoхCr1 –х)3Al2C. В процессе горения продукты синтеза плавятся, а полное разделение на оксидную (Al2O3) и “металлическую” (Cr–Mo–Al–C) части происходит для смесей с соотношением реагентов (1 – n)Cr2O3 + 2nMoO3 + (3 + 2n)Al + C при n = 0.4–0.6. Синтезированные материалы содержат также карбиды молибдена и интерметаллидные фазы хрома и молибдена, что обусловлено недостаточным временем существования расплава.
Количественное соотношение фаз в конечном продукте определяется составом исходной смеси. Максимальный выход МАХ-фазы с x = = 0.36 (Cr1 –хMoх)2AlC) 84 мас. % получен для смеси с n = 0.4. Синтезированная МАХ-фаза является твердым раствором с изоморфным замещением структурных позиций атомов Cr атомами Mo и параметрами элементарной ячейки бóльшими, чем у фазы Cr2AlC. С увеличением доли MoO3 в смеси содержание Mo в (Cr1 –хMoх)2AlC возрастает до x = 0.45, однако общее содержание МАХ-фазы в конечном продукте снижается до 8 мас. %.
При горении смеси с n = 0.6 получено новое четверное соединение (Mo0.5Cr0.5)3Al2C с кристаллической структурой типа β-Mn, являющееся легированной хромом фазой Mo3Al2C. Параметр его элементарной ячейки 6.7028(7) Å существенно ниже, чем у Mo3Al2C, что связано с меньшим радиусом атома Cr по сравнению с Mo.
Список литературы
Barsoum M.W. The MAX Phases: A New Class of Solids: Thermodynamically Stable Nanolaminates // Prog. Solid State Chem. 2000. V. 28. P. 201–281. https://doi.org/10.1016/S0079-6786(00)00006-6
Hettinger J.D., Lofland S.E., Finkel P., Meehan T., Palma J., Harrell K., Gupta S., Ganguly A., El-Raghy T., Barsoum M.W. Electrical Transport, Thermal Transport, and Elastic Properties of M2AlC (M = Ti, Cr, Nb, and V) // Phys. Rev. B. Condens. Matter. 2005. V. 72. P. 115–120. https://doi.org/10.1103/PhysRevB.72.115120
Tian W.B., Wang P.L., Zhang G., Kan Y., Li Y., Yan D. Synthesis and Thermal and Electrical Properties of Bulk Cr2AlC // Scr. Mater. 2006. V. 54. P. 841–846. https://doi.org/10.1016/j.scriptamat.2005.11.009
Lin Z., Zhou Y., Li M. Synthesis, Microstructure and Property of Cr2AlC // J. Mater. Sci. Technol. 2007. V. 23. № 6. P. 721–746.
Schneider J.M., Sun Z., Mertens R., Uestel F., Ahuja R. Ab-initio Calculations and Experimental Determination of the Structure of Cr2AlC // Solid State Commun. 2004. V. 130. № 7. P. 445–449. https://doi.org/10.1016/j.ssc.2004.02.047
Tian W., Vanmeensel K., Wang P., Zhang G., Li Y., Vleugels J., Biest O. Synthesis and Characterization of Cr2AlC Ceramics Prepared by Spark Plasma Sintering // Mater. Lett. 2007. V. 61. P. 4442–4445. https://doi.org/10.1016/j.matlet.2007.02.023
Xiao Li.O., Li S.B., Song G., Sloof W.G. Synthesis and Thermal Stability of Cr2AlC // J. Eur. Ceram. Soc. 2011. V. 31. P. 1497–1502. https://doi.org/10.1016/j.jeurceramsoc.2011.01.009
Panigrahi B.B., Chu M.-C., Kim Y.-I., Cho S.-J., Gra-cio J.J. Reaction Synthesis and Pressureless Sintering of Cr2AlC Powder // Am. Ceram. Soc. Bull. 2010. V. 93. № 6. P. 1530–1533. https://doi.org/10.1111/j.1551-2916.2009.03560.x
Xiao D., Zhu J., Wang F., Tang Y. Synthesis of Nano Sized Cr2AlC Powders by Molten Salt Method // J. Nanosci. Nanotechnol. 2015. V. 15. № 9. 7341–7345. https://doi.org/10.1166/jnn.2015.10590
Duan X., Shen L., D. Jia, Zhou Y., Zwaag S., Sloof W.G. Synthesis of High-purity, Isotropic or Textured Cr2AlC Bulk Ceramics by Spark Plasma Sintering of Pressure-less Sintered Powders // J. Eur. Ceram. Soc. 2015. V. 35. № 5. P. 1393–1400. https://doi.org/10.1016/j.jeurceramsoc.2014.11.008
Zhou Y.C., Meng F.L., Zhang J. New MAX-Phase Compounds in the V–Cr–Al–C System // J. Am. Ceram. Soc. 2008. V. 91. P. 1357–1360. https://doi.org/10.1111/j.1551-2916.2008.02279.x
Halim J., Chartier P., Basyuk T., Prikhna T., Caspie E.N., Barsoum M.W., Cabioc’h T. Structure and Thermal Expansion of (Crx,V1 – x)n + 1AlCn Phases Measured by X-ray Diffraction // J. Eur. Ceram. Soc. 2017. V. 37. P. 15–21. https://doi.org/10.1016/j.jeurceramsoc.2016.07.022
Caspie E.N., Chartier P., Porcher F., Damay F., Cabioc’h T. Ordering of (Cr,V) Layers in Nanolamellar (Cr0.5V0.5)n + + 1AlCn Compounds // Mater. Res. Lett. 2015. V. 3. № 2. P. 100–106.
Hamm C.M., Bocarsly J.D., Seward G., Kramm U.I., Birke C.S. Non-Conventional Synthesis and Magnetic Properties of MAX Phases (Cr/Mn)2AlC and (Cr/Fe)2AlC // J. Mater. Chem. 2017. V. 5. № 23. P. 5700–5708. https://doi.org/10.1039/C7TC00112F
Liu Z., Zheng L., Sun L., Qian Y., Wang J., Li M. (Cr2/3Ti1/3)3AlC2 and (Cr5/8Ti3/8)4AlC3: New MAX-phase Compoundsin Ti–Cr–Al–C System // J. Am. Ceram. Soc. 2014. V. 97. № 1. P. 67–69. https://doi.org/10.1111/jace.12731
Kim C., Hwang S., Ha J., Kang S., Cheong D. Synthesis of a Cr2AlC-Ti2AlC Ternary Carbide // J. Ceram. Proc. Res. 2010. V. 11. № 1. P. 82–85.
Karki A.B., Xiong Y.M., Vekhter I., Browne D., Adams P.W., Thomas K.R., Chan J.Y., Prozorov R., Kim H., Young D.P. Structure and Physical Properties of the Noncentrosymmetric Superconductor Mo3Al2C // Phys. Rev. B: Condens. Matter. 2010. V. 82. № 6. 064512. https://doi.org/10.1103/PhysRevB.82.064512
Bonalde I., Kim H., Prozorov R., Rojas C., Rogl P., Bauer E. Evidence for Conventional Superconducting Behavior in Noncentrosymmetric Mo3Al2C // Phys. Rev. B: Condens. Matter. 2011. V. 84(134506). P. 1–4. https://doi.org/10.1103/PhysRevB.84.134506
Merzhanov A.G. The Chemistry of Self-Propagating High-Temperature Synthesis // J. Mater. Chem. 2004. V. 14. № 12. P. 1779–1786. https://doi.org/10.1039/B401358C
Levashov E.A., Mukasyan A.S., Rogachev A.S., Shtansky D.V. Self-Propagating High-Temperature Synthesis of Advanced Materials and Coatings // Int. Mater. Rev. 2017. V. 62. № 4. P. 203–239. https://doi.org/10.1080/09506608.2016.1243291
Łopacinski M., Puszynski J., Lis J. Synthesis of Ternary Titanium Aluminum Carbides Using Self-Propagating High-Temperature Synthesis Technique // J. Am. Ceram. Soc. 2001. V. 84. № 12. P. 3051–3053 https://doi.org/10.1111/j.1151-2916.2001.tb01138.x
Zhu C.C., Zhu J., Wu H., Lin H. Synthesis of Ti3AlC2 by SHS and Thermodynamic Calculation Based on First Principles // Rare Met. 2015. V. 34. № 2. P. 107–110. https://doi.org/10.1007/s12598-013-0174-2
Konovalikhin S.V., Kovalev D.Yu., Sytschev A.E., Vadchenko S.G., Shchukin A.S. Formation of Nanolaminate Structures in the Ti–Si–C System: a Crystallochemical Study // Int. J. Self-Propag. High-Temp Synth. 2014. V. 23. № 4. P. 217–221. https://doi.org/10.3103/S1061386214040049
Gorshkov V.A., Miloserdov P.A., Luginina M.A., Sachkova N.V., Belikova A.F. High-Temperature Synthesis of a Cast Material with a Maximum Content of the MAX Phase Cr2AlC // Inorg. Mater. 2017. V. 53. № 3. P. 271–277. https://doi.org/10.1134/S0020168517030062
Gorshkov V.A., Miloserdov P.A., Khomenko N.Yu., Sachkova N.V. Production of Cast Materials Based on the Cr2AlC MAX Phase by SHS Metallurgy Using Coupled Chemical Reactions // Russ. J. Non-Ferr. Met. 2020. V. 61. № 3. P. 362–367. https://doi.org/10.3103/S1067821220030086
Горшков В.А., Карпов А.В., Ковалев Д.Ю., Сычев А.Е. Синтез, структура и свойства материала на основе MAX-фазы V2AlC // Физика металлов и металловедение. 2020. Т. 121. № 8. С. 842–848 https://doi.org/10.31857/S0015323020080033
Сычёв А.Е., Горшков В.А., Карпов А.В., Сачкова Н.В., Ковалёв И.Д., Беликова А.Ф. Синтез и свойства композиционного материала на основе твердого раствора (V,Cr)AlC // Физика металлов и металловедение. 2021. Т. 122. № 3. С. 306–313. https://doi.org/10.31857/S0015323021030141
Siegrist T. Crystallographica – a Software Toolkit for Crystallography // J. Appl. Crystallogr. 1997. V. 30. P. 418–419. http://www.crystallographica.co.uk.
International Centre for Diffraction Data. http://www.icdd.com/.
Фирсова В.А., Пятыгина Н.Г., Иванова Т.И. Метод Ритфельда – Rietveld. Свидетельство о регистрации программы для ЭВМ № 2010613016 от 06.05.10.
Crystallography Open Database. http://www.crystallography.net/cod.
Jain A., Ong S.P., Hautier G. The Materials Project: a Materials Genome Approach to Accelerating Materials Innovation // APL Mater. 2013. V. 1. № 1. 011002.https://doi.org/10.1063/1.4812323 https://materialsproject.org/.
Bauer E., Rogl G., Chen X.-Q., Khan R.T., Michor H., Hilscher G., Royanian E., Kumagai K., Li D.Z., Li Y.Y., Podloucky R. Rogl P. Unconventional Superconducting Phase in the Weakly Correlated Noncentrosymmetric Mo3Al2C Compound // Phys. Rev. B. 2010. V. 82. 064511. https://doi.org/10.1103/PhysRevB.82.064511
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы