Неорганические материалы, 2021, T. 57, № 9, стр. 940-948
Определение методом РФЭС степени окисления изотопа технеция 99Tc на активированных углях
Ю. А. Тетерин 1, 3, А. В. Макаров 2, *, А. В. Сафонов 2, Е. В. Захарова 2, К. И. Маслаков 3, А. Ю. Тетерин 1
1 НИЦ “Курчатовский институт”
123182 Москва, Пл. Академика Курчатова, 1, Россия
2 Институт физической химии и электрохимии им. А.Н. Фрумкина Российской академии наук
117342 Москва, ул. Обручева, 40, стр. 1, Россия
3 Московский государственный университет им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
* E-mail: ya.alexmakar@yandex.ru
Поступила в редакцию 29.12.2020
После доработки 08.04.2021
Принята к публикации 19.04.2021
Аннотация
Изучена степень окисления 99Tc, адсорбированного на поверхности углей АГ-3 (I) и КАУ (II) из водного раствора пертехнетата калия (KTcO4), методом РФЭС в интервале энергий связи Еb от 0 до 1250 эВ. На образце I измеренные параметры Eb(Tc3d5/2) составили 260.0, 258.2 и 258.3 эВ, что характеризует одновременное присутствие на нем трех форм: Tc7+, Tc5+ и Tc3+. В спектре Tc3d-электронов на поверхности образца II наблюдаются только два спин-дублета, характеризующие две степени окисления технеция – Tc3+ и Tc5+ с соотношением форм 23 и 77% соответственно.
ВВЕДЕНИЕ
При обращении с радиоактивными отходами большую опасность представляют долгоживущие радионуклиды, которые могут попасть в биосферу после разрушения инженерных барьеров. Среди продуктов деления 235U наиболее радиоэкологически опасным является 99Tc, что связано с его длительным периодом полураспада (213 000 лет), низкой сорбционной способностью и высокой подвижностью в аэробных условиях [1]. Для изоляции технеция необходимы подходящая матрица, а также геохимический барьер, способный локализовать радионуклид в ограниченном объеме на период в десятки тысяч лет.
Одним из перспективных материалов для иммобилизации технеция служит активированный уголь. Данный материал производится в больших объемах в России (более 12 тыс. т в год) и эффективно используется на многих водоочистных сооружениях [2]. С использованием активированного угля технеций может быть эффективно извлечен из больших объемов природной воды [3–5]. Механизм сорбции технеция на углях недостаточно изучен. Наиболее подходящей формой для иммобилизации является диоксид технеция с малой растворимостью, поэтому оценка валентного состояния технеция для определения механизма иммобилизации играет важную роль. На данный момент установлено, что время достижения сорбционного равновесия на разных углях значительно варьируется. Это может являться косвенным доказательством восстановительного механизма в иммобилизации технеция [6].
При определении методом РФЭС степени окисления Tc в веществах на основе величин энергий связи его остовных электронов основная проблема состоит в том, что разные авторы применяют неодинаковые способы калибровки энергии спектров [7–10]. Поскольку при изменении степени окисления технеция от 0 до 7+ сдвиг линии Tc3d5/2-электронов изменяется на 5.1 эВ (~0.7 эВ на единицу степени окисления, табл. 1), то возникают трудности при определении корректной величины степени окисления технеция в соединении, что приводит к несогласованности результатов различных работ. Корректные результаты могут быть получены в случае, если энергии связи определены по отношению к энергии связи C1s-электронов насыщенных углеводородов на поверхности образцов [11]. Отметим, что прецизионные данные РФЭС о соединениях технеция ограничены [7, 12, 13]. Например, отсутствуют данные для Tc2O7. Это в основном связано с высокой радиоактивностью и токсичностью таких соединений.
Таблица 1.
Энергии связи Eb*, ширины линий Г* и сечения фотоэффекта σ при 1486.6 эВ
| Tcnli Onli |
Eb, эВ (Γ, эВ) | Eat, эВ [25] | Etheor, эВ [26] | σ, кбарн/ат. [21] | ||
|---|---|---|---|---|---|---|
| KTcO4 | TcO2 | Tcmet | ||||
| РФЭС [12] | ||||||
| Tc5s | 7.0 | 5.67 | 0.608 | |||
| Tc4d5/2 | 1.2 | 6.63 | 6.86 | |||
| Tc4d3/2 | 2.0 | 7.24 | 4.77 | |||
| Tc4p3/2 | 45.0 | 41.2(3.2) | 40.1 (2.8) | 36.9 | 47.31 | 13.2 |
| Tc4p1/2 | 47.9 | 43.9(3.2) | 42.7 (2.8) | 42.8 | 53.24 | 6.82 |
| Tc4s | 75.2 (4.5) | 71.5 | 70.2 (6.5) | 68.8 | 59.03 | 6.57 |
| Tc3d5/2 | 259.7(1.8) | 255.9(1.8) | 254.6 (1.0) | 252.9 | 260.19 | 87.3 |
| Tc3d3/2 | 263.2(1.8) | 259.4(1.8) | 258.2 (1.0) | 256.4 | 264.66 | 60.3 |
| Tc3p3/2 | 433.1(3.5) | 429.5(3.6) | 428.3 (2.7 ) | 425.0 | 436.91 | 86.9 |
| Tc3p1/2 | 452.8(3.5) | 449.2(3.6) | 448.1 (2.7 ) | 444.9 | 457.11 | 44.2 |
| Tc3s | 551.4 | 547.8 | 546.3 (7.0) | 544.0 | 555.56 | 35.7 |
| O2p | ~7.7 | ~6.8 | 7.1 | 14.40 | 0.27 | |
| O2s | ~24.3 | ~23.4 | 23.7 | 24.33 | 1.91 | |
| O1s | ~532.6** | ~531.7** | 532.0 | 545.37 | 40 | |
Цель настоящей работы состояла в определении степени окисления технеция, сорбированного на активированных углях, методом РФЭС, который эффективен при подобных исследованиях [7–9, 12, 13].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Приготовление образцов. Для приготовления образцов I, II использовались промышленные активированные угли: АГ-3 – активированный графит (Sуд = 775 м2/г) и КАУ – кокосовый активированный уголь (Sуд = 977 м2/г).
Все химические вещества, используемые в представленном исследовании, относятся к классу реагентов и были получены из коммерческих источников: АГ-3 представляет собой активированный графит, изготовленный из низкотемпературной каменноугольной пыли, древесного угля и пека путем гранулирования с последующей парогазовой активацией [14]; КАУ – кокосовый активированный уголь, изготовленный из кокосовой скорлупы с последующей парогазовой активацией [15].
На данные образцы был сорбирован 99Tc в виде пертехнетат-иона $\left( {{\text{TcO}}_{4}^{ - }} \right).$ Сорбцию проводили при соотношении твердой фазы к жидкой 1 : 40, исходная концентрация водного раствора пертехнетата калия (KTcO4) составляла 10–3 моль/л, масса образца 0.5 г. Внешние условия – комнатная температура 293 ± 2 К, атмосферное давление и среда воздуха. Для определения времени установления сорбционного равновесия проводился периодический отбор жидких проб с измерением удельной активности раствора после центрифугирования. Для исследуемых образцов время наступления равновесия не превышало суток. После наступления сорбционного равновесия твердая фаза каждого образца была отделена от жидкой путем центрифугирования при 6000 об./мин в течение 10 мин, высушена при температуре 105°С, измельчена и впрессована в индий на алюминиевой подложке в виде тонких с зеркальной поверхностью пленок. Для исследования приготовлены два типа образцов: АГ-3–Тс (I) и КАУ–Тс (II).
Рентгеновская фотоэлектронная спектроскопия. РФЭС получены на спектрометре Kratos Axis Ultra DLD с AlKα-монохроматизированным рентгеновским излучением (1486.7 эВ) c низкоэнергетической пушкой для компенсации зарядки образца в вакууме 5 × 10–7 Па, при комнатной температуре. Область анализа поверхности образцов составляла около 300 × 700 мкм. Разрешение спектрометра, измеренное как ширина на полувысоте линии Au4f7/2-электронов, равно 0.7 эВ. Все энергии связи (Eb) в настоящей работе приведены относительно энергии связи C1s-электронов насыщенных углеводородов, принятой равной 285.0 эВ. Линии C1s-электронов образцов I и II наблюдались при 284.3 эВ. При этом Eb(Au4f7/2) = 84.0 эВ. Это согласуется с данными калибровки для неотожженного и отожженного при 3200°С пирографита относительно уровня Ферми золота [16–18]. Отметим, что для пластины из золота при Eb(Au4f7/2) = 84.0 эВ энергия связи C1s-электронов насыщенных углеводородов, адсорбированных на поверхности, равна Eb(C1s) = 284.1 эВ, а для эталонного графита – 284.3 эВ [16]. Это необходимо учитывать при сравнении полученных в настоящей работе результатов с данными других авторов. Погрешность при измерении величин энергий связи и ширины линий электронов равна ±0.1 эВ, а при измерении относительных интенсивностей – ±5%. Величины ширины линий на их полувысоте Г(эВ) приведены по отношению к величине Г(C1s) = 1.3 эВ. Спектральный фон, обусловленный упруго рассеянными электронами, для РФЭС вычитался по методу Ширли [19]. Деление спектров на отдельные компоненты выполнено с использованием стандартной программы SPRO-3/0, описание которой приведено в работе [20].
Количественный элементный анализ поверхности (толщиной ~3–5 нм [21]), основанный на том, что интенсивность (площадь) линий РФЭС пропорциональна концентрации ионов в исследуемом образце, проводился с использованием соотношения
(1)
${{{{n}_{i}}} \mathord{\left/ {\vphantom {{{{n}_{i}}} {{{n}_{j}}}}} \right. \kern-0em} {{{n}_{j}}}} = ({{{{I}_{i}}} \mathord{\left/ {\vphantom {{{{I}_{i}}} {{{I}_{j}}}}} \right. \kern-0em} {{{I}_{j}}}})({{{{\sigma }_{j}}} \mathord{\left/ {\vphantom {{{{\sigma }_{j}}} {{{\sigma }_{i}}}}} \right. \kern-0em} {{{\sigma }_{i}}}}){{[{{(h\nu --{{E}_{{bj}}})} \mathord{\left/ {\vphantom {{(h\nu --{{E}_{{bj}}})} {(h\nu --{{E}_{{bi}}})}}} \right. \kern-0em} {(h\nu --{{E}_{{bi}}})}}]}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}},$РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
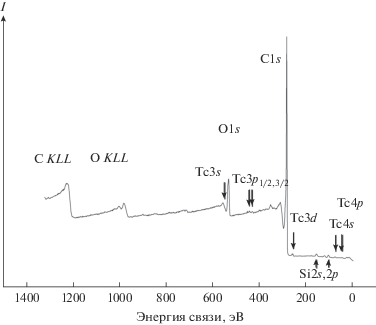
Образцы I, II изучены методом РФЭС в интервале энергий связи от 0 до 1250 эВ (рис. 1). На основании интенсивностей линий и энергий связи электронов с использованием уравнения (1) проведен количественный элементный и ионный анализ поверхности изученных образцов (I, II) по отношению к одному атому технеция (в скобках приведены доли различных ионов):
(I)
${\text{T}}{{{\text{c}}}_{{1.0}}}\left( {{\text{Tc}}_{{0.15}}^{{7 + }}{\text{Tc}}_{{0.85}}^{{5 + }}} \right){{{\text{O}}}_{{49.3 + 39.9}}}{{{\text{C}}}_{{500.7}}},$(II)
${\text{T}}{{{\text{c}}}_{{1.0}}}\left( {{\text{Tc}}_{{0.77}}^{{5 + }}{\text{Tc}}_{{0.23}}^{{3 + }}} \right){{{\text{O}}}_{{{\text{100}}{\text{.4}}}}}{{{\text{C}}}_{{551.0}}}.$Из данных количественного анализа образцов I и II следует, что на поверхности образца I в основном образуются ионы Tc5+, ионы Tc7+ присутствуют в малом количестве и отсутствуют у образца II.
Поскольку энергии связи O1s-электронов KTcO4 и TcO2 не определены, они были оценены с учетом уравнения [11]
(2)
${{E}_{b}}\left( {{\text{эВ}}} \right) = 2.27R_{{{\text{Э}} - {\text{O}}}}^{{ - 1}}\left( {{\text{нм}}} \right) + 519.4,$В данной работе в качестве эталонных данных были приняты величины энергий связи соединений KTcO4 и TcO2, полученные в работах [7, 12]. Эти энергии для удобства сравнения с данными других авторов и при анализе степени окисления технеция в соединениях приведены относительно энергии связи C1s-электронов, равной 285 эВ (табл. 1).
Энергии связи элементов на поверхности изученных образцов I, II приведены в табл. 2, а структура РФЭС отражена на рис. 1–5.
Таблица 2.
Энергии связи Eb* и ширины линий Г*
| Образец | N+ | EМО, эВ | Eb, эВ (Γ, эВ) | ∆Esl, эВ Tc3d | Eb, эВ (Γ, эВ) | |||
|---|---|---|---|---|---|---|---|---|
| Tc3d5/2 | Tc3d3/2 | O2s | O1s | C1s | ||||
| АГ-3–Тс | 5 7 |
7.7 12.7 18.3 | 258.2(1.5) 260.0(2.0) |
261.8(1.5) 263.7(2.0) |
3.6 3.7 |
24.0 27.5 |
532.3 536.3 |
284.3 (1.1) |
| КАУ–Тс | 5 3 |
258.5(1.8) 256.4(1.8) |
262.1(1.8) 260.0(1.8) |
3.6 3.6 |
531.6 534.1 |
284.3 (1.1) |
||
| Tcmet | 0 | 254.6(1.0) | 258.2(1.0) | 3.6 | ||||
| TcO2 [8] | 4 | 257.0 | ||||||
| K2TcOCl5 | 5 | 258.3(1.6) | 261.8(1.6) | 3.5 | ||||
| KTcO4 | 7 | 259.7(1.8) | 263.2(1.8) | 3.5 | 532.6 | |||
| ПГ** | 9.0 13.7 16.6 19.2 | 284.3 (0.8) |
||||||
В обзорном РФЭС образца I наблюдаются в основном линии элементов технеция, углерода и кислорода (рис. 1). В высокоэнергетической части спектра наблюдается структура, связанная с электронами C KLL и O KLL оже-спектров. В низкоэнергетической части спектра наблюдаются линии Si2s-, 2p-электронов примеси кремния в угле. Аналогичный спектр получен для образца II. В нем кроме рассмотренных линий наблюдаются линии подложки из индия: 18.1(2.1) (In4d); 444.6(1.6) (In4d5/2) и 452.2(1.6) эВ (In4d5/2). Это связано с тем, что уголь образца II был более крупнозернистым и при его прессовании в индиевую подложку между гранулами угля на поверхность выдавливался индий.
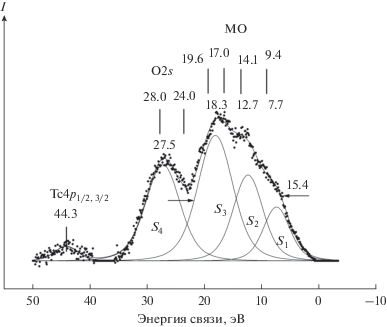
Спектры валентных электронов. В спектрах низкоэнергетической области образцов I, II наблюдаются линии электронов валентных молекулярных орбиталей (МО) от 0 до ~50 эВ (рис. 2). Наиболее интенсивные максимумы наблюдаются в области энергий связи С2s- и O2s-электронов. Поскольку сечение фотоэффекта C2s-электронов в 31.8 раза больше соответствующей величины для C2p-электронов [22], то спектр валентных электронов от 0 до 25.2 эВ в основном обусловлен C2s-электронами. Структура формирования внешних и внутренних валентных МО угля на качественном уровне описана ранее [27]. Из-за малой концентрации технеция на поверхности угля трудно количественно определить вклад Tc4d-, 5s-электронов в валентную зону угля. Однако оценить такой вклад можно. Поскольку валентная электронная конфигурация атома технеция – Tc4s24p64d55s26S2-1/2, то с учетом сечений фотоэффекта (см. 7-й столбец табл. 1) можно найти, что вклад в интенсивность спектра Тс4р-электронов вдвое больше вклада Tc4d55s2-электронов в интенсивность МО угля. А спектр Tc4p-электронов имеет небольшую интенсивность (рис. 2). В спектре валентных электронов угля наблюдаются максимумы при 7.7, 12.7 и 18.3 эВ. Энергии этих максимумов по своим значениям близки к величинам 9.0, 13.7, 16.6 и 19.2, которые характеризуют максимумы валентной зоны отожженного при 3200°С пирографита [18]. Ширина зоны активированного угля сравнима с шириной зоны пирографита, равной 25.2 эВ (рис. 2).
Спектр O2s-электронов имеет сложную структуру и наблюдается при 27.5 эВ. Величины энергий связи O2s-электронов, равные 24.0 и 28.0 эВ и соответствующие энергиям 532.3 и 536.3 эВ O1s-электронов, найдены в приближении, что разность энергий связи O1s- и O2s-электронов в атоме равна 508.3 эВ (см. 5-й столбец в табл. 1). В процессе изучения радиационных повреждений пирографита нейтронами при увеличении длительности облучения наблюдалось возникновение линии при 25 эВ O2s-электронов на поверхности [16–18]. Аналогичная картина наблюдается в спектре С2s-электронов (рис. 2).
Спектры остовных электронов. Спектры C1s-электронов образцов I, II состоят из интенсивных линий, со стороны больших энергий связи от которых наблюдаются на расстоянии ~1.5 эВ плечо, связанное с углеродом насыщенных углеводородов на поверхности образцов, и shake up-сателлиты на расстоянии ~6.5 эВ, характеризующие регулярность структуры (дальний порядок) графита (рис. 3). Ранее при изучении радиационных повреждений пирографита нейтронами с увеличением длительности облучения наблюдалось уширение линии C1s-электронов от 0.8 до 1.2 эВ и уменьшение в спектре линии С1s-электронов интенсивности shake up-сателлита при 6.5 эВ [16–18]. Для углей наблюдается уширенная линия C1s-электронов и уширенный shake up-сателлит, что связано с несовершенной структурой углей по сравнению со структурой отожженного пирографита (рис. 3).
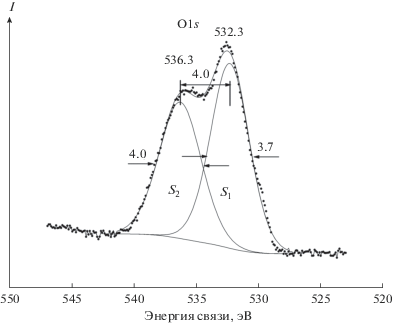
Спектры O1s-электронов образцов I, II имеют сложную структуру. В этом случае из-за интенсивных линий кислорода на поверхности трудно выделить линию O1s-электронов, относящихся к соединениям технеция. Линии кислорода на поверхности образца I наблюдаются при 532.3 и 536.3 эВ (рис. 4). На основании этих энергий можно оценить средние длины связи RЭ–O на поверхности угля из уравнения (2)
(3)
${{R}_{{{\text{Э}}--{\text{O}}}}}\left( {{\text{нм}}} \right) = 2.27{{({{E}_{b}}--519.4)}^{{--1}}}.$Они равны 0.176 нм (532.3 эВ) и 0.134 нм (536.3 эВ). Линия кислорода образца I, связанная с технецием, накладывается на высокоинтенсивную линию поверхностного кислорода при 532.3 эВ (рис. 4).
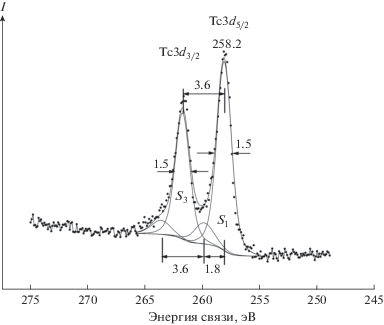
Спектр Tc3d-электронов образца I состоит из двух основных линий, обусловленных спин-орбитальным расщеплением с ∆Esl(Tc3d) = 3.6 эВ (рис. 5). Со стороны больших энергий связи наблюдаются сателлиты. Эти сателлиты не связаны с зарядкой образца, поскольку она отсутствовала при измерении. Они связаны со спектром Tc3d-электронов более высокой степени окисления технеция (табл. 2). Этот спектр с интенсивностью 15% наблюдается на расстоянии 1.8 эВ со стороны больших энергий связи от основного спектра. Энергия связи Eb(Tc3d5/2) = 260.0 эВ для образца I близка к значению 259.7 эВ для KTcO4, содержащего ионы Тс7+ (табл. 2). Величина Eb(Tc3d5/2) = 258.2 эВ основного спектра близка к соответствующему значению 258.3 эВ для K2TcOCl5, содержащего ионы Tc5+. Отметим, что спектр K2p-электронов при ~292 эВ не удается наблюдать (рис. 3), несмотря на то что сечение фотоионизации Тс3d-электронов только в 2.75 раза меньше соответствующей величины для K2p-электронов.
В спектре Tc3d-электронов поверхности образца II наблюдаются два спин-дублета, сдвинутые относительно друг друга на 2.1 эВ и характеризующие две степени окисления технеция (табл. 2). Энергия связи Tc3d5/2-электронов первого дублета, равная 256.4 эВ, характеризует ион Tc3+, а энергия связи Tc3d5/2-электронов второго дублета, равная 258.5 эВ, характеризует ион Tc5+. Концентрация ионов Tc5+ равна 77%, а ионов Tc3+ – 23% (см. ранее). В этом случае отсутствуют линии иона Tc7+.
ЗАКЛЮЧЕНИЕ
Методом РФЭС получены данные, доказывающие восстановительный механизм иммобилизации технеция на активированных углях из водного раствора пертехнетата калия (KTcO4) в окислительных условиях. На поверхности активированного графита технеций присутствовал одновременно в трех степенях окисления: 7+, 5+, 3+, а на кокосовом активированном угле – только в двух: 5+, 3+. Стоит отметить, что данные формы не характерны для технеция в растворах, особенно на воздухе, поскольку склонны к диспропорционированию до наиболее стабильных форм 7+ и 4+ в зависимости от окислительной среды.
Полученные данные свидетельствуют о наличии не только восстанавливающих, но и стабилизирующих факторов на поверхности выбранных углеродных материалов (возможно, функциональных групп органической природы), что показывает необходимость детального изучения химических и физико-химических характеристик актированных углеродных материалов и согласуется с данными [28] о высокой иммобилизационной способности АГ-3 и КАУ для технеция.
Список литературы
Лаверов Н.П., Юдинцев С.В., Коновалов Э.Е., Мишевец Т.О., Никонов Б.С., Омельяненко Б.И. Матрица для иммобилизации радиоактивного технеция // Докл. Академии наук. 2010. Т. 431. № 2. С. 196–200. https://doi.org/10.1134/S0012500810040026
Рябчиков Б.Е. Современные методы подготовки воды для промышленного и бытового использования: питьевая вода, пищевая пром-сть, энергетика. М.: ДеЛи принт, 2004. 328 с.
Daňo M., Viglašová E., Galamboš M., Rajec P., Novák I. Sorption Behaviour of Pertechnetate on Oxidized and Reduced Surface of Activated Carbon // J. Radioanal. Nucl. Chem. 2017. V. 314. № 3. P. 2219–2227. https://doi.org/10.1007/s10967-017-5532-3
Wang Y., Gao H., Yeredla R., Xu H., Abrecht M. Control of Pertechnetate Sorption on Activated Carbon by Surface Functional Groups // J. Colloid Interface Sci. 2007. V. 305. № 15. P. 209–217. https://doi.org/10.1016/j.jcis.2006.09.056
Li D., Seaman J.C., Kaplan D.I., Heald S.M., Sun C. Pertechnetate (Tc${\text{O}}_{4}^{ - }$) Sequestration from Groundwater by Cost-Effective Organoclays and Granular Activated Carbon under Oxic Environmental Conditions // Chem. Eng. J. 2019. V. 360. P. 1–9. https://doi.org/10.1016/j.cej.2018.11.146
Holm E., Gäfvert T., Lindahl P., Roos P. In situ Sorption of Technetium Using Activated Carbon // Appl. Radiat. Isot. 2000. V. 53. № 1–2. P. 153–157. https://doi.org/10.1016/S0969-8043(00)00127-5
Герасимов В.Н., Крючков С.В., Кузина А.Ф., Кулаков В.М., Пирожков С.В., Спицин В.И. Рентгеноэлектронное исследование соединений технеция // Докл. АН СССР. 1982. Т. 266. № 1. С. 148–152.
Thompson M., Nunn A.D., Treher E.N. X-ray Photoelectron Spectroscopy of Potential Technetium-Based Organ Imaging Agents // Anal. Chem. 1986. V. 58. P. 3100–3103. https://doi.org/10.1021/ac00127a041
Wester D.W., White D.H., Miller F.W., Dean R.T., Schreifels J.A., Hunt J.E. Synthesis and Characterization of Technetium Complexes with Phosphorus Containing Ligands. The Homoleptic Trimethylphosphite, Dimethylmethylphosphonite and Methyldiethylphosphinite Technetium (I) Cations // Inorg. Chim. Acta. 1987. V. 131. № 2. P. 163–169. https://doi.org/10.1016/S0020-1693(00)96019-5
Chatterjee S., Hall G.B., Johnson I.E., Du Y., Walter E.D., Washton N.M., Levitskaia T.G. Surprising Formation of Quasi-Stable Tc(VI) in High Ionic Strength Alkaline Media // Inorg. Chem. Front. 2018. V. 5. P. 2081–2091. https://doi.org/10.1039/C8QI00219C
Sosulnikov M.I., Teterin Yu.A. X-ray Photoelectron Studies of Ca, Sr, Ba and Their Oxides and Carbonates // J. Electron. Spectrosc. Relat. Phenom. 1992. V. 59. № 2. P. 111–126. https://doi.org/10.1016/0368-2048(92)85002-O
Герасимов В.Н., Крючков С.В., Герман К.Э., Кулаков В.М., Кузина А.Ф. Рентгеноэлектронное исследование строения комплексных соединений технеция: Препринт. М.: Ин-т атом. энергии, ИАЭ-5041/9, 1990. 32 с.
Перетрухин В.Ф., Ровный С.И., Ершов В.В., Герман К.Э., Козарь А.А. Получение металлического технеция для трансмутации в рутений // Журн. неорган. химии. 2002. Т. 47. № 5. С. 722–728.
ГОСТ Р 56357-2015. Уголь активный АГ-3. Технические условия. М.: Изд-во стандартов, 1999. 6 с.
Gratuito M.K.B., Panyathanmaporn T., Chumnanklang R.A., Sirinuntawittaya N.B., Dutta A. Production of Activated Carbon from Coconut Shell: Optimization Using Response Surface Methodology // Bioresour. Technol. 2008. V. 99. № 11. P. 4887–4895. https://doi.org/10.1016/j.biortech.2007.09.042
Баранов А.Н., Зеленков А.Г., Кулаков В.М., Смилга В.П., Тетерин Ю.А., Карпухин В.И., Туманов Ю.П., Чугунов О.К. Рентгеноэлектронное исследование пирографита, облученного нейтронами // Атомная энергия. 1979. Т. 46. № 5. С. 329–332.
Баранов А.Н., Зеленков А.Г., Кулаков В.М., Смилга В.П., Тетерин Ю.А., Карпухин В.И., Туманов Ю.П., Чугунов О.К. Рентгеноэлектронное исследование пирографита, облученного нейтронами // Электронная спектроскопия. Киев: Наукова думка, 1979. С. 25–34.
Баев А.С., Зеленков А.Г., Кулаков В.М., Одинов Б.В., Смилга В.П., Тетерин Ю.А., Туманов Ю.П., Чугунов О.К. Исследование радиационных повреждений пирографита методом рентгеновской фотоэлектронной спектроскопии // Журн. структур. химии. 1980. Т. 21. № 5. С. 29–33.
Shirley D.A. High-Resolution X-Ray Photoemission Spectrum of the Valence Bands of Gold // Phys. Rev. B. 1972. V. 5. № 12. P. 4709–4714. https://doi.org/10.1103/PhysRevB.5.4709
Панов А.П. Пакет программ обработки спектров SPRO и язык программирования SL: Препринт. М.: Ин-т атом. энергии, ИАЭ-6019/15, 1997. 31 с.
Немошкаленко В.В., Алешин В.Г. Электронная спектроскопия кристаллов. Киев: Наукова думка, 1976. 336 с.
Band I.M., Kharitonov Y.I., Trzhaskovskaya M.B. Photoionization Cross Sections and Photoelectron Angular Distributions for X-ray Line Energies in the Range 0.132–4.509 keV Targets: 1 ≤ Z ≤ 100 // At. Data Nucl. Data Tables. 1979. V. 23. № 5. P. 443–505. https://doi.org/10.1016/0092-640X(79)90027-5
Childs B.C., Braband H., Lawler K., Mast D.S., Bigler L., Stalder U., Forster P.M., Czerwinski K.R., Alberto R., Sattelberger A.P., Poineau F. Ditechnetium Heptoxide Revisited: Solid-State, Gas-Phase, and Theoretical Studies // Inorg. Chem. 2016. V. 55. № 20. P. 10445–10452. https://doi.org/10.1021/acs.inorgchem.6b01683
Rodriguez E.E., Poineau F., Llobet A., Sattelberger A.P., Bhattacharjee J., Waghmare U.V., Hartmann T., Cheetham A.K. Structural Studies of TcO2 by Neutron Powder Diffraction and First-Principles Calculations // J. Am. Chem. Soc. 2007. V. 129. № 33. P. 10244–10248. https://doi.org/10.1021/ja0727363
Trzhaskovskaya M.B., Yarzhemsky V.G. Dirac–Fock Photoionization Parameters for HAXPES Applications // At. Data Nucl. Data Tables. 2018. V. 119. P. 99–174. https://doi.org/10.1016/j.adt.2017.04.003
Huang K.N., Aoyagi M., Chen M.N., Crasemann B., Mark H. Neutral-Atom Electron Binding Energy from Relaxed-Orbital Relativistic Hartree-Fock-Slater Calculations // At. Data Nucl. Data Tables. 1976. V. 18. № 3. P. 243–291. https://doi.org/10.1016/0092-640X(76)90027-9
Ильин Е.Г., Паршаков А.С., Тетерин А.Ю., Маслаков К.И., Тетерин Ю.А. Исследование композита MoCl2(C30H30) методом рентгеновской фотоэлектронной спектроскопии // Журн. неорган. химии. 2011. Т. 56. № 11. С. 1871–1876.
Makarov A.V., Safonov A.V., Konevnik Yu.V., Teterin Yu.A., Maslakov K.I., Teterin A.Yu., Karaseva Ya.Yu., German K.E., Zakharova E.V. Activated carbon additives for technetium immobilization in bentonite-based engineered barriers for radioactive waste repositories // J. Hazard. Mater. 2021. V. 401. 123436 (7 p). https://doi.org/10.1016/j.jhazmat.2020.123436
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы