Неорганические материалы, 2022, T. 58, № 7, стр. 727-732
Синтез наноразмерного феррита кобальта и его каталитические свойства в фентоноподобных процессах
Е. В. Томина 1, 2, *, Н. А. Куркин 2, А. В. Дорошенко 2
1 Воронежский государственный лесотехнический университет им. Г.Ф. Морозова
394087 Воронеж, ул. Тимирязева, 8, Россия
2 Воронежский государственный университет
394018 Воронеж, Университетская пл., 1, Россия
* E-mail: tomina-e-v@yandex.ru
Поступила в редакцию 07.02.2022
После доработки 17.03.2022
Принята к публикации 18.03.2022
- EDN: RTPUVM
- DOI: 10.31857/S0002337X22070132
Аннотация
Осуществлен синтез наноразмерного СоFe2O4 методом цитратного горения. Нанопорошки охарактеризованы с точки зрения химической гомогенности, размера, дисперсии, морфологических особенностей. Установлено, что нанопорошок СоFe2O4 (средний размер частиц порядка 74 нм) является эффективным катализатором окисления органических поллютантов метиленового оранжевого (степень деструкции 76.6%) и 2,4-динитрофенола (степень деструкции 95.4%) в фентоноподобных процессах без дополнительного нагревания и облучения ультрафиолетом.
ВВЕДЕНИЕ
Разработка и синтез катализаторов на основе ферритов различного состава представляется перспективным направлением в силу целого ряда преимуществ. Такие катализаторы существенно дешевле аналогичных на основе платиновых и редкоземельных металлов, а прекурсоры для их изготовления легкодоступны [1]. Методы синтеза ферритов являются простыми, воспроизводимыми и масштабируемыми, но при этом позволяют получать катализаторы высокого качества с ультрадисперсными частицами [2]. Перспективность ферритов-шпинелей в этом плане (MFe2O4, где М = Zn, Ni, Mg, Co, Mn) определяется химической устойчивостью в кислых средах, термической стабильностью, высокоразвитой поверхностью, высокой намагниченностью насыщения, широкой возможностью управления их каталитическими, магнитными и структурными характеристиками за счет изменения методов синтеза и допирования их различными катионами [3–6].
В настоящее время катализаторы на основе ферритов уже имеют достаточно широкий спектр практических приложений, таких как окислительная дегидратация углеводородов, разложение спиртов, обработка выхлопных газов автомобилей [1]. В последнее время большой интерес вызывают Фентон-процессы, связанные с каталитическим разложением пероксида водорода (catalytic wet peroxide oxidation – CWPO). Эти процессы относятся к Advanced Oxidation Processes (AOPs), где пероксид водорода за счет разложения под действием катализатора выступает в качестве источника гидроксил-радикалов, являющихся мощными окислителями (редокс-потенциал от +2.0 до +2.8 В в зависимости от рН) [7, 8]. Фентон-процессы являются эффективными методами глубокой окислительной деструкции органических веществ, таких как различные красители, фенол и др., использующихся в большинстве производств по изготовлению пластмасс, тканей, бумаги, резины и являющихся высокотоксичными поллютантами окружающей среды. В классическом гомогенном варианте в реакциях Фентона в качестве катализатора используются растворимые соли железа, что приводит к высоким экологическим и экономическим затратам, поскольку высокая концентрация оставшихся ионов железа требует удаления. Эта проблема исчезает при использовании гетерогенных катализаторов Фентона, в частности ферритов. Для решения вышеприведенных задач феррит должен иметь прежде всего развитую площадь поверхности и ультрадисперсный размер частиц, что в максимальной степени может быть реализовано в наноразмерных ферритовых порошках.
Существует множество методов синтеза нанопорошков: механосинтез, метод соосаждения, гидротермальный синтез, сольвотермический метод, золь–гель-метод, метод термического разложения прекурсоров, сонохимический синтез, микроволновый синтез [9–17]. Технически простым методом синтеза высокодисперсных оксидных материалов является метод цитратного горения, который позволяет синтезировать однофазные нанопорошки с однородной микроструктурой при меньших температурах и меньшем времени реакции по сравнению с традиционными методами спекания [18–20].
Целью данной работы являлся синтез нанопорошка CoFe2O4 и исследование его каталитических свойств в фентоноподобных процессах окислительной деструкции поллютантов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез шпинели CoFe2O4 методом цитратного горения проводили согласно [21]. Фазовый состав образцов исследовали методом рентгеновской дифрактометрии (дифрактометр Empyrean B.V. с Cu-анодом (λ = 1.54060 Å)). Для идентификации фаз использовалась база данных JCPDC [22]. Размер областей когерентного рассеяния (ОКР) частиц на основании уширения линий рентгеновской дифракции рассчитывали по формуле Дебая–Шеррера [23]:
где β – физическое уширение, рад; m = 1; λ – длина волны рентгеновского излучения, нм; D – диаметр частицы, нм.Размер и морфологию частиц порошка CoFe2O4 определяли по данным просвечивающей электронной микроскопии (ПЭМ, просвечивающий электронный микроскоп Carl Zeiss Libra-120). Гистограмму распределения частиц по размерам строили с использованием программы ImageJ, версия 1.53k.
Количественный элементный состав синтезированных образцов определяли методом локального рентгеноспектрального микроанализа (ЛРСМА, растровый электронный микроскоп JSM-6380LV JEOL с системой микроанализа INCA 250).
Каталитические свойства феррита кобальта исследовали в модельных реакциях окисления метиленового оранжевого (МО) и 2,4-динитрофенола (ДНФ) пероксидом водорода. МО – синтетический органический краситель из группы азокрасителей, использующихся практически во всех технических областях применения красителей. ДНФ применяются для производства красителей, антисептиков, взрывчатых веществ, а также в качестве гербицидов или инсектицидов.
В растворы МО (концентрация 0.01 г/л) и ДНФ (концентрация 0.03 г/л) добавляли пероксид водорода, создавая его концентрацию в 10%. Значение pH раствора, равное 4.5, поддерживали ацетатным буфером. Затем в серию проб растворов добавляли по 0.25 г феррита кобальта и измеряли концентрацию МО и ДНФ через каждые 30 мин после начала реакции. Аналогично проводили контрольные измерения концентраций растворов МО и ДНФ без катализатора. Эксперимент проводили при дневном освещении. Концентрацию МО и ДНФ определяли методом фотоколориметрии (фотоколориметр КФК-2). Аналитические значения длины волны для МО – 440 нм, для ДНФ – 364 нм. Степень деструкции красителя рассчитывали по формуле
где W – степень деструкции; %, C0 – концентрация красителя в начальный момент времени, Cτ – концентрация красителя в данный момент времени.РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
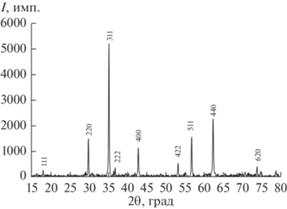
По данным РФА (рис. 1), синтезированный цитратным методом порошок феррита кобальта практически не содержит примесей, все рефлексы на дифрактограмме соответствуют CoFe2O4 (карточка 22-1086).
Средний размер ОКР частиц CoFe2O4, рассчитанный с использованием формулы Дебая–Шеррера (табл. 1), составляет 38 ± 4 нм.
Для синтезированного нанопорошка феррита кобальта наблюдается незначительная нестехиометрия по кислороду (табл. 2 ), что может быть связано с особенностью метода синтеза.
Таблица 2.
Данные элементного состава образца CoFe2O4 (ЛРСМА)
| Номинальный состав образцов (Н) | CoFe2O4 | ||
| Элементный состав, ат. % | Co | Н | 14.28 |
| Р | 14.44 | ||
| Fe | Н | 28.57 | |
| Р | 28.73 | ||
| O | Н | 57.15 | |
| Р | 56.83 | ||
| Реальный состав образцов (Р) | Co1.005Fe2O3.95 | ||
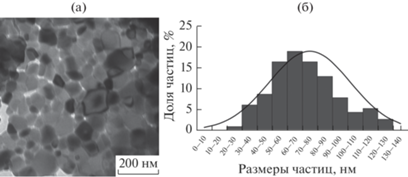
Для синтезированной кобальтовой шпинели характерна высокопористая микроструктура с развитой поверхностью (рис. 2). Образование развитой пористой структуры связано с обильным выделением газообразных продуктов (прежде всего, СO, CO2) в ходе окислительно-восстановительного процесса горения, что свойственно нанопорошкам, получаемых методом цитратного горения.
По данным ПЭМ, порошок феррита кобальта (рис. 3) представлен наночастицами неправильной округлой формы, некоторые частицы имеют огранку, выражена агломерация. Преобладающая фракция частиц имеет размер в интервале от 50 до 80 нм, средний размер частиц составляет 74 нм. Расчетные данные значений ОКР по данным РФА в целом коррелируют с результатами ПЭМ.
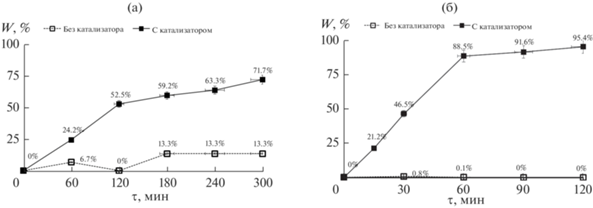
Экспериментально показано, что синтезированный цитратным методом нанопорошок феррита кобальта является катализатором разложения пероксида водорода и усиливает окислительную деструкцию МО и ДНФ в фентоноподобных реакциях (рис. 4). Так, концентрация МО в присутствии феррита кобальта через 2 ч после начала реакции уменьшается в 2 раза, через 5 ч – в 3.5 раза. В отсутствие катализатора после 5 ч реакции концентрация красителя уменьшается только на 15% (рис. 4а). Для ДНФ каталитический эффект СоFe2O4 выражен в еще большей степени: под действием феррита кобальта его концентрация уменьшается в 8 раз через 1 ч после начала реакции и более чем в 20 раз через 2 ч (рис. 4б). Без катализатора реакция окислительной деструкции ДНФ практически не протекает.
Рис. 4.
Кинетические кривые реакции окислительной деструкции МО (а) и ДНФ (б) без катализатора и с катализатором CoFe2O4.
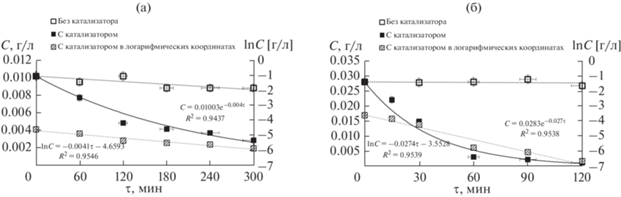
Кинетические кривые окислительной деструкции МО и ДНФ по форме соответствуют псевдопервому порядку реакции. Оценка констант скоростей проводилась путем линеаризации кинетических зависимостей в логарифмических координатах (рис. 4). Константа скорости окислительной деструкции МО в присутствии CoFe2O4 составила 0.0041 мин–1, а ДНФ – 0.0274 мин–1, что сопоставимо, например, с данными [24–26], полученными для более кислой реакционной среды при дополнительном облучении ультрафиолетом.
Для МО через 5 ч после начала реакции степень деструкции без катализатора составила 13%, с катализатором – 71%. Для ДНФ через 2 ч реакции степень деструкции без катализатора не превысила 5% а с катализатором достигла 95% (рис. 5).
Проведенная оценка каталитической активности нанопорошка CoFe2O4 в реакциях окислительной деструкции МО и ДНФ позволяет рассматривать наноразмерный феррит кобальта в качестве основы для создания эффективных катализаторов фентоноподобных процессов окисления органических поллютантов в водных средах.
ЗАКЛЮЧЕНИЕ
Методом цитратного горения синтезирован не содержащий примесей нанопорошок феррита кобальта с преобладающей фракцией частиц в интервале 50–80 нм. Установлена высокая каталитическая активность нанодисперсного порошка CoFe2O4 в фентоноподобных реакциях окисления органических токсикантов метиленового оранжевого и 2,4-динитрофенола без дополнительного облучения реакционной смеси ультрафиолетом и без дополнительного нагревания, что, безусловно, упростит и удешевит технологический процесс очистки водных сред. Степень деструкции МО без катализатора составляет 14.2%, с катализатором CoFe2O4 – 76.6%. Для ДНФ этот показатель составляет 5 и 95.4% соответственно.
Список литературы
Manova E., Tsoncheva T., Paneva D., Mitov I., Tenchev K., Petrov L. Mechanochemically Synthesized Nano-Dimensional Iron–Cobalt Spinel Oxides as Catalysts for Methanol Decomposition // Appl. Catal., A. 2004. V. 277. № 1. P. 119–127. https://doi.org/10.1016/j.apcata.2004.09.002
Kefeni K.K., Msagati A.M., Mamba B.B. Ferrite Nanoparticles: Synthesis, Characterisation and Applications in Electronic Device // Mater. Sci. Eng., B. 2017. V. 215. P. 37–55. https://doi.org/10.1016/j.mseb.2016.11.002
Petrova E., Kotsikau D., Pankov V., Fahmi A. Influence of Synthesis Methods on Structural and Magnetic Characteristics of Mg–Zn-Ferrite Nanopowders // J. Magn. Magn. Mater. 2019. V. 473. P. 85–91. https://doi.org/10.1016/j.jmmm.2018.09.128
Somnath S., Indu S., Kotnala R.K., Singh M., Kumar A., Dhiman P., Singh V.P., Verma K., Kumar G. Structural Magnetic and Mössbauer Studies of Nd-Doped Mg-Mn Ferrite Nanoparticles // J. Magn. Magn. Mater. 2017. V. 444. P. 77–86. https://doi.org/10.1016/j.jmmm.2017.08.017
Rao K.S., Nayakulu S.V.R., Varma M.C., Choudary G.S.V.R.K., Rao K.H. Controlled Phase Evolution and the Occurrence of Single Domain CoFe2O4 Nanoparticles Synthesized by PVA Assisted Sol-Gel Method // J. Magn. Magn. Mater. 2018. V. 451. № 1. P. 602–608. https://doi.org/10.1016/j.jmmm.2017.11.069
Mittova I.Ya., Perov N.S., Tomina E.V., Pan’kov V.V., Sladkopevtsev B.V. Multiferroic Nanocrystals and Diluted Magnetic Semiconductors as a Base for Designing Magnetic Materials // Inorg. Mater. 2021. V. 57. № 13. P. 22–48. https://doi.org/10.1134/S0020168521130033
Rehman F., Sayed M., Khan J.A., Shah L.A., Shah N.S., Khan H.M., Khattak R. Degradation of Crystal Violet Dye by Fenton and Photo-Fenton Oxidation Processes // Z. Phys. Chem. 2018. V. 232. № 12. P. 1771–1786. https://doi.org/10.1515/zpch-2017-1099
Артемьянов А.П., Земскова Л.А., Иванов В.В. Каталитическое жидкофазное окисление фенола в водных средах с использованием катализатора углеродное волокно/(железо, оксид железа) // Изв. вузов. Сер. Химия и хим. технология. 2017. Т. 60. № 8. С. 88–95.
Rafferty A., Prescott T., Brabazon D. Sintering Behaviour of Cobalt Ferrite Ceramic // Ceram. Int. 2008. V. 34. № 1. P. 15–21. https://doi.org/10.1016/j.ceramint.2006.07.012
Nabiyouni G., Julaee M., Ghanbari D., Aliabadi P.C., Safaie N. Room Temperature Synthesis and Magnetic Property Studies of Fe3O4 Nanoparticles Prepared by a Simple Precipitation Method // J. Ind. Eng. Chem. 2015. V. 21. P. 599–603. https://doi.org/10.1016/j.jiec.2014.03.025
Ding Z., Wang W., Zhang Y., Li F., Liu J.P. Synthesis, Characterization and Adsorption Capability for Congo Red of CoFe2O4 Ferrite Nanoparticles // J. Alloys Compd. 2015. V. 640. P. 362–370. https://doi.org/10.1016/j.jallcom.2015.04.020
Larumbe S., Perez-Landazabal J.I., Pastor J.M., Gomez-Polo C. Effect of a SiO2 Coating on the Magnetic Properties of Fe3O4 Nanoparticles // J. Appl. Phys. 2012. V. 111. P. 103911–103918. https://doi.org/10.1088/0953-8984/24/26/266007
Zakiyah L.B., Saion E., Al-Hada N.M., Gharibshahi E., Salem A., Soltani N., Gene S. Up-scalable Synthesis of Size-Controlled Copper Ferrite Nanocrystals by Thermal Treatment Method // Mater. Sci. Semicond. Process. 2015. V. 40. P. 564–569. https://doi.org/10.1016/j.mssp.2015.07.027
Tian Y., Yu B., Li X., Li K., Facile J. Solvothermal Synthesis of Monodisperse Fe3O4 Nanocrystals with Precise Size Control of One Nanometre as Potential MRI Contrast Agents // Mater. Chem. 2011. V. 21. P. 2476–2481. https://doi.org/10.1039/C0JM02913K
Томина Е.В., Перов Н.С., Миттова И.Я., Алехина Ю.А., Стекленева О.В., Куркин Н.А. Микроволновый синтез и магнитные свойства нанопорошка феррита висмута, допированного кобальтом // Изв. Академии наук. Сер. хим. 2020. № 5. С. 941–946.
Zhang Z., Yao G., Zhang X., Ma J., Lin H. Synthesis and Characterization of Nickel Ferrite Nanoparticles via Planetary Ball Milling Assisted Solid-State Reaction // Ceram. Int. 2015. V. 41. P. 4523–4530. https://doi.org/10.1016/j.ceramint.2014.11.147
Rashad M.M., Soltan S., Ramadan A.A., Bekheet M.F., Rayan D.A. Investigation of the Structural, Optical and Magnetic Properties of CuO/CuFe2O4 Nanocomposites Synthesized via Simple Microemulsion Method // Ceram. Int. 2015. V. 41. P. 12 237–12 245. https://doi.org/10.1016/j.ceramint.2015.06.046
Shashank D.B., Rakesh K.S., Vivek K., Nishant K., Shambhu K. Tailoring the Structural, Optical and Multiferroic Properties of Low Temperature Synthesized Cobalt Ferrite Nanomaterials, by Citrate Precursor Method // Mater. Today: Proc. 2021. V. 46. № 15. P. 6527–6533. https://doi.org/10.1016/j.matpr.2021.04.001
Ali T.M., Ismail S.M., Mansour S.F., Abdo M.A., Yehia M. Physical Properties Of Al-Doped Cobalt Nanoferrite Prepared by Citrate–Nitrate Auto Combustion Method // J. Mater. Sci. – Mater. Electron. 2021. V. 32. P. 3092–3103. https://doi.org/10.1007/s10854-020-05059-y
Mariosi F.R., Venturini J., Alexandre C.V., Bergmann C.P. Lanthanum-Doped Spinel Cobalt Ferrite (CoFe2O4) Nanoparticles for Environmental Applications // Ceram. Int. 2019. V. 46. № 3. P. 2772-2779. https://doi.org/10.1016/j.ceramint.2019.09.266
Ходосова Н.А., Томина Е.В., Бельчинская Л.И., Жабин А.В., Куркин Н.А., Волков, А.С. Физико-химические характеристики нанокомпозитного сорбента нонтронит/CoFe2O4 // Сорбционные и хроматографические процессы. 2021. Т. 21. № 4. С. 520–528. https://doi.org/10.17308/sorpchrom.2021.21
JCPDC PCPDFWIN: A Windows Retrieval/Display program for Accessing the ICDD PDF – 2 Data base, International Centre for Diffraction Data, 1997.
Brandon D., Kaplan U. Microstructure of Materials. Research and Control Methods. West Sussex: Wiley, 1999. P. 384.
Roshanfekr R.L., Farshi G.B., Irani, M., Sadegh S.M., Haririan I. Comparison Study of Phenol Degradation Using Cobalt Ferrite Nanoparticles Synthesized by Hydrothermal and Microwave Methods // Desalination Water Treatment. 2014. V. 56. № 12 P. 1–10. https://doi.org/10.1080/19443994.2014.97796
Папынов Е.К., Номеровский А.Д., Азон А. С., Главинская В.О., Буравлев И.Ю., Огнев А.В., Самардак А.С., Драньков А.Н., Красицкая С.Г., Тананаев И.Г. Макропористые магнитные оксиды железа и их композиты для жидкофазного каталитического окисления // Журн. неорган. химии. 2020. Т. 65. № 11. С. 1449–1460.
Chomkitichai W., Jansanthea, P., Channei D. Photocatalytic Activity Enhancement in Methylene Blue Degradation by Loading Ag Nanoparticles onto α-Fe2O3 // Russ. J. Inorg. Chem. 2021. V. 66. P. 1995–2003 https://doi.org/10.1134/S0036023621130027
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы