Журнал неорганической химии, 2019, T. 64, № 10, стр. 1041-1050
Координационные полимеры γ,γ'-дипиридила и моноядерных бензоатов M(OOCPh)2[O(H)Me]4 (M = Ni, Co)
Р. Р. Датчук 1, А. А. Гринева 1, М. А. Уварова 1, И. А. Якушев 1, Я. В. Зубавичус 2, 3, С. Е. Нефедов 1, *
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
2 Национальный исследовательский центр Курчатовский институт
123182 Москва, пл. Академика Курчатова, 1, Россия
3 Институт катализа СО РАН
630090 Новосибирск, пр-т Академика Лаврентьева, 5, Россия
* E-mail: snef@igic.ras.ru
Поступила в редакцию 29.03.2019
После доработки 10.04.2019
Принята к публикации 15.05.2019
Аннотация
Установлено, что медленная диффузия раствора аддукта γ,γ′-дипиридила в метаноле в метанольный раствор аддукта M[(OOCPh]2[O(H)Me]4 (1) при соотношении реагентов 1 : 1 при комнатной температуре приводит к образованию 1D-координационных полимеров {dipyM(OOCPh)2[O(H)Me]2}n (M = Ni (2), зеленый; Co (3), оранжевый) и {(dipy)2Co2(µ-OOCPh)2(η2-OOCPh)2 ⋅ MeOH}n (4, розовый). Оранжевый полимер 3 получен в качестве единственного продукта при разбавлении в 3 раза исходных реагентов и проведении диффузии при температуре 5°С. Полученные полимеры 2–4 исследованы методами химического и рентгеноструктурного анализа, а также ИК-спектроскопии.
ВВЕДЕНИЕ
Комплексы переходных металлов, содержащие лабильные молекулы координированного растворителя и/или анионы сильных кислот, широко используются как строительные блоки для синтеза новых би-, полиядерных соединений и кластеров, а также для получения координационных полимеров (КП) различной размерности [1–11]. Исследование химического поведения ранее неизвестных карбоксилатов [12] моноядерных аддуктов 3d-металлов M(OOСR)2[O(H)Me]4 (R = Ph, (C5H4)Mn(CO)3; M = ZnII, CoII, NiII) с анионами бензойной и цимантренкарбоновой кислот показало, что такие соединения могут терять в ходе реакций с донорными молекулами координированный спирт с образованием комплексов, состав и строение которых определяются природой переходного металла [13–16]. В частности, было показано, что растворение аддуктов цимантренатов M[(OOCC5H4)Mn(CO)3]2[O(H)Me]4 в полярных координирующих растворителях, таких как ацетонитрил или ТГФ, приводит к образованию трехъядерных комплексов состава M3[µ-(OOCC5H4) Mn(CO)3]4[µ-η2-(OOCC5H4)Mn(CO)3]2L4 (L = = NCMe, THF) [13–15]. В отличие от цимантренатов, бензоаты [16] практически не растворяются в традиционных органических растворителях, образуя с небольшим выходом монокристаллы КП, в которых биядерные трехмостиковые фрагменты связаны через дополнительную координацию аксиально расположенного концевого бензоат-аниона. Так, при растворении аддукта цинка в ацетонитриле образуется 1D-КП {Zn(µ-OOCPh)3Zn(µ-OOCPh)}n [17], а при растворении аддукта кобальта в хлороформе – {[Co2(µ,η2-OOCPh) (µ-OOCPh)2(O(H)Me)2](µ-OOCPh)(HCCl3)}n [18]. Взаимодействие в одинаковых условиях (соотношение и концентрация реагентов, природа растворителя, температура) аддуктов M[(OOCC5H4)Mn(CO)3]2[O(H)Me]4 (M = Ni(II), Co(II), Mn(II)) с бидентатным фенантролином – сильным четырехэлектронным донором – приводит к образованию комплексов PhennM[(OOCC5H4)Mn(CO)3]2 (Co(II), Mn(II), n = 2; M = Ni(II), n = 3), состав и строение которых определяются природой переходного металла-комплексообразователя [19]. В то же время при взаимодействии метанольных аддуктов цимантренатов Zn(II), Co(II), Ni(II) с γ,γʹ-дипиридилом, в котором донорные центры направлены в противоположные стороны, образуются 1D-полимеры различной геометрии [20]. В отличие от цимантрената цинка, бензоат цинка в аналогичной реакции при различных концентрациях реагентов образует 1D-КП {Zn(µ-dipy) (η2-OOCPh)(OOCPh)}n (соотношение 1 : 1) и {Zn[(µ-OMe)(µ-OOCPh)Zn(OOCPh)]2(µ-dipy)2}n (соотношении 2 : 1, сильное разбавление), при формировании последнего происходит неожиданное депротонирование метанола с образованием алкоголятных мостиков [17].
В продолжение проводимых исследований реакционной способности аддуктов бензоатов 3d-металлов с метанолом в настоящей работе на основании данных РСА рассмотрены особенности строения 1D-КП, полученных при взаимодействии моноядерных бензоатов никеля и кобальта с γ,γ'-дипиридилом.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все операции по синтезу и выделению комплексов проводили в атмосфере чистого аргона с использованием абсолютированных растворителей.
ИК-спектры кристаллических образцов регистрировали в интервале 4000–550 см–1 методом НПВО на ИК-Фурье-спектрометре NEXUS фирмы NICOLET с использованием приставки MIRacle фирмы PIKETechnologies с алмазным кристаллом.
РСА кристаллов 2, 3 выполнен по стандартной методике на автоматическом дифрактометре Bruker SMART Apex II, оборудованном CCD-детектором (λMo, графитовый монохроматор, ω-сканирование). Данные рентгеновской дифракции для комплекса 4 получены на рентгеновском пучке станции “Белок” Курчатовского центра синхротронного излучения в НИЦ “Курчатовский институт” (λ = 0.80246 Å, детектор Rayonix SX165, φ-сканирование). Для кристаллов 4 первичное индексирование, уточнение параметров элементарной ячейки, интегрирование отражений проведены с использованием программы iMOSFLM (программный пакет CCP4 [21]), учет поглощения – с помощью программы Scala [22].
Уточнение структур выполнено с помощью комплекса программ SHELXTL PLUS (PC-версия) [23–26].
Кристаллографические данные и детали уточнения структур приведены в табл. 1, основные геометрические параметры изученных комплексов – в табл. 2–4. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (CCDC 1903641–1903643).
Таблица 1.
Кристаллографические параметры и детали уточнения структур комплексов 2–4
| Параметр | 2 | 3 | 4 |
|---|---|---|---|
| Номер CCDC | 1 903 643 | 1 903 642 | 1 903 641 |
| Брутто-формула | C26H26N2NiO6 | C26H26N2CoO6 | C25H22N2CoO5 |
| М. м. | 521.20 | 521.42 | 489.37 |
| T, K | 150(2) | 150(2) | 100(2) |
| Цвет | Зеленый | Оранжевый | Розовый |
| Сингония | Тетрагональная | Тетрагональная | Триклинная |
| Пр. гр. | P4(3)2(1)2 | P4(3)2(1)2 | P |
| a, Ǻ | 15.042(3) | 15.1705(18) | 9.5416(19) |
| b, Ǻ | 15.042(3) | 15.1705(18) | 10.958(2) |
| c, Ǻ | 26.859(5) | 26.966(3) | 11.824(2) |
| α, град | 90 | 90 | 75.733(18) |
| β, град | 90 | 90 | 89.71(2) |
| γ, град | 90 | 90 | 66.95(2) |
| V, Å3 | 6078(2) | 6206.0(16) | 1096.7(4) |
| Z | 8 | 8 | 2 |
| dрасч, мг/м3 | 1.139 | 1.116 | 1.482 |
| μ, мм–1 | 0.674 | 0.588 | 1.154 |
| F(000) | 2176 | 2168 | 506 |
| Размеры кристалла, мм | 0.18 × 0.16 × 0.14 | 0.24 × 0.22 × 0.20 | 0.20 × 0.05 × 0.01 |
| θ-область сканирования, град | 2. 03–25.99 | 2.84–27.99 | 2.36–28.99 |
| Интервалы индексов отражений | –10 ≤ h ≤ 17, –17 ≤ k ≤ 17, –31 ≤ l ≤ 31 |
–18 ≤ h ≤ 20, –20 ≤ k ≤ 20, –29 ≤ l ≤ 35 |
–13 ≤ h ≤ 11, –15 ≤ k ≤ 15, –15 ≤ l ≤ 15 |
| Число отражений | 5335 | 7480 | 10405 |
| Число независимых отражений | 2624 [Rint = 0.1577] | 4610 [Rint = 0.0822] | 3997 [Rint = 0.0922] |
| GOOF | 0.997 | 0.946 | 1.052 |
| R[I > 2σ(I)] | R1 = 0.0732, wR2 = 0.1452 | R1 = 0.0591, wR2 = 0.1414 | R1 = 0.0778, wR2 = 0.1845 |
| R (по всем рефлексам) | R1 = 0.1776, wR2 = 0.1886 | R1 = 0.1067, wR2 = 0.1699 | R1 = 0.0942, wR2 = 0.1954 |
| max/min пики электронной плотности, e Ǻ–3 | 0.401 и –0.381 | 0.558 и –0.298 | 0.958 и –1.072 |
Таблица 2.
Основные длины связей и величины валентных углов в комплексе 2
| Связь | d, Å | Связь | d, Å |
|---|---|---|---|
| Ni(1)–O(1) | 2.015(8) | Ni(1)–O(3) | 2.037(7) |
| Ni(1)–N(1) | 2.069(8) | Ni(1)–O(5) | 2.067(7) |
| Ni(1)–N(2) | 2.086(8) | Ni(1)–O(6) | 2.080(7) |
| Угол | ω, град | Угол | ω, град |
| O(1)Ni(1)O(3) | 179.1(3) | O(1)Ni(1)N(1) | 90.6(3) |
| O(3)Ni(1)N(1) | 90.1(3) | O(1)Ni(1)O(5) | 88.6(3) |
| O(3)Ni(1)O(5) | 90.8(3) | N(1)Ni(1)O(5) | 87.5(3) |
| O(1)Ni(1)N(2) | 91.3(3) | O(3)Ni(1)N(2) | 89.4(3) |
| N(1)Ni(1)N(2) | 89.4(3) | O(5)Ni(1)N(2) | 176.9(3) |
| O(1)Ni(1)O(6) | 91.6(3) | O(3)Ni(1)O(6) | 87.8(3) |
| N(1)Ni(1)O(6) | 177.5(3) | O(5)Ni(1)O(6) | 93.8(3) |
Таблица 3.
Основные длины связей и величины валентных углов в комплексе 3
| Связь | d, Å | Связь | d, Å |
|---|---|---|---|
| Co(1)–O(3) | 2.047(4) | Co(1)–O(1) | 2.065(4) |
| Co(1)–O(5) | 2.117(4) | Co(1)–O(6) | 2.125(5) |
| Co(1)–N(1) | 2.132(5) | Co(1)–N(2) | 2.134(5) |
| Угол | ω, град | Угол | ω, град |
| O(3)Co(1)O(1) | 178.39(18) | O(3)Co(1)O(5) | 89.68(19) |
| O(1)Co(1)O(5) | 90.53(18) | O(3)Co(1)O(6) | 90.9(2) |
| O(1)Co(1)O(6) | 87.5(2) | O(5)Co(1)O(6) | 94.82(19) |
| O(3)Co(1)N(1) | 92.88(18) | O(1)Co(1)N(1) | 88.72(17) |
| O(5)Co(1)N(1) | 87.31(17) | O(6)Co(1)N(1) | 175.7(2) |
| O(3)Co(1)N(2) | 89.85(18) | O(1)Co(1)N(2) | 90.07(17) |
| O(5)Co(1)N(2) | 175.13(17) | O(6)Co(1)N(2) | 90.03(19) |
Таблица 4.
Основные длины связей и величины валентных углов в комплексе 4
| Связь | d, Ǻ | Связь | d, Ǻ |
|---|---|---|---|
| Co(1)–O(3) | 2.005(3) | Co(1)–O(4) | 2.047(3) |
| Co(1)–N(2) | 2.142(4) | Co(1)–N(1) | 2.144(4) |
| Co(1)–O(1) | 2.155(4) | Co(1)–O(2) | 2.221(3) |
| Угол | ω, град | Угол | ω, град |
| O(3)Co(1)O(4) | 115.70(14) | O(3)Co(1)N(2) | 88.98(14) |
| O(4)Co(1)N(2) | 89.36(14) | O(3)Co(1)N(1) | 91.17(14) |
| O(4)Co(1)N(1) | 91.41(14) | N(2)Co(1)N(1) | 179.06(15) |
| O(3)Co(1)O(1) | 94.05(13) | O(3)Co(1)O(1) | 94.05(13) |
| O(4)Co(1)O(1) | 150.22(13) | N(2)Co(1)O(1) | 92.75(15) |
| N(1)Co(1)O(1) | 86.31(15) | O(3)Co(1)O(2) | 154.29(14) |
| O(4)Co(1)O(2) | 90.01(13) | N(2)Co(1)O(2) | 91.67(14) |
| N(1)Co(1)O(2) | 87.79(14) | N(1)Co(1)O(2) | 87.79(14) |
| O(1)Co(1)O(2) | 60.24(12) |
Рентгеноструктурные исследования полимеров 2, 3 выполнены с использованием оборудования ЦКП ФМИ ИОНХ РАН, функционирующего при поддержке государственного задания ИОНХ РАН в области фундаментальных научных исследований.
Синтез комплексов
{dipyNi(OOCPh)2[O(H)Me]2}n (1). Раствор 0.1 г (0.23 ммоль) комплекса Ni(OOCPh)2[O(H)Me]4 в 5 мл метанола аккуратно покрывали раствором 0.036 г (0.23 ммоль) γ,γ'-дипиридила в 5 мл метанола и оставляли при комнатной температуре на 7 сут. Образовавшиеся зеленые монокристаллы отделяли от маточного раствора декантацией, промывали гексаном и сушили в токе аргона. Выход 71% (0.09 г).
ИК-спектр (ν, см–1): 3384 сл., 3271 сл., 3060 сл., 1596 ср., 1534 с., 1490 сл., 1445 сл., 1410 с., 1389 с., 1318 сл., 1218 сл., 1174 сл., 1068 сл., 1024 сл., 936 сл., 858 сл., 813 сл., 715 с., 675 с., 635 ср.
{dipyCo(OOCPh)2[O(H)Me]2}n (3). Раствор 0.1 г (0.23 ммоль) комплекса Co(OOCPh)2[O(H)Me]4 в 15 мл метанола аккуратно покрывали раствором 0.036 г (0.36 ммоль) γ,γ'-дипиридила в 15 мл метанола и выдерживали в холодильнике при температуре 5°С в течение 10 сут. Образовавшиеся крупные оранжевые монокристаллы отделяли от маточного раствора декантацией, промывали гексаном и сушили в токе аргона. Выход 86% (0.1 г).
ИК-спектр (ν, см–1): 3056 сл., 2452 сл., 1972 сл., 1622 ср., 1605 с., 1569 ср., 1545 с., 1500 ср., 1491 ср., 1431 ср., 1413 с., 1403 с., 1335 сл., 1291 сл., 1240 сл., 1221 ср., 1180 сл., 1151 сл., 1079 ср., 1023 с., 856 ср., 812 с., 747 сл., 721 с., 680 с., 671 с., 698 с., 630 с.
{(dipy)2Co2(µ-OOCPh)2(η2-OOCPh)2 ⋅ MeOH}n (4). Раствор 0.1 г (0.23 ммоль) комплекса Co(OOCPh)2[O(H)Me]4 в 5 мл метанола аккуратно покрывали раствором 0.036 мг (0.23 ммоль) γ,γ'-дипиридила в 5 мл метанола и оставляли при комнатной температуре на 7 сут. Образовавшиеся при этом мелкие золотисто-фиолетовые и несколько крупных оранжевых монокристаллов отделяли от маточного раствора декантацией, промывали гексаном и сушили в токе аргона. Оранжевые монокристаллы комплекса 3 отделяли от монокристаллов 4 механически. Выход 4 91% (0.1 г).
ИК-спектр (ν, см–1): 3048 сл., 2163 сл., 1710 сл., 1605 с., 1570 ср., 1547 с., 1500 сл., 1491 сл., 1431ср., 1417 с., 1404 с., 1291 сл., 1240 сл., 1222 ср.., 1070 сл., 1024 сл., 1007 сл., 921 сл., 856 ср., 813 с., 747 сл., 721 с., 699 ср., 681ср., 671 ср., 631 ср.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Обнаружено, что медленная диффузия раствора аддукта γ,γ'-дипиридила в метаноле в метанольный раствор M[(OOCPh]2[O(H)Me]4 (1) при соотношении реагентов 1 : 1 при комнатной температуре приводит к образованию 1D-КП {dipyM(OOCPh)2[O(H)Me]2}n (M = Ni (2), зеленый, выход 71%; Co (3), оранжевый, выход <0.01%) и {(dipy)2Co2(µ-OOCPh)2(η2-OOCPh)2 ⋅ MeOH}n (4, розовый, выход 91%). Оранжевый комплекс 3 получен в качестве единственного продукта при разбавлении в 3 раза исходных реагентов и проведении диффузии при температуре 5°С.
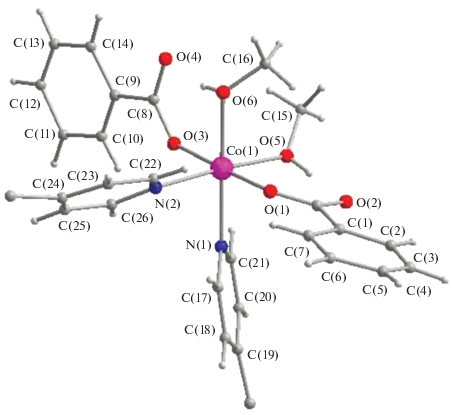
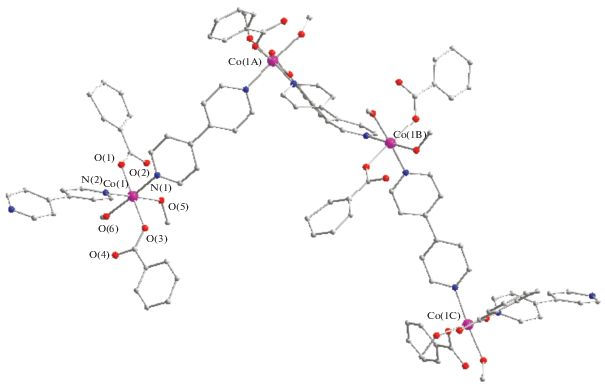
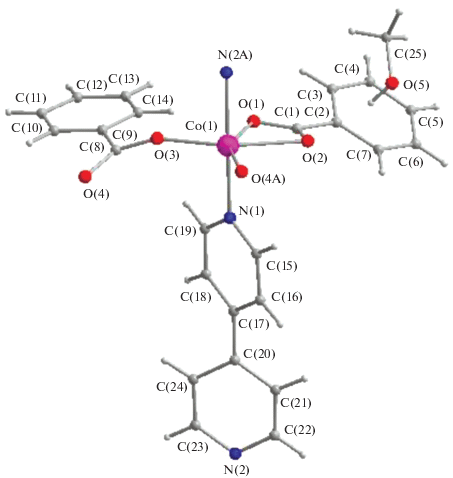
По данным РСА, в изоструктурных 1D-КП 2 и 3 (рис. 1–3, табл. 1–3) каждый атом металла имеет искаженное октаэдрическое окружение из четырех атомов кислорода, два из которых принадлежат координированным молекулам метанола (Ni–O 2.067(7), 2.080(7) Å, Co–O 2.114(5), 2.115(5) Å), а два – двум бензоат-анионам (Ni–O 2.015(8), 2.037(7) Å, Co–O 2.040(4)–2.068(4) Å), и двух атомов азота противолежащих дипиридилов, формирующих полимер (Ni–N 2.0769(8), 2.086(8) Å, Co–N 2.133(3)–2.135(3) Å). Необходимо отметить, что в полимерах 2 и 3 олигомеры “закручены” по спирали, в отличие от 1D-КП с карбоксилатами никеля и кобальта на основе цимантренкарбоновой кислоты, в которых атомы металлов располагаются на одной линии, где находятся также атомы азота и два сшивающих шестичленные гетероциклы атома углерода. При этом в координированном дипиридиле угол разворота между гетероциклами равен 16.4° и 20.7° в 2 и 3 соответственно, в некоординированном дипиридиле – 37.2°.
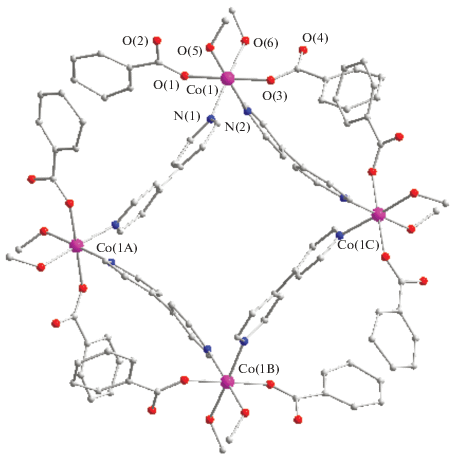
В КП 2 и 3 молекула дипиридила, связывающая атомы металлов в полимер, является изогнутой и соединяющие гетероциклы атомы углерода отклоняются от линии металл–металл на расстояние 0.639 и 0.732 Å, а кольца развернуты друг относительно друга на 23.2° и 22.8° соответственно (рис. 3).
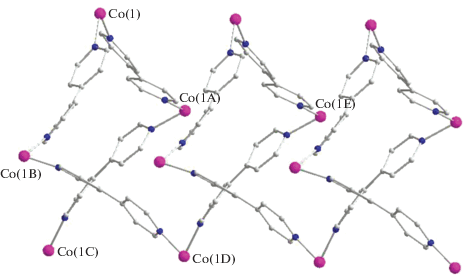
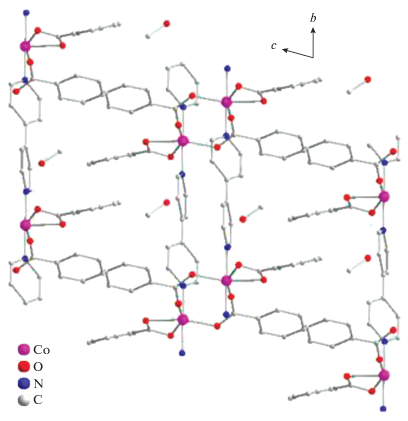
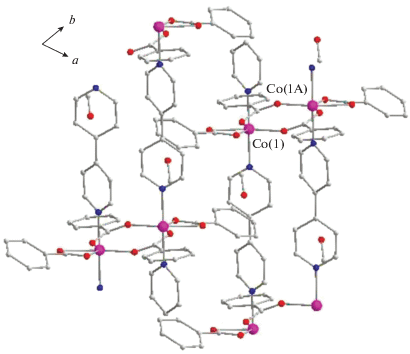
В спирали (рис. 4) треугольники M(1)M(1A)M(1B) (длины сторон М…М 11.028, 11.129, 17.907 Å в 2 и 11.263, 11.140, 18.461 Å в 3) расположены параллельно с шагом 26.85 и 21.25 Å и соединены в цепь атомом M(1D) (расстояния 11.129, 11.265 Å от атома M(1B) и 11.028, 11.142 Å от атома M(1Е), угол M(1B)M(1D)M(1E) 111.2° и 111.0° в 2 и 3 соответственно).
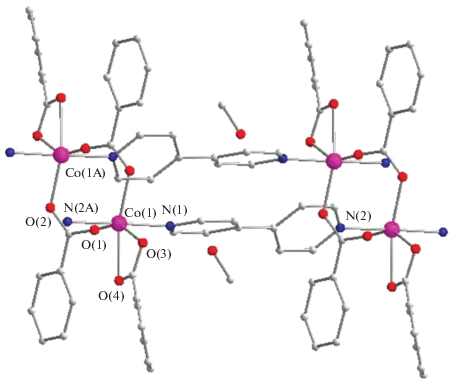
Помимо оранжевого продукта, полимера 3, в реакции образуются золотисто-фиолетовые монокристаллы комплекса {(dipy)2Co2(µ-OOCPh)2(η2-OOCPh)2 ⋅ MeOH}n (4, табл. 1, 4, рис. 5). В линейном 1D-КП, по данным РСА, биядерные фрагменты Co2(µ-OOCPh)2(η2-OOCPh)2 (Co…Co 4.1513(6) Å, Co–O 2.005(3), 2.047(3) Å (µ-OOCPh); 2.155(4), 2.221(3) Å (η2); Co–N 2.142(4), 2.144(4) Å) соединены молекулами dipy, причем два дипиридила, “сшивающие” такие димеры в полимер, располагаются в практически параллельных плоскостях, но оказываются искаженными (угол разворота колец 33.4°) (рис. 6–8). В кристаллах полимера присутствует сольватная молекула метанола, образующая водородную связь с атомом кислорода О(2) (О(2)…О(5) 2.88 Å), что приводит к незначительному удлинению связи Co–O(2), но существенному изменению геометрии по сравнению с охарактеризованным ранее аналогичным 1D-КП, не содержащим сольватных молекул, в котором соответствующие длины связей равны: Co…Co 4.057(4) Ǻ, Co–O 2.006(3), 2.014(3) Å (µ-OOCPh); 2.170(3), 2.191(3) Å (η2); Co–N 2.158(3), 2.163(3) Å, а дипиридильный лиганд оказывается практически плоским (угол NC5/NC5 равен 7°) [27]. Такой полимер образуется при медленном испарении и диффузии раствора дипиридила в раствор нитрата кобальта и аммонийной соли бензойной кислоты в воде. Необходимо отметить, что аналогичная реакция нитрата никеля приводит к 1D-КП [dipyNi(OOCPh)2(OH2)2]n который, так же как и 2, имеет геометрию спирали и кристаллизуется в кристаллографической группе P43212. В той же группе кристаллизуются и комплексы аналогичного строения – 1D-КП 2, но они содержат в пустотах сольватные молекулы хлороформа и нитробензола [28]. Причем геометрия самой спирали лишь в деталях меняется в зависимости от природы молекулы-гостя [28].
ЗАКЛЮЧЕНИЕ
Показано, что аддукты бензоатов 3d-металлов с метанолом, так же как и мноядерные аддукты цимантренатов, частично или полностью теряют координированные молекулы спирта с образованием 1D-КП, состав и строение которых определяются как природой используемого металла, так и природой заместителя в карбоксилат-анионе. Кроме того, остающиеся в 2 и 3 координированные молекулы метилового спирта и η2-координация карбоксилата в 4 позволяют предположить возможность модификации полученных комплексов в реакциях с разноообразными O- и N-донорными молекулами.
Список литературы
Cotton F.A., Wilkinson G., Murillo C.A. et al. // Advanced Inorganic Chemistry. John Wiley & Sons, Inc., 1999. P. 493.
Mehrotra R.C., Bohra R. // Metal carboxylates. London: Acad. Press, 1983. P. 396.
Cotton F.A., Lin C., Murillo C.A. // Acc. Chem. Res. 2001. V. 34. № 10. P. 759. https://doi.org/10.1021/ar010062+
Mikuriya M., Yoshioka D., Handa M. // Coord. Chem. Rev. 2006. V. 250. № 17–18. P. 2194. https://doi.org/10.1016/j.ccr.2006.01.011
Еременко И.Л., Новоторцев В.М., Сидоров А.А. и др. // Рос. хим. журн. 2004. Т. 48. № 1. С. 49.
Cook T.R., Zheng Y.-R., Stang P.J. // Chem. Rev. 2013. V. 113. P. 734. https://doi.org/10.1021/cr3002824
Stock N., Biswas S. // Chem. Rev. 2012. V. 112. P. 933. https://doi.org/10.1021/cr200304e
Furukawa H., Cordova K.E., O’Keeffe M. et al. // Science. 2013. V. 341. P. 97. https://doi.org/10.1126/science.1230444
Stavila V., Talin A.A., Allendorf M.D. // Chem. Soc. Rev. 2014. V. 43. P. 5994. https://doi.org/10.1039/C4CS00096J
Uvarova M., Sinelshchikova A., Golubnichaya M. et al. // Crystal Growth Design. 2014. V. 14. № 11. P. 5976. https://doi.org/10.1021/cg501157e
Mitrofanov A.Yu., Rousseli Y., Guilard R. et al. // New J. Chem. 2016. V. 40. P. 5896. https://doi.org/10.1039/C5NJ03572D
CCDC CSD ver.5.39 (updates Aug. 2018).
Ageshina A.A., Uvarova M.A., Nefedov S.E. // Russ. J. Inorg. Chem. 2015. V. 60. P. 1085. [Агешина А.А., Уварова М.А., Нефедов С.Е. // Журн. неорган. химии. 2015. Т. 60. № 9. С. 1192. https://doi.org/10.7868/ S0044457X15090020]https://doi.org/10.1134/S0036023615090028
Ageshina A.A., Uvarova M.A., Nefedov S.E. // Russ. J. Inorg. Chem. 2015. V. 60. P. 1218. [Агешина А.А., Уварова М.А., Нефедов С.Е. // Журн. неорган. химии. 2015. Т. 60. № 10. С. 1334. https://doi.org/10.7868/ S0044457X15100025]https://doi.org/10.1134/S0036023615100022
Uvarova M.A., Ageshina A.A., Nefedov S.E. // Russ. J. Inorg. Chem. 2015. V. 60. P. 1210. [Уварова М.А., Агешина А.А., Нефедов С.Е. // Журн. неорган. химии. 2015. Т. 60. № 10. С. 1326. https://doi.org/10.7868/ S0044457X15100190]https://doi.org/10.1134/S0036023615100198
Datchuk R.R., Grineva A.A., Uvarova M.A., Nefedov S.E. // Russ. J. Inorg. Chem. 2017. V. 62. № 10. P. 1315. [Датчук Р.Р., Гринева А.А., Уварова М.А., Нефедов С.Е. // Журн. неорган. химии. 2017. Т. 62. № 10. С. 1324. https://doi.org/10.7868/S0044457X17100063]https://doi.org/10.1134/S0036023617100059
Grineva A.A., Grechova O.D., Datchuk R.R. et al. // Russ. J. Inorg. Chem. 2019. V. 64 № 8. С. 850. https://doi.org/10.1134/S0044457X1908004X
Grineva A.A., Uvarova M.A., Datchuk R.R. et al. // Russ. J. Inorg. Chem. 2018. V. 63. P. 610. [Гринева А.А., Уварова М.А., Датчук Р.Р. и др. // Журн. неорган. химии. 2018. Т. 63. № 5. С. 579. https://doi.org/10.7868/S0044457X18050082]https://doi.org/10.1134/S0036023618050091
Grineva A.A., Datchuk R.R., Uvarova M.A. et al. // Russ. J. Inorg. Chem. 2018. V. 63. P. 468. [Гринева А.А., Датчук Р.Р., Уварова М.А. и др. // Журн. неорган. химии. 2018. Т. 63. № 4. С. 438. https://doi.org/10.7868/S0044457X18040086]https://doi.org/10.1134/S0036023618040095
Uvarova M.A., Grineva A.A., Datchuk R.R. et al. // Russ. J. Inorg. Chem. 2018. V. 63. P. 618. [Уварова М.А., Гринева А.А., Датчук Р.Р. и др. // Журн. неорган. химии. 2018. Т. 63. № 5. С. 587. https://doi.org/10.7868/ S0044457X18050094]https://doi.org/10.1134/S0036023618050108
Battye T.G.G., Kontogiannis L., Johnson O. et al. // Acta Crystallogr. D. 2011. V. 67. P. 271. https://doi.org/10.1107/S0907444910048675
Evans P.R. // Acta Crystallogr. D. 2006. V. 62. P. 72. https://doi.org/10.1107/S0907444905036693
SMART (control) and SAINT (integration) Software, Version 5.0, Bruker AXS Inc., Madison, WI, 1997.
SAINT: Area-Detector Integration Sofware. Bruker: Madison, 603 Wisconsin, USA, 2012.
Sheldrick G.M. SADABS. Program for scaling and Correction of Area Detector Data, University of Göttingen, 1997.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3. https://doi.org/10.1107/S2053229614024218
Song Y.J., Kwak H., Lee Y.M. et al. // Polyhedron. 2009. V. 28. P. 1241. https://doi.org/10.1016/j.poly.2009.02.014
Biradha K., Seward C., Zaworotko M.J. // Angew. Chem., Int. Ed. 1999. V. 38. P. 492. https://doi.org/10.1002/(SICI)1521-3773(19990215)38: 4<492::AID-ANIE492>3.0.CO:2-%23
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии