Журнал неорганической химии, 2022, T. 67, № 9, стр. 1339-1349
Композитные сорбционные материалы на основе смешанных ферроцианидов K-Ni и K-Zn для извлечения цезия из морской воды
А. Н. Драньков a, *, В. А. Балыбина a, И. Ю. Буравлев a, О. О. Шичалин a, А. Н. Федорец a, С. Г. Красицкая a, Д. А. Саланин a, И. Г. Тананаев a, Е. К. Папынов a
a Дальневосточный федеральный университет
690922 Владивосток, п. Аякс, 10, Россия
* E-mail: artur.drankov@gmail.com
Поступила в редакцию 22.02.2022
После доработки 22.03.2022
Принята к публикации 30.03.2022
- EDN: EVCGTT
- DOI: 10.31857/S0044457X22090033
Аннотация
Представлен оригинальный способ получения композитных сорбционных материалов на основе смешанных ферроцианидов K-Ni и K-Zn в составе с силоксан-акрилатной эмульсией и полиэтиленом. Оригинальность способа заключается в гидрофобизации материала путем внедрения в структуру ферроцианидов волокон полиэтилена. Исследована морфология поверхности и структура полученных сорбентов с помощью растровой электронной микроскопии, рентгенофазового анализа и низкотемпературной адсорбции азота. Изучены особенности извлечения микро- и макроконцентраций катионов Cs+, а также радионуклидов 137Cs из морской воды в статических условиях. Проведена аппроксимация экспериментальных значений сорбции по уравнениям Ленгмюра, Фрейндлиха и рассчитаны значения предельной сорбции Gmax и константы адсорбционного равновесия Kl. Показано, что лучшими сорбционными характеристиками обладают сорбенты, синтезированные с использованием полиэтилена, с достижением степени очистки морской воды от ионов цезия до 99%. Среднее значение коэффициента распределения цезия в морской воде составляет 3.7 × 104 мл/г при соотношении т : ж = 1000 мл/г, что указывает на перспективность их применения для очистки морской воды от радиоактивного цезия.
ВВЕДЕНИЕ
Одним из наиболее опасных радионуклидов антропогенного происхождения, входящих в состав жидких радиоактивных отходов (ЖРО), является 137Cs [1]. Данный радионуклид характеризуется высокими показателями проникающей радиации и миграционной способности в объектах окружающей среды и живых организмах [2–6]. Поэтому важной задачей радиохимии является очистка радиационно загрязненных вод от радионуклидов цезия. Большинство ЖРО низкого и среднего уровня активности имеют нейтральную или слабощелочную среду, рН варьируется в диапазоне от 6 до 9 [7]. При выборе метода очистки радиоактивных растворов определяющим фактором является форма нахождения радиоактивных элементов в их составе. Качественное и количественное распределение указанных форм зависит от природы элемента и состава жидкой фазы. Цезий в широком диапазоне рН находится в виде однозарядных катионов Сs+. В случае присутствия в растворах взвесей и коллоидов гидроксидов или алюмосиликатов (глин) цезий переходит в псевдоколлоидное и грубодисперсное состояние, однако образование комплексных соединений для цезия нехарактерно [8]. В том случае, когда цезий находится в растворе в ионном виде, целесообразно применять для извлечения радионуклида сорбционные методы очистки. В качестве альтернативных и более перспективных сорбционных систем могут выступать материалы на основе смешанных ферроцианидов [9, 10]. Известными сорбционными материалами для очистки морской воды от цезия являются хитозан-ферроцианидные сорбенты (ХФС) на основе ферроцианидов (ФЦ) K-Ni, K-Cu и K-Zn [11]. В динамических условиях эффективность сорбции 137Cs и элюирования ХФС K-Zn превышает 95%. Предложена двухступенчатая схема концентрирования 137Cs из морской воды. Первый этап – это удаление радионуклида из морской воды с помощью ХФС K-Zn, второй этап – сорбция 137Cs из элюата с использованием ХФС Ni-K [12]. В работе [13] доказана эффективность применения целлюлозно-неорганического сорбента на основе ферроцианида железа-калия “АНФЕЖ” для сорбционного извлечения природных и техногенных радионуклидов из ЖРО, в состав которых входит морская вода. В ходе исследования сорбционных характеристик полученного в данной работе материала в динамических условиях (пропускание 1000 л воды со скоростью 150 мл/(см2 мин)) было выявлено, что он обладает высокими показателями селективности по отношению к радионуклиду 137Cs (степень извлечения достигает 95%) и способен извлекать его даже из больших количеств морской воды (до 1000 л). В другой работе [14] показано, что для извлечения 137Cs с применением фосфоромолибдата аммония и сорбентов на его основе в динамических условиях морскую воду необходимо подкислять до рН 1–2 азотной кислотой для повышения эффективности сорбции. Однако это накладывает ряд ограничений на использование данных сорбентов, связанных с их использованием, например, в экспедиционных условиях.
Известно, что наряду с указанными сорбентами малорастворимые ФЦ переходных металлов Fe, Co, Cu, Ni, Zn, Ti, а также сорбенты на их основе обладают высоким сродством к цезию [15]. В отличие от фосфоромолибдата аммония сорбционные свойства ферроцианидов в диапазоне рН 3–11 [16] практически не изменяются, поэтому они широко используются для извлечения 137Cs из высокоминерализованных жидких сред, в том числе из морской воды. Селективность ФЦ по отношению к цезию связана с наличием вакансий в позициях Fe(CN)6 кристаллической решетки. При этом способность ионов щелочных элементов входить в состав ФЦ определяется кристаллохимическим соответствием их кристаллической решетки и поглощаемых катионов. В процессе сорбции ФЦ могут поглощать ионы щелочных металлов как по ионообменному механизму, так и в результате молекулярной сорбции. В чистом виде ФЦ практически не используются, так как представляют собой высокодисперсные порошки с низкой гидромеханической прочностью. Использование ФЦ в составе композитных сорбентов повышает их гидромеханическую прочность и делает возможным применение в динамических условиях [17]. В качестве матрицы в композитных сорбентах на основе ФЦ, пригодных для извлечения 137Cs из морской воды, могут выступать углеродные волокна [18], целлюлоза [19], хитозан [20], эмульсии [21, 22].
Из анализа литературных данных следует, что для извлечения 137Cs из морской воды наиболее подходят ферроцианиды переходных металлов, сорбционно-селективные характеристики которых не зависят от рН жидкой фазы. Предпочтительным является использование сорбентов на основе ферроцианидов K-Ni и K-Zn, так как они позволяют извлекать радиоцезий с эффективностью более 95%.
В настоящей работе представлен новый оригинальный способ получения сорбционных материалов композитного типа на основе смешанных ферроцианидов K-Ni и K-Zn в составе с силоксан-акрилатной эмульсией и полиэтиленом. Сорбционные свойства в отношении синтезированных материалов исследованы сорбцией стабильного изотопа цезия Cs+ из растворов дистиллированной и морской воды.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реактивы. Для синтеза сорбционных материалов использовали следующие прекурсоры: хлорид никеля (NiCl2), хлорид цинка (ZnCl2) и ферроцианид калия K4[Fe(CN)6] (ООО “НеваРеактив”, Россия). В качестве темплата применяли силоксан-акрилатную эмульсию марки “rilluxSilicon-916” (содержание твердой фазы 50%, производитель Brillux (Польша)) [23] и полиэтилен высокого давления (ПЭВД, ПАО “Казаньоргсинтез”, Россия). Все химические вещества были аналитической чистоты и использовались без дополнительной очистки.
Синтез сорбента на основе смешанного ФЦ Ni-K в составе с силоксан-акрилатной эмульсией и полиэтиленом
Синтез проводили медленным добавлением 100 мл смеси 0.18 М раствора NiCl2 и 10 мл эмульсии к 100 мл 0.08 М раствора K4[Fe(CN)6] при интенсивном перемешивании в течение 60 мин. По окончании сформировавшийся осадок промывали дистиллированной водой и сушили при 100°С в сушильном шкафу в атмосфере воздуха. Полученный материал представлял собой гранулы неправильной формы зеленого цвета.
Следующей стадией являлось получение композита с использованием полимерной матрицы на основе ПЭВД путем интегрирования полученных частиц смешанных ферроцианидов на поверхность органического темплата по следующей схеме: в плоскодонную колбу объемом 250 мл с обратным холодильником помещали 1 г волокон полиэтилена и добавляли 150 мл толуола при интенсивном перемешивании и нагревании до 120°С на магнитной мешалке до полного растворения компонентов с образованием гомогенной смеси. Затем в полученный раствор вносили ФЦ Ni-K (фракция 0.2–0.3 мм) и перемешивали на магнитной мешалке в течение 60 мин.
В ходе постепенного остывания гетерогенного раствора происходил процесс агломерации, в ходе которого молекулы полиэтилена, затвердевая вследствие кристаллизации, скрепляли между собой твердые частицы ФЦ Ni-K. Полученный композит отфильтровывали и сушили в течение 24 ч при комнатной температуре в сушильном шкафу в атмосфере воздуха. Полученный сорбент представлял собой пористый полимер, в объеме которого находились интегрированные частицы ФЦ Ni-K светло-зеленого цвета.
Методика синтеза сорбента на основе смешанного ФЦ Zn-K в составе с силоксан-акрилатной эмульсией и полиэтиленом
Синтез данного сорбента проводили аналогично описанной выше методике с учетом получения смеси компонентов на основе 100 мл 0.18 М раствора ZnCl2, 10 мл эмульсии и 100 мл 0.08 М раствора K4[Fe(CN)6], в том числе с последующей стадией темплатного синтеза.
Полученный сорбент представлял собой пористый полимер, в объеме которого находились интегрированные частицы ФЦ Zn-K белого цвета.
Методы исследования. Идентификацию фаз полученных образцов проводили с помощью рентгенофазового анализа (РФА, CuKα-излучение, Ni-фильтр, средняя длина волны (λ) 1.5418 Å, диапазон углов съемки 10°–80°, шаг сканирования 0.02°, скорость регистрации спектров 5 град/мин) на рентгеновском дифрактометре D8 Advance Bruker-AXS (Германия). Определение удельной поверхности осуществляли на приборе ASAP 2020 MP Micromeritics GmbH (США) методом физической адсорбции азота при температуре 77 K, данные обсчитывали по методу БЭТ. Анализ остаточного содержания Cs+ в пробах выполняли методом атомно-адсорбционной спектрометрии (ААС) на приборе АА-7000 Shimadzu (Япония). Изображения поверхности образцов были получены с использованием растровой электронной микроскопией (РЭМ) на приборе Carl Zeiss Ultra 55 (Германия) с приставкой для энергодисперсионного микроанализа (ЭДС) Bruke (Германия).
Исследование сорбции стабильного изотопа цезия (133Cs) из растворов в статических условиях
Исследование сорбционных свойств материалов на основе смешанных ФЦ Ni-K и Zn-K осуществляли путем сорбции стабильного изотопа цезия (133Cs) из растворов в статических условиях.
В качестве растворов в данном эксперименте использовали дистиллированную и морскую воду. Концентрация введенного стабильного цезия в каждом растворе составляла ~150 мг/л. Навеску сорбента (10 мг) помещали в пробирку Эппендорфа и приливали 10 мл раствора стабильного цезия (т : ж = 1000 мл/г). Серию пробирок закрепляли на вертикальном шейкере и перемешивали со скоростью 20 об/мин. Сорбция проходила в течение 48 ч. Далее сорбент отделяли от раствора на фильтре “синяя лента” и определяли остаточное содержание ионов Cs+ методом ААС.
Расчет степени очистки (RE, %) проводили по формуле:
где С0 – исходная концентрация Cs+ в растворе, мг/л; С1 – концентрация Cs+ в растворе после сорбции, мг/л.Для математической обработки экспериментальных данных изотерм сорбции использовали общеизвестные модели сорбции на границе тв/ж.
Уравнение Фрейндлиха:
где С – равновесная концентрация Cs+ (мг/л); Kf – константа Фрейндлиха, характеризующая относительную адсорбционную способность и представляющая собой величину адсорбции при равновесной концентрации, равной единице; m – показатель неоднородности обменных центров, характеризующий изменение теплоты адсорбции в зависимости от степени их заполнения.Уравнение Ленгмюра:
где Gmax – значение предельной сорбции (мг/г); С – равновесная концентрация Cs+ (мг/л); Kl – константы адсорбционного равновесия, характеризующие энергию связи адсорбент–адсорбат.Комбинированное уравнение Ленгмюра–Фрейндлиха:
где Gmax – значение предельной сорбции (мг/г); С – равновесная концентрация Cs+ (мг/л); Klf – константы адсорбционного равновесия, характеризующие энергию связи адсорбент–адсорбат; m – показатель неоднородности обменных центров, характеризующий изменение теплоты адсорбции в зависимости от степени их заполнения. Аппроксимацию экспериментальных данных указанными уравнениями в нелинейной форме проводили с использованием программы “SciDavis”.Испытания сорбционных характеристик образцов по отношению к радионуклиду 137Cs
Сорбционные характеристики образцов определяли на примере сорбции микроколичеств радионуклида 137Cs. Эксперименты проводили в статических условиях путем непрерывного перемешивания навески воздушно-сухого сорбента массой ~0.1 г, взвешенной с точностью 0.0001 г, с 20 мл раствора в течение 48 ч [24]. Затем смесь фильтровали через бумажный фильтр “белая лента” и определяли в фильтрате удельную активность 137Cs прямым радиометрическим методом с использованием спектрометрического комплекса СКС-50М (Грин стар технолоджиз, Москва). По результатам анализов рассчитывали значения коэффициента распределения (Kd) соответствующего радионуклида по формуле:
(5)
${{K}_{d}} = \frac{{{{A}_{{\text{0}}}} - {{A}_{p}}}}{{{{A}_{p}}}}\frac{{{{V}_{p}}}}{{{{m}_{c}}}},$В качестве жидкой фазы использовали раствор NaNO3 с концентрацией 1 моль/л и морскую воду, отобранную в Севастопольской бухте Черного моря, соленость 18.1, рН 7.75–8.25. Перед началом экспериментов в растворы вносили индикаторные количества радионуклида 137Cs (~105 Бк/л).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В табл. 1 приведены полученные материалы на основе смешанных ФЦ K-Ni и K-Zn в составе с силоксан-акрилатной эмульсией и полиэтиленом, которые представляют собой пористые композиты с интегрированными частицами ФЦ.
Таблица 1.
Обозначение образцов и состав сорбционных материалов
| Обозначение образцов | Состав сорбционного материала |
|---|---|
| ФЦ K-Ni | Смешанный ферроцианид калия-никеля |
| ФЦ K-Zn | Смешанный ферроцианид калия-цинка |
| ФЦ K-Ni-Pe | ФЦ K-Ni с добавлением полиэтилена |
| ФЦ K-Zn-Pe | ФЦ K-Zn с добавлением полиэтилена |
| ФЦ K-Ni-Pe-Em | ФЦ K-Ni с полиэтиленом и силоксан-акрилатной эмульсией |
| ФЦ K-Zn-Pe-Em | ФЦ K-Zn с полиэтиленом и силоксан-акрилатной эмульсией |
Согласно данным РФА (рис. 1), полученные материалы имеют высокоорганизованную кристаллическую структуру, о чем свидетельствует высокая интенсивность их дифракционных максимумов на рентгенограммах анализируемых материалов. Следует также отметить, что степень кристалличности исходного образца (ФЦ K-Ni) ниже, чем композитных материалов, полученных с использованием органических темплатов. Особенно велик прирост степени кристалличности образцов при введении волокон полиэтилена, что может быть связано с более равномерным распределением центров кристаллизации по объему образца и увеличением их количества за счет дезагрегации частиц ФЦ. Не исключен также процесс формирования кристаллической структуры в присутствии ФЦ из-за большей гибкости и подвижности макромолекул полиэтилена, в связи с этим возможно образование более крупных кристаллитов по сравнению с исходным образцом.
Рис. 1.
Рентгенограммы полученных образцов: 1 – ФЦ K-Ni; 2 – ФЦ K-Ni-Pe, 3 – ФЦ K-Ni-Pe-Em, состав образцов представлен табл. 1.

На всех дифрактограммах композитов на основе ФЦ K-Zn (рис. 2) присутствуют пики, которые могут быть отнесены к кристаллической фазе K2Zn3[Fe(CN)6]2. Аморфных гало на дифрактограммах не наблюдается, что говорит о высокой степени кристалличности исследованных материалов.
С целью визуализации кристаллических структур полученных смешанных ФЦ были построены их структурные 3D-модели (рис. 3) с использованием программного обеспечения VESTA [25]. Параметры элементарной ячейки синтезированных ферроцианидов совпадают с расчетными и соответствуют кубической форме a = b = c = = 9.96000 Å [26]. Исходя из модели Кеггина, основу структуры ФЦ составляет полианионный каркас, химический состав которого можно выразить формулой ${\text{M}}_{{2n}}^{х}{\text{M}}_{{(2 - n)}}^{у}$[Fe(CN)6], где Мх = K+, Cs+; Му = Co2+, Ni2+, Cu2+, Zn2+, Fe2+ и др. [27], которые обладают повышенной избирательностью к ионам Cs, о чем свидетельствует увеличение селективности в ряду Na+ < K+ < ${\text{NH}}_{4}^{ + }$ $ \ll $ Rb+ < Cs+ [28]. Высокая избирательность ФЦ к цезию объясняется ионно-ситовым эффектом, обеспечивающим предпочтительную адсорбцию конкретных катионов [29]. Поэтому подобная модель объясняет возможность у ФЦ как ионного обмена, так и молекулярной сорбции.
Микроскопические исследования позволили установить, что поверхность исходного ФЦ K-Ni (рис. 4а) имеет монолитную структуру, на поверхности которой присутствуют мелкие частицы, вероятно, образовавшиеся в процессе пробоподготовки. Образцы, полученные с силоксан-акрилатной эмульсией (рис. 4б), имеют более развитую поверхность. Видно, что поверхность материала изменяется с монолитной на рыхлую, характеризующейся присутствием частиц ферроцианидов, размер которых не превышает 100 нм. При использовании полиэтилена происходит образование пористой структуры материала, состоящей из мелких кристаллитов неправильной формы, которые связывают между собой волокна полиэтилена (рис. 4в, 4г).
Рис. 4.
РЭМ-изображения поверхности смешанных ФЦ K-Ni: а – исходный, б – с добавлением силоксан-акрилатной эмульсии, в – с добавлением полиэтилена, г – с добавлением полиэтилена и силоксан-акрилатной эмульсии.

На рис. 5 приведены РЭМ-изображения поверхности материалов на основе смешанных ФЦ K-Zn. Можно заметить, что исходный образец (рис. 5а) имеет структурированную поверхность в виде хорошо ограненных кубических кристаллитов. Образцы, полученные с эмульсией, характеризуются мелкозернистой пористой структурой, размер кристаллитов намного меньше размера исходного ФЦ (рис. 5б). Введение полиэтилена и эмульсии (аналогично выше представленному образцу ФЦ K-Ni) также приводит к формированию более рыхлой структуры в виде полимера с интегрированными частицами ФЦ K-Zn (рис. 5в) и увеличению пористости в присутствии эмульсии (рис. 5г).
Рис. 5.
РЭМ-изображения поверхности смешанных ФЦ K-Zn: а – исходный, б – с добавлением силоксан-акрилатной эмульсии, в – с добавлением полиэтилена, г – с добавлением полиэтилена и силоксан-акрилатной эмульсии.

По данным ЭДС (табл. 2) было установлено, что количественное отношение вводимых металлов Ni/Zn к K варьируется в пределах 1.9–2.21, содержание K остается на одном уровне и не зависит от способа получения материалов. Наличие хлора в образцах, вероятно, связано с его частичным захватом формирующимся осадком в процессе синтеза. Соотношение Ni : Zn и ферроцианидной составляющей сохраняется в пределах 1 : 2.
Таблица 2.
Содержание оксидных фаз магнитных композитов, полученных гидротермальным методом при различных температурах
| Образец | Содержание элементов, мас. % | ||||||
|---|---|---|---|---|---|---|---|
| Ni | Zn | Fe | K | Cl | O | N | |
| Ц K-Ni | 24.02 | – | 13.32 | 12.73 | 5.41 | 10.84 | 33.67 |
| Ц K-Ni-Pe | 27.09 | – | 13.18 | 12.46 | 3.60 | 18.18 | 25.19 |
| ФЦ K-Zn | – | 25.14 | 12.94 | 13.38 | 0.32 | 12.39 | 35.82 |
| ФЦ K-ZN-Pe | – | 30.74 | 13.25 | 13.33 | 2.82 | 10.41 | 28.89 |
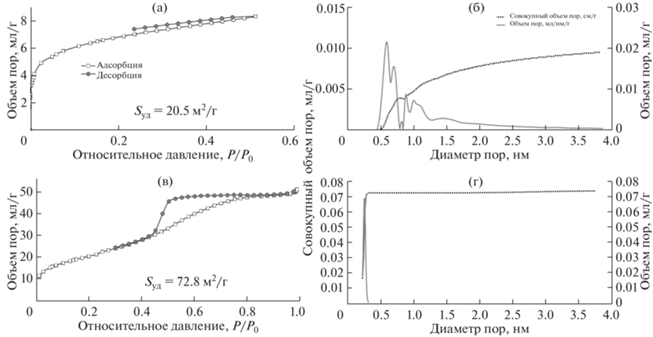
В результате увеличения числа контактов между частицами ферроцианидов и волокон полиэтилена формируются более крупные агломераты, за счет чего структура и поверхность материала становятся более развитыми и пористыми (рис. 5а–5с). На рис. 6a показано, что изотерма низкотемпературной адсорбции–десорбции азота для образца ФЦ K-Zn-Pe относится к типу I, по классификации IUPAC, характерному для микропористых тел с относительно малой долей внешней поверхности (20.5 м2/г). Адсорбция в микропорах описывается изотермой типа H1, для которой характерно наличие почти горизонтального плато. Методом DFT (рис. 6а) установлено, что полное заполнение пор происходит при очень низком относительном давлении, которое подтверждается идентичным диапазоном размера микропор (0.5–2 нм). Очевидное отличие имеет образец (ФЦ K-Ni-Pe), величина SБЭТ увеличивается до 72.8 м2/г, и переход формы петли гистерезиса изотермы адсорбции–десорбции азота от типа Н1 к типу Н2 указывает на формирование мезопор в составе образца (рис. 6б). Это подтверждается расчетом по методу DFT, где на графике распределения пор по размерам видно, что в объеме образца формируются мезопоры размером 4–8 нм (рис. 6б).
Рис. 6.
Изотермы низкотемпературной сорбции–десорбции азота и гистограммы распределения пор по размеру, рассчитанному по методу DFT, для ФЦ: а, а* – ФЦ K-ZN + Pe; б, б* – ФЦ K-Ni + Pe.
Определение сорбционных характеристик к стабильному изотопу цезия (133Cs)
Исследованы сорбционные свойства композитных сорбентов на основе смешанных ФЦ K-Ni и K-Zn в составе с силоксан-акрилатной эмульсией и полиэтиленом путем сорбции стабильного изотопа цезия из растворов дистиллированной и морской воды, концентрация введенного стабильного цезия в каждом растворе равна ~150 мг/л. На основании остаточного содержания цезия в анализируемых пробах с помощью метода ААС были рассчитаны сорбционные показатели исследуемых материалов. Согласно классификации [30], изотермы сорбции ионов цезия (рис. 7) можно отнести к H-типу, который отличается вертикальным начальным участком, что обусловлено высоким сродством сорбционных центров к ионам цезия. Полученные изотермы характеризуются четко выраженным плато, что свидетельствует о достижении адсорбционного равновесия и заполнении всех сорбционных центров. Экспериментальные данные изотерм сорбции ионов Cs+ были обработаны с использованием моделей Ленгмюра и Фрейндлиха (рис. 7).
Рис. 7.
Изотермы сорбции: a – ФЦ K-Ni-Pe, б – ФЦ K-Ni-Pe-Em, в – ФЦ K-Zn-Pe, г – ФЦ K-Zn-Pe-Em; 1 – аппроксимация экспериментальных значений (○), 2 – с использованием уравнения Ленгмюра, 3 – с использованием уравнения Фрейндлиха.

В табл. 3 приведены соответствующие значения константы адсорбционного равновесия (Kl) и предельной сорбции (Gmax). На основании высоких значений коэффициентов корреляции (R2) можно сделать вывод, что полученные значения описываются уравнением Ленгмюра. Показано, что наибольшей сорбционной емкостью обладает образец ФЦ K-Zn-Pe-Em, что, вероятно, связано с повышенным количеством активных центров сорбции допированных частиц ферроцианида цинка на поверхности полиэтилена и силаксан-акрилатной эмульсии в процессе получения композиционных материалов. Степень очистки исследуемых растворов от цезия с применением в качестве сорбентов композитных материалов на основе смешанных ФЦ K-Ni и K-Zn в составе с силоксан-акрилатной эмульсией и полиэтиленом может достигать 99% практически для всех исследуемых образцов, исключение составляет образец ФЦ K-Zn-Pe, который способен извлекать цезий из растворов с эффективностью до 96%.
Таблица 3.
Константы уравнений Ленгмюра и Фрейндлиха, рассчитанные после аппроксимации экспериментальных данных
| Уравнение | Параметр | ФЦ K-Ni-Pe | ФЦ K-Ni-Pe-Em | ФЦ K-Zn-Pe | ФЦ K-Zn-Pe-Em |
|---|---|---|---|---|---|
| Ленгмюра | Gmax | 249.34 ± 32.3 | 172 ± 10.8 | 246 ± 10.6 | 253 ± 35.8 |
| Kl | 0.010 ± 0.004 | 0.73 ± 0.31 | 0.009 ± 0.003 | 0.181 ± 0.002 | |
| R2 | 0.96 | 0.95 | 0.96 | 0.99 | |
| Фрейндлиха | Kf | 27.8 ± 5.16 | 53.98 ± 5.48 | 24.17 ± 11.54 | 37.82 ± 10.36 |
| m | 0.236 ± 0.047 | 0.266 ± 0.024 | 0.448 ± 0.11 | 0.299 ± 0.064 | |
| R2 | 0.91 | 0.98 | 0.88 | 0.89 |
На основании высоких значений коэффициентов корреляции (R2) и соответствия рассчитанных и экспериментальных значений сорбционной емкости можно сделать вывод, что экспериментальные данные достоверно описываются уравнениями Ленгмюра и Фрейндлиха. Это свидетельствует о протекании преимущественно мономолекулярной адсорбции на начальной стадии, что характерно для ионообменного механизма сорбции. Показано, что наибольшей сорбционной емкостью обладают образцы, полученные с использованием полиэтилена, что, вероятно, связано с его химическими свойствами и образованием дополнительных активных ионообменных центров.
Определение сорбционных характеристик к радионуклиду 137Cs
В работе изучены сорбционные свойства полученных сорбентов по отношению к 137Cs, извлекаемому из модельных растворов, состав которых представлен в табл. 4. В табл. 5 представлены значения коэффициентов распределения (Kd) 137Cs при сорбции из модельных растворов с использованием различных сорбентов, применяемых на практике, а их описание и производители приведены в табл. 4.
Таблица 4.
Описание и характеристики известных используемых сорбентов для сорбции 137Cs
| Сорбент | Производитель | Состав | Размер частиц, мм | Техническое условие |
|---|---|---|---|---|
| NaA | Ишимбайский химико-катализаторный завод, Республика Башкирия, Россия | Натриевая форма цеолита типа А | 0.2–0.5 | 2163-003-15285215-2006 |
| NaFeA | ДВФУ, Владивосток | Магнитный цеолит типа А | 0.2–0.5 | – |
| Клиноптилолит | Месторождение “Сокирница”, Украина | Цеолит | 0.2–0.5 | 14.5-00292540.001-2001 |
| Термоксид 35 | ООО “ТЕРМОКСИД” (Заречный, Свердловск область) |
Гидроксид циркония, никель-калий ферроцианид |
0.4–1.5 | 2641-019-57983206-2012 |
| ФТ-1 | ИХ ТРЭМС КНЦ РАН, Апатиты | Фосфат титана | 0.3–0.5 | – |
| ТС-1 | ИХ ТРЭМС КНЦ РАН, Апатиты | Титаносиликат калия-натрия | 0.3–0.5 | – |
| ФНС-10 | НПП Эктос-Атом, ОАО, Москва |
Никель-калий ферроцианид |
0.2–0.5 | 2641-012-57989206-2012 |
| МДМ | Промышленная партия, производитель ИФХЭ РАН | Сорбент на основе модифицированного диоксида марганца | 0.2–0.5 | 2641-001-51255813-2007 |
Таблица 5.
Значения коэффициентов распределения (Kd) 137Cs на различных сорбентах при сорбции из модельных растворов
| Сорбент | Kd137Cs (мл/г) на сорбентах | ||
|---|---|---|---|
| 0.1 ммоль/л NaNO3 | 1.0 ммоль/л NaNO3 | морская вода | |
| NaFeA | 2.5 × 103 | 0.2 × 103 | 1.7 × 103 |
| NaA | 8.9 × 103 | 0.7 × 103 | 0.2 × 103 |
| Клиноптилолит | 1.6 × 103 | 0.1 × 103 | 1.5 × 103 |
| ФТ-1 | 7.3 × 103 | 0.8 × 103 | 8.8 × 103 |
| ТС-1 | 5.7 × 104 | 2.9 × 104 | 1.8 × 104 |
| ФНС-10 | 8.4 × 104 | 6.0 × 104 | 1.1 × 104 |
| Термоксид 35 | 1.2 × 105 | 8.1 × 104 | 3.1 × 104 |
| ФЦ K-Zn-Pe | 2.7 × 103 | 2.2 × 103 | 4.2 × 103 |
| ФЦ K-Ni-Pe | 5.2 × 105 | 1.8 × 105 | 3.7 × 104 |
Результаты исследования показывают, что наиболее высокими сорбционными характеристиками по отношению к 137Cs обладает образец ФЦ K-Ni-Pe, значение Kd для которого превышает значения для промышленно используемых сорбентов на два порядка (табл. 5).
ЗАКЛЮЧЕНИЕ
Проведен синтез композитных материалов на основе смешанных ФЦ K-Ni и K-Zn в составе с силоксан-акрилатной эмульсией и полиэтиленом. Установлено, что фазовый состав материалов характеризуется высокоорганизованной кристаллической структурой, однако ФЦ K-Ni представлен смешанным составом твердой фазы в виде Ni(ClO3)2 и К2Ni[Fe(CN)6]. Полученные материалы имеют пористую структуру с размером пор в диапазоне 0.5–8 нм и удельной поверхностью 20.5–72.8 м2/г. Изучены особенности извлечения микро- и макроконцентраций катионов Cs+, а также радионуклидов 137Cs из морской воды в статических условиях. Проведена аппроксимация экспериментальных значений сорбции по уравнениям Ленгмюра, Фрейндлиха и рассчитаны значения предельной сорбции Gmax и константы адсорбционного равновесия Kl. Показано, что лучшими сорбционными характеристиками обладают сорбенты, синтезированные с использованием полиэтилена, с достижением степени очистки морской воды от ионов цезия до 99%. Среднее значение коэффициента распределения цезия в морской воде составляет 3.7 × 104 мл/г при соотношении т : ж = 1000 мл/г, что указывает на перспективность их применения для очистки морской воды от радиоактивного цезия. Результаты исследования представляют перспективу для синтеза эффективных и практически востребованных селективных сорбентов, получаемых простым и дешевым способом.
Список литературы
Авраменко В.А., Железнов В.В., Майоров В.Ю. и др. // Современные проблемы науки и образования. 2013. № 5.
Alshuraiaan B., Pushkin S., Kurilova A. et al. // Energies. 2021. V. 14. № 12. P. 3079. https://doi.org/10.3390/en14123709
Diaz-Maurin F., Sun H.C., Yu J. et al. // Mater. Res. Soc. 2019. № 4. P. 959. https://doi.org/10.1557/adv.2018.636
Gupta N.K., Sengupta A., Gupta A. et al. // J. Environ. Chem. Eng. 2018. V. 6. № 2. P. 2159. https://doi.org/10.1016/j.jece.2018.03.021
Avramenko V.A., Burkov I.S., Zheleznov V.V. et al. // At. Energ. 2002. V. 92. № 6. P.488.
Avramenko V.A., Egorin A.M., Papynov E.K. et al. // Radiochem. 2017. V. 59. № 4. P. 407. https://doi.org/10.1134/S1066362217040142
Милютин В.В., Гелис В.М., Козлитин Е.А. и др. // Вопросы радиационной безопасности. 2013. № 4. С. 23.
Тананаев И.Г., Авраменко В.А. // Журн. Белорус. гос. ун-та. Экология. 2017. № 4. С. 33.
Tananaev I.V., Seifer G.B., Kharitonov Yu.Ya. et al. Ferrocyanide Chemistry. M.: Nauka, 1971.
Sharygin L.M., Borovkova O.L., Kalyagina M.L. et al. // Radiochem. 2013. V. 55. № 1. P. 91. https://doi.org/10.1134/S1066362213010177
Zemskova L.A., Egorin A.M., Tokar E.A. // Russ. J. Inorg. Chem. 2021. V. 66. P. 1268. https://doi.org/10.1134/S0036023621090175
Tokar’ E., Zemskova L., Tutov M. et al. // J. Radioanal. Nucl. Chem. 2020. V. 325. P. 567. https://doi.org/10.1007/s10967-020-07248-9
Remez V.P., Zelenin V.I., Smirnov A.L. et al. // Sorbts. Khromatogr. Prots. 2009. V. 9. P. 739.
Bezhin N.A., Dovhyi I.I., Milyutin V.V. et al. // J. Radioanal. Nucl. Chem. 2021. V. 327. P. 1095. https://doi.org/10.1007/s10967-020-07588-6
Han F., Zhang G.H., Gu P.J. et al. // Radioanal. Nucl. Chem. 2013. V. 295. P. 369. https://doi.org/10.1007/s10967-012-1854-3
Prout W.E., Russell E.R., Groh H.J. et al. // J. Inorg. Nucl. Chem. 1965. V. 27. P. 473. https://doi.org/10.1016/0022-1902(65)80367-0
Vincent C., Hertz A., Vincent T. et al. // Chem. Eng. J. 2014. V. 236. P. 202. https://doi.org/10.1016/j.cej.2013.09.087
Zheleznov V.V., Vysotskii V.L. // At. Energ. 2002. V. 92. P. 493. https://doi.org/10.1023/A:1020270300242
Kosyakov V.N., Veleshko A.N., Veleshk I.E. // Radiochem. 2006. V. 48. P. 589. https://doi.org/10.1134/S1066362206060099
Egorin A., Tokar E., Zemskova L. et al. // Radiochim. Acta. 2016. V. 104. P. 657. https://doi.org/10.1080/01496395.2017.1321669
Papynov E.K., Dran’kov A.N., Tkachenko I.A. et al. // Russ. J. Inorg. Chem. 2020. V. 65. № 6. P. 820. https://doi.org/10.1134/S0036023620060157
Balybina V., Dran’kov A., Tananaev I. et al. // Mater. Sci. Forum. 2021. V.1045. P. 141. https://doi.org/10.4028/www.scientific.net/MSF.1045.141
Papynov E.K., Mayorov V.Y., Palamarchuk M.S. et al. // J. Sol-Gel Sci. Technol. 2013. V. 68. P. 374. https://doi.org/10.1007/s10971-013-3039-0
Dran’kov A., Shichalin O., Papynov E. et al. // Nucl. Eng. Technol. 2022. https://doi.org/10.1016/j.net.2021.12.010
Momma K., Izumi F. // J. Appl. Crystallogr. 2011. V. 44. P. 1272. https://doi.org/10.1107/S0021889811038970
Watanabe S., Sawada Y., Nakaya M. et al. // J. Appl. Phys. 2016. V. 119. № 23. https://doi.org/10.1063/1.4954070
Вольхин В.В., Зильберман М.В., Колесова С.А. и др. // Журн. прикл. химии. 1975. Т. 48. С. 54.
Valsala T.P., Joseph A., Shah J.G. et al. // J. Nucl. Mater. 2009. V. 384. № 2. P. 146.
Loos-Neskovic C., Ayrault S., Badillo V. et al. // J. Solid State Chem. 2004. V. 177. № 6. P. 1817.
Giles C.H., MacEwan T.H., Nakhwa S.N. et al. // J. Chem. Soc. 1960. V. 14. P. 3973. https://doi.org/10.1039/jr9600003973
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии




