Журнал неорганической химии, 2023, T. 68, № 5, стр. 651-657
Термодинамическое моделирование процесса синтеза пленок оксидов ванадия и его экспериментальная реализация
В. А. Шестаков a, b, *, В. А. Селезнев c, С. В. Мутилин c, В. Н. Кичай a, Л. В. Яковкина a
a Институт неорганической химии им. А.В. Николаева СО РАН
630090 Новосибирск, пр-т Академика Лаврентьева, 3, Россия
b Новосибирский государственный архитектурно-строительный университет
630008 Новосибирск, ул. Ленинградская, 113, Россия
c Институт физики полупроводников им. А.В. Ржанова СО РАН
630090 Новосибирск, пр-т Академика Лаврентьева, 13, Россия
* E-mail: vsh@niic.nsc.ru
Поступила в редакцию 01.12.2022
После доработки 02.02.2023
Принята к публикации 03.02.2023
- EDN: SOHBQS
- DOI: 10.31857/S0044457X23600019
Аннотация
Проведено термодинамическое моделирование и экспериментальное исследование процесса синтеза пленок оксидов ванадия при разных температурах из прекурсора тетракис-этилметиламинованадий V[NC3H8]4 в присутствии кислорода и атмосфере аргона. При термодинамическом моделировании использовали метод расчета химических равновесий, основанный на минимизации энергии Гиббса системы. В экспериментальной части работы для синтеза пленок применяли методику атомно-слоевого осаждения. Результаты термодинамического моделирования и экспериментальные данные соответствуют друг другу и могут быть использованы для разработки методик синтеза пленочных покрытий на основе оксидов ванадия.
ВВЕДЕНИЕ
Диоксид ванадия (VO2) относится к сильнокоррелированным электронным квантовым материалам, в котором проявляется сверхбыстрый (26 фс) [1] обратимый фазовый переход I рода полупроводник–металл при температурах 68°С [2–5]. При этом в нем происходит структурный фазовый переход: моноклинная (VO2(M)) кристаллическая решетка преобразуется в тетрагональную (VO2(R)). Фазовый переход в VO2 сопровождается резким изменением (на несколько порядков по величине) его электрических и оптических характеристик [6–9]. Такие уникальные свойства фазового перехода в VO2 открывают многообещающие возможности для применения этого соединения в ряде новых устройств электроники и фотоники, в частности в нейроморфных системах, резистивных переключателях, элементах памяти, тепловых переключателях, голографических носителях информации, перестраиваемых отражающих зеркалах, энергоэффективных окнах и многих других [10–19].
Отмеченный фазовый переход сопровождается изменением постоянной решетки почти на 1%, что приводит к появлению сильных механических напряжений в материале VO2 с последующим образованием трещин [20]. Поэтому, как правило, VO2 синтезируется в виде тонких пленок [21–27]. В настоящее время используется широкий набор методов для получения пленок VO2: золь-гель метод [28], магнетронное распыление [29], химическое осаждение из газовой фазы [30] и др. [31–33]. Наиболее контролируемым, позволяющим синтезировать предельно тонкие однородные слои VO2, является атомно-слоевое осаждение (АСО) [34]. Суть метода заключается в постоянной подаче инертного газа-носителя в камеру-реактор и раздельному попеременному введению газообразных реагентов в этот поток так, что химические реакции, приводящие к росту пленок, протекают только в хемосорбированных слоях, т.е. с исключением реакций в газовой фазе.
Одна из основных трудностей в синтезе высококачественных пленок VO2 заключается в наличии в системе V–О многих оксидных форм и различных полиморфов [35]. Ванадий может существовать в четырех степенях окисления: 2+, 3+, 4+, 5+, в результате фазовая диаграмма V–O богата различными оксидами ванадия, которые могут образовываться в пленке. Отдельную задачу представляет формирование кристаллических пленок VO2 сразу в процессе низкотемпературного АСО, при котором, как правило, получаются кристаллические пленки V2O5 или аморфные пленки VOx, которые с помощью послеростового термического отжига переводятся в VO2 [36–39].
Цель настоящей работы состояла в определении возможности установления оптимальных условий синтеза пленок VO2 на кремнии методом АСО с использованием в качестве прекурсора тетракис-этилметиламинованадий V[NC3H8]4 (TEMAV) на основе термодинамического моделирования. Термодинамическое моделирование используется для расчета содержания конденсированных фаз и состава газовой фазы в системе, находящейся в термодинамическом равновесии. Оно позволяет предсказать образование фаз и фазовых комплексов11, образующихся в результате процессов синтеза, поэтому широко используется для описания процессов получения покрытий из газовой фазы [40–43]. Например, результаты термодинамического моделирования CVD-процесса в системе Si–B–N–C–H [40] показали возможность образования тех же самых фазовых комплексов, которые экспериментально получены в работе [44]. В работе [43] результаты моделирования не только полностью соответствуют экспериментальным данным, но и позволяют объяснить некоторые особенности синтеза диоксида ванадия.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Методика термодинамического расчета. Равновесный состав газовой фазы и фазовых комплексов определяли посредством минимизации энергии Гиббса системы при заданных Т и Р. В процессе расчета использовали базу данных и стандартное программное обеспечение банка данных по свойствам материалов электронной техники (БНД СМЭТ) [45]. В качестве дополнения применяли термодинамические данные по оксидам, карбидам и нитридам ванадия из [46, 47]. При расчете принимали следующие допущения. Предполагали, что в системе присутствуют конденсированные фазы постоянного состава и равновесный идеальный газ, образованный из молекулярных форм (специй); химический состав системы в зоне осаждения соответствует элементному составу входной газовой смеси, а газовая фаза в зоне осаждения находится в термодинамическом равновесии с конденсированными фазами. В качестве исходной термодинамической информации использовали стандартные термодинамические характеристики индивидуальных веществ: ${{\Delta }_{f}}H_{{298}}^{0},$ $S_{{298}}^{0},$ $C_{p}^{0}$ = f(T), имеющиеся в вышеуказанном банке данных и приведенных выше дополнительных источниках. Из-за отсутствия информации о термодинамических свойствах возможных в системе фаз переменного состава эти фазы не учитывали.
Синтез тонких пленок оксидов ванадия. Тонкие пленки VOx осаждали на подложках Si(100) и SiO2/Si методом плазменно-стимулированного атомно-слоевого осаждения (ПС-АСО) с чередующимися импульсами TEMAV в качестве прекурсора ванадия и плазмы Ar/O2 в качестве окислителя. Процесс осаждения проводили при трех различных температурах подложки (150, 170, 200°C) и давлении 30 Па в реакторе SI ALD LL (Sentech, Германия) [48], оснащенном лазерным эллипсометром для мониторинга процесса АСО в режиме реального времени (ALD-RTM, Sentech). Схема реактора подробно описана в работах [49, 50]. Подложки помещали на массивный заземленный металлический электрод-нагреватель, температуру которого задавали с точностью ±0.1°C программным ПИД-регулятором. В качестве газа-носителя TEMAV и для продувки камеры реактора использовали Ar высокой чистоты (99.9998%) с расходом 100 ст. см3/мин. Источник с прекурсором и газовые линии его подачи подогревали до температуры 90°С для исключения его конденсации. Через источник плазмы пропускали аргон с расходом 120 ст. см3/мин. Во время этапа плазмы через источник плазмы пропускали кислород (высокой чистоты 99.999%) с расходом 120 ст. см3/мин, а по линии прекурсора продолжал поступать аргон. Плазму генерировали удаленным источником емкостно-связанной плазмы (CCP), так, что в процессе ПС-АСО подложка была расположена отдельно от области генерации плазмы, удалена от высокоэнергетических ионов и ультрафиолетового излучения, которые могли бы привести к повреждению поверхности подложки [49, 50]. Используемый источник CCP работал на частоте 13.56 МГц при мощности плазмы 200 Вт.
Рис. 1.
Содержание конденсированных фаз в фазовом комплексе и молекулярных форм в газовой фазе, образующихся при разложении 1 моля V(NC3H8)4.
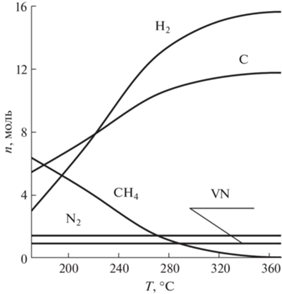
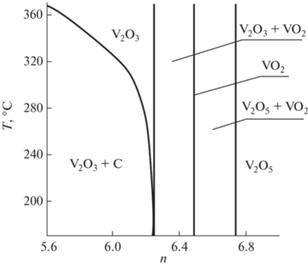
Рис. 2.
Зависимость характера фаз и фазовых комплексов, образующихся во второй стадии процесса, от величины параметра n.
Каждый цикл ПС-АСО состоял из четырех этапов: 1) импульс паров прекурсора TEMAV длительностью 80 мс; 2) продувка Ar; 3) импульс кислородной плазмы; 4) продувка Ar. В экспериментах кроме температуры подложки задавали длительность воздействия кислородной плазмой во втором полуцикле осаждения, которая составляла 15 или 60 с. Цикл периодического осаждения повторяли до тех пор, пока не достигали желаемой толщины пленки 5 или 30 нм.
Перед загрузкой в реактор подложки химически обрабатывали в смеси H2SO4 : H2O2 = 3 : 1 в течение 15 мин, промывали в чистой деионизованной воде и высушивали струей чистого сухого воздуха. После загрузки подложек в реактор по линиям плазмы и прекурсора подавали аргон, в реакторе задавали давление 30 Па и в течение 30 мин достигали стабилизации температуры подложки. Перед началом процесса ПС-АСО проводили обработку подложек кислородной плазмой в течение 10 мин при мощности 200 Вт без подачи прекурсора в реактор. Данная обработка способствовала удалению углеродно-органических загрязнений с поверхности подложки. Динамику процесса осаждения, толщину пленок оксидов ванадия, а также скорость их роста за цикл определяли in situ методом эллипсометрии.
Характеризация синтезированных пленок. Фазовый состав кристаллической структуры получаемых пленок исследовали методами рентгеновской дифракции и комбинационного рассеяния света (КРС). Измерения проводили на дифрактометре Shimadzu XRD-7000 (CuKα-излучение, Ni-фильтр, 2θ = 5°–60°, шаг 0.03, накопление 1–5 с в режиме θ–2θ). Индицирование дифрактограмм проводили c использованием программы Search Match и данных картотеки PDF [51]. Спектры КРС регистрировали при комнатной температуре в геометрии обратного рассеяния на спектрометре Т64000 Horiba Jobin Yvon со спектральным разрешением 0.5 см–1. Для возбуждения использовали линию Ar+-лазера с длиной волны 514.5 нм.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Термодинамичеcкое моделирование. Первая стадия процесса синтеза представляет собой разложение прекурсора TEMAV (V(NC3H8)4). Расчеты проводили для процесса разложения одного моля этого соединения в присутствии аргона при давлении 30 Па, в интервале температур 170–370°C. В процессе расчета учитывали возможность образования следующих конденсированных фаз: V, VN, VN0.465, V2C, VC0.88, C (графит), а также 77 молекулярных форм газовой фазы.
Как показали расчеты, единственным фазовым комплексом, образующимся в данных условиях, является VN + С. На рис. 1 показано содержание нитрида ванадия и графита в фазовом комплексе, а также различных молекулярных форм (Н2, N2, CH4) в газовой фазе в зависимости от температуры реактора.
Как можно видеть из рис. 1, содержание графита в комплексе уменьшается с понижением температуры синтеза. Учитывая это обстоятельство, а также, что температура разложения V(NC3H8)4 около 170°С [36], можно сделать вывод об оптимальности температуры 170°С для данной реакции22. Дополнительные расчеты показали, что изменение общего давления в реакторе в интервале 10–100 Па не меняет тенденций, показанных на рис. 1.
Вторая стадия синтеза предполагает взаимодействие фазового комплекса, образовавшегося на первой стадии, с кислородом. При синтезе в условиях давления 30 Па и температуры 170°С этот комплекс включает в себя 1 моль VN и 5.43 моля графита что соответствует реакции (рис. 1):
(1)
$\begin{gathered} {\text{V}}{{\left( {{\text{N}}{{{\text{C}}}_{{\text{3}}}}{{{\text{H}}}_{{\text{8}}}}} \right)}_{{\text{4}}}}{\text{ = VN + 5}}{\text{.43C + }} \\ {\text{ + }}\,\,{\text{1}}{\text{.5}}{{{\text{N}}}_{{\text{2}}}} + {\text{2}}{\text{.86}}{{{\text{H}}}_{{\text{2}}}} + {\text{6}}{\text{.57C}}{{{\text{H}}}_{{\text{4}}}}{\text{.}} \\ \end{gathered} $Далее расчеты проводили для этого комплекса. В процессе расчета учитывали возможность образования следующих конденсированных фаз: V, V3O7, V6O13, V8O15, V7O13, V6O11, V5O9, V4O7, V2O5, VO2 (две фазы), V2O3, VO, VN0.465, VN, VC0.88, V2C, C (графит), а также 48 молекулярных форм газовой фазы.
Состав системы, рассматриваемой при моделировании второй стадии синтеза, может быть представлен в виде Ar + 5.43C + VN + nO2. На рис. 2 представлена диаграмма, показывающая какие фазы и фазовые комплексы образуются в системе при различных значениях параметра n в диапазоне температур 170–370°C и давлении 30 Па. Отметим, что чистому VO2 отвечает значение n = 6.49.
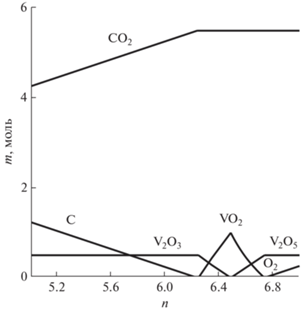
На рис. 3 показано содержание графита, оксидов ванадия, а также двуокиси углерода и кислорода в газовой фазе в зависимости от того же параметра при тех же условиях33. Эта информация позволяет описать механизм второй стадии процесса синтеза как последовательность следующих реакций:
(3)
${\text{2VN}} + {\text{1}}{\text{.5}}{{{\text{O}}}_{{\text{2}}}} = {{{\text{V}}}_{{\text{2}}}}{{{\text{О}}}_{{\text{3}}}} + {{{\text{N}}}_{{\text{2}}}}{\text{,}}$(4)
${{{\text{V}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}} + {\text{0}}{\text{.5}}{{{\text{O}}}_{{\text{2}}}} = {\text{2V}}{{{\text{O}}}_{{\text{2}}}}{\text{,}}$(5)
${\text{2V}}{{{\text{O}}}_{{\text{2}}}} + {\text{0}}{\text{.5}}{{{\text{O}}}_{{\text{2}}}} = {{{\text{V}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{5}}}}{\text{.}}$Рис. 3.
Содержание фаз в фазовых комплексах, а также молекулярных форм в газовой фазе на второй стадии процесса синтеза в зависимости от величины параметра n.
Отметим, что увеличение температуры при второй стадии синтеза приводит к образованию в газовой фазе существенного количества СО в результате реакции равновесия 2СО2 = 2СО + О2. В остальном это, как и изменение давления в реакторе в интервале 10–100 Па, не влияет на механизм процесса.
Экспериментальное подтверждение разложения прекурсора TEMAV при температурах выше 170°С. На рис. 4 приведены данные о толщине осаждаемой пленки, измеренные методом эллипсометрии in situ в режиме реального времени, показывающие реакции хемосорбции прекурсора TEMAV и лигандного обмена при различных температурах подложки. Пунктирная кривая на рис. 4 показывает изменение температуры подложки от времени. Видно, что впрыск прекурсора TEMAV приводит к резкому увеличению эффективной толщины осаждаемой пленки, которая уменьшается и выходит на насыщение в процессе продувки реактора аргоном. На данном полуцикле происходит хемосорбция молекул TEMAV на поверхности подложки, а также удаление их излишков с поверхности. Импульс кислородной плазмы приводит к уменьшению эффективной толщины пленки, так как происходит отрыв лигандов от хемосорбированных молекул TEMAV и образование оксида ванадия.
Рис. 4.
Динамика изменения толщины пленки в течение шести циклов ПС-АСО в зависимости от температуры синтеза, демонстрирующая реакции хемосорбции TEMAV и лигандного обмена при различных температурах подложки. Толщину пленок измеряли методом эллипсометрии in situ в режиме реального времени.
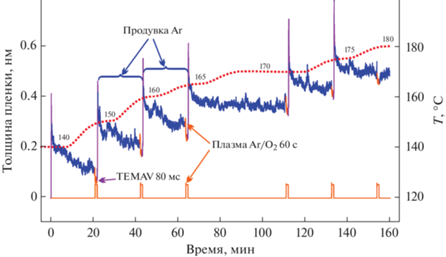
Отметим, что в диапазоне температур подложки от 140 до 165°С обработка кислородной плазмой приводит к более значительному уменьшению эффективной толщины пленки по сравнению с более высокими температурами (Т > 170°C). Начиная с температуры подложки 170°C, импульс кислородной плазмы оказывает существенно меньшее влияние на уменьшение толщины пленки. Данная закономерность свидетельствует в пользу того, что при температурах подложки 170°С и выше происходит разложение прекурсора TEMAV. Полученные результаты хорошо согласуются с литературными данными [36].
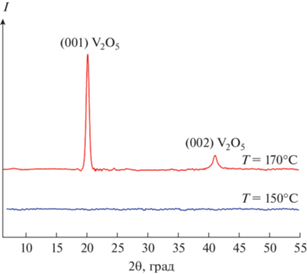
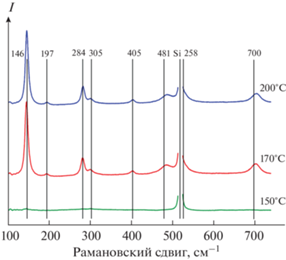
Атомно-слоевое осаждение пленок V2O5 и их характеризация. Результаты термодинамического моделирования показали, что V2O5 может быть получен при параметре n O2 > 6.7. Для подтверждения этих расчетов АСО-пленок было проведено при больших концентрациях кислорода в реакторе. На рис. 5 представлены спектры КРС пленок V2O5 толщиной 5 нм, выращенных с помощью ПС-АСО на подложках SiO2/Si при температурах 150, 170 и 200°С. Вертикальными линиями отмечены 8 различимых мод (пиков), характерных для орторомбической фазы V2O5, относящейся к пр. гр. Pmnn [52]. Видно, что температура синтеза, составляющая 150°C, недостаточна для формирования кристаллической фазы V2O5. Кристаллическая фаза, согласно данным КРС, формируется при температурах подложки Т ≥ 170°С, когда происходит разложение прекурсора. Похожие результаты получены с помощью рентгенофазового анализа пленок оксидов ванадия толщиной 30 нм, синтезированных при температурах 150 и 170°C (рис. 6). Как следует из рис. 6, пленка, синтезированная при температуре 150°C, не имеет пиков, характерных для кристаллических фаз оксидов ванадия. Пленка, синтезированная при температуре 170°C, имеет два пика, характерных для чистой поликристаллической орторомбической фазы V2O5, относящейся к пр. гр. Pmnn. Таким образом, проведенные эксперименты по синтезу пленок и их исследованию подтверждают результаты термодинамического моделирования.
Рис. 5.
Спектры КРС пленок оксидов ванадия толщиной 5 нм, синтезированных ПС-АСО на подложках SiO2/Si при температурах 150, 170 и 200°С. Интенсивный пик от Si подложки при 520.5 см–1 исключен из спектров для наглядности представленных данных. Вертикальными линиями отмечены 8 различимых мод (пиков), характерных для орторомбической фазы V2O5.
ЗАКЛЮЧЕНИЕ
Результаты термодинамического моделирования демонстрируют, что VO2 может быть получен лишь в очень узкой области изменения содержания кислорода в исходной смеси, а V2O5 формируется при высоком содержании кислорода, что подтверждается полученными экспериментальными данными.
Экспериментально показано, что температура разложения прекурсора TEMAV составляет около 170°C и выше, что согласуется с литературными данными [36]. С помощью комбинационного рассеяния света и рентгенофазового анализа показано, что температура синтеза 170°С и выше приводит к формированию в пленках кристаллической фазы V2O5 при высоком содержании кислорода в исходной смеси. Таким образом, результаты термодинамического моделирования находятся в согласии с экспериментальными данными.
Список литературы
Jager M.F., Ott C., Kraus P.M. et al. // Proc. Natl. Acad. Sci. 2017. V. 114. № 36. P. 9558. https://doi.org/10.1073/pnas.1707602114
Morin F.J. // Phys. Rev. Lett. 1959. V. 3. № 1. P. 34. https://doi.org/10.1103/PhysRevLett.3.34
Shao Z., Cao X., Luo H. et al. // NPG Asia Mater. 2018. V. 10. № 7. P. 581. https://doi.org/10.1038/s41427-018-0061-2
Liu K., Lee S., Yang S. et al. // Mater. Today. 2018. V. 21. № 8. P. 875. https://doi.org/10.1016/j.mattod.2018.03.029
Lu C., Lu Q., Gao M. et al. // Nanomaterials. 2021. V. 11. № 1. P. 114. https://doi.org/10.3390/nano11010114
Schlag H.J., Scherber W. // Thin Solid Films. 2000. V. 366. № 1–2. P. 28. https://doi.org/10.1016/S0040-6090(00)00711-2
Kana Kana J.B., Ndjaka J.M., Vignaud G. et al. // Opt. Commun. 2011. V. 284. № 3. P. 807. https://doi.org/10.1016/j.optcom.2010.10.009
Sun J., Pribil G.K. // Appl. Surf. Sci. 2017. V. 421. P. 819. https://doi.org/10.1016/j.apsusc.2016.09.125
Briggs R.M., Pryce I.M., Atwater H.A. // Opt. Express. 2010. V. 18. № 11. P. 11192. https://doi.org/10.1364/oe.18.011192
Prinz V.Y., Mutilin S.V., Yakovkina L.V. et al. // Nanoscale. 2020. V. 12. № 5. P. 3443. https://doi.org/10.1039/C9NR08712E
Mutilin S.V., Prinz V.Y., Seleznev V.A. et al. // Appl. Phys. Lett. 2018. V. 113. № 4. P. 043101. https://doi.org/10.1063/1.5031075
Mutilin S.V., Prinz V.Y., Yakovkina L.V. et al. // CrystEngComm. 2021. V. 23. № 2. P. 443. https://doi.org/10.1039/D0CE01072C
You Zhou, Ramanathan S. // Proc. IEEE. 2015. V. 103. № 8. P. 1289. https://doi.org/10.1109/JPROC.2015.2431914
Yang Z., Ko C., Ramanathan S. // Annu. Rev. Mater. Res. 2011. V. 41. № 1. P. 337. https://doi.org/10.1146/annurev-matsci-062910-100347
Nakano M., Shibuya K., Ogawa N. et al. // Appl. Phys. Lett. 2013. V. 103. № 15. P. 153503. https://doi.org/10.1063/1.4824621
Kats M.A., Blanchard R., Zhang S. et al. // Phys. Rev. X. 2013. V. 3. № 4. P. 041004. https://doi.org/10.1103/PhysRevX.3.041004
Rios C., Hosseini P., Wright C.D. et al. // Adv. Mater. 2014. V. 26. № 9. P. 1372. https://doi.org/10.1002/adma.201304476
Faucheu J., Bourgeat-Lami E., Prevot V. // Adv. Eng. Mater. 2018. P. 1800438. https://doi.org/10.1002/adem.201800438
Ke Y., Wang S., Liu G. et al. // Small. 2018. V. 14. № 39. P. 1802025. https://doi.org/10.1002/smll.201802025
Liu T.-J.K., Kuhn K. CMOS and Beyond. Cambridge: Cambridge University Press, 2014. https://doi.org/10.1017/CBO9781107337886
Zhu H.-F., Du L.-H., Li J. et al. // Appl. Phys. Lett. 2018. V. 112. № 8. P. 081103. https://doi.org/10.1063/1.5020930
Ko C., Yang Z., Ramanathan S. // ACS Appl. Mater. Interfaces. 2011. V. 3. № 9. P. 3396. https://doi.org/10.1021/am2006299
Qazilbash M.M., Brehm M., Chae B.-G. et al. // Science. 2007. V. 318. № 5857. P. 1750. https://doi.org/10.1126/science.1150124
Zimmers A., Aigouy L., Mortier M. et al. // Phys. Rev. Lett. 2013. V. 110. № 5. P. 056601. https://doi.org/10.1103/PhysRevLett.110.056601
Chang Y.J., Yang J.S., Kim Y.S. et al. // Phys. Rev. B. 2007. V. 76. № 7. P. 075118. https://doi.org/10.1103/PhysRevB.76.075118
Qazilbash M.M., Tripathi A., Schafgans A.A. et al. // Phys. Rev. B. 2011. V. 83. № 16. P. 165108. https://doi.org/10.1103/PhysRevB.83.165108
Stroud D. // Phys. Rev. B. 1975. V. 12. № 8. P. 3368. https://doi.org/10.1103/PhysRevB.12.3368
Inomata N., Usuda T., Yamamoto Y. et al. // Sensors Actuators A Phys. 2022. V. 346. P. 113823. https://doi.org/10.1016/j.sna.2022.113823
Li G., Xie D., Zhong H. et al. // Nat. Commun. 2022. V. 13. № 1. P. 1729. https://doi.org/10.1038/s41467-022-29456-5
Yakovkina L.V., Mutilin S.V., Prinz V.Y. et al. // J. Mater. Sci. 2017. V. 52. № 7. P. 4061. https://doi.org/10.1007/s10853-016-0669-y
Zhang Y., Xiong W., Chen W. et al. // Nanomaterials. 2021. V. 11. № 2. P. 1. https://doi.org/10.3390/nano11020338
Xue X., Zhou Z., Peng B. et al. // RSC Adv. 2015. V. 5. № 97. P. 79249. https://doi.org/10.1039/C5RA13349A
Shi R., Shen N., Wang J. et al. // Appl. Phys. Rev. 2019. V. 6. № 1. https://doi.org/10.1063/1.5087864
Li J., An Z., Zhang W. et al. // Appl. Surf. Sci. 2020. V. 529. P. 147108. https://doi.org/10.1016/j.apsusc.2020.147108
Brahlek M., Zhang L., Lapano J. et al. // MRS Commun. 2017. V. 7. № 1. P. 27. https://doi.org/10.1557/mrc.2017.2
Prasadam V.P., Bahlawane N., Mattelaer F. et al. // Mater. Today Chem. 2019. V. 12. P. 396. https://doi.org/10.1016/j.mtchem.2019.03.004
Bai G., Niang K.M., Robertson J. // J. Vac. Sci. Technol. A. 2020. V. 38. № 5. P. 052402. https://doi.org/10.1116/6.0000353
Niang K.M., Bai G., Robertson J. // J. Vac. Sci. Technol. A. 2020. V. 38. № 4. P. 042401. https://doi.org/10.1116/6.0000152
Kozen A.C., Joress H., Currie M. et al. // J. Phys. Chem. C. 2017. V. 121. № 35. P. 19341. https://doi.org/10.1021/acs.jpcc.7b04682
Шестаков В.А., Косинова М.Л. // Изв. АН. Сер. хим. 2021. Т. 70. № 2. С. 283. https://doi.org/10.1007/s11172-021-3083-9
Шестаков В.А., Косинова М.Л. // Журн. неорг. химии. 2021. Т. 66. № 11. С. 1585. https://doi.org/10.31857/S0044457X21110155
Шестаков В.А., Косяков В.И., Косинова М.Л. // Журн. неорган. химии. 2020. Т. 65. № 6. С. 829.https://doi.org/10.31857/S0044457X20060215
Шестаков В.А., Яковкина Л.В., Кичай В.Н. // Журн. неорган. химии. 2022. Т. 67. № 12. С. 1746. https://doi.org/10.31857/S0044457X22600608
Merenkov I.S., Katsui H., Khomyakov M.N. et al. // J. Eur. Ceram. Soc. 2019. V. 39. № 16. P. 5123. https://doi.org/10.1016/j.jeurceramsoc.2019.08.006
Титов В.А., Косяков В.И., Кузнецов Ф.А. Проблемы электронного материаловедения. Новосибирск: Наука, 1986.
Kang Y.-B. // J. Eur. Ceram. Soc. 2012. V. 32. № 12. P. 3187. https://doi.org/10.1016/j.jeurceramsoc.2012.04.045
Barin I. Termodynamical Data of Pure Substances. N.Y., 1989.
Mahmoodinezhad A., Janowitz C., Naumann F. et al. // J. Vac. Sci. Technol. A. 2020. V. 38. № 2. P. 022404. https://doi.org/10.1116/1.5134800
Henkel K., Gargouri H., Gruska B. et al. // J. Vac. Sci. Technol. A Vacuum, Surfaces, Film. 2013. V. 32. № 1. P. 01A107. https://doi.org/10.1116/1.4831897
Haeberle J., Henkel K., Gargouri H. et al. // Beilstein J. Nanotechnol. 2013. V. 4. № 1. P. 732. https://doi.org/10.3762/bjnano.4.83
Powder diffraction Files Inorganic Phases. International Centre for Diffraction Data, Pennsylvania, USA, 2010
Ureña-Begara F., Crunteanu A., Raskin J.P. // Appl. Surf. Sci. 2017. V. 403. P. 717. https://doi.org/10.1016/j.apsusc.2017.01.160
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии