Почвоведение, 2021, № 4, стр. 420-428
Биохимические факторы формирования состава болотных вод и миграция веществ в системе геохимически сопряженных ландшафтов олиготрофных болот
Л. И. Инишева a, *, Н. В. Юдина b, А. В. Головченко c, А. В. Савельева b
a Томский государственный педагогический университет
634061 Томск, ул. Киевская, 60, Россия
b Институт химии нефти СО РАН
634021 Томск, пр-т Академический, 4, Россия
c МГУ им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
* E-mail: inisheva@mail.ru
Поступила в редакцию 08.04.2020
После доработки 03.07.2020
Принята к публикации 27.10.2020
Аннотация
Болотные экосистемы на территории Западной Сибири играют средообразующую роль и обеспечивают экологическое равновесие в биосфере. Целью исследований было изучение химических и биологических процессов болотного почвообразования, его влияния на формирование состава болотных вод и их миграцию в поверхностные воды. Исследования проводили в южно-таежной зоне Западной Сибири на малом водосборе болотной р. Ключ на ландшафтном профиле (катене) в пределах сопряженных ландшафтов олиготрофных болот. В автономной, транзитной и аккумулятивной позициях ландшафтного профиля изучали химические и микробиологические свойства торфов, определяли их влияние на формирование химического состава болотных вод в каждой позиции катены. Получено, что преимущественное развитие определенных растительных ассоциаций (сфагновых мхов фускум, магелланикум, а также пушицы и осоки) обусловливает накопление органических веществ, существенно различающихся по химическому составу. По торфяному профилю выявлена биохимическая активность до подстилающей породы, которая существенно влияет на формирование химического состава болотных вод. Эти процессы образуют индивидуальные химические свойства болотных вод в каждой позиции ландшафтного профиля. Определены факторы формирования миграционного потока и вынос химических соединений с ландшафтного профиля. За период вегетации вынос макроэлементов со стоком составил Ca2+ до 4843 кг/км2, Feобщ до 51.7 и ${\text{SO}}_{4}^{{2 - }}$ до 1419.0 кг/км2; микроэлементов: Pb до 2.253 × 10–3 кг/км2, Cu до 10.037 × 10–3, Mn до 317.29 × 10–3, Zn до 41.191 × 10–3, Ni до 8.151 × 10–3, Тi до 29.651 × 10–3 кг/км2. Вынос органических соединений в пересчете на углерод достигал 583.2 кг/км2. Доказано влияние стока болотных вод (особенно органического компонента) на состав вод р. Ключ. Полученные результаты по химическому составу болотных вод в системе сопряженных ландшафтов олиготрофных болот и их миграция с заболоченного водосбора могут быть использованы при составлении прогноза геохимической ситуации в поверхностных водах заболоченных территорий.
ВВЕДЕНИЕ
Больший вклад в заболоченность вносит азиатская часть страны – 84%, на европейскую территорию России приходится только 16%. Это соотношение сохраняется как для болот (85 и 15%), так и для заболоченных (мелкооторфованных) земель (84 и 16%). Для большинства регионов страны характерно преобладание заболоченных земель над болотами. Исключение – север европейской территории России, Дальний Восток и Западная Сибирь, чей вклад в площадь заболоченных мелкооторфованных земель составляет 18% при 42% для болот [3]. Поэтому болотные экосистемы на территории Западной Сибири, занимая до 80% в отдельных частях ее территории, играют средообразующую роль и обеспечивают экологическое равновесие. Торф в болотах является одним из начальных звеньев в цепи превращения органического вещества (ОВ) в биосфере. Вернадский [2] впервые показал масштабность ОВ как гидрохимического фактора особой важности. В болотах Западной Сибири содержится более 1000 км3 болотной воды или 15 годовых стоков Иртыша и Оби. Поэтому изучение свойств болот, формирующихся под их влиянием болотных вод, активность миграционных процессов, характерных для малых заболоченных бассейнов, представляет интерес для составления прогноза геохимической ситуации в поверхностных водах Западной Сибири [23, 24, 26–28].
Цель работы – изучить активность химических и микробиологических процессов, протекающих в торфяном профиле, и их влияние на формирование состава болотных вод, а также определить условия миграция и вынос веществ с заболоченного водосбора в реки.
ОБЪЕКТЫ И МЕТОДЫ
Стационар “Васюганье” расположен в междуречье рек Бакчар–Икса, представляет северо-восточные отроги Васюганского болота. Согласно районированию болот [13], исследуемая территория входит в состав западносибирской таежной болотной области бореально-атлантических выпуклых олиготрофных моховых болот активного заболачивания и интенсивного торфонакопления и относится к южно-таежной провинции западносибирских олиготрофных сосново-кустарничково-сфагновых и грядово-мочажинных мезотрофных и эвтрофных сосново-березово-осоково-гипновых и осоково-гипновых болот.
Исследования проводили в пределах малого заболоченного водосбора р. Ключ на геохимически сопряженных ландшафтах олиготрофных болот. Истоки реки расположены на периферии верхового болотного массива. Длина без русловых склонов по линиям стекания от р. Ключ до истоков водораздела достигает 2.5–6.0 км, площадь водосбора 58 км2. На территории массива верхового болота параллельно линиям стекания был заложен ландшафтный профиль, протяженностью 800 м, который закреплен реперами и обоснован в плановом отношении, выполнена нивелировка поверхности. В геологическом развитии болотный массив образовался при зарастании мелководного озера.
Ландшафтный профиль представляет часть склона водораздельного массива, по которому осуществляется сброс избыточных поверхностных и болотных вод, начиная с автономной позиции (биогеоценоз (БГЦ) – осоковая топь). Далее следует транзитная позиция ландшафтного профиля (БГЦ – сосново-кустарничково-сфагновый с низкой сосной), по которой воды мигрируют в аккумулятивную позицию (БГЦ – сосново-кустарничково-сфагновый с высокой сосной), выполняющую роль геохимического барьера. На первых двух позициях мощность торфяного профиля достигает 3 м, в аккумулятивной – 1 м. Подстилающие породы – глины с содержанием раковин пресноводных моллюсков.
Верхний слой (1 м) торфяного профиля автономной позиции сложен верховым фускум и сфагновым мочажинным торфами. Затем следует 0.4-метровый слой переходного торфа; в основании профиля находится 1.6-метровый пласт низинного торфа: осокового, травяного и папоротникового. В торфяном профиле транзитной позиции с поверхности залегает фускум и магелланикум торф мощностью 1.5 м; далее располагается слой торфа переходного типа мощностью 0.4 м, который сменяется слоем осокового низинного торфа; в основании лежит слой папоротникового торфа. Верхний слой торфяного профиля аккумулятивной позиции представлен сосново-пушицевым торфом мощностью 30 см, затем идут переходные виды торфов (древесно-сфагновый и древесно-травяной). В основании профиля лежит слой низинного осокового торфа. Подробное описание пунктов исследования и их физико-химические характеристики приведены в работе Инишевой с соавт. [9].
На ландшафтном профиле р. Ключ проводили наблюдения за стоком на оборудованном гидрометрическом посту, изучали уровень болотных вод (УБВ) каждую декаду месяца [15]. Групповой химический состав ОВ торфов определяли по методу Инсторфа [20], болотных и речных вод – из сухих осадков, трижды обрабатывая их 0.1 н. раствором NаОН при температуре 80°С с последующим выделением гуминовых (ГК) и фульвокислот (ФК).
Регистрацию ИК-спектров ФК проводили на ИК-фурье спектрометре Nikolet 5700 c Raman модулем (корпорация Thermo Electron, США) в таблетках с KBr при соотношении 1 : 300 соответственно в области длин волн от 400 до 4000 см–1 c компенсацией сигналов адсорбированной воды. Обработку спектров и определение оптической плотности вели с помощью программного обеспечения Omnic 7.2 Thermo Nicolet Corporation. Для количественной оценки интенсивности полос поглощения применяли метод базовых линий и относительных оптических плотностей [11]. Содержание железа в ГК определяли методом рентгенофлюоресцентного анализа.
Микробную биомассу определяли методом прямого счета с использованием люминесцентной микроскопии. При количественном учете клеток бактерий и актиномицетного мицелия препараты окрашивали водным раствором акридина оранжевого, для окраски мицелия и спор грибов применяли калькофлуор белый. Использовали формулы для расчета биомассы [4, 14].
Болотную воду на анализ отбирали в колодцах каждой позиции ландшафтного профиля, а также в р. Ключ при выходе с болота и при впадении в р. Бакчар. Макрокомпоненты в водах анализировали по общепринятым методикам [21], гуминовые и фульвокислоты – по [20].
Все лабораторные исследования проводили в Испытательной лаборатории (№ РОСС RU.0001.516054). Статистическую обработку результатов анализа осуществляли в пакете Miсrosoft Office.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Рассмотрим общетехническую характеристику и химический состав ОВ торфов, слагающих торфяные залежи ландшафтного профиля (табл. 1). Степень разложения возрастает с глубиной залегания при переходе от верхового типа залежи к переходному и далее к низинному типу. В этом направлении плавно изменяется величина рН от кислой до слабокислой реакции. Ботаническая принадлежность торфов оказывает существенное влияние на состав ОВ. Преимущественное развитие определенных растительных ассоциаций – сфагновых мхов (фускум, магелланикум, пушицы и осоки) обусловливает накопление ОВ, существенно различающихся по химическому составу. Так, анализ состава ОВ верхних и нижних слоев торфяных профилей выявил различие по содержанию легко- и трудногидролизуемых веществ. В транзитной и аккумулятивной части ландшафтного профиля отмечается более высокое содержание легкогидролизуемых веществ в зоне разгрузки вод, которая служит геохимическим барьером на ландшафтном профиле. Перераспределение водорастворимых соединений в торфах наблюдается по всему профилю (0.1–1.65 мас. %) с наибольшим содержанием в аккумулятивной позиции (1.2–1.6 мас. %), что подтверждает наличие процесса латерального сноса веществ.
Таблица 1.
Характеристика органического вещества торфов ландшафтного профиля
| Глубина, см |
Вид, тип торфа | Степень разложения, % | Зольность, % | рНKCl | Содержание, мас. % | Спектральные коэффициенты ГК | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| ВР | ЛГ | ТГ | ГК | $\frac{{{{D}_{{1610}}}}}{{{{D}_{{1460}}}}}$ | $\frac{{{{D}_{{1720}}}}}{{{{D}_{{1460}}}}}$ | $\frac{{{{D}_{{1270}}}}}{{{{D}_{{1460}}}}}$ | |||||
| Автономная позиция | |||||||||||
| 0–50 | Сфагново-мочажинный, В | 10 | 10.9 | 2.9 | 0.3 | 33.4 | 10.5 | 30.5 | 1.50 | 1.56 | 1.32 |
| 50–100 | Сфагново-мочажинный, В | 20 | 6.0 | 3.4 | 0.4 | 29.5 | 9.7 | 33.0 | 1.32 | 1.28 | 1.32 |
| 100–150 | Осоково-сфагновый, П | 35 | 4.7 | 3.9 | 0.2 | 42.5 | 14.1 | 28.0 | 1.31 | 1.28 | 1.34 |
| 150–200 | Осоковый, П | 50 | 4.8 | 4.2 | 0.1 | 31.5 | 15.0 | 29.2 | 1.32 | 1.30 | 1.34 |
| 200–250 | Травяной, Н | 50 | 5.8 | 4.5 | 0.1 | 14.8 | 10.2 | 46.6 | 1.47 | 1.53 | 1.23 |
| 250–270 | Папоротниковый, Н | 50 | 24.5 | 4.5 | 0.2 | 15.4 | 10.5 | 45.9 | 1.31 | 1.44 | 1.37 |
| Транзитная позиция | |||||||||||
| 0–50 | Фускум, В | 5 | 2.7 | 2.6 | 0.9 | 30.6 | 15.2 | 25.1 | 1.53 | 1.74 | 1.31 |
| 50–75 | Фускум, В | 5 | 2.0 | 2.5 | 1.2 | 16.6 | 16.4 | 25.2 | 1.48 | 1.64 | 1.32 |
| 75–100 | Медиум, В | 5 | 2.1 | 2.6 | 0.4 | 32.6 | 14.3 | 19.8 | 1.41 | 1.64 | 1.36 |
| 100–150 | Медиум, В | 10 | 2.3 | 3.0 | 0.4 | 33.5 | 10.3 | 19.0 | 1.39 | 1.58 | 1.37 |
| 150–200 | Сосново-пушицевый, В | 50 | 6.0 | 5.0 | 0.3 | 23.6 | 13.8 | 37.1 | 1.42 | 1.42 | 1.35 |
| 200–250 | Осоковый, Н | 50 | 4.3 | 4.2 | 0.3 | 16.3 | 17.2 | 25.2 | 1.41 | 1.41 | 1.36 |
| 250–300 | Травяной, Н | 45 | 24.5 | 4.4 | 0.1 | 38.6 | 16.0 | 21.2 | – | – | – |
| Аккумулятивная позиция | |||||||||||
| 0–25 | Сосново-пушицевый, В | 45 | 5.2 | 3.6 | 1.6 | 22.4 | 4.2 | 27.6 | 1.45 | 1.63 | 1.37 |
| 25–50 | Древесно-пушицевый, П | 45 | 6.5 | 4.5 | 1.6 | 28.3 | 8.1 | 22.7 | 150 | 1.60 | 1.45 |
| 50–75 | Древесно-пушицевый, П | 55 | 8.0 | 5.0 | 1.2 | 36.6 | 9.2 | 23.0 | 1.48 | 1.48 | 1.33 |
| 75–100 | Древесно-пушицевый, П | 60 | 9.8 | 5.1 | 0.4 | 32.7 | 11.0 | 39.8 | 1.49 | 1.48 | 1.27 |
Состав ГК на разных позициях ландшафтного профиля определяется генезисом формирования торфяного профиля. Оценить структурно-групповой состав ГК позволяют спектральные коэффициенты, соответствующие определенным группам и фрагментам в периферической и ядерной части макромолекулы. В торфах аккумулятивной позиции повышается ароматичность макромолекул ГК (D1610/D1460). Максимальное содержание карбоксильных групп (D1720/D1460) отмечено в ГК сфагновых торфов транзитной части. Фенольные гидроксилы представлены в ГК торфов в равной степени по всему ландшафтному профилю. Высокая обменная емкость ГК обеспечивает образование прочных комплексных соединений с ионами металлов [12]. Например, содержание железа в ГК автономной позиции составляет 0.10–0.25%, в то время как в аккумулятивной позиции достигает 1.25%, что подтверждает их миграцию в ландшафтном профиле к аккумулятивной его позиции.
Важным условием формирования химического состава болотных вод является активность микробиологического сообщества в каждом торфяном профиле геохимически сопряженных ландшафтов олиготрофных болот. Одним из показателей активности микроорганизмов является их биомасса. Суммарная микробная биомасса в торфяном профиле транзитной позиции варьирует от 0.5 до 6 мг/г торфа, в профиле аккумулятивной позиции – от 1.6 до 22.7 мг/г, что в 3 раза выше, чем биомасса в профиле транзитной позиции (табл. 2). Это подтверждает более благоприятные условия для активности микроорганизмов в зоне разгрузки мигрирующих вод. В каждой позиции ландшафтного профиля также образуется индивидуальный микробиологический профиль в соответствии с ботаническим составом. В целом наблюдается убывание микробной биомассы вниз по профилю. Однако в торфяном профиле транзитной позиции убывание начинается с глубины 1 м при смене верхового типа на переходный. В верхнем метровом слое олиготрофного генезиса микробная биомасса поддерживается на уровне 5–6 мг/г торфа.
Таблица 2.
Экстремальные и средние показатели микробной биомассы в торфяном профиле транзитной и аккумулятивной позициях ландшафтного профиля
| Глубина, см |
Биомасса, мг/г | ||||
|---|---|---|---|---|---|
| бактерии | актиномицетный мицелий | грибной мицелий | споры грибов | суммарная биомасса | |
| Транзитная позиция | |||||
| 0–50 | $\frac{{0.7{\kern 1pt} --{\kern 1pt} 1.1}}{{0.9 \pm 0.2}}$ | $\frac{{0.03{\kern 1pt} --{\kern 1pt} 0.05}}{{0.04}}$ | $\frac{{0.7{\kern 1pt} --{\kern 1pt} 3.1}}{{2.0}}$ | $\frac{{0.9{\kern 1pt} --{\kern 1pt} 4.7}}{{3.0 \pm 0.3}}$ | $\frac{{2.3{\kern 1pt} --{\kern 1pt} 8.7}}{{6.0}}$ |
| 50–75 | $\frac{{0.6{\kern 1pt} --{\kern 1pt} 0.7}}{{0.7 \pm 0.1}}$ | $\frac{{0.02{\kern 1pt} --{\kern 1pt} 0.0}}{{70.04}}$ | $\frac{{0.8{\kern 1pt} --{\kern 1pt} 2.7}}{{1.4}}$ | $\frac{{0.9{\kern 1pt} --{\kern 1pt} 5.6}}{{2.8 \pm 0.3}}$ | $\frac{{2.5{\kern 1pt} --{\kern 1pt} 9.0}}{{5.0}}$ |
| 75–100 | $\frac{{0.3{\kern 1pt} --{\kern 1pt} 0.5}}{{0.7 \pm 0.2}}$ | $\frac{{0.01{\kern 1pt} --{\kern 1pt} 0.03}}{{0.02}}$ | $\frac{{0{\kern 1pt} --{\kern 1pt} 5.6}}{{1.9}}$ | $\frac{{1.0{\kern 1pt} --{\kern 1pt} 5.2}}{{2.8 \pm 0.4}}$ | $\frac{{2.7{\kern 1pt} --{\kern 1pt} 7.8}}{{5.4}}$ |
| 100–150 | $\frac{{0.1{\kern 1pt} --{\kern 1pt} 0.4}}{{0.3 \pm 0.03}}$ | $\frac{{0.00{\kern 1pt} --{\kern 1pt} 0.01}}{{0.01}}$ | 0 | $\frac{{0.5{\kern 1pt} --{\kern 1pt} 1.9}}{{1.0 \pm 0.2}}$ | $\frac{{0.7{\kern 1pt} --{\kern 1pt} 2.3}}{{1.3}}$ |
| 150–200 | $\frac{{0.1{\kern 1pt} --{\kern 1pt} 0.2}}{{0.1 \pm 0.03}}$ | $\frac{{0.00{\kern 1pt} --{\kern 1pt} 0.01}}{{0.01}}$ | 0 | $\frac{{0.1{\kern 1pt} --{\kern 1pt} 0.6}}{{0.4 \pm 0.1}}$ | $\frac{{0.3{\kern 1pt} --{\kern 1pt} 0.8}}{{0.5}}$ |
| 200–300 | $\frac{{0.1{\kern 1pt} --{\kern 1pt} 0.2}}{{0.2 \pm 0.03}}$ | $\frac{{0.00{\kern 1pt} --{\kern 1pt} 0.01}}{{0.01}}$ | 0 | $\frac{{0.2{\kern 1pt} --{\kern 1pt} 1.0}}{{0.5 \pm 0.2}}$ | $\frac{{0.3{\kern 1pt} --{\kern 1pt} 1.1}}{{0.7}}$ |
| Аккумулятивная позиция | |||||
| 0–25 | $\frac{{1.4{\kern 1pt} --{\kern 1pt} 2.8}}{{2.1 \pm 0.3}}$ | $\frac{{0.01{\kern 1pt} --{\kern 1pt} 0.07}}{{0.05}}$ | $\frac{{9.9{\kern 1pt} --{\kern 1pt} 27.1}}{{19.7}}$ | $\frac{{0.9{\kern 1pt} --{\kern 1pt} 1.1}}{{0.9 \pm 0.1}}$ | $\frac{{13.8{\kern 1pt} --{\kern 1pt} 30.0}}{{22.7}}$ |
| 25–50 | $\frac{{0.7{\kern 1pt} --{\kern 1pt} 1.3}}{{1.0 \pm 0.1}}$ | $\frac{{0.01{\kern 1pt} --{\kern 1pt} 0.02}}{{0.01}}$ | $\frac{{1.3{\kern 1pt} --{\kern 1pt} 14.7}}{{6.3}}$ | $\frac{{0.3{\kern 1pt} --{\kern 1pt} 1.1}}{{0.9 \pm 0.1}}$ | $\frac{{2.5{\kern 1pt} --{\kern 1pt} 17.1}}{{8.2}}$ |
| 50–75 | $\frac{{0.4{\kern 1pt} --{\kern 1pt} 1.4}}{{0.8 \pm 0.1}}$ | $\frac{{0.00{\kern 1pt} --{\kern 1pt} 0.02}}{{0.01}}$ | $\frac{{1.4{\kern 1pt} --{\kern 1pt} 9.9}}{{4.9}}$ | $\frac{{1.3{\kern 1pt} --{\kern 1pt} 3.8}}{{2.3 \pm 0.3}}$ | $\frac{{3.3{\kern 1pt} --{\kern 1pt} 13.0}}{{8.0}}$ |
| 75–100 | $\frac{{0.3{\kern 1pt} --{\kern 1pt} 0.4}}{{0.3 \pm 0.03}}$ | $\frac{{0.00{\kern 1pt} --{\kern 1pt} 0.02}}{{0.01}}$ | $\frac{{0{\kern 1pt} --{\kern 1pt} 0.3}}{{0.2}}$ | $\frac{{0.7{\kern 1pt} --{\kern 1pt} 1.9}}{{1.1 \pm 0.3}}$ | $\frac{{1.2{\kern 1pt} --{\kern 1pt} 2.4}}{{1.6}}$ |
Аналогичная закономерность прослеживалась и в динамике грибного комплекса. Так, отмечается приуроченность грибного мицелия к верхним слоям и уменьшение в глубоких слоях жизнеспособной грибной биомассы, что обусловлено не только отсутствием у многих из грибов альтернативных путей получения энергии, но и накоплением жирных кислот, этанола, восстановленных соединений серы и железа в токсичных концентрациях. По всему торфяному профилю были выявлены споры грибов. Их биомасса варьировала от 0.1 до 4.7 мг/г. Известно, что жизнеспособность грибных спор может уменьшаться вниз по профилю верховых болот. Тем не менее, в глубоких слоях торфяного профиля обнаружены споры, способные к прорастанию. Их доля варьирует от 10 до 40%. Также изменялась в торфяном профиле биомасса бактерий от 0.1 до 2.8 мг/г и биомасса актиномицетного мицелия – от 0 до 0.07 мг/г. Очевидно, что в глубоких слоях возрастает роль прокариотных организмов, функции которых многогранны. Исследователи объясняют разными причинами активность микроорганизмов в глубоких слоях, в том числе проникновением в глубину торфяного профиля вод, насыщенных кислородом [5, 6]. Известно, что в условиях затопления в торфяном профиле в процессе торфогенеза происходит образование макро- и микроструктур с включениями кислорода. Учитывая активность биохимических процессов, содержание подвижного ОВ, структурно-групповой состав ГК в торфах ландшафтного профиля, можно предположить, что химический состав стока с заболоченного водосбора будет формироваться не только за счет атмосферных осадков, как это полагают некоторые исследователи [7, 22], но и за счет биохимических и микробиологических процессов, протекающих непосредственно в торфяном профиле [8, 10].
Рассмотрим состав болотных вод на ландшафтном профиле заболоченного водосбора р. Ключ за разные годы. Исследования проводили в 1995–2013 гг. Из них 8 лет относятся по гидротермическому коэффициенту (ГТК) к среднемноголетним (около 1.5 ГТК), 6 лет – к средне засушливым (ГТК 0.8–1.1), 3 года к средне влажным (ГТК 1.7–2.4) и 1 год – сухой (ГТК 0.3). Репрезентативность этого показателя обоснована в работах Будыко [1]. В табл. 3 приведены экстремальные значения отдельных элементов, сгруппированные по годам с разными показателями ГТК.
Таблица 3.
Экстремальные значения компонентов в болотных и речных водах за теплый период в разные по погодным условиям годы, мг/л
| Позиция, река | рН | Cа2+ | Mg2+ | ${\text{NH}}_{4}^{ + }$ | Feобщ | ${\text{NO}}_{3}^{ - }$ | ГК | ФК |
|---|---|---|---|---|---|---|---|---|
| Среднемноголетние годы по ГТК | ||||||||
| Автономная | 3.6–4.4 | 1.0–6.0 | 0.2–2.9 | 0.2–2.7 | 0.1–3.8 | 0.2–1.3 | 3.4–10.7 | 41.8–74.8 |
| Транзитная | 3.4–4.3 | 0.8–7.5 | 0.5–4.4 | 0.2–3.8 | 0.1–3.8 | 0.2–2.5 | 5.4–13.1 | 40.7–88.4 |
| Аккумулятивная | 3.4–4.7 | 3.0–11.2 | 1.0–9.6 | 0.3–4.1 | 0.2–7.2 | 0.2–6.0 | 2.4–19.6 | 44.4–92.8 |
| Ключ | 5.8–7.1 | 8.0–34.1 | 4.1–15.2 | 0.1–3.9 | 0.1–5.9 | 0–2.1 | 1.7–14.0 | 41.0–100.3 |
| Бакчар | 7.1–7.8 | 1.2–62.8 | 4.1–18.8 | 0.1–3.8 | 0.4–4.9 | 0.3–0.9 | 0.2–14.0 | 20 .0–79.0 |
| Условно засушливые годы по ГТК | ||||||||
| Автономная | 3.7–4.3 | 0.4–5.7 | 0.2–2.1 | 0.2–0.8 | 0–0.3 | 0–1.7 | 2.0–18.2 | 20.5–81.4 |
| Транзитная | 3.6–5.5 | 0.4–8.7 | 0.6–3.7 | 0.3–1.1 | 0.1–6.7 | 0.1–2.7 | 4.1–11.2 | 35.2–66.9 |
| Аккумулятивная | 4.5–6.2 | 1.1–9.8 | 1.2–2.9 | 0.3–1.3 | 0.2–0.7 | 0.2–2.0 | 2.6–18.2 | 35.9–95.5 |
| Ключ | 6.5–7.4 | 3.2–46.5 | 2.4–10.7 | 0.1–8.4 | 0.1–6.4 | 0.1–1.6 | 2.6–14.1 | 12.1–86.9 |
| Бакчар | 7.1–7.9 | 5.1–101.0 | 5.7–16.7 | 0–0.5 | 0–0.3 | 0.1–1.1 | 1.2–15.8 | 20.0–64.0 |
| Влажные годы по ГТК | ||||||||
| Автономная | 3.9–4.4 | 0.1–5.3 | 0.2–6.2 | 0.2–0.6 | 0.1–1.2 | 0.1–1.3 | 1.7–12.9 | 31.2–88.4 |
| Транзитная | 3.6–4.9 | 0.1–4.1 | 0.3–11.8 | 0.3–0.8 | 0.2–0.4 | 0.2–2.4 | 4.6–11.7 | 22.7–80.5 |
| Аккумулятивная | 4.3–5.6 | 0.9–7.0 | 0.9–11.1 | 0.4–0.9 | 0–0.8 | 0.1–1.1 | 4.6–11.3 | 24.1–95.0 |
| Ключ | 6.3–7.1 | 3.0–30.0 | 0.8–12.8 | 0.2–5.9 | 0.2–9.2 | 0.1–2.0 | 1.7–14.6 | 37.4–112.0 |
В автономной позиции ландшафтного профиля весенний мигрирующий поток представляет собой талые снежные воды, перемешанные с болотными водами оттаявшего слоя. Именно с этой части болота начинается миграция в сторону аккумулятивной позиции и далее в реки Ключ и Бакчар. Реакция среды в болотных водах по минимальным значениям во все годы относилась к градации кислых вод, по максимальным значениям также к кислым, но в болотных водах транзитной и аккумулятивной позиций реакция среды становилась слабокислой. В р. Ключ значения рН изменялись в пределах 5.8–7.4, Бакчар – 7.1–7.9.
Экстремальные значения содержания ионов кальция в болотных водах постепенно увеличивались по ландшафтному профилю к его аккумулятивной позиции. Ионов кальция в соответствии с рН больше содержалось в реках. Та же закономерность была характерна для магния. Но если в болотных водах содержание ионов Са2+ и Mg2+ было близко между собой, то в речных водах преобладали ионы Са2+. Во влажные годы проявилась тенденция уменьшения содержания ионов Са2+, но она компенсировалась увеличением количества ионов Mg2+, содержание которых во влажные годы в торфяных профилях было больше по всем позициям ландшафтного профиля. Отчасти это объясняется биогенной формой миграции элементов от почвообразующих пород, содержащих раковины пресноводных моллюсков. Это обстоятельство привело к формированию залежей, частично обогащенных минеральными соединениями, в том числе ионами кальция и магния. В результате образовался мезотрофный тип болот. Таким образом, петрографический состав пород водосбора оказывает влияние на вещественный состав мигрирующих болотных вод.
В течение теплого периода доля участия болотных вод в формировании стока увеличивалась, изменялся и гидрохимический состав мигрирующих вод. В отдельные периоды болотные воды имели повышенное содержание аммония, нитратов и общего железа, но по значениям они были ниже, чем в р. Ключ. Можно предположить, что увеличение их содержания в р. Ключ происходило за счет частичного стока с сельскохозяйственной территории, по которой протекает р. Ключ до впадения в р. Бакчар. Но при сравнении с предельно допустимыми концентрациями питьевых и рыбохозяйственных вод болотная и речная воды по данным компонентам характеризуются как чистые [16, 17].
Какова ситуация в болотных водах с ОВ? Известно, что в верховых болотах, характеризующихся низким значением рН, нарушаются некоторые геохимические закономерности, так как в силу вступают индивидуальные свойства торфов, связанные с особенностями состава их ОВ [19]. Содержание ГК в болотных водах автономной позиции ландшафтного профиля изменялось от 1.7 до 18.2 мг/л, транзитной – от 4.1 до 13.1 мг/л и аккумулятивной – от 2.4 до 19.6 мг/л. Значения ГК в р. Ключ колебались от 1.7 до 14.1 мг/л, в р. Бакчар от 0.2 до 15.8 мг/л. Фульвокислот в болотных водах было значительно больше, чем ГК, их содержание по всему ландшафтному профилю варьировало от 20.5 до 95.5 мг/л, в р. Ключ − от 12.1 до 112 мг/л и в р. Бакчар − от 20.0 до 79.0 мг/л. Практически близкие значения ГК и ФК в болотных водах и в р. Ключ свидетельствуют о болотном происхождении ее вод. В р. Бакчар, имеющей большой объем воды, отмечается уменьшение содержания этих показателей.
Важная роль в формировании химического состава болотных вод принадлежит ФК, содержание которых значительно больше ГК, что отмечается и другими исследователями [18, 25]. Превышение содержания ФК в исследуемых болотных водах составляло 5–20 раз, чаще до 10, что вполне соответствует содержанию ГК и ФК в торфах, слагающих ландшафтный профиль.
Исследование в торфах и осадках болотных вод ландшафтного профиля ИК-спектров ГК и их спектральных коэффициентов, позволило выявить структуру мигрирующих ОВ. Как правило, количество гидроксильных, фенольных гидроксилов, карбоксильных групп и ароматических фрагментов повышается в молекулах водорастворимых веществ в августе, сентябре, что объясняется повышением микробиологической активности прогретого до 15°С метрового слоя торфяного профиля и активным взаимодействием биохимических процессов в системе торфяная залежь–болотные воды. В болотной воде автономной позиции соотношение оптических плотностей гидроксильных групп D3400/D1460 колебалось от 0.89 до 1.49, фенольных гидроксилов D1270/D1460 – 0.78–0.86, карбоксильных групп D1720/D1460 – 1.16–1.28 и ароматических фрагментов D1620/D1460 – 1.20–1.85. В водорастворимых веществах транзитной и аккумулятивной позиции повышалась доля фенольных гидроксилов D1270/D1460 до 0.96 и карбоксильных групп D1720/D1460 – 1.73 по сравнению с автономной позицией. Водорастворимые вещества р. Ключ по свойствам аналогичны болотным водам аккумулятивной позиции. Для водорастворимых веществ р. Бакчар характерно незначительное содержание перечисленных функциональных групп, вследствие разбавления поверхностными водами, стекающими с водосборной территории иной гидрохимической ситуации.
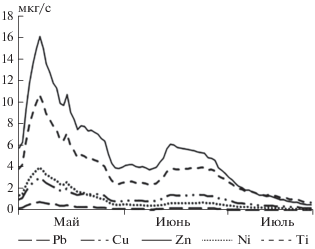
Выше отмечалось, что миграционный поток на заболоченном водоразделе наблюдался в основном в весенний период при снеготаянии. Объем стока в средних значениях за этот период был равен 70 мм, что составляло 92% от годового стока (96 мм). Величина стока в летнюю межень измерялась величиной 7.7 мм или 8% от годового стока. Проведенные расчеты показывают, что вынос углерода в форме гуминовых веществ (29 кг/км2 в год или 29 мг/м2) достигает в отдельные периоды 98% от общего выноса углерода с ландшафтного профиля, при этом наибольшая доля принадлежит углероду ФК (рис. 1). Гуминовые вещества обеспечивают вынос ионов металлов. Так, за весенний период вынос элементов со стоком составил: Pb – 2.253 × × 10–3 кг/км2, Cu – 10.037 × 10–3, Mn – 317.29 × 10–3, Zn – 41.191 × 10–3, Ni – 8.151 × 10–3, Тi – 29.651 × × 10–3 кг/км2 (рис. 2). Близкие результаты, например по Pb, получены и другими исследователями [29].
Таким образом, динамика выноса элементов с заболоченных водосборов определяется преимущественно ходом стока воды и содержанием вновь образованных водорастворимых веществ в торфах ландшафтного профиля. Подтверждением этого являлась синхронность распределения ежедневных расходов воды и содержания в ней некоторых химических элементов.
Вынос подвижных макроэлементов рассмотрим в годы с объемом стока 158 и 72 мм. Общий объем выноса химических элементов с квадратного километра соответственно по годам составил 31 200 и 12 070 кг, в том числе Ca2+ 4843 и 997 кг, Feобщ 51.7 и 22.6 кг; ${\text{SO}}_{4}^{{2 - }}$ 1419.0 и 1177.0 кг. Вынос органических соединений в пересчете на углерод был соответственно равен 478.0 и 583.2 кг/км2. Таким образом, вынос элементов определяется не только объемом стока (то есть метеоусловиями), но и уровнем болотных вод, микробиологическими и биохимическими процессами в торфяных залежах.
Проведенные исследования показали, что роль болот в литогенезе как фактора химической дифференциации элементов на путях от областей сноса до аккумулятивных позиций очевидна.
ЗАКЛЮЧЕНИЕ
Образование и развитие болот имеет ряд особенностей, которые отличают их от других природных экосистем. Торфяной профиль формируется преимущественно в условиях субаквальной консервации растений-торфообразователей и полностью является органогенным. В результате взаимодействия растений-торфообразователей и микробного сообщества происходят процессы трансформации ОВ в торфяном профиле. Отмечено, что эти процессы отражают особенности позиционной принадлежности в системе геохимически сопряженных ландшафтов олиготрофных болот и формируют особый состав болотных вод.
Доказано, что химический состав миграционного потока с заболоченного водосбора формируется не только за счет атмосферных осадков и грунтовых вод, но и за счет их участия в болотном генезисе. Важную роль при этом имеет площадь водосбора и объем стока за период вегетации.
Повышенное содержание отдельных компонентов в составе болотных вод сопряженных ландшафтов олиготрофных болот соответствует мезотрофному типу болотного генезиса, вследствие наличия карбонатов в почвообразующих породах исследуемой территории.
Сопоставление многолетних данных по гидрохимическому режиму болот разного генезиса с водами рек выявило особенности сезонной и пространственной изменчивости химического состава болотных вод и влияние их стока (в особенности органического компонента) на состав вод рек Ключ и Бакчар.
За период вегетации вынос макроэлементов со стоком составил Ca2+ до 4843 кг/км2, Feобщ до 51.7; ${\text{SO}}_{4}^{{2 - }}$ до 1419.0 кг/км2; микроэлементов: Pb до 2.253 × 10–3 кг/км2, Cu до 10.037 × 10–3, Mn до 317.29 × 10–3, Zn до 41.191 × 10–3, Ni до 8.151 × 10–3, Тi до 29.651 × 10–3 кг/км2. Вынос органических соединений в пересчете на углерод достигал значения 583.2 кг/км2. Полученные результаты по содержанию элементов в разных по генезису болотных водах могут быть использованы в последующем для прогноза геохимической ситуации на гумидных территориях.
Список литературы
Будыко М.И. Изменения климата. Л.: Гидрометеоиздат, 1974. 280 с.
Вернадский В.И. Биосфера. Избр. соч. М.: АН СССР, 1960. Т. 5. С. 7–102.
Вомперский С.Э., Сирин А.А., Сальников А.А., Цыганова О.П., Валяева Н.А. Оценка площади болотных и заболоченных лесов России // Лесоведение. 2011. № 5. С. 3–11.
Головченко А.В., Добровольская Т.Г., Звягинцев Д.Г. Микробиологические основы оценки торфяника как профильного почвенного тела // Вестник ТГПУ. 2008. Вып. 4(78). С. 46–53.
Добровольская Т.Г., Головченко А.В., Якушев А.В., Юрченко Е.Н., Манучарова Н.А., Чернов И.Ю. Бактериальные комплексы верхового торфяника в условиях различного микрорельефа // Почвоведение. 2017. № 4. С. 483–489.
Дырин В.А., Красноженов Е.П. Активность микрофлоры в целинной и рекультивируемой торфяно-болотных почвах // Вестник ТГПУ. 2007. Вып. 6. С. 33–38.
Ефремова Т.Т., Ефремов С.П., Мелентьева Н.В. Водные ресурсы болот России и оценка их химического состава // География и природных ресурсов. 1998. № 2. С. 79–84.
Ефремова Т.Т., Ефремов С.П., Калачева Г.С. Органические микропримеси, экстрагируемые хлороформом из болотных и речных вод бассейна Средней Оби // Водные ресурсы. 2018. Т. 45. № 5. С. 526–536.
Инишева Л.И., Виноградов В.Ю., Голубина О.А., Ларина Г.В. Порохина Е.В., Шинкеева Н.А., Шурова М.В. Болотные стационары Томского государственного педагогического университета. Томск: Изд-во ТПУ, 2010. 118 с.
Калюжный И.Л. Гидрохимический режим и химический состав вод мезоолиготрофных болотных массивов Кольского полуострова // Вестник Кольского научного центра РАН. 2016. № 3. С. 114–125.
Камнева А.И., Бакирова Е.В., Паволоцкая З.В. О связи с гуминовыми кислотами в бурых углях Бородинского месторождения // Химия твердого топлива. 1972. № 3. С. 33–36.
Кононова М.М. Органическое вещество почвы. Его природа, свойства и методы изучения. М.: Изд-во АН СССР, 1963. 314 с.
Лисс О.Л., Абрамова Л.И., Аветов Н.А., Березина Н.А., Инишева Л.И., Курнишкова Т.В., Слука З.А., Толпышева Т.Ю., Шведчикова Н.К. Болотные системы Западной Сибири и их природоохранное значение. Тула: Гриф и К°, 2001. 584 с.
Методы почвенной микробиологии и биохимии / Под ред. Звягинцева Д.Г. М.: Изд-во Моск. ун-та, 1991. 303 с.
Наставления гидрометеорологическим станциям и постам. Л.: Гидрометеоиздат, 1978. Вып. 6. 384 с.
Об утверждении нормативов качества воды водных объектов рыбохозяйственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйственного значения. 2016. https://minjust. consultant.ru/ documents/22231
Обобщенный перечень предельно допустимых концентраций (ПДК) и ориентировочно безопасных уровней воздействия (ОБУВ) вредных веществ для воды рыбохозяйственных водоемов. М.: Минрыбхоз СССР, 1990. 265 с.
Рассказов Н.М. Основные особенности химического состава болотных вод (на примере юго-восточной части Западной Сибири) // Известия Томского политех. ун-та. 2005. Т. 308. № 4. С. 55–58.
Савичев О.Г. Геохимические показатели болотных вод в таежной зоне Западной Сибири // Известия РАН. Сер. географическая. 2015. № 4. С. 47–57.
Технический анализ торфа. М.: Недра, 1992. 358 с.
Унифицированные методы исследования качества вод. М.: СЭВ, 1983. Т. 2. Ч. 1. 195 с.
Федорова Е.В., Суслова С.М., Ярушина Н.Б. Вынос химических веществ стоком половодья с “условно фоновых” водосборов Уральского региона // Водное хозяйство России. 2000. Т. 2. С. 159–171.
Goldhaber M.B., Mills C.T., Morrison J.M., Stricker C.A., Mushet D.M., La Baugh J.W. Hydrogeochemistry of prairie pothole region wetlands: Role of long-term critical zone processes // Chem. Geol. 2014. V. 387. P. 170–183.
Guo L., Cai Y., Belzile C., Macdonald R. Sources and export fluxes of inorganic and organic carbon and nutrient species from the seasonally ice-covered Yukon River // Biogeochemistry. 2012. V. 107. № 1–3. P. 187–206.
Haiber S., Herzog H., Burba P., Gosciniak J., Lambert V. Quantification of carbohydrate structures in size fractionated aquatic humic substances by two-dimensional nuclear magnetic resonance // Fresenius J. Anal. Chem. 2001. V. 369. P. 457–460.
Holmes R.M., McClelland J.W., Peterson B.J., Tank S.E., Bulygina E., Eglinton T.I., Gordeev V.V., Gurtovaya T.Y., Raymond P.A., Repeta D.J., Staples R., Striegl R.G., Zhulidov A.V., Zimov S.A. Seasonal and annual fluxes of nutrients and organic matter from large rivers to the Arctic Ocean and surrounding seas // Estuaries Coasts. 2012. № 35. P. 369–382. /https://doi.org/10.1007/s12237-011-9386-6
Magritsky D.V. Annual suspended matter flow of the Russian rivers belonging to the Arctic Ocean basin and its anthropogenic transformation // Vestnik Moscow State Univer. Ser. Geogr. 2010. V. 5(6). P. 17–24.
Moiseenko T.I., Skjelkvale B.L., Gashkina N.A., Shalabodoc A.D., Khoroshavin V.Yu. Water chemistry in small lakes along a transect from boreal to arid ecoregions in European Russia: effects of air pollution and climate change // Appl. Geochem. 2013. № 28. P. 69–79.
Shotyk W., Rausch N., Nieminen T.M., Ukonmaanaho L., Krachler V. Isotopic composition of Pb in peat and porewaters from three contrasting ombrophic bogs in Finland: Evidence of chemical diagenesis in response to acidification // Environ. Sci. Technol. 2016. V. 50. P. 9943–9951.
Дополнительные материалы отсутствуют.