Почвоведение, 2022, № 5, стр. 600-614
Идентификация соединений тяжелых металлов в техногенно преобразованных почвах методами последовательного фракционирования, XAFS-спектроскопии и XRD порошковой дифракции
Д. Л. Пинский a, Т. М. Минкина b, *, Т. В. Бауэр b, Д. Г. Невидомская b, В. А. Шуваева b, С. С. Манджиева b, В. С. Цицуашвили b, М. В. Бурачевская b, В. А. Чаплыгин b, А. В. Барахов b, А. А. Велигжанин c, Р. Д. Светогоров c, Е. В. Храмов c, А. Д. Иовчева a
a Институт физико-химических и биологических проблем почвоведения РАН
142290 Московская область, Пущино, ул. Институтская, 2, Россия
b Южный федеральный университет
344006 Ростов-на-Дону, ул. Большая Садовая, 105/42, Россия
c Национальный исследовательский центр “Курчатовский институт”
123182 Москва, пл. Академика Курчатова, 1, Россия
* E-mail: tminkina@mail.ru
Поступила в редакцию 11.12.2021
После доработки 18.12.2021
Принята к публикации 30.12.2021
- EDN: LVHMTM
- DOI: 10.31857/S0032180X22050070
Аннотация
Изучена трансформация техногенных соединений Cu и Zn в хемоземах (Spolic Technosols) с высокими и очень высокими концентрациями металлов, сформированных на месте природного отстойника промышленных предприятий в пойме р. Северский Донец – главного притока р. Дон (Ростовская область, Россия). Проведено сравнение хемоземов с незагрязненной луговой почвой, расположенной за пределами импактной зоны. Состояние Cu и Zn оценено с использованием трех схем последовательных экстракций: Миллера, Тессье и BCR, а также синхротронных методов рентгеновской порошковой дифракции (XRD) и структурного анализа спектров (XAFS). Показано, что распределение металлов в почве в значительной степени связано с их свойствами: электроотрицательностью, гидролизуемостью и способностью к образованию π-связи. Установлено, что Cu концентрируется в основном в остаточной (>42%) и связанной с органическим веществом (<27%) фракциях. Подвижность Zn в исследуемых почвах больше, чем Cu. Основная его часть (<56%) находится в остаточной и связанной с Fe и Mn оксидами фракциях (<48%), особенно с кристаллическими формами Fe(III). Впервые проведено комбинированное использование трехступенчатой схемы BCR в сочетании с методами XAFS и XRD. Большая часть пиков, присутствующих на дифрактограммах образцов почвы после первой и второй стадий экстрагирования, соответствует аутигенным серосодержащим минералам: вюртциту (ZnS с гексагональной структурой), сфалериту (ZnS с кубической структурой), ковеллину (CuS), борниту (Cu5FeS4). Образец почвы после извлечения окисляемой фракции наиболее насыщен сульфидами, в то время как в образце почвы после извлечения восстанавливаемой фракции доминируют филлосиликаты. Результаты анализа спектроскопии рентгеновского поглощения выявили для высокозагрязненных почв молекулярно-структурные изменения соединений Zn и Cu, показывающие трансформацию металла в различной природной обстановке, что важно для оценки протекторной функции почв.
ВВЕДЕНИЕ
Стремительный рост потребления цветных металлов современной промышленностью неизбежно приводит к загрязнению объектов окружающей среды и, главным образом, почв соединениями тяжелых металлов (ТМ) техногенной природы. Их биодоступность превышает гомеостатический контроль живого организма [36]. Поэтому, поступая в трофические цепи, они становятся потенциально опасными. Некоторые из ТМ, как например, Cu и Zn, являясь важнейшими микроэлементами, в то же время проявляют высокую токсичность по отношению к животным и человеку, и относятся к первому и второму классам опасности.
Металлы и металлоиды играют ключевую роль в функционировании и устойчивости почвенных экосистем. В настоящее время среди ученых и специалистов достигнуто понимание того, что трансформация ТМ почвами, приводящая к образованию различных соединений металлов, является ключевым фактором, регулирующим их поведение и функции в системе почва–растение и, следовательно, возможность вхождения ТМ в трофические цепи [44]. В ненарушенных естественных почвах, возраст которых измеряется от нескольких сотен до нескольких тысяч лет (в зависимости от условий формирования), трансформация ТМ, поступающих из исходных пород, происходит очень медленно [1, 32]. Соотношение соединений металлов в почвах при отсутствии загрязнения является отражением стабильности процессов почвообразования.
Однако в результате научно-технического прогресса концентрации ТМ в окружающей среде и особенно в почвах импактных зон возросли до величин, значительно превышающих допустимые нормы [13]. Трансформация техногенных соединений ТМ в таких почвах сильно ускорена из-за термодинамических дисбалансов, возникающих при осуществлении процессов окисления, карбонизации, осаждения вторичных минералов и других факторов [34, 36].
В связи с этим важно иметь представления о том, как в процессе почвообразования происходила трансформация техногенных соединений металлов в зависимости от свойств почв и особенностей загрязнения.
Для изучения соединений ТМ в загрязненных почвах широко используют метод последовательных селективных экстракций. Экстракционные методы химического анализа, различаясь в деталях, принципиально близки. Эти методы основаны на использовании экстрагентов, переводящих в раствор соединения металлов, предположительно удерживаемые твердофазными компонентами почв за счет разных механизмов и с разной прочностью [28]. Весьма актуальны исследования поглощения ТМ различными почвенными компонентами, такими как органическое вещество, глинистые минералы, Fe–Mn гидроксиды, карбонаты.
При работе с такой сложной полидисперсной гетерогенной системой, как почва, практически все используемые схемы последовательных селективных экстракций имеют весьма серьезные недостатки. К ним относятся недостаточно высокая селективность используемых экстрагентов, особенно при экстрагировании непрочно связанных форм; неполное извлечение ТМ из целевых фаз-носителей; повторная адсорбция и переосаждение [9, 21, 22, 33, 38]. К этому следует добавить, что прочность связи ТМ с поверхностью почвенных частиц, а значит и их экстрагируемость, в большой степени зависят от состава жидкой фазы, свойств металлов и степени заполнения поверхности сорбента (уровня загрязнения) [7, 32]. В ходе последовательного извлечения из почвы загрязняющих веществ происходят неконтролируемые изменения системы в целом, что, безусловно, влияет на результаты исследования [28, 33]. Сложность нахождения форм соединений металлов особенно ярко проявляется в отношении высоко динамичных техногенных почвенных экосистем. Для повышения информативности данных методов их применение сочетают с другими инструментальными методами диагностики [25, 27, 33]. Рентгеновская спектроскопия поглощения на основе синхротронного излучения является в настоящее время одним из наиболее перспективных методов неразрушающей диагностики локальной атомной и электронной структур материалов без дальнего порядка в расположении атомов. Инструментальное обеспечение спектроскопических исследований постоянно совершенствуется. Неуклонно растет число исследований, выполненных с использованием данного метода [23, 40]. Поэтому представляется целесообразным изучение соединений ТМ с использованием методов экстракционного фракционирования и методов спектроскопии рентгеновского поглощения.
Цель работы – изучение состояния катионов Zn и Cu в техногенно преобразованных почвах с использованием методов последовательных селективных экстракций и рентгеновского синхротронного излучения.
ОБЪЕКТЫ И МЕТОДЫ
Район исследования представляет собой импактную территорию поймы р. Северский Донец – одного из главных притоков р. Дон (Юг России), которая в 1950–1990-х гг. использовалась в качестве бассейна для отвода сточных вод химического завода и представляет собой высохшую старицу оз. Атаманское (48°21′00″ N, 40°14′31″ E), которая является вторичным источником загрязнения окружающей среды [27]. Для изучения этого района была создана геохимическая сетка из 100 участков мониторинга. Исследуемая площадь составила около 12 га. Отбор почвенных образцов на территории высохшего озера проводили на глубину 0–20 см согласно ГОСТ 28168-89.
Почвы на данной территории сформировались в течение нескольких десятилетий в результате выхода на поверхность загрязненных донных отложений при обмелении и высыхании озера. Исследуемые техногенно трансформированные почвы представляют собой хемоземы (Spolic Technosols). На основе выполненных литохимических опробований на территории высохшего озера было выбрано два участка мониторинга с высоким (хемозем-1) и аномально высоким (хемозем-2) уровнями антропогенного загрязнения. Хемозем-1 расположен в пределах южной части высохшего оз. Атаманское на левом берегу р. Северский Донец, в 500 м к северу от уреза. Хемозем-2 находится на южной оконечности озера, где, как предполагается, имел место выход трубы, по которой сбрасывались отходы химических предприятий. В качестве фона использовали луговую почву (Mollic Fluvisol) на участке мониторинга, расположенном в 1200 м от озера, в краевой части поймы на правом берегу р. Северский Донец, в 100 м к югу от уреза.
Физические и химические характеристики исследованных почв проанализированы общепринятыми стандартными методами: рН потенциометрическим методом при соотношении почва : вода 1 : 2.5; содержание органического углерода (Сорг) – титриметрическим методом (бихроматное окисление по Тюрину) [3]; емкость катионного обмена – по методу М.Ш. Шаймухаметова [12]; содержание карбонатов комплексонометрическим методом по методу С.А. Кудрина [3]; гранулометрический состав почвы методом пипетки с пирофосфатной подготовкой пробы [2]. Элементный состав почв определен рентгенофлуоресцентным методом на спектрометре Спектроскан МАКС-GV (Спектрон, Россия).
Существует много схем последовательного фракционирования ТМ в почвах [6–8]. В большинстве случаев используются оригинальные, “авторские” методы экстрагирования ТМ. Наибольшее распространение получил метод Тессье, который к настоящему моменту имеет более 7700 цитирований, а также метод BCR, рекомендованный European Community Bureau of Reference и модифицированный добавлением остаточной фракции [31, 42 ]. В данной работе использовали метод Тессье и модифицированную схему BCR, а также метод Миллера [26], который позволяет более детально изучить закономерности трансформации ТМ на оксидах Fe и Mn (табл. 1). Концентрации металлов в каждой фракции выражены в абсолютных и относительных единицах измерения, что позволяет оценивать долю Cu и Zn в каждой фракции от общего количества экстрагированных металлов.
Таблица 1.
Методы последовательных экстракций тяжелых металлов из почв
| Авторы | Фракции | Процедуры |
|---|---|---|
| Miller et al. (1986) | Водорастворимая | 0.5 г почвы + 20 мл Н2О, перемешивание 16 ч |
| Обменная | 20 мл 0.5 М Ca(NO3)2, перемешивание 16 ч | |
| Связанная с карбонатами | 20 мл 0.44 М CH3COOH + 0.1 M Ca(NO3)2 перемешивание 8 ч | |
| Связанная с оксидами Mn | 20 мл 0.1 М NH2OH·HCl + 0.1 M HNO3, 30 мин | |
| Связанная с органическим веществом | 20 мл 0.1 М К2P2О7, 24 ч | |
| Связанная с аморфными оксидами Fe | 20 мл 0.175 М (NH4)2С2O4 + 0.1 M H2C2O4 (темнота) 4 ч | |
| Связанная с кристаллическими оксидами Fe | 25 мл (NH4)2С2O4 + 0.1 M H2C2O4, 85°С, ультрафиолетовое облучение, 3 ч | |
| Остаточная | 1 мл царской водки, 10 мл HF, 110°C, 2 ч в герметичном контейнере | |
| Tessier et al. (1979) | Обменная | 1 M MgCl2 (рН 7.0) при постоянном перемешивании (1 ч) (почва : раствор 1 : 8) |
| Связанная с карбонатами | 1 M NaCH3COO, pH 5.0 (CH3COOH) экстрагировать при комнатной температуре 5 ч (почва : раствор 1 : 8) | |
| Связанная с Fe–Mn оксидами | 0.04 M NH2OH·HCl в 25% CH3COOH при температуре 96 ± 3°С, 8 ч с перемешиванием (почва : раствор 1 : 20) | |
| Связанная с органическим веществом | 0.02 M HNO3 и 5 мл 30% H2O2, доведенная до pH 2 HNO3, смесь нагревать до 85 ± 2°С в течение 3 ч время от времени перемешивая. После охлаждения 3.2 M NH4CH3COO в 20% (v/v) HNO3 добавить и перемешивать постоянно в течение 30 мин (почва : раствор 1 : 20) | |
| Остаточная | HF + HClO4, затем концентрированную HNO3 после выпаривания (почва : раствор 1 : 25) | |
| Модифицированная BCR (Pueyo et al., 2008) | Кислоторастворимая (обменная и слаборастворимая в кислоте фракция, первая стадия) | 0.11 M CH3COOH раствор встряхивать 16 ч (почва : раствор 1 : 40) |
| Восстанавливаемая (связанная с гидроксидами и оксидами Fe и Mn, вторая стадия) | 0.5 М NH2OH·HCl встряхивать 16 ч, рН 2 при подкислении реагента добавлением 2.5% (v/v) раствора HNO3 (почва : раствор 1 : 40) | |
| Окисляемая (связанная с органическим веществом, третья стадия) | 8.8 M H2O2 при нагревании (1 ч при 85 ± 2°C) до испарения почти досуха, затем 50 мл 1 М NH4CH3COO, рН 2, подкисление этого реагента добавлением 2.5% (v/v) раствора HNO3 (почва : раствор 1 : 70) | |
| Остаточная (после третьей стадии) | Царскую водку (HCl (37%) и HNO3 (70%)) добавить после выпаривания (почва : раствор 1 : 9) |
Для идентификации фаз, удерживающих Cu2+ и Zn2+ в техногенно нарушенной почве, использовали сочетание синхротронных методов структурного анализа спектров (XAFS) и рентгеновской порошковой дифракции (XRD) образца после каждой стадии последовательного экстрагирования с использованием международной схемы BCR [40]. Применяли такие неразрушающие методы XAFS как анализ расширенной тонкой структуры спектров поглощения рентгеновских лучей (EXAFS) и анализ структуры ближнего края спектров поглощения рентгеновских лучей (XANES). Функции радиального парного распределения вокруг атомов металлов были получены с помощью преобразования Фурье k-взвешенных функций EXAFS в диапазоне волновых чисел фотоэлектронов 2.6–12.5 Å–1. В силу ограничений, связанных с чувствительностью экспериментального оборудования для измерения XAFS-спектров, была использована почва с аномально высоким уровнем загрязнения (хемозем-2).
Экспериментальные данные EXAFS и XANES спектров (K-край Zn и Cu – 9659 эВ) были получены на станции “Структурное материаловедение”, расположенной на канале 1.3б Курчатовского центра синхротронного излучения НИЦ “Курчатовсй институт”. Источником синхротронного излучения на канале 1.3б служит поворотный магнит с полем 1.7 Тл накопительного кольца “Сибирь-2”. При генерации синхротронного излучения энергия электронного пучка составляет 2.5 ГэВ, средний ток 60–70 мА [15].
Обработка экспериментальных EXAFS спектров в рутинном режиме проводилась Фурье-фильтрацией с последующей подгонкой варьируемых параметров модели локальной атомной структуры с использованием программных комплексов FEFFIT [35] и Viper.
Анализ рентгеновской дифракции XRD проводили на станции рентгеноструктурного анализа “Белок/XSA”. Длина волны монохроматического излучения составляла 0.8 Å (энергия фотона 15498 эВ). Образец помещали в криопетлю размером 300 мкм. Дифрактограммы регистрировали детектором 2D Rayonix SX165. После удаления фона и нормировки дифрактограмм для всех дифракционных пиков определены относительные интенсивности, углы Брегга и соответствующие им межплоскостные расстояния, а также проведена идентификация пиков с использованием кристаллографических баз данных и выявлены минеральные компоненты, остающиеся в твердых фазах после каждой селективной экстракции. Для каждого образца было получено по три дифрактограммы от разных проб и проведено их сравнение с целью оценки однородности образцов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Физико-химические характеристики почв. Анализ физико-химических свойств почв (табл. 2) показал, что в незагрязненной луговой почве отмечается высокое содержание Сорг (4.3 ± 0.3%) при нейтральной реакции среды (7.5 ± 0.2). Содержание Сорг в хемоземах изменяется в диапазоне 2.4–4.4%, значения pH – в пределах 7.7–8.2, то есть имеют слабощелочную реакцию среды. В составе поглощающего комплекса доминирует Ca2+. Гранулометрический состав исследуемых почв тяжелосуглинистый. Содержание частиц физической глины (<0.01 мм) составляет 48.4–52.1%; ила (<0.001 мм) 26.0–33.0%. В луговой почве отмечается близкое содержание данных фракций. Валовое содержание ТМ в почвах выбранных площадок мониторинга сильно разнится и значительно превышает предельно допустимые концентрации исследуемых элементов по СанПиН 2.1.3684-21. При этом Zn является основным загрязняющим элементом в исследуемых почвах. Концентрация его в хемоземе-2 составляет более 6.2% по массе.
Таблица 2.
Основные физико-химические свойства изученных почв
| Почва | Уровень загрязне-ния | pHводн | Физическая глина (<0.01 мм), % | Ил (<0.001 мм), % | Сорг, % | Обменные катионы, смоль(+)/кг | Cu | Zn | |
|---|---|---|---|---|---|---|---|---|---|
| Ca2+ | Mg2+ | ||||||||
| мг/кг | |||||||||
| Луговая | Фон | 7.5 ± 0.2 | 55.8 ± 2.4 | 32.0 ± 1.9 | 4.3 ± 0.3 | 4.6 ± 0.2 | 31.8 ± 2.6 | 37 ± 2 | 110 ± 5 |
| Хемозем-1 | Высокий | 8.2 ± 0.2 | 48.4 ± 2.6 | 26.0 ± 0.4 | 2.4 ± 0.1 | 23.7 ± 1.2 | 3.8 ± 0.1 | 526 ± 21 | 2369 ± 68 |
| Хемозем-2 | Аномально высокий | 7.7 ± 0.1 | 52.1 ± 3.8 | 33.0 ± 2.6 | 4.4 ± 0.2 | 35.2 ± 1.7 | 5.3 ± 0.3 | 147 ± 9 | 62 032 ± 597 |
Оценка состояния Cu и Zn в хемоземах по результатам фракционирования. Данные перераспределения экзогенных Cu и Zn между фракциями, выделенными с использованием различных методов, представлены в табл. 3.
Таблица 3.
Фракционный состав Сu, Zn в луговой почве и хемоземах в пойме р. Северский Донец, мг/кг
| Почва | Ме-талл | Фракция | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| водораст-воримая | обменная | связанная с карбона-тами | связанная с Mn оксидами | связанная с аморфными оксидами Fe | связанная с кристал-лическими оксидами Fe | связанная с оксидами Fe–Mn | связанная с органическим веществом | остаточная | ||
| Метод Миллера | ||||||||||
| Луговая | Cu | 0.0 ± 0.0 | 0.4 ± 0.02 | 1.2 ± 0.1 | 0.4 ± 0.05 | 0.8 ± 0.1 | 1.6 ± 0.2 | — | 5.2 ± 0.6 | 30.2 ± 1.7 |
| Zn | 0.02 ± 0.0 | 1.7 ± 0.2 | 5.8 ± 0.7 | 1.1 ± 0.1 | 2.4 ± 0.2 | 3.6 ± 0.3 | — | 6.8 ± 0.8 | 92.0 ± 7.0 | |
| Хемозем-1 | Cu | 1.2 ± 0.1 | 30.4 ± 1.5 | 39.6 ± 2.2 | 3.4 ± 0.2 | 27.9 ± 1.8 | 37.1 ± 2.6 | — | 127.2 ± 10.6 | 257.2 ± 17.8 |
| Zn | 13.8 ± 0.7 | 260.8 ± 21.6 | 118.5 ± 13.2 | 16.8 ± 1.1 | 193.4 ± 12.8 | 363.7 ± 28.1 | — | 136.8 ± 14.6 | 1246.4 ± 68.3 | |
| Хемозем-2 | Cu | 0.4 ± 0.03 | 4.6 ± 0.3 | 6.8 ± 0.3 | 1.6 ± 0.1 | 3.3 ± 0.2 | 6.8 ± 0.7 | — | 32.8 ± 2.4 | 89.6 ± 6.5 |
| Zn | 1365 ± 57 | 7232 ± 346 | 4587 ± 179 | 1213 ± 53 | 7096 ± 411 | 12 846 ± 764 | — | 4943 ± 178 | 22 767 ± 1013 | |
| Метод Тессье | ||||||||||
| Луговая | Cu | — | 0.4 ± 0.1 | 1.2 ± 0.2 | — | — | — | 3.0 ± 0.2 | 6.0 ± 0.7 | 25.9 ± 1.8 |
| Zn | — | 1.0 ± 0.1 | 4.7 ± 0.5 | — | — | — | 9.2 ± 0.6 | 8.2 ± 1.1 | 77.5 ± 9.6 | |
| Хемозем-1 | Cu | — | 26.9 ± 3.2 | 43.8 ± 2.7 | — | — | — | 92.9 ± 12.3 | 141.6 ± 11.6 | 217.8 ± 15.9 |
| Zn | — | 264.9 ± 17.8 | 173.6 ± 9.3 | — | — | — | 642.4 ± 32.7 | 180.2 ± 15.3 | 1116.9 ± 48.3 | |
| Хемозем-2 | Cu | — | 3.9 ± 0.4 | 8.3 ± 0.6 | — | — | — | 13.2 ± 0.9 | 29.2 ± 2.1 | 88.3 ± 7.3 |
| Zn | — | 8070 ± 263 | 6350 ± 198 | — | — | — | 23653 ± 1624 | 5446 ± 217 | 18 559 ± 903 | |
| Метод BCR | ||||||||||
| Луговая | Cu | — | — | 1.2 ± 0.1 | — | — | — | 3.7 ± 0.2 | 5.7 ± 0.7 | 27.8 ± 3.6 |
| Zn | — | — | 4.3 ± 0.5 | — | — | — | 9.6 ± 1.1 | 7.3 ± 0.5 | 81.5 ± 9.7 | |
| Хемозем-1 | Cu | — | — | 56.9 ± 6.7 | — | — | — | 89.6 ± 5.9 | 126.3 ± 13.8 | 241.2 ± 22.7 |
| Zn | — | — | 327.4 ± 26.3 | — | — | — | 564.8 ± 27.6 | 139.1 ± 11.9 | 1325.7 ± 89.4 | |
| Хемозем-2 | Cu | — | — | 18.0 ± 0.9 | — | — | — | 12.0 ± 1.0 | 33.8 ± 3.7 | 83.1 ± 9.1 |
| Zn | — | — | 11 720 ± 106 | — | — | — | 29 954 ± 2356 | 2794 ± 146 | 17 559 ± 1491 | |
Для выявления общих закономерностей перераспределения металлов между фракциями в хемоземах проводили сопоставление результатов нахождения металлов во фракциях, полученных при использовании разных схем фракционирования, и их сравнение с луговой почвой. Установлено, что содержание металлов во всех фракциях луговой почвы, кроме остаточной (до 61 и 85% от суммы фракций), очень низкое и характерно для всех используемых схем фракционирования. Низкая подвижность и доминирование Zn и Cu в остаточной фракции подтверждает отсутствие в данной почве существенного количества металлов техногенного происхождения.
В хемоземах накопление Cu и Zn во всех фракциях выше, чем в луговой почве. Особенно заметные различия наблюдаются во фракциях, связанных с органическим веществом и полуторными оксидами Fe и Mn. Основные различия в результатах фракционирования ТМ в хемоземах, полученные с использованием разных методов, заключаются в разной экстрагирующей способности применяемых реагентов. Из рассматриваемых методов схема Миллера отличается от остальных использованием более “слабых” экстрагентов при выделении ТМ, связанных с органическим веществом и оксидами Fe и Mn. В связи с этим содержание металлов в данных фракциях по схемам Тессье и BCR несколько больше, чем при применении схемы Миллера (рис. 1). В то же время использование схемы Миллера выявило роль аморфных и кристаллических оксидов Fe в удерживании металлов в хемоземах. При взаимодействии с Zn кристаллические оксиды Fe проявляют большее сродство к данному элементу, чем аморфные, что обусловлено давностью загрязнения исследуемой территории, поскольку кристаллизация оксидов Fe в почве происходит достаточно длительное время [14].
Рис. 1.
Фракционный состав соединений Cu (a) и Zn (b), выявленный по методам Миллера, Тессье и BCR в луговой почве и хемоземах, % от суммы фракций.
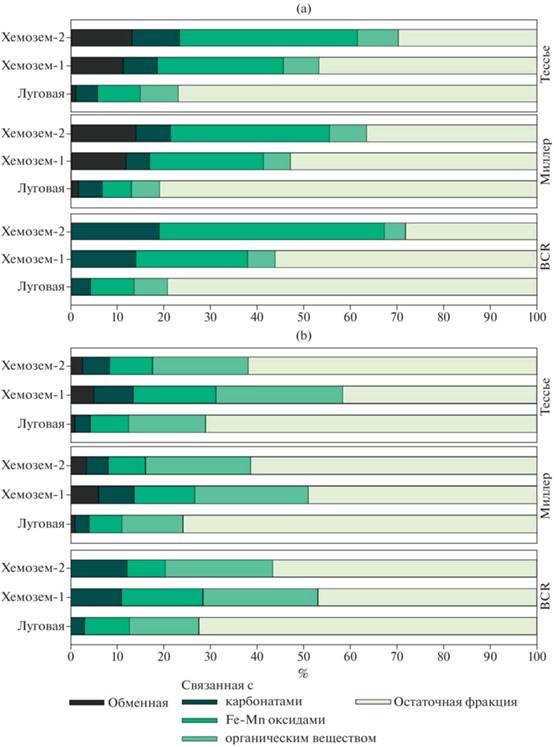
Данные для фракций, связанных с окcидами Mn и Fe в схеме Миллера, просуммировали и рассматривали как единое целое. При таком подходе оказывается, что процентное содержание Cu и Zn во фракциях, связанных с оксидами Fe и Mn в схеме Миллера, незначительно отличается от величин, найденных по схемам Тессье и BCR и однонаправленно изменяется в зависимости от суммы фракций в хемоземах. Так, доля Cu во фракциях, связанных с оксидами Fe и Mn, по схеме Миллера, Тессье и BCR в хемоземе-1 составляет 13.05, 17.6 и 17.4% соответственно; в хемоземе-2 – 8.02, 9.2 и 8.2%. Доля Zn во фракциях, связанных с оксидами Fe и Mn, по схеме Миллера, Тессье и BCR в хемоземе-1 составляет 24.4, 27.0 и 24.0% соответственно; в хемоземе-2 – 34.1, 38.1 и 48.3% (рис. 1). Меньше всего металлов переходит в водорастворимую фракцию – ≤0.3% Cu и ≤2.2% Zn, а больше всего – в остаточную и связанную с окcидами Fe и Mn и органическим веществом. Доля Cu во фракциях, экстрагированных из загрязненных почв, увеличивается в ряду: водорастворимая $ \ll $ обменная < связанная с карбонатами < связанная с оксидами Fe и Mn в разных формах < связанная с органическим веществом $ \ll $ остаточная. Исключение составляют водорастворимая и остаточная фракции. В водорастворимых фракциях содержание Cu различается незначительно. В остаточной фракции хемозема-2 доля Cu больше, чем в соответствующей фракции хемозема-1. Следовательно, Cu в хемоземе-1 в целом удерживается фазами-носителями менее прочно, чем в хемоземе-2. Значительная часть металла перераспределяется между другими менее устойчивыми фазами-носителями. Бόльшая доля Cu, связанная с остаточной фракцией хемозема-2, по сравнению с хемоземом-1, подтверждает эту закономерность.
Доля Zn во фракциях увеличивается для хемозема-1 в ряду: водорастворимая $ \ll $ связанная с органическим веществом < связанная с карбонатами ≤ обменная < связанная с оксидами Fe и Mn в разных формах < остаточная; для хемозема-2: водорастворимая < связанная с органическим веществом < связанная с карбонатами ≤ обменная < < остаточная < связанная с оксидами Fe и Mn в разных формах. Изменение порядка распределения Zn в экстрагируемых фракциях по сравнению с Cu свидетельствует, прежде всего, об изменении характера взаимодействия поглощенных металлов с фазами-носителями, что связано с изменением химического состава этих фракций, а также с индивидуальными свойствами металлов. Содержание Cu в хемоземе-1 в 3.5 раза больше, чем в хемоземе-2, а Zn в 26 раз меньше. Помимо того, что исследуемые металлы, в основном, концентрируются в остаточной фракции, значительное количество меди концентрируется также во фракции, связанной с органическим веществом почвы (25.3%), тогда как Zn в большей степени концентрируется во фракции, связанной с оксидами Fe и Mn [11].
Доля Cu в остаточной фракции луговой почвы составляет 84.9%, в остальных фракциях – 15.1%. Из них во фракции, связанной с органическим веществом – 10.1%. Это меньше, чем в хемоземах, но значительно больше, чем во фракциях, экстрагированных из карбонатов и оксидов Fe и Mn. Цинк распределяется в фоновой почве более равномерно. Наибольшее количество Zn экстрагируется из остаточной фракции (61.3%), в остальных фракциях – 38.7%. Из них во фракции, связанной с оксидами Fe и Mn – 16.7%. Порядок распределения Cu в фоновой почве такой же как в хемоземах-1 и 2, а Zn такой же как в хемоземе-1. Таким образом, и в загрязненных, и в фоновой почвах Cu сорбируется значительно прочнее, чем Zn. Следовательно, Zn обладает большей подвижностью, миграционной способностью и доступностью растениям. Важную роль в поглощении Cu хемоземами играет органическое вещество почв (до 27% от суммы фракций), содержание которого обусловлено физико-химическими, биологическими и экологическими условиями, ограничивающими скорость его деструкции [5]. Zn интенсивнее накапливается в Fe–Mn(гидр)оксидах (до 48%), что согласуется с данными многих исследователей [17, 38].
Индивидуальные свойства Cu и Zn оказывают существенное влияние на характер взаимодействия с почвами и, следовательно, на фракционный состав этих металлов [10]. Существуют разные подходы к объяснению этого явления. Некоторые исследователи связывают это с гидролитическими свойствами металлов. Так, первая константа гидролиза Cu (pK1 ∼ 7.3–8.0) больше, чем первая константа гидролиза Zn (pK1 ∼ 9.0–9.4). Следовательно, ионы Cu2+ будут более прочно сорбироваться почвой, чем Zn2+ [9]. Кроме того, в почвах с высоким pH преобладают частично гидролизованные формы металлов (MOH+), которые сорбируются почвами в больших количествах, чем двухвалентные катионы [19]. Этот механизм также играет важную роль в поглощении ТМ, особенно щелочными почвами.
Эванс [16] связывал сродство почв к металлам с их электроотрицательностью. Так как электроотрицательность Cu больше, чем Zn (2 > 1.6 соответственно), то сорбция Cu почвами предпочтительней, чем Zn. Макбрайд [24] считал, что, электроотрицательность является важным фактором, определяющим способность ТМ к хемосорбции и предложил порядок размещения элементов по этому показателю: Cu > Ni > Co > Pb > Cd > Zn > > Mg > Sr. Мисоно с соавт. [29] предложили использовать двухпараметрическую шкалу для оценки кислотности ионов металлов по Льюису. Один параметр связан с электроотрицательностью, другой, рассчитываемый, исходя из заряда иона и ионного радиуса, характеризует “мягкость связи”, то есть способность к образованию ковалентной π-связи. Для Cu он больше, чем для Zn, и потому сродство почвы к Cu больше, чем к Zn [36].
Стабилизация ТМ в кристаллических решетках глинистых минералов и обратный процесс их высвобождения протекают достаточно медленно вследствие сложного многостадийного механизма этого процесса. Поэтому за 60 лет, в течение которых исследуемые почвы подвергались загрязнению, произошло накопление Cu и Zn в остаточных фракциях исследуемых почв. В то же время с ростом общей концентрации металла в почве отмечается тенденция к уменьшению доли остаточной фракции c 57–62 до 42–49% для Cu и 47–56 до 37–28% для Zn. Одновременно с этим происходит увеличение доли более подвижных и термодинамически менее устойчивых фракций (обменной, связанной с карбонатами). Во всех случаях подвижность Zn выше, чем Cu. Подобные закономерности были отмечены в работах [7, 18], где сообщалось об относительно высокой подвижности Zn в техногенно-нарушенных почвах, что делает его более мобильным, чем Cu. Однако, следует отметить, что несмотря на аномально высокий уровень валового содержания Zn в исследуемых почвах (>62 000 мг/кг), относительное содержание Zn в обменной и связанной с карбонами фракциях невысокое (14–19% в зависимости от используемого метода фракционирования). Этому способствуют высокое содержание органического вещества, слабощелочная реакция среды, преобладание высокодисперсных илистых и мелкопылеватых фракций в исследуемых почвах (табл. 1) и отсутствие постоянно действующего источника загрязнения.
Таким образом, закономерности формирования фракционного состава Cu и Zn в гидрогенных техногенно-трансформированных почвах, полученные с использованием разных схем последовательного фракционирования, позволяют выявить общие и специфические особенности в распределении металлов между фракциями в хемоземах, связанные как со свойствами почв, характером загрязнения, так и с индивидуальными свойствами металлов. При повышении уровня загрязнения доля ТМ в остаточной фракции уменьшается и возрастает их доля в более подвижных соединениях. При этом доля Zn в более подвижных первых фракциях всегда выше, чем Cu. Это в значительной мере связано с различиями данных элементов в гидролизуемости, электроотрицательности и “мягкости связи” (по Мисоно). Аккумуляция Cu и Zn в остаточной фракции фоновой почвы свидетельствует о том, что большая часть металлов прочно закреплена в кристаллических решетках алюмосиликатов.
Оценка состояния Cu и Zn в хемоземах по результатам XRD. Получены синхротронные рентгендифрактограммы для образца хемозема-2 после каждой стадии последовательного экстрагирования по методу BCR (табл. 4). Наибольшие различия в интенсивности отдельных максимумов обнаружены при сопоставлении дифрактограмм образца почвы после первого этапа экстрагирования – удаления кислоторасторимых форм. На дифрактограммах образцов почвы после второго этапа экстрагирования были выявлены вариации интенсивностей отдельных максимумов. Образец почвы после проведения третьей стадии оказался наиболее однородным по составу минеральных кристаллических фаз, на что указывает практически полное совпадение дифрактограмм всех трех повторностей.
Таблица 4.
Углы (2θ), межплоскостные расстояния (d) и интенсивности дифракционных рефлексов (I) на рентгенограммах трех почвенных фракций
| Угол 2θ, град | d | Интенсивность, I, отн. ед. | Минералы | ||
|---|---|---|---|---|---|
| почва после первой стадии экстрагирования | почва после второй стадии экстрагирования | почва после третьего экстрагирования | |||
| 9.75 | 4.72219 | – | – | 0.14 | – |
| 10.32 | 4.46202 | 0.28 | 0.31 | 0.17 | Монтмориллонит |
| 10.82 | 4.2564 | 0.44 | 0.29 | 0.23 | Кварц |
| 12.22 | 3.7703 | 0.10 | – | – | Гипс |
| 12.91 | 3.56958 | 0.15 | 0.06 | – | – |
| 13.15 | 3.50471 | 0.03 | – | 0.04 | – |
| 13.79 | 3.34278 | 1.00 | 1.00 | 1.00 | Кварц |
| 14.40 | 3.20188 | – | 0 | 0.10 | – |
| 14.76 | 3.1242 | 0.49 | 0.46 | – | Вюртцит |
| 15.15 | 3.04423 | 0.57 | – | – | Гипс/Вюртцит |
| 15.60 | 2.95693 | – | – | 0.07 | – |
| 16.10 | 2.86568 | 0.08 | – | – | Гипс |
| 16.63 | 2.77496 | 0.31 | 0.13 | 0 | Вюртцит |
| 17.18 | 2.68676 | 0.03 | – | – | Гипс |
| 18.00 | 2.565 | 0.15 | 0.21 | 0.16 | Монтмориллонит |
| 18.57 | 2.48722 | 0.10 | – | – | – |
| 18.81 | 2.45577 | 0.13 | 0.14 | 0.12 | Кварц |
| 19.34 | 2.38908 | 0.05 | 0.06 | 0.05 | – |
| 19.74 | 2.34114 | 0.10 | 0.06 | – | – |
| 20.27 | 2.28054 | 0.15 | 0.08 | 0.09 | Кварц |
| 20.68 | 2.2358 | 0.05 | 0.05 | 0.07 | Кварц |
| 21.74 | 2.12801 | 0.13 | 0.10 | 0.09 | Кварц |
| 22.17 | 2.08723 | 0.10 | – | – | – |
| 23.37 | 1.98144 | 0.08 | 0.07 | 0.06 | Кварц |
| 23.71 | 1.95342 | 0.13 | – | – | Вюртцит |
| 24.24 | 1.91133 | 0.37 | 0.28 | 0 | Вюртцит |
| 24.70 | 1.87627 | 0.21 | – | – | Вюртцит |
| 25.50 | 1.81834 | 0.20 | 0.17 | 0.17 | Кварц |
| 25.98 | 1.7853 | 0.07 | – | – | – |
| 27.02 | 1.71779 | 0.19 | 0.08 | – | – |
| 27.79 | 1.67109 | 0.12 | 0.12 | 0.08 | Кварц |
| 28.50 | 1.63029 | 0.26 | 0.25 | – | Вюртцит |
| 29.00 | 1.60277 | 0.13 | – | – | – |
| 30.19 | 1.54098 | 0.16 | 0.17 | 0.14 | Кварц |
| 30.58 | 1.52179 | 0.08 | – | – | – |
| 31.00 | 1.50166 | 0.17 | 0.17 | 0.08 | Монтмориллонит |
| 32.06 | 1.45325 | 0.03 | 0.04 | 0.03 | – |
| 32.83 | 1.42007 | 0.08 | 0.03 | – | – |
| 33.96 | 1.37414 | 0.18 | 0.18 | 0.17 | Кварц |
| 34.55 | 1.35138 | 0.09 | 0.07 | – | – |
| 36.09 | 1.29551 | 0.06 | 0.06 | – | – |
| 36.29 | 1.28861 | 0.07 | 0.08 | 0.07 | Кварц |
| 37.27 | 1.25588 | 0.07 | 0.08 | 0.07 | Кварц |
| 37.70 | 1.24207 | 0.09 | 0.09 | – | – |
| 38.14 | 1.22826 | 0.06 | 0.06 | 0.04 | Кварц |
| 39.10 | 1.19924 | 0.08 | 0.08 | 0.07 | Кварц |
| 39.69 | 1.18212 | 0.07 | 0.07 | 0.07 | Кварц |
| 40.73 | 1.15317 | 0.05 | 0.03 | 0.03 | – |
| 42.60 | 1.10475 | 0.06 | 0.07 | – | – |
| 43.55 | 1.08179 | 0.07 | 0.06 | 0.05 | – |
Одним из доминирующих компонентов в образцах почвы после всех стадий фракционирования является кварц. Большая часть пиков, присутствующих на дифрактограммах образцов почвы после первой и второй стадий, соответствуют аутигенным серосодержащим минералам: вюртциту (ZnS с гексагональной структурой), сфалериту (ZnS с кубической структурой), ковеллину (CuS), борниту (Cu5FeS4). Почва после первой стадии экстрагирования наиболее насыщена сульфидами, в то время как в остатке почвы после второго этапа доминируют филлосиликаты. Монтмориллонит в образцах определяется предположительно после всех этапов фракционирования. То же самое можно сказать об редко встречающемся ангидрите и волластоните. Следует отметить, что положение и интенсивности пиков зависят от многих факторов, в том числе от состояния минеральных компонентов в образце. Очевидно, химическая обработка почвы в ходе последовательных селективных экстракций, направленная на извлечение определенных компонентов, существенным образом отражается на состоянии кристаллитов в остатке. Специфическое взаимодействие экстрагентов с минеральными и органическими компонентами почв оказывает сильное неконтролируемое влияние на состояние минеральных компонентов в образце и образца в целом. Возможно, именно с этим связаны вариации интенсивностей отдельных максимумов на дифрактограммах [4]. Положение отдельных компонентов в спектрах XRD может быть также следствием этих процессов.
Оценка состояния Cu и Zn в хемоземах по результатам XAFS-спектроскопии. Чувствительность предкраевой области спектров поглощения (XANES) к геометрии связей может быть использована для предварительного качественного анализа окружения Cu и Zn в образцах почвы после каждой из трех стадий последовательного экстрагирования. Тип атомов, входящих в ближайшее окружение атомов Cu в образцах хемозема после применения последовательного экстрагирования, определен по предкраевой области Cu K-края спектров XANES (рис. 2a). В качестве эталонных были использованы несколько медьсодержащих соединений, в которых ближайшие координационные сферы атомов Cu образованы атомами кислорода (Cu(CH3COO)2, CuCO3 и CuSO4), а также атомами серы (CuS, Cu2S). В CuSO4 металл координирован четырьмя атомами кислорода c двумя короткими и двумя длинными связями Cu–O (1.91 и 2.05 Å), следующая координационная сфера имеет радиус 2.37 Å и содержит еще два атома кислорода. В Cu(CH3COO)2 медь также находится в тетраэдрическом кислородном окружении и длины связей Cu–O варьируются от 1.90 до 2.05 Å. В Cu2S атомы Cu координированы тремя атомами серы, а ближайшее расстояние Cu–S составляет 2.29 Å. В CuS радиус первой координационной сферы, образованной тремя атомами серы, равен 2.17 Å. Значительная разница в положении края поглощения и величин основных особенностей спектра в образцах с Cu–S и Cu–O связями позволяет надежно различать эти типы окружения Cu в образцах почвы после применения последовательных селективных экстракций.
Рис. 2.
Экспериментальные XANES спектры К-края Cu (a) и Zn (b), а также Фурье-преобразование Cu (с) и Zn (d) EXAFS спектров исследуемых образцов хемозема после каждой стадии последовательного экстрагирования по схеме BCR и стандартных Cu- и Zn-содержащих соединений соответственно.
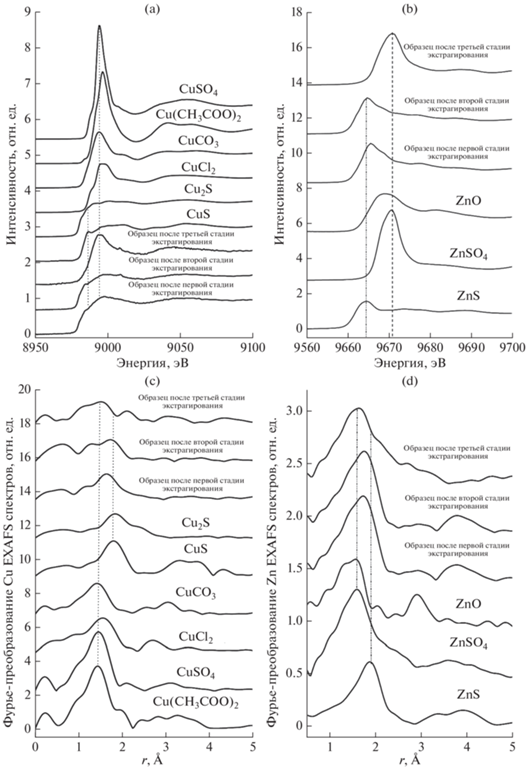
Спектры Cu K-края XANES образцов хемозема после первого и второго этапов фракционирования имеют вид, очень близкий к спектрам медьсодержащих соединений с серой (CuS и Cu2S), что является свидетельством наличия большого количества связей Cu–S. Дополнительным подтверждением служит характер радиального распределения атомов, о котором можно судить по FT EXAFS спектрам (рис. 2b). Спектр Cu K-края XANES образца после третьего этапа имеет явно выраженный максимум, который характерен для спектров стандартов с кислородным окружением Cu. Преобладание связей Cu–O во фракции после третьего этапа демонстрирует схожее положение края поглощения с референсными соединениями.
Путем подгонки спектров исследованных образцов хемозема линейной комбинацией спектров эталонных соединений дана оценка вклада различных веществ (табл. 5) в данные фракции. Результаты свидетельствуют, что в образцах после первого этапа характерно преобладание Cu2S и CuCO3, однако здесь имеются небольшие примеси CuSO4 и CuCl2. Cпектры образцов почвы после второго этапа с высокой точностью совпадают со спектрами Cu2S. Для образца почвы после третьего этапа характерно высокое содержание CuCO3 (50% от вклада всех соединений Cu), также Cu2S (30% от вклада всех соединений Cu) и наличие незначительных примесей CuSO4 (12% от вклада всех соединений Cu).
Таблица 5.
Результаты моделирования экспериментальных спектров XANES К-края Cu и Zn в образцах хемозема после каждой стадии последовательного экстрагирования методом BCR и спектров эталонных соединений, % от общей доли медьсодержащих соединений в образце
| XANES К-края Cu, Zn | После первой стадии | После второй стадии | После третьей стадии |
|---|---|---|---|
| CuSO4 | 4 | 0 | 12 |
| CuCO3 | 0 | 0 | 50 |
| Cu2S | 86 | 100 | 33 |
| CuS | 0 | 0 | 0 |
| CuCl2 | 10 | 0 | 0 |
| ZnSO4 | 65 | 0 | 25 |
| ZnO | 0 | 50 | 18 |
| ZnS | 35 | 50 | 57 |
На рис. 2c представлены Zn K-края, XANES спектры для образцов почвы после различных этапов экстрагирования в сравнении с эталонными соединениями: ZnSO4, вюртцитом (ZnS) и цинкитом (ZnO). Спектры для референсных Zn-содержащих соединений с известной структурой с Zn–S (ZnS) и Zn–O связями (ZnO и ZnSO4) показывают значительную разницу в положении края поглощения, что позволяет различить типы окружения Zn в образцах хемозема.
Спектры Zn K-края, XANES образца почвы после третьего этапа экстракции демонстрируют сходство с референсными спектрами, в которых Zn координирован кислородом (ZnO, ZnSO4), где главный пик поглощения находится около 9670 эВ. Спектры XANES образцов почвы после первых двух этапов близки к спектру, ZnS, где главная особенность поглощения находится около 9665 эВ. Однако он также содержит более высокоэнергетические варианты, указывая на возможность смешанных Zn–S и Zn–O связей в образцах хемозема.
Так же, как XANES, Фурье-трансформанты (FT) EXAFS спектров K-края Zn для образцов выделенных фракций демонстрируют явные различия, свидетельствующие о том, что формы металла в этих образцах различны. Образец после третьего этапа фракционирования имеет большее сходство с аналогичным спектром ZnSO4, что подтверждают результаты анализа ближней структуры спектров поглощения. Отсутствие пика, соответствующего второй координационной сфере (Zn–Zn), указывает на то, что ZnO не является преобладающей компонентой образца. В образцах почвы после первого и второго этапов экстракции основные пики на FT EXAFS спектрах сдвинуты в область больших значений R (рис. 2d), что указывает на возможность наличия связей Zn–S в этом образце и находится в согласии с результатами анализа XANES.
Исходя из предположения о том, что образцы хемозема после фракционирования содержат фазы Zn–S и Zn–O, были проведены более точные количественные оценки путем подгонки околокраевой области спектров почвенных соединений линейной комбинацией спектров эталонных соединений. Результаты показали, что основные различия между фракциями связаны с соотношением содержания ZnSO4 и ZnO. Сульфат цинка (ZnSO4) является основным компонентом (65%) во фракции после первого этапа, что согласуется с преобладанием связи Zn–O в первой оболочке, определенной по данным EXAFS.
Высокий уровень согласия между линейными комбинированными спектрами и экспериментальными спектрами образцов исследуемых фракций почвы показывает, что ZnS присутствует в заметных количествах во всех образцах. В то же время почва после второго и третьего этапов содержат связи Zn–S 57 и 50%, соответственно, в виде минерального вюртцита (ZnS). Согласно результатам, полученным для верхнего горизонта сильно загрязненных почв в Пальтертоне (США), доминирующее закрепление Zn происходило в форме сульфида-сфалерита (ZnS) [33].
Моделирование экспериментальных спектров К-края Zn XANES в образцах хемозема после второго и третьего этапов экстракции почвы установило присутствие ZnO. Отмечается, что при загрязнении почвы цинкитом (ZnO), минерал трансформируется и преимущественно входит в состав Zn-содержащих триоктаэдрических структур [43].
Применение линейной комбинации спектров XANES и EXAFS после каждой стадии фракционирования Zn и Cu из сильнозагрязненного хемозема позволило значительно улучшить идентификацию специфической формы металлов, определяемой по электронной и молекулярной структуре. Методом EXAFS установлена возможность гетеровалентного изоморфного замещения ионов Al3+ в октаэдрических позициях глинистых минералов катионами Cu2+ и Zn2+ [28, 37].
ЗАКЛЮЧЕНИЕ
Изучены особенности трансформации Cu и Zn в луговой и техногенно-преобразованных гидроморфных почвах (хемоземах) импактной зоны отстойника сточных вод. Исследование Cu и Zn методами последовательных селективных экстракций показало, что распределение их по фракциям определяется составом и свойствами исследуемых почв, уровнем их загрязнения, а также химическими свойствами металлов. Наибольшее количество Cu сосредоточено в остаточной фракции хемоземов; Zn – в остаточной и во фракции оксидов Fe и Mn. Отличительной особенностью формирования форм соединений металлов в почвах исследуемой территории является повышенное содержание поллютантов во фракции кристаллических оксидов Fe по сравнению с аморфными и доминирование остаточной фракции, что свидетельствуют о давности и высоком уровне загрязнения.
Для идентификации фаз, удерживающих металлы в хемоземах, использован комбинированный прием на основе структурного анализа спектров XAFS и рентгеновской дифракции (XRD) оставшегося образца после каждой стадии последовательного экстрагирования с использованием схемы BCR. Показано, что гидроморфные условия и техногенный характер почвообразования способствуют проявлению сидерофильности ТМ. Применение линейной комбинации спектров XANES и EXAFS после каждой стадии последовательного экстрагирования Zn и Cu в сильнозагрязненных хемоземах значительно улучшило идентификацию видообразования металлов. Значительная разница в положении края поглощения и величин основных особенностей спектра в образцах с Cu–S и Cu–O связями позволяет надежно различать эти типы окружения Cu в образцах выделенных фракций. Методами XANES и EXAFS установлена возможность гетеровалентного изоморфного замещения ионов Al3+ в октаэдрических позициях глинистых минералов катионами Cu2+ и Zn2+.
Для изучения почв методы синхротронного излучения используются пока еще недостаточно, что обусловлено сложностью организации почвы, ее гетерогенностью и полидисперсностью. Но в связи с расширением возможностей этих методов в последние годы есть все основания ожидать получения принципиально новых знаний о почвах и механизмах поглощения ими различных химических веществ.
Список литературы
Александровский А.Л. Роль времени в развитии и эволюции почв // Национальный атлас почв. М., 2011. С. 66–67.
Вадюнина А.Ф., Корчагина З.А. Методы исследования физических свойств почв и грунтов. М.: Агропромиздат, 1986. 416 с.
Воробьева Л.А. Теория и практика химического анализа почв. М.: ГЕОС, 2006. 400 с.
Дерхам Х.М. Взаимодействие тяжелых металлов (медь и цинк) с органическими и минеральными компонентами почв. Дис. … канд. биол. н. М., 2009. 196 с.
Заварзина А.Г., Данченко Н.Н., Демин В.В., Артемьева З.И., Когут Б.М. Гуминовые вещества – гипотезы и реальность (обзор) // Почвоведение. 2021. № 12. С. 1449–1480. https://doi.org/10.31857/S0032180X21120169
Ладонин Д.В., Карпухин М.М. Фракционный состав соединений никеля, меди, цинка и свинца в почвах, загрязненных оксидами и растворимыми солями металлов // Почвоведение. 2011. № 8. С. 953–965.
Пампура Т.В., Пинский Д.Л., Остроумов В.Г., Гершевич В.Д., Башкин В.Н. Экспериментальное изучение буферности чернозема при загрязнении медью и цинком // Почвоведение. 1993. № 2. С. 104–111.
Переломов Л.В., Пинский Д.Л. Формы Мn, Рb и Zn в серых лесных почвах Среднерусской возвышенности // Почвоведение. 2003. № 6. С. 682–691.
Пинский Д.Л. Современные представления о механизмах поглощения тяжелых металлов почвами // Эволюция, функционирование и экологическая роль почв как компонента биосферы. Пущино, 2020. С. 55–64.
Пинский Д.Л., Минкина Т.М., Федоров Ю.А., Бауэр Т.В., Невидомская Д.Г. Особенности поглощения Cu(II), Pb(II) и Zn(II) черноземом обыкновенным из растворов нитратов, хлоридов, ацетатов и сульфатов // Почвоведение. 2014. № 1. С. 22–29.
Холодов B.А., Кирюшин А.В., Ярославцева Н.В., Фрид А.С. Связывание меди(II) необратимо сорбированными на каолините и свободными гуминовыми веществами // Почвоведение. 2014. № 7. С. 803–811.
Шаймухаметов М.Ш. К методике определения поглощенных Са и Мg в черноземных почвах // Почвоведение. 1993. № 12. С. 105–111.
Bauer T.V., Pinskii D.L., Minkina T.M., Shuvaeva V.A., Soldatov A.V., Mandzhieva S.S., Tsitsuashvili V.S., Nevidomskaya D.G., Semenkov I.N. Application of XAFS and XRD methods for describing the copper and zinc adsorption characteristics in hydromorphic soils // Environmental Geochemistry and Health. 2020. P. 1–13.
Burachevskaya M., Minkina T., Bauer T., Mandzhieva S., Gulsage J. (Gülser C.), Kızılkaya R., Sushkova S., Rajput V. Assessment of extraction methods for studying the fractional composition of Cu and Zn in uncontaminated and contaminated soils // Euras. J. Soil Sci. 2020. V. 9. № 3. P. 231–241. https://doi.org/10.18393/ejss.734601
Chernyshov A.A., Veligzhanin A.A., Zubavichus Y.V. Structural materials science end-station at the Kurchatov synchrotron radiation source: Recent instrumentation upgrades and experimental results // Nuclear Instruments and Methods in Physics Research Section A: Accelerators, Spectrometers, Detectors and Associated Equipment. 2009. V. 603. № 1–2. P. 95–98. https://doi.org/10.1016/j.nima.2008.12.167
Evans Z.C., Ryswyk H.V., Huertos M.L., Srebotnjak T. Robust spatial analysis of sequestered metals in a Southern California Bioswale // Sci. Total Environ. 2019. V. 650. P. 155–162. https://doi.org/10.1016/j.scitotenv.2018.08.441
Fernández-Ondoño E., Bacchetta G., Lallena A.M., Navarro F.B., Ortiz I., Jime’nez M.N. Use of BCR sequential extraction procedures for soils and plant metal transfer predictions in contamnated mine tailings in Sardinia // J. Geochemical Exploration. 2017. V. 172. P. 133–141. https://doi.org/10.1016/j.gexplo.2016.09.013
Ghayoraneh M., Qishlaqi A. Concentration, distribution and speciation of toxic metals in soils along a transect around a Zn/Pb smelter in the northwest of Iran // J. Geochem. Exploration. 2017. V. 180. P. 1–14. https://doi.org/10.1016/j.gexplo.2017.05.007
Gomes P.C., Fontes M.P.F., da Silva A.G., Mendoca E.S., Netto A.R. Selectivity sequence and competitive adsorption of heavy metal by Brazilian soils // Soil Sci. Soc. Am J. 2001. V. 65. № 4. P. 1115–1121. https://doi.org/10.2136/sssaj2001.6541115x
Huang L., Jin Q., Tandon P., Li A., Shan A., Du J. High-resolution insight into the competitive adsorption of heavy metals on natural sediment by site energy distribution // Chemosphere. 2018. V. 197. P. 411–419. https://doi.org/10.1016/ j.chemosphere.2018.01.056
Kirpichtchikova T.A., Manceau A., Spadini L., Panfili F., Marcus M.A., Jacquet T. Speciation and solubility of heavy metals in contaminated soil using X-ray microfluorescence, EXAFS spectroscopy, chemical extraction, and thermodynamic modeling // Geochim. Cosmochim. Acta. 2006. V. 70. № 9. P. 2163–2190. https://doi.org/10.1016/j.gca.2006.02.006
Leermakers M., Mbacho B.E., Husson A., Lagneau V., Descostes M. An alternative sequential extraction scheme for the determination of trace elements in ferrihydrite rich sediments // Talanta. 2019. V. 199. P. 80–88. https://doi.org/10.1016/j.talanta.2019.02.053
Manceau A., Marcus M.A., Tamura N. Quantitative speciation of heavy metals in soils and sediments by synchrotron X-ray techniques // Rev. Mineral. Geochem. 2002. V. 49. № 1. P. 341–428. https://doi.org/10.2138/gsrmg.49.1.341
McBride M.B. Environmental chemistry of soils. New York. Oxford University Press, 1994. 416 p.
Mekapogu M., Nadimikeri J., Madri P.K., Devi S. A study on zinc speciation of Tungabhadra River sediments, Kurnool, south India: A tool in metal pollution monitoring // International J. Sediment Res. 2018. V. 33. № 4. P. 510–517. https://doi.org/10.1016/j.ijsrc.2017.11.001
Miller P.W., Martens D.C., Zelazny L.W. Effect of sequence in extraction of trace metals from soils // Soil Sci. Soc. Am. J. 1986. V. 50. № 3. P. 598–601. https://doi.org/10.2136/sssaj1986.03615995005000030011x
Minkina T., Nevidomskaya D., Bauer T., Shuvaeva V., Soldatov A., Mandzhieva S., Zubavichus Y., Trigub A. Determining the speciation of Zn in soils around the sediment ponds of chemical plants by XRD and XAFS spectroscopy and sequential extraction. // Sci. Total Environ. 2018. V. 634. P. 1165–1173. https://doi.org/10.1016/j.scitotenv.2018.04.118
Minkina T., Nevidomskaya D., Burachevskaya M., Bauer T., Shuvaeva V., Soldatov A., Mandzhieva S., Zubavichus Y. Possibilities of chemical fractionation and X-ray spectral analysis in estimating the speciation of Cu2+ with soil solid-phase components // Appl. Geochem. 2019. V. 102. P. 55–63. https://doi.org/10.1016/j.apgeochem.2019.01.005
Misono M., Ochiai E.I., Saito Y., Yoneda Y. A new dual parameter scale for the strength of Lewis acids and bases with the evaluation of their softness // J. Inorg. Nuclear Chem. 1967. V. 29. № 11. P. 2685–2691. https://doi.org/10.1016/0022-1902(67)80006-X
Nannoni F., Protano G., Riccobono F. Fractionation and geochemical mobility of heavy elements in soils of a mining area in northern Kosovo // Geoderma. 2011. V. 161. № 1–2. P. 63–73. https://doi.org/10.1016/j.geoderma.2010.12.008
Pueyo M., Mateu J., Rigol A., Vidal M., López-Sánchez J.F., Rauret G. Use of the modified BCR three-step sequential extraction procedure for the study of trace element dynamics in contaminated soils // Environ. Poll. 2008. V. 152. № 2. P. 330–341. https://doi.org/10.1016/j.envpol.2007.06.020
Salvador-Blanes S., Minasny B., McBratney A. B. Modelling long-term in situ soil profile evolution: Application to the genesis of soil profiles containing stone layers // Eur. J. Soil Sci. 2007. V. 58. № 6. P. 1535–1548. https://doi.org/10.1111/j.1365-2389.2007.00961.x
Scheinost A.C., Kretzschmar R., Pfister S., Roberts D.R. Combining selective sequential extractions, X-ray absorption spectroscopy, and principal component analysis for quantitative zinc speciation in soil // Environ. Sci. Technol. 2002. V. 36. № 23. P. 5021–5028. https://doi.org/10.1021/es025669f
Sere G., Schwartz Ch., Ouvrard S., Renat J.-Ch., Watteau F., Villemin G., Morel J.L. Early pedogenic evolution of constructed Technosols // J. Soils Sediments. 2010. V. 10. № 7. P. 1246–1254.
Smolentsev G.Y., Soldatov A.V. Quantitative local structure refinement from XANES: multi-dimensional interpolation approach // J. Synchrotron Radiation. 2006. V. 13. № 1. P. 19–29. https://doi.org/10.1107/S0909049505038975
Sposito G. The chemistry of soils. New York: Oxford University Press, 1989. 344 p.
Strawn D.G., Baker L.L. Speciation of Cu in a contaminated agricultural soil measured by XAFS, µ-XAFS, and µ-XRF // Environ. Sci. Technol. 2008. V. 42. № 1. P. 37–42. https://doi.org/10.1021/es071605z
Sulkowski M., Hirner A.V. Element fractionation by sequential extraction in a soil with high carbonate content // Appl. Geochem. 2006. V. 21. № 1. P. 16–28. https://doi.org/10.1016/j.apgeochem.2005.09.016
Sutherland R.A., Tack F.M.G., Tolosa C.A., Verloo M.G. Operationally defined metal fractions in road deposited sediment, Honolulu, Hawaii // American Society of Agronomy, Crop Science Society of America, and Soil Science Society of America, 2000. V. 29. № 5. P. 1431–1439. https://doi.org/10.2134/jeq2000.00472425002900050009x
Singh B., Grafe M. Synchrotron-Based techniques in soils and sediments. Amsterdam: Elsevier, 2010. 480 p.
Tessier P.G.C., Campbell M.B. Sequential extraction procedure for the speciation of particulate trace metals // Analyt. Chem. 1979. V. 51. № 7. P. 844–851. https://doi.org/10.1021/ac50043a017
Ure A., Quevaullier P.H., Muntau H., Griepink B. Speciation of heavy metals in soils and sediments. An account of the improvement and harmonization of extraction techniques undertaken under the auspices of the BCR of the CEC // Int.J. Environ. Analyt. Chem. 1993. V. 51. № 1–4. P. 135–151. https://doi.org/10.1080/03067319308027619
Voegelin A., Tokpa G., Jacquat O., Barmettler K., Kretzshmar R. Zinc fractionation in contaminated soils by sequential and single extractions: Influence of soil properties and zinc content // J. Environ. Quality. 2008. V. 37. № 3. P. 1190–1200. https://doi.org/10.2134/jeq2007.0326
Zwolak A., Sarzyńska M., Szpyrka E., Stawarczyk K. Sources of Soil Pollution by Heavy Metals and Their Accumulation in Vegetables: a Review // Water Air and Soil Pollution. 2019. V. 230. № 7. P. 1–10.
Дополнительные материалы отсутствуют.


