Поверхность. Рентгеновские, синхротронные и нейтронные исследования, 2019, № 5, стр. 99-104
Химический состав, структура и функциональные свойства покрытий каналов микроканальных пластин
Б. М. Кучумов 1, *, С. В. Забуслаев 2, **, Ю. В. Шевцов 1, Ю. В. Шубин 1, С. В. Трубин 1, А. И. Романенко 1, И. К. Игуменов 1
1 Институт неорганической химии Сибирского отделения РАН
630090 Новосибирск, Россия
2 АО “Катод”
630047 Новосибирск, Россия
* E-mail: kbm@niic.nsc.ru
** E-mail: zabuslayev@mail.ru
Поступила в редакцию 25.02.2018
После доработки 17.03.2018
Принята к публикации 17.03.2018
Аннотация
Для обеспечения необходимой электрической проводимости микроканальных пластин предложено использовать тонкую пленку RuOx путем ее нанесения на стенки каналов с помощью импульсного метода осаждения металлоорганических соединений из газовой фазы. На образцах-спутниках исследован химический состав, структура, электропроводность и вторичная электронная эмиссия. Показано, что пленка RuOx имеет глобулярное строение с характерным размером ~100 нм. Ядро глобулы (средний размер ~21 нм) представляет собой смесь фаз Ru и RuО2 в соотношении примерно 4 : 6. Остальная часть глобулы аморфна, а отношение Ru к RuО2 в ней составляет ~5.4 : 4.6. Электропроводность пленок носит металлический характер. После отжига на воздухе при температурах до 800°С коэффициент вторичной электронной эмиссии RuOx возрастает от 2.5 до ~4.
ВВЕДЕНИЕ
Микроканальные пластины с успехом используются не только в приборах ночного видения, но и в самых различных сферах и областях науки и техники: в экспериментальной физике, аэрокосмической технике, атомной технике, неразрушающем контроле качества, биологии, экологии, медицине, астрономии [1, 2].
При использовании микроканальных пластин на стеклянной основе в качестве усилителей потока электронов возникает ряд проблем, таких как разложение и десорбция разнообразных продуктов, прежде всего, катионов щелочных металлов, которые приводят к деградации проводящего и эмиссионного слоев [3].
Для улучшения характеристик усилителей яркости изображений, основным элементом которых является микроканальная пластина, было предложено модифицировать стенки каналов путем последовательного нанесения различных функциональных слоев, блокирующих выход ионов щелочных металлов из объема на поверхность канала, обеспечивающих необходимое электрическое сопротивление и повышенный коэффициент вторичной электронной эмиссии [4].
В настоящей работе основное внимание уделено проблеме формирования на поверхности каналов пластин проводящего слоя, в качестве которого был выбран оксид рутения (RuO2). Оксид рутения обладает рядом уникальных физических свойств, в том числе проводимостью электронного типа, и характеризуется высокой стабильностью электрофизических и физико-химических параметров [5, 6].
Стандартные микроканальные пластины содержат 106 каналов диаметром ~6 мкм и длиной 300 мкм (аспектное отношение 50). Практически единственным методом формирования покрытий в подобных системах являются различные варианты метода химического осаждения из газовой фазы (MOCVD – Metalorganic Chemical Vapour Deposition) [2, 4].
Основной задачей настоящей работы было исследование процессов формирования внутри каналов микроканальных пластин с блокирующим слоем из диоксида гафния проводящих слоев оксида рутения и исследование их свойств.
МЕТОДИКА ЭКСПЕРИМЕНТОВ И МЕТОДЫ ИССЛЕДОВАНИЯ
Осаждение слоев проводили в оригинальном импульсном MOCVD-реакторе, оснащенном дискретными “горячими” источниками паров прекурсоров с пневматическим управлением, которое осуществлялось программными средствами на компьютере [7].
Подложками служили микроканальные пластины (диаметр каналов 6–7 мкм) и образцы-свидетели на пластинах кремния, покрытых тонким слоем HfO2 (70–85 нм), чистых пластинах кремния (100) и ситалла (500 мкм). В экспериментах по выращиванию оксидных пленок рутения проводили от 20 до 200 циклов осаждения. Единичный цикл представляет последовательность следующих операций. После достижения требуемого вакуума реакционную камеру отсекают от системы откачки и в нее подают порцию газообразного прекурсора в течение 20 с. Далее в реакционную камеру подают смесь газов-реактантов, время экспозиции 30–60 с. На заключительной стадии осуществляют откачку реакционной камеры в течение 30 с до остаточного давления ~10–2 Торр.
Температуру нагрева подложек варьировали в интервале 350–370°С. В качестве прекурсора был использован трис-ацетилацетонат рутения Ru(acac)3. Температура испарителя прекурсора составляла 187 ± 2°С. Газом-реактантом была смесь кислорода и паров воды.
Единичная загрузка Ru(acac)3 в испаритель составляла ~100 мг, давление прекурсора в реакционной камере объемом 1000 мл3 было ~0.2 Торр. Подача газов-реактантов обеспечивала четырехкратное превышение содержания кислорода в реакционной камере над стехиометрическим соотношением. Толщина пленки, выращиваемой за один цикл осаждения, составляла около ~3 Å.
Состав, структура и функциональные свойства полученных слоев были изучены различными методами. Морфологию поверхности исследовали с помощью растрового электронного микроскопа JEOL JSM-6700F. Распределение химического состава по длине каналов пластины изучали методом энергодисперсионного анализа в растровом электронном микроскопе Hitachi TM3000 с использованием блоков Scan Generator, XFlash MIN SVE и программы Quantax 70. Структурно-фазовый состав исследовали на рентгеновском дифрактометре Shimadzu XRD-7000 (CuKα-излучение, Ni-фильтр).
Химический состав поверхности образца (ламинатной структуры RuOx/HfO2/Si) был определен методом рентгеновской фотоэлектронной спектроскопии (РФЭС) на спектрометре фирмы SPECS. Для возбуждения РФЭ-спектров использован источник монохроматического излучения алюминия с энергией линии AlKα 1486.74 эВ, мощность источника составляла 200 Вт, диаметр рентгеновского пучка около 1 мм. Полученные спектры обрабатывали с помощью специализированного программного обеспечения CASA, поставляемого с прибором. Калибровку энергии связи осуществляли методом внутреннего стандарта по энергии линии Hf4f7/2 17.6 эВ в массивном образце оксида гафния HfO2 [8]. Заряд с поверхности образца снимали пушкой с медленными электронами. Ускоряющее напряжение и ток катода подбирали по минимуму ширины линии на половине высоты пика. Для очистки образца от поверхностных загрязнений использовали бомбардировку ионами аргона при давлении в камере 3 × 10–6 Торр, напряжение 2.5 кВ, время очистки 35 мин.
Коэффициенты вторичной электронной эмиссии σ измеряли в вакууме ~10–6 Па на ранее созданной установке, подробно описанной в [9]. Первичный ток электронного пучка IP определяли с использованием цилиндра Фарадея, в который собирались все первичные электроны. Затем под электронно-оптическую систему подводили исследуемый образец. С помощью блока управления получали развертку по энергии электронов и измеряли зависимость вторичного тока IS от энергии электронов первичного пучка ЕP. Истинное значение σ(EP) определяли как отношение IS/IP .
Калибровку установки проводили на образце платины, для которой зависимость σ(ЕР) детально исследована и описана в литературе. Относительная погрешность измерения σ составляет 3% в режиме измерения на постоянном токе первичного пучка электронов и 5% в импульсном режиме.
Температурные зависимости электросопротивления измеряли четырехконтактным методом в интервале температур 4.2–300 К. Экспериментальные данные регистрировали с помощью системного вольтметра Solartron 7061 и выводили на компьютер в реальном времени.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Распределение химических элементов по длине канала. Оптимизацию процессов осаждения конформных слоев RuOх по длине каналов микроканальных пластин проводили в широком интервале экспериментальных параметров. При выборе режимов осаждения использовали данные, полученные ранее в экспериментах с модельными щелевыми структурами, состоящими из микроканальной пластинки и крышки, в интервале аспектных отношении 2–10.
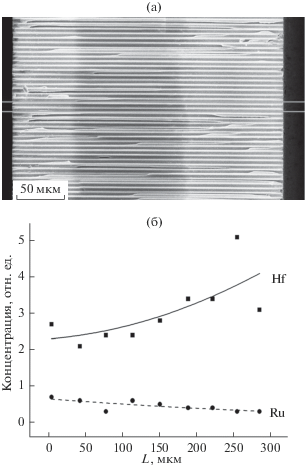
Пластинка, на стенки каналов которой были нанесены два слоя – HfO2/RuOх, была использована для анализа распределения металлов по длине каналов. Слои HfO2 были получены на той же установке по методике, описанной в [7]. На рис. 1а представлено РЭМ-изображение каналов, полученных при разломе микроканальной пластины, а распределение компонентов по длине каналов – на рис. 1б. Как видно из рисунка, удалось достичь достаточно однородного распределения Ru по длине канала.
Рис. 1.
РЭМ-изображение канала разломанной микроканальной пластинки (а) и распределение Hf и Ru по его длине (б).
Морфология полученных слоев. Результаты исследования морфологии поверхности слома образцов-свидетелей RuOx/HfO2/Si представлены на рис. 2, из которого видно, что подслой HfO2 конформно покрывает поверхность кремния, а глобулы RuOx со средним размером ~100 нм неоднородно распределены по поверхности Si.
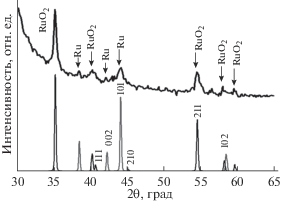
Структура. На рис. 3 представлена дифрактограмма образца RuOх/Si. Съемка проводилась при пошаговом сканировании в области углов 2θ = 30°–65°. Размер кристаллитов (области когерентного рассеяния – ОКР) определяли по уширению дифракционных рефлексов с помощью программы WINFIT 1.2.1 [10]. Образец содержит в качестве основной фазы оксид рутения (RuO2). Средний размер ОКР 21 нм. Отношение атомных концентраций Ru к RuO2 в них составляет ~4 : 6. Если сопоставить эти данные с характерным размером глобул ~100 нм, полученным методом растровой электронной микроскопии, и учесть размытие пиков на рис. 3, то можно предположить, что их основная часть аморфная.
Рис. 3.
Дифрактограмма образца RuOх/Si: верхняя кривая – экспериментальный спектр, нижняя – расчетный. Ru – гексагональная модификация (PDF № 6-663), пр. гр. P63/mmc (№ 194); a = 2.7058 Å, c = 4.2819 Å; Dm = 12.200, Dx = 12.438 г/см3; Z = 2. RuO2 – тетрагональная модификация (PDF № 70-2662), пр. гр. P42/mnm (№ 136); a = 4.48 Å, c = 3.105 Å; Dx = = 7.062 г/см3; Z = 2.
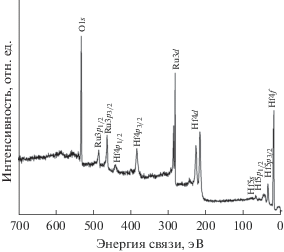
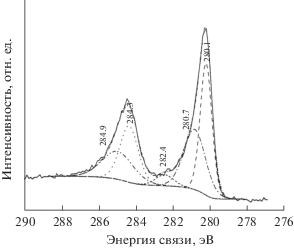
Химический состав. Состав поверхности после бомбардировки ионами аргона представлен на графике обзорного спектра (рис. 4). На рис. 5 показан детальный спектр линии Ru3d. Рутений в образце находится в двух состояниях – с энергией связи Ru3d7/2 280.1 и 280.7 эВ. Это соответствует металлическому и оксидному (RuO2) состояниям со степенями окисления рутения ноль и четыре соответственно [11]. Содержание металлического рутения в слое составляет 54 ± 5 ат. %, а RuO2 – 46 ± 5 ат. %. Тут нет противоречия с данными рентгенофазового анализа, так как кристаллическая часть глобулы по объему составляет ~1/1000. Вероятно, при образовании кристаллического ядра глобулы избыточный рутений вытесняется в ее объем.
Незначительный пик при энергии связи 282.4 эВ по данным базы [12] можно интерпретировать как углерод в карбиде. Отнести его к какому-либо конкретному соединению не представляется возможным вследствие малого количества. Линия кислорода O1s также состоит из трех компонент со значениями энергии связи 530.1, 530.7 и 532.0 эВ (рис. 4). Такие состояния характерны для оксида гафния (530.1 эВ), оксида рутения RuO2 (530.7 эВ) и адсорбированной на металлах группы СО [12].
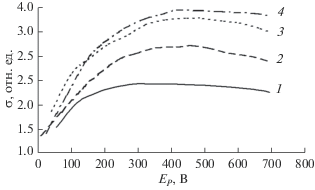
Вторичная электронная эмиссия. Были измерены коэффициенты вторичной электронной эмиссии как исходных слоев RuOх на Si подложках, так и отожженных на воздухе при различных температурах 600, 700 и 800°С (рис. 6). Для исходных слоев максимальное значение составляет ~2.5. Отжиг приводит к увеличению коэффициента до ~4. Вероятно, происходит окисление металлического рутения, так как коэффициент вторичной электронной эмиссии для оксидов, как правило, выше, чем для соответствующих металлов.
Рис. 6.
Зависимость коэффициента вторичной электронной эмиссии для пленки RuOx/Si от энергии падающих электронов в случае исходного RuOх (1) и после отжига при 600 (2), 700 (3), 800°С (4).
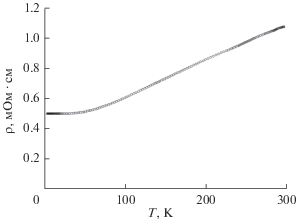
Электросопротивление. Температурная зависимость удельного электросопротивления пленки RuOx (эллипсометрическая толщина ~50 нм), осажденной на кремнии, приведена на рис. 7. РЭМ-изображение этих слоев представлено на рис. 8а. Эта температурная зависимость соответствует металлам во всем интервале температур, что обусловлено металлическим характером проводимости как Ru, так и RuO2, присутствующих в пленках RuOx, а также хорошими металлическими контактами между глобулами.
Отношение сопротивлений ρ300К/ρ4.2К ~ 2 также указывает на поликристалличность пленки и ее неоднородность, что подтверждается данными электронной микроскопии (рис. 8). Более тонкая пленка (менее 10 нм по данным эллипсометрии) при комнатной температуре имеет электросопротивление существенно больше 108 Ом (рис. 8б), что обусловлено значительными разрывами контактов между глобулами.
ЗАКЛЮЧЕНИЕ
Изменение соотношения парциальных давлений газовой фазы прекурсора и газов-реактантов и температурных параметров процесса осаждения слоев определяет функциональные свойства полученных оксидных поликристаллических слоев. Оптимизация этих параметров позволила получить достаточно однородное распределение оксида рутения по длине канала микроканальной пластинки.
По данным рентгенофазового анализа полученные поликристаллические пленки содержат в своем составе две фазы Ru и RuO2 в соотношении ~4 : 6, и средний размер кристаллической части составляет ~21 нм. Отношение содержания Ru и RuO2 в пленке RuOx за счет наличия значительной доли аморфной фазы в глобулах со средним размером 100 нм, составляет ~5.4 : 4.6 по данным РФЭС.
Управлять электросопротивлением полученных слоев можно, изменяя как соотношение Ru/RuO2 (но при этом останется достаточно высокая проводимость и необходимы более высокие температуры осаждения), так и плотность глобул RuOx на поверхности подложки (электросопротивление может достигать очень высоких значений) посредством изменения числа циклов осаждения слоев и используя диэлектрические подложки, на которых плотность зарождающихся глобул RuOx значительно ниже.
Измеренные значения коэффициента вторичной электронной эмиссии показали, что пленка RuOx не ухудшает эмиссионных характеристик, так как они сравнимы или выше характеристик стандартного состава поверхности каналов микроканальной пластинки на основе SiO2.
Список литературы
Siegmund O.H.W., McPhatea J.B., Tremsina A.S. et al. // Phys. Procedia. 2012. V. 37. P. 803.
O’Mahony A., Craven Ch.A., Minot M.J. et al. // J. Vac. Sci. Tech. A. 2016. V. 34. № 1. P. 01A128. http://doi.org/https://doi.org/10.1116/1.4936231.
Кулов С.К., Савенко В.И., Щапова Ю.В. и др. // Инженерный вестн. Дона. 2011. № 2.
Yan B., Liu Sh., Heng Yu. // Nanoscale Res. Lett. 2015. № 10. P. 162.
Zhong H., Heuss G., Suh Y.-S. et al. // J. Electronic Mater. 2001. V. 30. № 12. P. 1493.
Lin J.J., Huang S.M., Lin Y.H. et al. // J. Phys.: Condens. Matt. 2004. V. 16. P. 8035.
Шевцов Ю.В., Кучумов Б.М., Семенов А.Р., Игуменов И.К. // Приборы и техника эксперимента. 2013. № 3. С. 116.
Renault O., Samour D., Damlencourt J.-F. et al. // Appl. Phys. Lett. 2002. V. 81. P. 3627.
Забуслаев С.В., Габдулин П.Г., Шевцов Ю.В. и др. // Заводская лаборатория. Диагностика материалов. 2013. Т. 79. С. 38.
Krumm S. // Mater. Sci. Forum. 1996. V. 228–231. P. 183.
Moulder J.F., Stickle W.F., Sobol P.E., Bomben K.D. // Handbook of X-ray Photoelectron Spectroscopy. Physical Electronics, Inc., 1995. P. 115.
National Institute of Standards and Technology (NIST). https://srdata.nist.gov/xps.
Дополнительные материалы отсутствуют.
Инструменты
Поверхность. Рентгеновские, синхротронные и нейтронные исследования