Расплавы, 2021, № 1, стр. 21-45
Коррозия перспективных металлических материалов во фторидных расплавах для жидкосолевых реакторов
Е. В. Никитина a, b, *, Э. А. Карфидов a, b, Ю. П. Зайков a, b
a Институт высокотемпературной электрохимии УрО РАН
Екатеринбург, Россия
b Уральский Федеральный Университет
Екатеринбург, Россия
* E-mail: neekeetina@mail.ru
Поступила в редакцию 02.07.2020
После доработки 25.09.2020
Принята к публикации 08.10.2020
Аннотация
Сопоставлено коррозионное поведение металлических материалов во фторидных расплавах различного состава, изученное зарубежными и отечественными авторами с шестидесятых годов двадцатого века до наших дней, оценено влияние внешних и внутренних факторов коррозии, выявлены общие для всех расплавов характеристики высокотемпературной электрохимической коррозии и выделено влияние химической природы расплава. Во введении обоснована актуальность обзора, его важность и значимость для развития современного материаловедения, физической химии и электрохимии, в частности в области электрохимического материаловедения – для разработки коррозионностойких материалов в ядерной отрасли, в частности, для жидкосолевых реакторов. В основной части содержится краткое описание современного состояния высокотемпературной коррозиологии применительно к исследованиям в расплавах фторидов, специфики способов защиты от коррозии в расплавленных солевых электролитах. Представлен обзор методов исследования коррозионных аспектов взаимодействия металлических материалов с расплавленными солевыми электролитами с учетом электрохимической активности фторидных расплавов различного состава. Проанализированы имеющиеся экспериментальные данные и выявлены фундаментальные закономерности коррозионно-электрохимического поведения металлических материалов в расплавленных солевых электролитах. Предложены эффективные способы защиты от коррозии применительно к высокотемпературным средам, сделаны выводы о целесообразности использования различных металлических материалов в расплавленных солях.
ВВЕДЕНИЕ
Разрушение и деградация материалов под действием химически агрессивных сред – коррозия – серьезная проблема для любого технологического процесса. В солевых расплавах высокая температура и концентрация агрессивных веществ, высокая скорость протекания процесса усиливают до катастрофических масштабов данную проблему как с экономической точки зрения, так и с точки зрения экологической безопасности для промышленности, работающей с солевыми расплавами.
Высокотемпературные электролиты не позволяют применять многие методы снижения коррозионных потерь, применяющиеся в низкотемпературных средах. При этом принципиально изменяется механизм коррозии металлических материалов, резко возрастает ее скорость, изменяется характер коррозионных поражений, и разрушения зачастую приобретают катастрофический характер. Теоретическое описание высокотемпературных коррозионных процессов в настоящее время далеко от совершенства.
Условия работы элементов конструкции ЖСР предъявляют следующие требования к металлическому сплаву:
• высокое сопротивление к окислению;
• совместимость с жидкосолевым топливом и теплоносителем промежуточного контура;
• высокая жаропрочность;
• высокая радиационная стойкость;
• технологичность (возможность штамповки, проката, обработки резанием, свариваемость и т.д.).
Успешное использование расплавленных фторидов щелочных металлов требует создания таких реакторных материалов, которые обладают высокой коррозионной стойкостью в расплавах с характерными для ЖСР-С составами. Это является одной из важнейших нерешенных проблем [1–3]. Экспериментальные данные по коррозии металлических материалов в расплавленных солях содержат ограниченное количество коррозионных характеристик для анализа, к тому же стандарты экспериментальных условий недостаточны или отсутствуют [4].
Расплавленные фторидные соли обладают свойствами, которые позволяют их использовать в качестве солевых растворителей в жидкосолевом реакторе-сжигателе (ЖСР-С) [5–9].
Несмотря на то, что фториды щелочных металлов являются одними из самых агрессивных солей с точки зрения деградации конструкционного материала, применяемого в реакторостроении, именно эти солевые расплавы обладают огромными преимуществами из-за высокой теплопроводности, низкой вязкости, высоких температур кипения, наибольшей теплоемкости на единицу объема и нечувствительности к излучению.
Хотя растворимость трифторида плутония выше в расплаве фторидов лития, натрия, калия, бериллийсодержащий фторидный расплав перспективнее как с точки зрения поглощения нейтронов, так и коррозионной стойкости из-за отсутствия в расплаве иона калия.
Большие преимущества конструкции реакторных систем IV поколения с расплавленными солями заключаются в эффективном использовании топлива, минимальном количестве радиоактивных отходов и экономичном использовании при безопасной и экологически чистой эксплуатации [10–12]. Расплавленные соли можно использовать в качестве теплоносителя реактора или передаточной среды в высокотемпературных технологических тепловых контурах (от ядерных реакторов до производства водорода). Однако серьезнейшей проблемой является коррозия металлических материалов и катастрофическая деградация керамических.
Основные имеющиеся литературные данные по исследованиям коррозии материалов в расплавленных фторидах относятся к проводимым в Национальной лаборатории Ок-Риджа (ORNL) c 1940-х годов исследованиям [13–15]. Кроме того, существует ряд исследований по изучению коррозионных процессов во фторидах щелочных металлов и отечественных авторов, высоким экспериментальным и теоретическим уровнем отличаются работы В.В. Игнатьева [16–18].
Данные работы были также начаты в 40–50-х годах, однако, только в последние годы предполагается реальное использование фторидных расплавов в ядерных технологиях. Необходимо снизить объемы направляемых на захоронение радиоактивных отходов, предполагается извлечение при переработке ОЯТ нептуния, америция, кюрия с последующей их трансмутацией. Для этих целей в настоящее время в России активно ведутся работы по созданию специализированного ЖСР-С минорных актинидов [19–22].
Несмотря на многолетние исследования, в настоящее время не обнаружено устойчивых материалов, не предложены приемлемые способы защиты металлических материалов от катастрофических коррозионных разрушений, имеющих различную природу, существует относительно мало экспериментальных достоверных данных по коррозии.
Попытки снизить скорость коррозии в расплавленных солевых системах сталкиваются с серьезными подчас непреодолимыми ограничениями. В большинстве высокотемпературных технологий, где используются расплавленные соли вообще, традиционно используются сплавы, содержащие высокие концентрации хрома, кремния или алюминия, поскольку эти элементы легко образуют пассивные оксидные пленки, которые по всей вероятности замедляют перенос частиц между металлом и окружающей средой, препятствуя дальнейшей коррозии [23, 24]. Однако в расплавленных галогенидных солях эти оксиды либо не образуются, либо являются нестабильными из-за очень низкой активности кислорода в расплавленных солях. Следовательно, разрушение в значительной степени зависит от межфазных реакций между расплавленной солью и поверхностью чистого металла. Другими словами, механизм коррозии в расплавленных солях намного сложнее, чем в водных средах; образование пассивирующего оксидного слоя на коррозионностойких сплавах становится термодинамически невозможным, в связи с чем, использование многих коррозионностойких сплавов ограничено [25, 26].
Коррозия в жидкосолевых средах реакторов обусловлена несколькими факторами, включающими как термодинамические, так и кинетические аспекты; образованием фторидов компонентами материала (табл. 1 и 2), коррозией из-за присутствия примесей (влаги, кислорода, металлов) и продуктов деления. Компоненты сплава, которые образуют галогениды с самыми отрицательными величинами изобарно-изотермического потенциала, с наибольшей вероятностью переходят из сплава в расплав. Для большинства конструкционных сплавов селективное растворение хрома из сплава в соль в виде фторида является доминирующей формой разрушения материала [27]. Сплав, растворенный из более горячих зон, переносится в более холодные области. Основные примеси должны быть удалены, чтобы предотвратить сильную коррозию металла контейнера. К типичным примесям относятся влага и оксидные примеси, которые вместе с градиентом температуры и гальванической коррозией считаются основными движущими силами коррозии [7, 28]. Кроме того, легирующие элементы, растворенные в расплавленных солях, ускоряют коррозию за счет термодинамического переноса [8]. Также следует отметить влияние возможного образования гелия за счет нейтронного облучения и то, что пузырьки гелия могут способствовать к экстремальному набуханию, шероховатости поверхности и образованию коррозионных волдырей на поверхности [13].
Таблица 1.
Относительные термодинамические стабильности фторидных соединений, образованных из элементов, употребляемых как добавки к сплавам (данные Глассера)
| Элементы | Наиболее устойчивое фторидное соединение | ΔG° при 800°C ккал/г · атом F | ΔG° при 800°C ккал/г · атом F |
|---|---|---|---|
| Al | AlF3 | –87 | –92 |
| Ti | TiF3 | –85 | –90 |
| V | VF2 | –80 | –84 |
| Cr | CrF2 | –72 | –77 |
| Fe | FeF2 | –66 | –66 |
| Nb | NbF5 | –58 | –60 |
| W | WF5 | –46 | –48 |
Предполагалось, что наиболее перспективными и поэтому хорошо изученными коррозионностойкими конструкционными материалами являются сплавы на основе никеля, например инконель и хастеллои. Алюминий как компонент конструкционных материалов наиболее подвержен растворению [29], а склонность к коррозии легирующих компонентов возрастает от никеля и кобальта к железу, хрому, алюминию. Однако имеющиеся литературные данные [30] разрознены и порой противоречивы. Подобные противоречия обусловлены различным качеством проводимых экспериментальных исследований, в том числе, недостаточной предварительной очисткой солей и инертной атмосферы над расплавом.
Инженерная реализация ЖСР существенно зависит от того, насколько успешно может быть решена проблема подбора и создания соответствующих конструкционных материалов [30].
Целью этой работы было собрать и критически изучить результаты имеющихся экспериментальных исследований по коррозии металлических материалов в расплавленных фторидах, а так же систематизировать и разграничить факторы, влияющие на коррозию металлических материалов различного состава и наметить возможные пути защиты от коррозии.
Результаты имеющихся в открытом доступе исследований коррозии с 1960 по 2020 год были обобщены и критически отсортированы по экспериментальным характеристикам, на основе результатов анализа, приведенного в этой работе, даны рекомендации, которыми можно руководствоваться в исследованиях расплавов фторидов применительно к материалам для жидко-солевых реакторов.
АНАЛИЗ ЛИТЕРАТУРНЫХ ДАННЫХ
1. Методы проведения исследований. Структура проведения коррозионных исследований
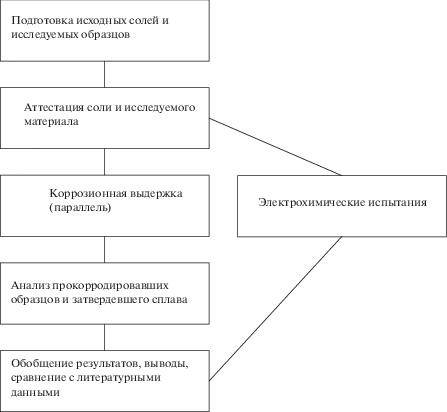
Практически все коррозионные исследования выполняются по одной определенной схеме, однако на определенных этапах случаются различные вариации их проведения, связанные с конкретными требованиями качества исполнения исследования и компетенции исполнителей. Принципиальный общепринятый алгоритм (последовательность) выполнения коррозионных исследований представлен на рис. 1.
Любая небрежность при постановке эксперимента на любом этапе, а так же несвоевременная поверка и калибровка аттестационного оборудования может привести к абсолютно недостоверным получаемым данным.
1.1. Подготовительный этап
Подготовка соли. Галогенидные соли в исходном состоянии обычно содержат значительные количества влаги и прочих примесей. Это означает, что соли должны быть очищены перед использованием [31–36] и аттестованы. Товарная марка используемых солей для приготовления эвтектик никак не может приниматься за истину, пока не будет проведена качественная аттестация. Это связано как с возможными технологическими сбоями в работе изготовителя, так и нарушением условиями их хранения.
Для удаления примесей, присутствующих в солях, во многих работах использовался процесс очистки, в котором соли в расплавленном состоянии продувают барботажными газами для удаления влаги и примесных галогенидов металлов.
Следует отметить, что в ряде применяемых и исследуемых эвтектик присутствует фторид калия – крайне гигроскопичная соль. Однако практически весь высокочистый и пригодный для проведения достоверных экспериментов фторид калия производится и поставляется в виде эквимольного соединения KF–HF. В связи с этим требуется последующая операция удаления фторида водорода из получаемой эвтектики. Это требуется чтобы исключить как его влияние на изучаемые коррозионные процессы, так и воздействие образующихся в ходе экспериментов возгонов, оказывающих разрушительное действие на основной материалы, из которого выполняют исследовательские ячейки – кварц и металл.
Исследователи ORNL использовали смесь HF–H2 для удаления оксидов, сульфидов и металлических примесей из солей фтора, и обнаружили, что этот процесс очень эффективен [14]. Этот процесс был позже использован исследователями из Висконсина [37–39] и Китайской академии наук [40, 41].
В диссертационной работе В.В. Игнатьева особое внимание уделено продувке фтороводорода [16]. В российской экспериментальной практике для удаления влагосодержащих примесей и фторида водорода также широко используется метод очистки солей методом электролиза в контролируемом токе кислорода. Суть данного метода заключается в катодном выделении водорода и анодном – кислорода при заданных токовых характеристиках. Чаще всего в роли катода и анода применяются графитовые стержни, как достаточно инертный материал для данного электрохимического процесса в применяемой среде. Данный метод безопаснее первого, хотя также имеет ряд недостатков, а именно: требует более дорогого и сложного аппаратурного обеспечения, а так же не очищает расплав от большинства катионов металлов.
Подготовка образцов. Подготовка исследуемого материала во всех работах практически идентична. Исследуемый металл нарезается на удобные по площади образцы. Образцы шлифуются с помощью карбидно-кремниевого абразива (различной зернистости), а затем очищаются ультразвуком и последовательно промываются деионизированной водой, ацетоном и метанолом. После этого регистрируется начальная площадь поверхности и масса каждого образца, что в дальнейшем, как и исходная масса соли, используется для расчета ряда коррозионных характеристик.
В ряде случаев, в том числе для электрохимических испытаний исследуемый материал инкапсулируют, что позволяет четко ограничить контактирующую с расплавом поверхность. В электрохимии подобная необходимость также связана с общеизвестной проблемой смачиваемости: нарастания/вытягивания/наползания соли в результате взаимодействия на трехфазной границе. Подобный эффект оказывает негативное влияние на достоверность вольтамперных характеристик, поскольку помимо изменения удельной площади поверхности контакта, добавляется фактор возможного соприкосновения электролита с материалом токоподводов.
Чаще всего в качестве материала для инкапсуляции во фторидах применяется нитрид бора, однако применение данной технологии предполагает необходимость проведения аттестации данного материала, во избежание загрязнения электролита и внутрисистемных взаимодействий.
Аттестация солевой и газовой фаз, металлических образцов. Исходные образцы, смесь солей и газ аттестуют для большей достоверности получаемых коррозионных данных с помощью различных физико-химических методов. В основном применяются следующие методы анализа:
Микрорентгеноспектральный. Позволяет с помощью электронного микроскопа получить информацию о химическом составе образца в произвольно выбранном участке микроскопических размеров.
Гравиметрический. Метод количественного анализа, основанный на точном измерении массы вещества. Использует закон сохранения массы веществ, в том числе, при коррозии.
Рентгенофлюоресцентный. Метод, основанный на сборе и последующем анализе спектра, возникающего при облучении исследуемого материала рентгеновским излучением.
Атомно-абсорбционная спектрометрия. Распространенный в аналитической химии инструментальный метод количественного элементного анализа по атомным спектрам поглощения (абсорбции) для определения содержания металлов в том числе, в растворенных отвердевших расплавах и т.д.
1.2. Коррозионные эксперименты. Виды исследований
Коррозионные испытания в расплавленных солях можно разделить на две основные категории: статические эксперименты, которые включают эксперименты с капсулами и тиглями, а также эксперименты с проточным расплавом солей, использующие контуры с тепловой конвекцией и принудительной конвекцией (петли с накачкой).
Наиболее широко используются статические испытания в расплавленных солях, они широко используются в качестве скрининговых испытаний. Статические испытания могут проводиться в открытом тигле с инертным покрывающим газом или в герметичной капсуле [42, 43]. Без наложения теплового градиента на протекающую соль образец и соль достаточно скоро достигают равновесия, поэтому статические испытания недостаточны для прогнозирования коррозионных процессов при работе реальных реакторов с расплавленной солью, необходимы и проточные эксперименты с тепловым градиентом. Однако капсульные эксперименты являются полезным и экономичным способом проведения экспериментов по первоначальной проверке коррозионной стойкости кандидатных материалов, сравнения сплавов и проведения исследований взаимодействия металлических материалов и прежде всего их отдельных компонентов для изучения физико-химических процессов в солевой среде, газовой атмосфере и твердой фазе.
Испытания в тиглях. Для испытания в тигле образец экспонируют в открытом тигле, содержащем расплавленную соль, в инертной газовой атмосфере. Из-за высокой растворимости кислорода и влаги в расплавленной соли [44] испытания в открытых капсулах, даже в очень чистых атмосферах, подвержены коррозии, обусловленной примесями. Однако испытания в тиглях удобны для электрохимических экспериментов. Гомес-Видаль и соавт. [42–44] и Вигнарубен [45, 46] осуществляли электрохимические измерения в расплавленной соли с использованием открытых тиглей. Для подобных экспериментальных работ чаще всего используется тигель из стеклоуглерода, как наиболее доступного, достаточно инертного (имеющего малую закрытую пористость) и стойкого материала (во фторидах). Применимость платиновых тиглей ограничена их стоимостью.
Герметичные капсульные испытания. Чтобы предотвратить попадание примесей во время эксперимента, коррозионные испытания могут проводиться в герметичных капсулах, метод, используемый исследователями из нескольких учреждений, включая Университет Висконсина [47, 48] и Китайскую академию наук [40, 41, 49]. Такие эксперименты обычно используют металлические капсулы с одним образцом в каждой, которые заполнены твердой солью, заварены в инертной атмосфере и нагреты в печи. Использование герметичных капсул позволяет контролировать загрязнение, выходящее за рамки практического применения с открытыми тиглями, но значительно дороже, чем испытания на тигле, и не позволяет проводить наблюдение или измерение на месте во время воздействия.
Тепловая конвекционная проверка. Эксперименты с тепловой конвекционной петлей добавляют “дополнительный реализм” к испытаниям на коррозию в расплавах соли из-за наложения разницы температур между горячими и холодными участками, которая одновременно управляет потоком через петли и коррозию из-за разности в растворимости продуктов коррозии в зависимости от температуры.
Обширная работа была проделана в Oak Ridge National Laboratory (ORNL) в 1960-х и 1970-х годах с использованием тепловой конвекции для изучения коррозии различных конструкционных материалов во фторидных солях [50–53]. При этом использовали конструкцию, в которой одну сторону петли нагревали с помощью печей сопротивления, в то время как другую сторону не теплоизолировали или активно охлаждали для увеличения температурного градиента.
1.3. Анализ солевой и газовой фазы, металлических материалов после завершения коррозионного эксперимента
После завершения контакта образцов с фторидным расплавом и их извлечения и (или) отмывки производится анализ различными физическими, химическими и физико-химическими методами для определения коррозионных характеристик, выявления механизма, закономерностей происходящих в системе процессов и т.д. Как правило, используется глубинный показатель коррозии, для этого дополнительно требуется измерение плотности образца. При определении количественных показателей коррозионного процесса важное значение имеет технология отмывки образцов с учетом растворимости продуктов коррозии материалов и компонентов исходной солевой смеси в различных растворителях.
Для исследования коррозионных процессов материалов обычно применяются различные методы измерений, в том числе, например, сканирующая электронная микроскопия (РЭМ) [13, 17], методы синхротронного излучения [13], методы лазерной абляции – LA-ICP-MS [18, 19] и спектроскопия лазерного индуцированного пробоя (LIBS) [20, 21].
1.4. Электрохимия
Электрохимические методы, такие как вольтамперометрия, идеально подходят для изучения термодинамических и кинетических закономерностей коррозионных процессов. Электрохимические испытания позволяют определить ряд коррозионных характеристик, важных при изучении коррозии в расплавленных фторидах щелочных металлов, например потенциал и ток коррозии, скорость коррозии и т.д. Наиболее распространенные и современные приборы для измерения различных вольтамперных характеристик – потенциостаты фирмы “AutoLAB”, в основном изучают процессы взаимодействия металлического материала с коррозионноактивной средой в следующих режимах:
• анодная потенциостатическая поляризация, линейная развертка – электрохимическая диагностика системы;
• гальваностатическая линейная развертка – электрохимическая диагностика;
• циклическая вольтамперометрия – диагностика электрохимической системы;
• импедансометрия – определение мгновенной скорости коррозии.
2. Внутренний фактор – состав и структура материала. Исследуемые металлы
С точки зрения сопротивляемости к окислению, а также коррозионной устойчивости в среде расплавленных фторидов, наиболее приемлемыми свойствами, несомненно, обладают сплавы с высоким содержанием никеля. Был предложен [14] механизм межкристаллитной коррозии таких материалов. Коррозия сплавов на основе никеля, содержащих Fe и Сг, в расплавах фторидных солей является комбинацией следующих типов окислительных реакций [3]:
• реакций, связанных с примесями в солях (здесь и далее легирующие элементы в твердом растворе)
• реакций, связанных с примесями в объеме или на поверхности металла, ведущих к реакции, например:
Влияние этих необратимых реакций, может быть уменьшено поддержанием низкого содержания примесей в солях и на поверхности металла. Также имеют значение неотъемлемые для фторидных систем процессы:
Реакция UF4 с хромом сильно зависит от среды протекания реакции. В расплавах, состоящих преимущественно из NaF–ZrF4 или NaF–ВеF2, в реакции образуется только двухвалентный хром, т.е.
Однако в случае смеси NaF–КF–LiF–UF4, реакция между хромом и UF4 приводит к образованию как двухвалентного, так и трехвалентного хрома. В равновесии приблизительно 80% полного количества ионов хрома в смеси являются трехвалентными
Химическое равновесие между этими двумя компонентами нарушается в системах с однородным составом сплава, где циркулирующая соль непрерывно испытывает изменение температуры. В таких системах хром имеет тенденцию к постоянному удалению из более горячих участков и осаждению в более холодных участках.
Вследствие окисления хрома компонентами топливонесущей соли, сплавы с большим процентным содержанием этого элемента не были удовлетворительными в качестве контейнерных материалов, за исключением температур, при которых скорость диффузии в сплавах является относительно низкой.
Соответственно, были также проведены исследования коррозионного поведения нескольких промышленных сплавов, в которых хром не был основной легирующей добавкой. На основе этих испытаний было найдено, что сплавы никеля и молибдена являются наиболее многообещающими для контейнерной системы с достижением относительно высоких рабочих температур в реакторе. К сожалению, промышленно доступные никель-молибденовые сплавы, показывающие отличные коррозионные свойства, не являются вполне подходящими для предполагаемых реакторных систем вследствие трех неблагоприятных характеристик:
1) плохая обрабатываемость;
2) тенденция к упрочнению при старении и охрупчиванию при эксплуатационных температурах между 650 и 815°С;
3) низкая устойчивость к окислению атмосферой при повышенных температурах.
Окалина, образующаяся на этих сплавах при их выдержке в воздухе с высокой температурой, была по типу молибдата никеля NiМоО4, который при термическом циклировании между 760 и 350°С испытывал фазовый переход и раскалывался вследствие результирующего изменения объема.
Однако в ходе разработки сплавов стало возможным устранить нежелательные свойства промышленных материалов с сохранением присущей им коррозионной устойчивости. Первоначальной целью было получение сплава, который не охрупчивается при термических воздействиях, связанных с работой реактора. При экспериментах с различными составами бинарных никель-молибденовых сплавов было установлено, что понижение концентрации молибдена до уровня 15–17% позволяет избежать нежелательных эффектов упрочнения при старении, было необходимо увеличить окислительные и прочностные характеристики системы с помощью дополнительных легирующих элементов.
Многолетние исследования в этих направлениях многих мировых центров показали, что сплав на основе никеля, содержащий 17% Мо, 7% Сг, 5% Fe и другие металлы, обозначенный как хастеллой Н, обладает наилучшим сочетанием прочности и коррозионной устойчивости среди испытанных композиций сплавов. Этот сплав был создан в Окриджской [10] национальной лаборатории в качестве материала для хранения расплавленных фтористых солей. Он устойчив по отношению к расплавленным фторидным солям (циркония, бериллия, лития, натрия, калия, тория и урана) в температурном интервале 704–871°С. Заметное окисление данного сплава при контакте с кислородсодержащей атмосферой отсутствует при температурах до 649°С. В испытаниях (без облучения) более чем двухлетней продолжительности глубинный показатель коррозии сплава хастеллой Н расплавленными фторидными солями при температурах до 704°С составлял менее чем 0.025 мм/год, поэтому традиционно ожидается, что именно этот сплав будет наиболее востребован для конструкционного оформления устройств в средах, содержащих фториды при высоких температурах.
Этот сплав содержит 17% Мо для обеспечения жаропрочности и 6–8% хрома для сопротивления окислению. Испытания хастеллоя Н на экспериментальных петлях и в процессе работы реактора MSRE показали, что этот сплав обладает достаточной жаропрочностью, не подвержен радиационному распуханию при флюенсе до 10 нейтр./см), а его коррозия в среде расплавленных фторидов, содержащих полный набор продуктов деления, очень низка [10]. Однако радиационная стойкость сплавов этого типа недостаточна, механические свойства сплава претерпели значительные изменения при флюенсе быстрых нейтронов (Е > 0.5 МэВ), набранном за 166 сут экспозиции в реакторе, равном 3 · 1020 нейтр./см2 и средней температуре образцов 650°С [30]. Потребовалась его дальнейшая модификация для уменьшения явлений радиационного охрупчивания и межкристаллитного растрескивания.
В Окридже также изучались свойства никель-молибденовых сплавов с различными упрочняющими легирующими добавками, причем в условиях циркуляции расплава от 815 до 650°С. Сплавы, выбранные для изучения, содержали от 17 до 20% Мо и различные процентные доли Сr, А1, Тi, V, Fe, Nb, W. Контуры из отдельных сплавов подвергались воздействию солевой смеси (11.2NaF–45.3LiF–41KF–2.5UF4 мол. %) в течение 500 и 1000 ч. Измерение концентраций продуктов коррозии в солевых образцах после испытания показало возрастание коррозионной чувствительности при введении легирующих добавок в следующем порядке: Fe, Nb, V, Сг, W, Тi и А1. За исключением вольфрама, подверженность этих элементов коррозии возрастала приблизительно в том же порядке, что устойчивости фторидных соединений этих элементов. Однако металлографические исследования поверхностей контуров показали относительно слабое воздействие добавок для всех сплавов, за исключением сплавов, содержащих совместные добавки алюминия с титаном или алюминия с хромом [30]. Концентрации продуктов коррозии, связанные с легирующими добавками железа, ниобия, вольфрама были намного меньше, когда эти элементы присутствовали в многокомпонентных сплавах, по сравнению с простыми тройными сплавами. Причина такого поведения связана с наличием более химически активных легирующих добавок в многокомпонентных сплавах. Концентрации продуктов коррозии хрома для сплавов, содержащих алюминий и хром, были такими же, что и в сплавах, содержащих только хром. Аналогично, наличие алюминия не изменило количество продуктов коррозии титана в титансодержащих сплавах. В то же время, концентрации продуктов коррозии, связанные с хромом, титаном или алюминием, не изменялись при наличии других легирующих добавок [30].
Оптические, электронно-микроскопические исследования микроструктуры, структурно-фазовый анализ совместно с данными по коррозионным и механическим характеристикам показывают, что основной причиной межкристаллитного растрескивания является гетерофазность твердого раствора, которая приводит к выделению избыточных карбидных и интерметаллидных фаз, как в матрице, так и особенно на границах зерен. Благотворное влияние алюминия на повышение стойкости к межкристаллитной коррозии (МКК) состоит в уменьшении и изменении характера выделения карбидных фаз по границам зерен: карбидная фаза выделяется не сплошным, а прерывистым образом в виде частиц округлой формы, удаленных на достаточно большие расстояния друг от друга. Уменьшением гетерофазности объясняется также и факт улучшения коррозионных характеристик сплава при Т = 800°С и τ = 2400 ч [30].
Дальнейшие работы привели к созданию модифицированной композиции хастеллоя Н, имеющей более низкое содержание Мо (до 12%) и Si (0.1%) и от 1 до 2% Nb в качестве карбидообразующей присадки. Такой сплав оказался значительно менее подверженным охрупчиванию под действием нейтронов и межкристаллитному растрескиванию при внедрении атомов теллура. По оценкам, выполненным в ORNL, сплав, легированный ниобием в пределах 1–2%, обеспечит требуемые прочностные и коррозионные характеристики в течение 30 лет работы топливного контура с максимальной температурой до 650°С.
Разработка жаропрочного и коррозионностойкого сплава, совместимого с расплавленными фторидами и имеющего высокую радиационную стойкость, проводилась также и в СССР.
В проведенных в СССР и Российской Федерации работах по созданию сплава на никелевой основе, удовлетворяющего требованиям, предъявляемым к конструкционному материалу ЖСР на расплавах фторидных солей с топливными компонентами и продуктами деления, в качестве базового использовали сплав хастеллой Н-мод. Оптимизацию сплава вели по двум направлениям: повышение коррозионной стойкости сплава к избирательной коррозии хрома и повышение стойкости сплава к теллуровой МКК, приводящей к межкристаллитному растрескиванию при деформации растяжения.
Первую часть задачи предполагалось решать уменьшением содержания хрома в сплаве с компенсацией неизбежной потери в жаростойкости применением дополнительного легирования элементами, повышающими жаростойкость никелевых сплавов. К таким элементам относятся кремний и алюминий. Предполагалось также проводить легирование сплава элементами, уменьшающими термодинамическую активность хрома в никелевом сплаве. К таким элементам относятся вольфрам, ниобий, рений, ванадий, алюминий, медь. Естественно, что любые варианты легирования не должны были заметно ухудшать другие свойства сплава: механические характеристики в условиях облучения в поле быстрых нейтронов до флюенса около 1020 нейтр./см2, необходимую технологичность, свариваемость и т.д.
Исследования экспериментальных сплавов проводились в расплаве молярного состава 71.7LiF–16BeF2–12ThF4–0.3UF4. Кроме того, в расплав вводились фториды элементов, которые образуются в процессе деления урана, а также металлический теллур в количествах, соответствующих двум режимам работы реактора: 1) конвертерному (без очистки от продуктов деления) после 8 лет работы реактора на мощности 2 ГВт; 2) режиму с очисткой от продуктов деления [15].
Эксперименты велись при температурах 650 и 800°С. Скорость равномерной коррозии определялась по изменению массы образцов для времен экспозиции 200, 1000 и 2500 ч. Было показано, что наиболее интенсивная коррозия в таких системах завершается в течение 150–200 ч. Теллуровая коррозия никелевых сплавов была предметом наиболее интенсивных исследований. Исследованию подверглись около 70 вариантов различно легированных сплавов. Выяснилось, что механические свойства и скорость равномерной коррозии опытных сплавов мало зависят от типа легирования, оставаясь практически во всех случаях на приемлемом уровне. В табл. 3 представлены результаты исследований для наиболее интересных вариантов сплава.
Таблица 3.
Основные условия и результаты коррозионных испытаний никелевых сплавов
| Солевой расплав | Конструкционный материал | Температура испытания, °C | Время экспозиции, ч | Скорость циркуляции, м/с | Скорость коррозии, мкм/год | Наличие МКК | Наличие содержания основных примесей в расплаве до (C0) и после (Cк) экспозиции, 10–4% | |||
|---|---|---|---|---|---|---|---|---|---|---|
| Fe | Ni | Cr | H2O (не больше) |
|||||||
| LiF–NaF–KF | ХН80МТ | 620 | 180 | 0 | –16 | Нет | 170 | 13 | 11 | 2 · 103 |
| 0.8 | –22 | с очисткой | ||||||||
| ХН80МТ10 | 620 | 280 | 0 | –65 | Нет | |||||
| 0 | » | |||||||||
| NaF–NaBF4 | ХН80МТ | 630 | 500 | 0 | –150 | Есть | ||||
| ХН80МТ10 | 630 | 500 | 0 | –12 | Нет | |||||
| LiF–BeF2–ThF4–UF4 | ХН80МТ | 600 | 500 | 0 | –9 | Нет | 400 | 2000 | 10 | 103 с очисткой |
| ХН80МТ10 | –6 | » | ||||||||
| ХН80МТ | 750 | 500 | 0 | –12 | Есть | |||||
| ХН80МТ10 | –10 | Нет | ||||||||
| ХН80МТ | 750 | 500 | 0.1 | –3 | Есть | 400 | 2000 | 10 | 103 с очисткой | |
| ХН80МТ10 | –6 | Нет | 1000 | 1400 | 100 | |||||
| ХН80МТ | 680 | 500 | 0.1 | 1.5 | » | |||||
| ХН80МТ10 | 0.7 | » | ||||||||
Интенсивность межкристаллитной коррозии образцов, экспонированных в потоке расплава, содержащего теллур, для каждого из исследованных сплавов без нагрузки была существенно ниже, чем под нагрузкой. Особенно это проявлялось для сплавов с низким сопротивлением теллуровой МКК. Так для сплава “моникр” в ненапряженном состоянии межкристаллитное разрушение наблюдалось на всей поверхности образца на глубину до 44 мкм (K = 3590 шт.-мкм/см). Глубина растрескивания под нагрузкой достигала 220 мкм, а интенсивность растрескивания была максимальной по сравнению с другими сплавами, испытанными в схожих условиях. Образец сплава “моникр” при механических испытаниях после экспозиции в расплаве разрушился при минимальном напряжении и с очень низким относительным удлинением (хрупкое разрушение). Существенно, что в условиях без нагрузки теллуровая межкристаллитная коррозия сплава “моникр” при низком значении окислительно-восстановительного потенциала среды в динамических испытаниях была существенно ниже, чем в ампульных экспериментах с сильно выраженными окислительными свойствами расплава. Для сплава ХН80М-ВИ сопротивление растрескиванию было существенно выше, чем у сплава “моникр”. Для образца ХН80М-ВИ, испытанного без нагрузки, наблюдалась невысокая интенсивность межкристалитной коррозии. Однако в нагруженном состоянии сплава ХН80М-ВИ интенсивность растрескивания возрастала более чем в 2 раза, а глубина трещин доходила до 125 мкм. Результаты испытаний сплава ХН80М-ВИ [30] согласуются с данными ORNL [50–56]. Там для сплава, легированного 1.5% Nb, в сходных условиях испытаний (температура 700°С, время экспозиции 250 ч) в топливной соли LiF–BeF2–UF4, содержащей теллурид хрома, были получены близкие результаты. Снижение величины сопротивления теллуровой межкристаллитной коррозии сплава ХН80М-ВИ в нагруженном состоянии накладывает ограничение на ресурс его работы в топливном контуре реактора или требует понижения его рабочей температуры.
Из трех кандидатных сплавов ХН80МТЮ имел максимальную коррозионную стойкость и в настоящее время рассматривается как основной материал для конструкционного оформления узлов жидкосолевого реактора. Интенсивность его растрескивания в два раза ниже, чем у сплава ХН80М-ВИ. Предполагая, что для этих сплавов процесс диффузии теллура по границам зерен будет подчиняться общим закономерностям, температурный режим работы сплава ХН80МТЮ может быть несколько выше, чем у ХН80М-ВИ. Таким образом, наиболее перспективным из рассмотренных сплавов, способным обеспечить требуемые параметры работы конструкционного материала реактора представляется сплав ХН80МТЮ. Однако, чтобы сделать окончательные выводы необходимо проведение дополнительных более длительных ресурсных испытаний (1500 ч) этого сплава под напряжением в термоконвекционных петлях с расплавом выбранного состава, содержащем добавки теллура.
Несмотря на то, что ниобий повышает сопротивление межкристаллитному растрескиванию, содержание титана необходимо уменьшить до приемлемого уровня, который обеспечивает требуемую радиационную стойкость сплава. Такой способ легирования, хотя и позволяет существенно улучшить коррозионные и радиационные характеристики материала, но не является радикальным решением обозначенных проблем.
Легирование стандартного сплава хастеллой Н 0.5% алюминия не улучшило его коррозионных свойств, хотя заметно повысило его механические характеристики. Легирование сплава алюминием при снижении содержания титана до 0.5% привело к существенному улучшению как коррозионных, так и механических свойств. Скорость равномерной коррозии и величина параметра K достигают своего минимального значения при содержании А1 в сплаве около 2.5%.
Также исследовалось влияние комплексного легирования Nb, А1, Ті, Re, Мn на сопротивление никель-молибденовых сплавов к теллуровому разрушению. Как показали ампульные испытания, стойкость сплава (0.6 Ті и 1.0 Nb) в расплаве с высокими окисляющими свойствами была выше, чем у сплава ХН80М-ВИ. Это расходилось с результатами испытаний в ORNL [52–68], где даже небольшие добавки титана к сплаву, легированному только ниобием, отрицательно влияли на стойкость к межкристаллитной коррозии. Попытка усилить сопротивление титан-ниобиевого сплава к теллуровой межкристаллитной коррозии была сделана путем добавок к этому сплаву Re, Мn и Y. Результаты испытаний этих сплавов под напряжением в расплаве 15LiF‒58NaF–27BeF2 показывают, что добавки Re и Y незначительно усиливают сопротивление сплавов теллуровому растрескиванию и сплав, легированный только ниобием, значительно превосходит их по стойкости. Добавка Мn дает существенное усиление стойкости сплава к теллуровой межкристаллитной коррозии.
Оптические, электронно-микроскопические исследования микроструктуры, результаты рентгенофазового анализа, а также данные о коррозионных и механических характеристиках показывают, что основной причиной межкристаллитного растрескивания сплавов является гетерофазность твердого раствора, которая характеризуется избыточными карбидными и интерметаллидными фазами, как в матрице, так и особенно на границах зерен. Благотворное влияние алюминия состоит в изменении характера формирования карбидных фаз по границам зерен: карбидная фаза выделяется дискретно в виде частиц круглой формы, удаленных друг от друга на достаточно большое расстояние. Легирование алюминием повысило стойкость к межкристаллитному растрескиванию только при снижении концентрации титана до 0.5%, что привело к уменьшению содержания интерметаллидной фазы Ni (Al, Ті). Улучшение коррозионных характеристик при Т = 800°С также объясняется уменьшением гетерофазности твердого раствора сплава. Как показал рентгенофазовый анализ, именно в этих условиях наблюдается повышенное растворение в сплаве избыточных карбидных включений и интерметаллидной фазы Ni (Al, Ті). Легирование алюминием заметно повышает жаропрочность сплава и поэтому при определенных ограничениях алюминий может заменить хром в этом сплаве.
Результаты последующих исследований комплекса механических, коррозионных и радиационных свойств различных плавок ХН80МТ позволили предложить модифицированный сплав ХН80МТЮ (ЭК-50) легированный Ті и А1 в качестве конструкционного материала для топливного контура торий-уранового ЖСР. Сплав ЭК-50((ХН80МТЮ) по сравнению со сплавом хастеллой Н имеет некоторые отличия: в нем меньшее содержание хрома (5.5 вместо 7%), меньшее содержание титана (0.8 вместо 1–2%) и добавлен еще один легирующий элемент – алюминий (до 1%). Предварительные ампульные испытания показали, что этот сплав обладает существенно более высокой стойкостью к межкристаллитному растрескиванию, чем хастеллой Н, а его скорость равномерной коррозии в расплавах фторидов не превышает 2 мкм/год при температуре до 800°С [16]. Исследования проводились на механически напряженных образцах, и было обнаружено, что напряженное состояние не влияет на скорость коррозии.
Радиационная стойкость исследовалась при флюенсе до 5.1020 нейтр./см2. При таком флюенсе механические характеристики сплава практически не ухудшались [16].
ВНЕШНИЕ ФАКТОРЫ КОРРОЗИИ
1. Состав атмосферы над расплавом. Степень очистки исходного газа над расплавом
В коррозионных испытаниях практически в большинстве случаев используется инертная атмосфера над расплавами, поскольку при контакте с кислородом происходит катастрофическая коррозия конструкционных материалов высокотемпературных реакторов.
Для большей достоверности получаемых коррозионных данных необходимо предварительно тщательно очищать применяемый инертный газ, наличие даже небольших количеств кислородосодержащих примесей может увеличивать глубинный и весовой показатели коррозии на несколько порядков величины.
В настоящее время, чаще всего применяется аргон. Раньше в ряде работ использовался гелий. Для очистки аргона, обычно, применяют различные печи с медной или циркониевой стружкой, температура нагрева составляет 350 и 550°С соответственно.
2. Коррозионная активность среды (степень очистки солей от примесей, являющихся главными причинами коррозии)
С точки зрения коррозионного действия, FLiNaK значительно агрессивнее FLiBe и цирконий-содержащих фторидных композиций. Ионы корродирующих компонентов материала с анионами фтора образуют комплексные ионы сложного состава, более прочные в присутствии ионов калия.
Оуян и соавт. [69, 70] непосредственно сравнивали скорости коррозии в солях с различным уровнем влажности и обнаружили, что скорости коррозии быстро увеличивались с содержанием влаги.
Существует значительная разница в истинной чистоте солей, используемых в разных исследованиях, из-за различий в методах обработки и очистки. Без каких-либо стандартизированных методов оценки чистоты солей соли, рассматриваемые как “очищенные”, могут все еще содержать высокие уровни примесей и, следовательно, могут демонстрировать высокие скорости коррозии.
Обращает на себя внимание значительный разброс в коррозионных характеристиках одного и того же материала в работах различных исследователей (табл. 3). И превосходство никель-молибденовых сплавов типа хастеллой Н, хастеллой Н мод и российский улучшенный вариант ХН80МТЮ над другими материалами на основе никеля и даже железа (нержавеющие конструкционные стали) не является бесспорным.
Данные ясно показывают, что очистка соли является важным фактором в определении скорости коррозии материалов во фторидных солях различного состава. Наиболее яркой особенностью анализа большого объема разнообразных результатов по коррозии металлических материалов в расплавленных фторидах, является бимодальное распределение данных – очень длительное время и очень низкие скорости коррозии, очень короткие времена и очень высокие скорости коррозии [4]. Скорости коррозии являются самыми высокими в начале воздействий из-за начального периода коррозии, обусловленной примесями [10], в конечном итоге уступающей коррозии, обусловленной растворимостью, которая в случае контура протекает в стационарном состоянии, определяемом термическим градиентом [33, 35], или в статических экспериментах скорость коррозии, по-видимому, замедляется при достижении предела растворимости растворяющихся частиц. Другим объяснением временной зависимости, наблюдаемой в этой работе, является самоотбор, поскольку эксперименты с высокой скоростью коррозии не могут проводиться в течение длительного времени, иначе образцы любого практического размера полностью растворятся.
Стоит отметить, что единственными длительными экспериментами, которые проводились более 3000 ч, были петлевые эксперименты Keizer et al. [53] и Koger et al. [54‒56] в Окридже. В этих экспериментах использовалась чистая топливо-содержащая фторидная соль, и они демонстрировали “удивительно низкие” скорости коррозии.
Данные, рассмотренные в работе [71], показывают, что, по мнению авторов, нержавеющая сталь превосходит сплав 800H и никелевые сплавы. Это может быть объяснено относительно низким содержанием хрома в нержавеющей стали [72–74] по сравнению со многими из сплавов с более высоким содержанием хрома, таких как сплав 800H и большинство сплавов никеля.
Влияние материала контейнера также было важным фактором. Важно отметить, что в большинстве исследований, в которых исследовались нечистые соли, использовались керамические или никелевые контейнеры (тигли, как правило, изготавливаются из керамики, а испытания тиглей часто используются в исследованиях с загрязненными солями). При сравнении типов контейнеров целесообразно ограничить обсуждение только исследованиями с использованием очищенных солей. Сообщается, что графит ускоряет коррозию сплавов [75, 76], а также было обнаружено, что он выделяет углерод в соль, которая может осаждаться на сплавах [77–79]. Также было показано, что кварц разлагается в высокотемпературных солях, поэтому возможно, что продукты коррозии попадают в соль и влияют на реакцию, что объясняет относительно низкие характеристики материала контейнера.
Основные выводы и заключения по перспективам коррозионных исследований для жидкосолевого реактора на сегодняшний день, обобщенные Когером [54–56], Игнатьевым и Суренковым [57–59]. Исследователи [60–79] считают, что основным причиной коррозии и деградации сплава в расплавленных фторидах является селективное растворение хрома из сплава и переход его в солевую фазу [80]. Заслуживает внимания тот факт, что во время теплоконвекционных испытаний было обнаружено, что образцы на горячей стороне петли обычно теряют массу из-за растворения хрома, в то время как образцы на холодной стороне набирают массу из-за осаждения хрома с горячей стороны. Температурный градиент важен, потому что растворимость хрома зависит от температуры соли.
Необходимо исследование коррозии материалов, в том числе индивидуальных металлов в условиях градиента температуры для разделения химических и электрохимических причин коррозии (никель в условиях градиента температур, либо термогальванический элемент, либо разное произведение растворимости фторида никеля при различных температурах, как возможные причины для объяснения переноса никеля с горячих участков на холодные).
Эксперименты с фторидными солями Мэнли и соавт. [14] показали, что после начальной стадии деградации, вызванной примесями, коррозия металлических материалов замедляется до постоянной скорости, определяемой осаждением и растворением частиц из-за изменения растворимости, вызванного тепловым градиентом. Величина скорости коррозии в стационарном состоянии по оптимистичному мнению авторов аналогична таковой в условиях в работающем реакторе, обширные эксперименты были также проведены исследователями в Курчатовском институте [16].
Исследователи в Брукхейвенской национальной лаборатории [38] и ORNL [32, 35] изучали коррозию в петлях с накачкой, иногда называемых петлями с принудительной конвекцией. Из-за больших затрат, связанных с созданием и эксплуатацией этих контуров, они не являются распространенными для проведения коррозионных экспериментов, и в перекачиваемых контурах не было обнаружено новых проблем совместимости. Однако в перспективе коррозионные испытания могут проводиться наряду с другими экспериментами, такими как термогидравлика, что делает использование петли с насосом для коррозионных испытаний более экономичным.
Дополнительные факторы. На коррозию конструкционных сплавов в высокотемпературных реакторах с фторидно-солевым охлаждением влияет присутствие углерода.
Стабильность карбидов легирующих элементов усиливает их коррозию, однако это же свойство может быть полезно, если эти стабильные карбиды используются для защиты материалов. Испытания на экспонирование чистых элементов Cr, Fe, Ni, W и Mo в графитовых тиглях при 700°С проводились в расплавленной соли FLiNaK в течение 100 ч. после экспонирования на поверхностях образцов Cr, Mo и W были обнаружены карбидные частицы. Ранжирование этих элементов от наименьшей до наибольшей коррозионной стойкости по потере массы на единицу площади составляло Cr < < Fe < W < Mo < Ni.
Слой карбида хрома, полученный предварительной цементацией, был устойчив к воздействию расплавленного фторида и замедлял коррозию основного металла хрома, что позволяет рассматривать его как перспективный материал для защитного покрытия.
Легирование исходного материала
Проблема равномерной коррозии отобранных никель-молибденовых сплавов решена путем легирования конструкционного материала элементами, уменьшающими термодинамическую активность хрома в никель-молибденовом сплаве. Проблема межкристаллитной коррозии, вызванной воздействием теллура, может быть решена легированием сплава ниобием, алюминием или ванадием.
Однако чтобы считать, что проблема конструкционного материала для ЖСР решена, необходимо провести долговременные неизотермические петлевые испытания с жидкосолевым носителем выбранного состава, а также изготовить крупные плавки такого материала и продемонстрировать возможность изготовления из него типичных деталей конструкции (для хастеллоя Н такая работа была выполнена). Сплав ХН80МТЮ, хотя это довольно обычный материал, но весьма недешевый, его применение целесообразно только для таких элементов конструкции, для которых невозможно использовать более дешевые материалы, и с этой точки зрения чрезвычайно привлекательны аустенитные нержавеющие стали, хорошо освоенные промышленностью [81]. Эти стали подвергаются сильной коррозии в среде расплавленных фторидов, содержащих топливные добавки, но в “чистых” теплоносителях, таких как система Li, Be/F, коррозионная стойкость их вполне удовлетворительна.
Скорость коррозии стали типа SS-316, модифицированной титаном или отечественной стали типа 12X18Н9Т сильно зависит от окислительно-восстановительного потенциала солевой композиции. При достаточно низком окислительном потенциале, обеспечиваемым добавлением в соль металлического бериллия, скорость коррозии становится столь низкой, что можно рассчитывать на длительный ресурс работы этих сталей. Нержавеющие стали, легированные титаном, достаточно стойки к радиационному облучению. Например, распухание стали 12Х18Н9Т при 3 · 10 нейтр./см при температуре 600°С не превышает 0.2%, коррозионные испытания стали 12Х18Н10Т в среде Li, Be/F при температуре до 750°С и выдержке до 2000 ч показали, что скорость ее коррозии не превышает 1.5 мкм/год, и коррозионные эффекты не оказывают заметного влияния на механические свойства [16]. Прочностные характеристики этих сталей достаточно высоки при температурах до 600°С.
Как уже отмечалось, практически все коррозионные процессы в среде жидких солей связаны с наличием в солях тех или иных примесей, из которых наиболее опасными являются вода и газообразный кислород. Следовательно, тщательная очистка солевых расплавов в первую очередь от этих примесей должна существенно снизить коррозионную активность солевой среды. Коррозионные взаимодействия в солевых расплавах между элементами конструкционного материала и примесями носят в основном окислительно-восстановительный характер. Из этого следует, что, регулируя окислительно-восстановительный потенциал, можно воздействовать на интенсивность протекания таких реакций до их полного подавления [82].
Контролируемая очистка солевых расплавов от первоначальных примесей и от продуктов деления урана, возникающих в процессе работы реактора, а также поддержание окислительно-восстановительного потенциала на необходимом уровне, являются эффективными способами борьбы со всеми видами коррозионных поражений металлических конструкционных материалов жидкосолевых реакторов [83–88].
ЗАКЛЮЧЕНИЕ
Целесообразным будет первоочередное проведение термодинамического анализа взаимодействия компонентов конструкционных материалов с расплавами фторидов различного состава, квантово-механического анализа возможных фторидных комплексов и их устойчивости.
При проведении новых экспериментальных исследований необходимы следующие мероприятия:
• стандартизация исходных солей, состава газовой атмосферы (и образцов);
• исследование образующихся продуктов в солевой и газовой фазе (влияние примесей различных соединений кислорода, воды, фтористого водорода);
• исследование состава примесей, образующихся в ходе выдержки в расплавах, их зависимость от температуры и времени выдержки;
• расчет констант и степени высокотемпературного гидролиза основных компонентов фторидных расплавов; оценка ионной силы расплава для фторидных композиций различного состава;
• исследование перехода компонентов солевой фазы в газообразное состояние и наоборот – составление материального баланса процесса коррозии;
• сопоставление высокотемпературной коррозии в газовой фазе и в расплавленных солях, разделение температурного и химического факторов коррозии.
Работа выполнена при поддержке Российского фонда фундаментальных исследований, проект № 20-21-00022 Росатом.
Список литературы
Dolan T.J. Molten Salt Reactors and Thorium Energy. Woodhead Publishing, 2017.
Sridharan K., Allen T.R.R. Corrosion in Molten Salts // From Lab to Applications. 2013. P. 241–267.
Ignatiev V., Surenkov A. 5–corrosion phenomena induced by molten salts in Generation IV nuclear reactors // Struct. Mater. Gener. IV Nucl. React. 2017. P. 153–189.
Raiman S.S., Lee S. Aggregation and data analysis of corrosion studies in molten chloride and fluoride salts // J. Nuclear Materials. 2018. 511. P. 523–535.
Комаров В.Е, Смоленский В.В., Афоничкин В.К. Перспективы использования расплавленных солей в радиохимических технологиях // Расплавы. 2000. № 2. С. 59–65.
LeBlanc D. // Nucl. Eng. Des. 2010. 240. P. 1644–1656. https://doi.org/10.101j.nucengdes.2009.12.033
Khokhlov V., Ignatiev V., Afonichkin V. Evaluating physical properties of molten salt reactor fluoride mixtures // J. Fluorine Chemistry. 2009. 130. P. 30–37.
Barnes J., Coutts R., Horne T., Thai J. Characterization of molten salts for application in molten salt reactors. PAM Review. 2019.
Magnusson J., Memmott M., Munro T. Review of thermophysical property methods applied to fueled and un-fueled molten salts // Annals of Nuclear Energy. 2020. 146. P. 107608.
IAEA. Advances in Small Modular Reactor Technology Developments. 2016.
Serp J., Allibert M., Benes O. Delpech S., Feynberg O. and other. The molten salt reactor (MSR) in generation IV: overview and perspectives // Prog. Nucl. Energy. 2014. 77. P. 308–319.
Williams D.F. Assessment of candidate molten salt coolants for the advanced highi-temperature reactor (AHTR), 2006.
Ядерные реакторы. Ч. 3. Материалы для ядерных реакторов. М.: Изд-во иностранной литературы, 1956.
Менли В., Кубс Д., де Ван Д, Дуглас Д., Инуи Х., Пэтриарка П., Роч Т., Скотт Д. Металлургические проблемы, связанные с использованием расплавленных систем фторидов // Ядерное горючее и реакторные материалы. 1959. С. 36–52.
Manly W.D., Adamson G.M., Coobs J.H., DeVan J.H., Douglas D.A., Hoffman E.E., Patriarca P., Aircraft reactor experiment-metallurgical aspects. ORNL-2349, 1957.
Игнатьев В.В. Создание экспериментальных установок и базы данных для выбора и усовершенствования жидкосолевых топливных композиций и теплоносителей в ядерных реакторах. Дисс. ... д. т. н. 2009.
Ignatiev V., Surenkov A., Gnidoi I., Fedulov V., Uglov V., Afonichkin V., Bovet A., Subbotin V., Panov A., Toropov A. // Nucl. Technol. 2008. 164. P. 130–142. https://doi.org/10.13182/NT08-A4014
Игнатьев В.В., Суренков А.И., Гнидой И.П., Углов В.С., Конаков С.А. Экспериментальное исследование теллуровой коррозии никель-молибденовых сплавов в расплаве солей фторидов лития, бериллия и урана // Атомная энергия. 2016. 120. № 6. С. 326–330.
Игнатьев В.В., Крюков О.В., Хаперская А.В. и др. Жидкосолевой реактор для замыкания ядерного топливного цикла по всем актиноидам // Атомная энергия. 2018. 125. № 5. С. 251–255.
Ignatiev V., Feynberg O., I. Gnidoi, et al. Molten salt actinide recycler and transforming system without and with Th-U support: Fuel cycle flexibility and key material properties // Ann. Nucl. Energy. 2014. 64. P. 408–420.
Пономарев Л.И., Белоногов М.Н., Волков И.А. и др. Быстрый жидкосолевой реактор на основе эвтектики LiF–NaF–KF как сжигатель Np, Am, Cm // Атомная энергия. 2019. 126. № 3. С. 123–132.
Игнатьев В.В., Фейнберг О.С., Смирнов В.П. и др. Анализ характеристик топливного контура жидкосолевого ядерного реактора с активной зоной полостного типа // Атомная энергия. 2019. 126. № 3. С. 137–143.
Wagner C. The formation of thin oxide films on metals // Corrosion Sci. 1973. 13. P. 23–52.
Young D.J. High Temperature Oxidation and Corrosion of Metals. Elsevier Science, 2016.
Guo S., Zhang J., Wub W., Zhou W. Corrosion in the molten fluoride and chloride salts and materials development for nuclear applications // Progress in Material Science. 2018. 97. P. 448–487.
Wang Y., Zhang S., Ji X., Wang P., Li W. Material corrosion in molten fluoride salts // Int. J. Electrochem. Sci. 2018. 13. P. 4891–4900.
DeVan J.H., Evans R.B. Corrosion behavior of reactor materials in fluoride salt mixtures. ORNL-TM-328, 1962.
Mehos M., Turchi C., Vidal J., Vagner M., Ma Z., Ho C., Kolb W., Andraka C., Kruizenga A. Concentrating Solar Power Gen3 Demonstration Roadmap. NREL, 2017.
Zheng G., He L., Carpenter D., Sridharan K. Corrosion-induced microstructural developments in 316 stainless steel during exposure to molten Li2BeF4 (FLiBe) salt // J. Nuclear Materials. 2016. 482. P. 147–155.
Бакай А.С., Чечкин А.В., Жук В.В. Механические, физические, коррозионные и радиационные свойства сплавов типа Хастеллой Н в расплавах фторидных солей: Обзор. Харьков: ННЦ ХФТИ, 2005.
Граймс У.Р. Проблемы подбора материалов для реакторов с расплавленными солями // Материалы и горючее для высокотемпературных ядерных энергетических установок. 1966. С. 84–96.
Новиков В.М., Федулов В.И., Ругес О.В., Тараканов Л.А. Исследование коррозионной стойкости конструкционных материалов для жидкосолевых реакторов // ВАНТ. Атомно-водородная энергетика и технология. 1981. 10. № 3. С. 74–76.
Горбовицкая Т.Н., Кантс Л.К., Лея Г.В. и др. Влияние ионизирующего облучения на коррозию стали 12Х18Н10Т и сплава ХН80МТ в расплавах фторидных солей // ВАНТ. Атомно-водородная энергетика и технология. 1983. 16. № 3. С. 80–82.
Koger J.W. Alloy compatibility with LiF–BeF2 salts containing ThF4 and UF4. ORNL/TM/4286, 1972.
Janz G.J. // Molten Salts Handbook. 1967. P. 383–387. https://doi.org/10.1016/B978-0-12-395642-2.50032-0
Sridharan K., Anderson M., Allen T., Corradini M., Olson L., Ambrosek J., Ludwig D. Liquid salts as media for process heat transfer from VHTRs: forced convective channel flow thermal hydraulics, Materials, and Coating, 2012.
Olson L.C., Ambrosek J.W., Sridharan K., Anderson M.H., Allen T.R. Materials corrosion in molten LiF–NaF–KF salt // J. Fluorine Chem. 2009. 130. P. 67–73.
Kelleher B.C., Dolan K.P., Brooks P., Anderson M.H., Sridharan K. // J. Nucl. Eng. Radiat. Sci. 2015. 1. № 4. P. 041010. https://doi.org/10.1115/1.4030963
Zheng G., Kelleher B., Cao G., Anderson M., Allen T., Sridharan K. // J. Nucl. Mater. 2015. 46. P. 143–150. https://doi.org/10.1016/J.Jnucmat.2015.03.004
Qiu J., Zou Y., Yu G., Liu H., Jia Y., Li Z., Huai P., Zhou X., Xu H. Compatibility of container materials with Cr in molten FLiNaK salt // J. Fluorine Chem. 2014. 168. P. 69–74.
Hou J., Yu G., Zeng C., Ai H., Xie R., Chen Y., Zhou X., Xie L., Wang J. Effects of exposing duration on corrosion performance in weld joint of Ni–Mo–Cr alloy in FLiNaK molten salt // J. Fluorine Chem. 2016. 191. P. 110–119.
Gomez-Vidal J.C., Tirawat R. Corrosion of alloys in a chloride molten salt (NaCl–LiCl) for solar thermal technologies // Sol. Energy Mater. Sol. Cells. 2016. 157. P. 234–244.
Gomez-Vidal J.C.C., Fernandez A.G.G., Tirawat R., Turchi C., Huddleston W. Corrosion resistance of alumina-forming alloys against molten chlorides for energy production. I: pre-oxidation treatment and isothermal corrosion tests // Sol. Energy Mater. Sol. Cells. 2017. 166. P. 222–233.
Lorimer J.W., Gujral P.D. Solubility data series // Int. Union Pure Appl. Chem. 1979. 45/46.
Vignarooban K., Pugazhendhi P., Tucker C., Gervasio D., Kannan A.M. // Sol. Energy. 2014. 103. P. 62–69. https://doi.org/10.1016/j.solener.2014.02.002
Vignarooban K., Xu X., Wang K., Molina E.E., Li P., Gervasio D., Kannan A.M. // Appl. Energy. 2015. 159. P. 206–213. https://doi.org/10.1016/j.apenergy.2015.08.131
Sabharwall P., Ebner M., Sohal M., Sharpe P., Anderson M., Sridharan K., Ambrosek J., Olson L., Brooks P. Molten Salts for High Temperature Reactors: University of Wisconsin Molten Salt Corrosion and Flow Loop Experiments – Issues Identified and Path Forward, 2010.
Cheng W.-J., Sellers R.S., Anderson M.H., Sridharan K., Wang C.-J., Allen T.R. Zirconium effect on the corrosion behavior of 316L stainless steel alloy and Hastelloy-N superalloy in molten fluoride salt // Nucl. Technol. 2017. 183. P. 248–259.
Yang X., Zhang D., Liu M., Feng S. and other // Corrosion Sci. 2016. 109. P. 62–67. https://doi.org/10.1016/J.Corsci.2016.03.029
Keiser J.R., DeVan J.H., Lawrence E.J. Compatibility of molten salts with type 316 stainless steel and lithium // J. Nucl. Mater. 1979. P. 295–298.
Keiser J.R., Manning D.L., Clausing R.E. Corrosion resistance of some nickel base alloys to molten fluoride salts containing UF4 and tellurium in: Molten Salts, The Electrochemical Society. N.Y., 1976. P. 315–328.
Distefano J.R., DeVan J.H., Keiser J.R., Klueh R.L., Eatherly W.P. Materials considerations for molten salt accelerator based plutonium conversion systems. ORNL/TM/12925/R1, 1995.
Keiser J.R. Compatability studies of potential molten salt breeder reactor materials in molten fluoride salts. ORNL/TM/5783, 1977.
Koger J.W. Evaluation of Hastelloy N alloy after nine years exposure to both a molten fluoride salt and at at temperatures from 700 to 560°C. ORNL/TM/4189, 1972.
Koger J. Intergranular corrosion of Hastelloy N. ORNL-4782, 1972.
Koger J.W., Litman A.P. Compatibility of molybdenum-base alloy TZM, with LiFBeF2–ThF4–UF4 (68–20–11.7–0.3 mole percent) at 1100°C. ORNL/TM/2724, 1969.
gnatiev V., Surenkov A. Alloys compatibility in molten salt fluorides: Kurchatov Institute related experience // J. Nucl. Mater. 2013. 441. P. 592–603
Ignatiev V., Surenkov A., Gnidoy I., Kulakov A., Uglov V., Vasiliev A., Presniakov M. Intergranular tellurium cracking of nickel-based alloys in molten Li, Be, Th, U/F salt mixture // J. Nucl. Mater. 2013. 440. P. 243–249.
Суренков А.И., Игнатьев В.В., Абалин С.С., Конаков С.А., Углов В.С. Коррозионная и механическая стойкость никелевых сплавов в жидкосолевых ядерных реакторах // Атомная энергия. 2008. 124. № 1. С. 34–37.
Zheng G.Q., Kelleher B., He L.F., Cao G.P., Anderson M., Allen T. Sridharan, K. High-temperature corrosion of UNS N10003 in Molten Li2BeF4 (FLiBe) salt // Corrosion. 2015. 71. № 10. P. 1257–1266.
Sabharwall P, Clark D., Glazoff M., Zheng G., Sridharan K., Anderson M. Advanced heat exchanger development for molten salts // Nucl. Eng. Des. 2014. 280. P. 42–56.
De Van J.H. Effect of alloying additions of corrosion behavior of nickel-molybdenum alloys in fused fluoride mixtures. ORNL TM-2021, 1969.
Liu M., Zheng J., Lu Y., Li Z., Zou Y., Yu X., Zhou X. Investigation on corrosion behavior of Ni-based alloys in molten fluoride salt using synchrotron radiation techniques // J. Nucl. Mater. 2013. 440. P. 124–128.
Danon A.E., Muránsky O., Karatchevtseva I., Zhang Z., Li Z. J., Scales N., Kruzic J.J., Edwards L. // Corrosion Sciences. 2020. 164. P. 108 306. https://doi.org/10.1016/j.corsci.2019.108306
Dai Q., Ye X.-X., Ai H., Chen Sh., Jiang L., Liang J. and other. Corrosion of Incoloy 800H alloys with nickel cladding in FLiNaK salts at 850°C // Corrosion Science. 2018. 1331. P. 349–357.
Olson L.C., Fuentes R.E., Martinez-Rodriguez M.J., Ambrosek J.W., Sridharan K., Anderson M.H., Garcia-Diaz B.L., Gray J., Allen T.R. Impact of corrosion test container material in molten fluorides // J. Sol. Energy Eng. 2015. 137. P. 061007.
Dong L., Peng Q., Zhang Z., Shoji T., E.-H.H. Han, W. Ke, L. Wang, Effect of dissolved hydrogen on corrosion of 316NG stainless steel in high temperature water // Nucl. Eng. Des. 2015. 295. P. 403–414.
Ye X.X., Ai H., Guo Z., Huang H.F., Jiang L., Wang J.Q., Li Z.J., Zhou X.T. The hightemperature corrosion of Hastelloy N alloy (UNS N10003) in molten fluoride salts analysed by STXM, XAS, XRD, SEM, EPMA, TEM/EDS // Corros. Sci. 2016. 106. P. 249–259.
Ouyang F.-Y., Chang C.-H., You B.-C., Yeh T.-K., Kai J.-J. Effect of moisture on corrosion of Ni-based alloys in molten alkali fluoride FLiNaK salt environments // J. of Nuclear Materials. 2013. 437. № 1–3. P. 201–207.
Ouyang F.-Y., Chang C.-H., Kai J.-J. // J. Nucl. Mater. 2014. 446. P. 81–89. https://doi.org/10.1016/j.jnucmat.2013.11.045
Warchilováa T., Dillingerováa V., Škodac R., Šimod T., Matald O., Vaculoviča T., Kanickýa V. Corrosion of nickel-based structural materials for nuclear reactors by molten fluoride salt: From bulk content of corrosion products to elemental imaging of corrosion changes // Spectrochimica Acta. Part B. 2018. 148. P. 113–117.
Кириллов В.Б., Федулов В.И. Коррозионная стойкость стали 12Х18Н10Т в расплаве фтористых солей // ФХММ. 1980. № 6. С. 22–25.
Бельчук М.В., Липодаев В.Н., Новичкова О.В., Федулов В.И. К вопросу о свариваемости высоконикелевых жаропрочных коррозионно-стойких сплавов // Проблемы технологии сварки теплоустойчивых и жаропрочных высоколегированных сталей и сплавов. Николаев: Металлургия, 1985.
Zheng G.Q., Kelleher B., Cao G.P., Anderson M., Allen T., Sridharan K. Corrosion of 316 stainless steel in high temperature molten Li2BeF4 (FLiBe) salt // J. Nucl. Mater. 2015. 461. P. 143–150.
Chan K.J., Ambrecht R.J., Luong J.M., Choi W.T., Singh P.M. Carburization effects on the corrosion of Cr, Fe, Ni, W, and Mo in fluoride-salt cooled high temperature reactor (FHR) coolant // Annals of Nuclear Energy. 2018. 120. P. 279–285.
Ai H., Hou J., Ye X.X., Zeng C.L., Sun H., Li X.Y., Yu G.J., Zhou X.T., Wang J.Q. Influence of graphite-alloy interactions on corrosion of Ni–Mo–Cr alloy in molten fluorides // J. Nucl. Mater. 2018. 503. P. 116–123.
Brupbacher, M.C., Zhang, D., Buchta, W.M., Graybeal, M.L., Rhim, Y.-R., Nagle, D.C., Spicer, James B. Synthesis and characterization of binder-free Cr3C2 coatings on nickel-based alloys for molten fluoride salt corrosion resistance // J. Nucl. Mater. 2015. 461. P. 215–220.
Sellers R.S., Cheng W.J., Kelleher B.C., Anderson M.H., Sridharan K., Wang C.J., Allen T.R. Corrosion of 316L stainless steel Alloy and hastelloy-N superalloy in molten eutectic LiF–NaF–KF salt and interaction with graphite // Nucl. Technol. 2014. 188. № 2. P. 192–199.
Scarlat R.O., Laufer M.R., Blandford E.D., Zweibaum N., Krumwiede D.L., Cisneros A.T., Andreades C., Forsberg C.W., Greenspan E., Hu L.W., Peterson P.F. Design and licensing strategies for the fluoride-salt-cooled, high-temperature reactor (FHR) technology // Prog. Nucl. Energy. 2014. 77. P. 406–420.
Qiu J., Zou Y., Yu G., Liu H., Jia Y., Li Zh., Huai P., Zhou X., Xu H. Compatibility of container materials with Cr in molten FLiNaK salt // J. Fluorine Chem. 2014. 168. P. 69–74.
Olson L., Sridharan K., Anderson M., Allen T. Nickel-plating for active metal dissolution resistance in molten fluoride salts // J. Nucl. Mater. 2011. 411. P. 51–59.
Ozeryanaya I.N. Corrosion of metals by molten-salts in heat-treatment processes // Met. Sci. Heat Treat. 1985. 27. № 3–4. P. 184–188.
Fabre S., Cabet C., Cassayre L., Chamelot P., Delepech S., Finne J., Massot L., Noel D. Use of electrochemical techniques to study the corrosion of metals in model fluoride melts // J. Nucl. Mater. 2013. 441. P. 583–591.
Delpech S., Cabet C., Slim C., Picard G.S. Molten fluorides for nuclear applications // Mater. Today. 2010. 13. № 12. P. 34–41.
Abram T., Ion S. Generation-IV nuclear power: a review of the state of the science // Energy Policy. 2008. 36. P. 4323–4330.
Uhlir J. Chemistry and technology of Molten Salt Reactors – history and perspectives // J. Nucl. Mater. 2007. 360. P. 6–11.
Moir R.W. Recommendations for a restart of molten salt reactor development // Energy Convers. Manag. 2008. 49. P. 1849–1858.
Le Brun C. Molten salts and nuclear energy production // J. Nucl. Mater. 2007. 360. P. 1–5.
Дополнительные материалы отсутствуют.