Расплавы, 2021, № 2, стр. 172-186
Фазовые равновесия для Zn–Ag сплава при вакуумной дистилляции
А. А. Королев a, К. Л. Тимофеев a, b, Г. И. Мальцев a, *
a Акционерное общество “Уралэлектромедь”
Верхняя Пышма, Россия
b Негосударственное частное образовательное учреждение высшего образования
“Технический университете УГМК”
Верхняя Пышма, Россия
* E-mail: maltsewg@yandex.ru
Поступила в редакцию 19.11.2020
После доработки 04.12.2020
Принята к публикации 08.12.2020
Аннотация
При рафинировании чернового свинца от примесей металлическим цинком на поверхности жидкого расплава образуется серебристая пена (СП), содержащая свинец, цинк и серебро. Для разделения компонентов СП возможно применить вакуумную перегонку, являющуюся одной из самых экологически безопасных и высокопроизводительных технологий в пирометаллургии. Для предварительного выбора температуры и давления системы, оценки эффективности разделения компонентов при вакуумной перегонке используют фазовые диаграммы. Цель работы состоит в расчете равновесных состояний “газ–жидкость” VLE (vapor liquid equilibrium), включая зависимости состава фаз от температуры (Т–х) при заданном давлении для бинарных сплавов Zn–Ag при вакуумной перегонке на основе моделей MIVM (мolecular interaction volume model) и упрощенной – SMIVM (simple мolecular interaction volume model), включающей меньшее число изменяющихся параметров системы, в частности, при фиксированных значениях координационных чисел Zi и молекулярного объема Vmi компонентов сплавов. В результате подтверждена адекватность модели SMIVM в используемом расчетном методе. Получена оригинальная информация о влиянии температуры и остаточного давления в системе на степень возгонки и разделения металлов из Zn–Ag сплавов переменного состава. Определены величины давления насыщенного пара (Па) для цинка $р_{{{\text{Zn}}}}^{*}$ = 5.79 ⋅ 102–3.104 ⋅ 104 и серебра $р_{{{\text{Ag}}}}^{*}$ = 5.25 ⋅ 10–9–5.1 ⋅ 10–5 при Т = 823–1073 К. Большие различия в величинах $р_{{{\text{Zn}}}}^{*}$ и $р_{{{\text{Ag}}}}^{*}$ обусловливают высокие значения коэффициента разделения lg βZn = = 8.32–12.18 и предполагают возможность раздельного выделения возгонкой цинка в газовую фазу (βZn > 1) и концентрирование серебра в жидкой фазе. Увеличение содержания мольных долей серебра в составе сплава от 0.1 до 0.9 и температуры системы с 823 до 1073 К приводит к росту мольной доли серебра в газовой фазе с 1 ⋅ 10–15 до 8.5 ⋅ 10–7. Для равновесного состояния жидкой и газовой фаз системы Zn–Ag рассчитаны величины термодинамических функций: $G_{m}^{E}$ = 0.08–1.36 кДж/моль; $ - H_{m}^{E}$ = = 1.52–5.73 кДж/моль; $S_{m}^{E}$ = 1.57–5.38 Дж/моль ⋅ К. Равновесные фазовые диаграммы VLE Zn–Ag сплава могут быть использованы на предварительных этапах проектирования опытно-промышленного оборудования для технологии вакуумной перегонки, а также для выбора диапазонов температуры и давления в системе с целью получения Zn- и Ag-содержащих продуктов заданного состава.
ВВЕДЕНИЕ
При очистке чернового свинца от примесей металлическим цинком на поверхности жидкого расплава образуется серебристая пена (СП), содержащая свинец, цинк и серебро. Для разделения компонентов СП возможно применить вакуумную перегонку, являющуюся одной из самых экологически безопасных и высокопроизводительных технологий в пирометаллургии [1, 2]. Предварительный анализ поведения полиметаллических сплавов в процессе дистилляции, в частности, состав продуктов возгонки и степень разделения компонентов сплава при заданных значениях температуры и давления осуществляют при помощи рассчитанных равновесных фазовых диаграмм VLE (vapor liquid equilibrium), например, температура–состав “Т–х” и давление–состав “Р–х”. Возможность разделения компонентов сплавов методом возгонки обусловлена различием в давлении насыщенных паров чистых металлов (Р *) при одинаковой температуре и характеризуется коэффициентами разделения (β) при распределении металлов между газовой и жидкой фазами [3]. Для определения β необходимо рассчитать коэффициенты активности компонентов (γi, γj) в зависимости от температуры и состава cплава [4] с использованием соответствующей модели MIVM [5]. При расчете используют значения координационных чисел (Z), молярных объемов (Vm) и потенциальных энергий парного взаимодействия (В) компонентов сплава [6]. Диаграммы VLE помогают выявить вероятностные диапазоны температуры и давления процесса дистилляции, соответствующие заданной степени разделения компонентов исходного сплава и составу образующихся конденсата и огарка. В ряде предыдущих исследований [7–9] MIVM использовали для прогнозирования термодинамических свойств сплавов, с констатацией их надежности для различных цветных металлов – компонентов сплавов. Поскольку процесс расчета MIVM является относительно сложным, особенно расчет первых координационных чисел Zi и молекулярного объема Vmi компонентов сплавов, использовали метод прогнозирования, включающий меньшее число параметров системы, так называемый упрощенный MIVM или SMIVM. Таким образом, в данной работе активность компонентов сплавов Zn–Ag и фазовые диаграммы VLE были рассчитаны с использованием двух моделей – MIVM и SMIVM. Важно подтвердить возможность использования модели SMIVM в расчетном методе, позволяющем точно и быстро определять VLE при вакуумной перегонке. Фазовые диаграммы VLE, полученные в этом исследовании, обеспечивают интуитивно понятный и простой способ прогнозирования распределения компонентов Zn–Ag сплавов между фазами, в зависимости от состава изделий, температуры и давления в системе вакуумной перегонки. Оптимальные параметры процесса можно оперативно получить из VLE фазовых диаграмм.
Целью работы являлось исследование влияния температуры и давления в системе на полноту извлечения и степень разделения цинка и серебра из состава СП, а также прогнозирование качественного и количественного составов фаз вакуумной возгонки компонентов Zn–Ag сплава посредством расчета равновесных диаграмм “жидкость–газ”, учитывающих зависимость состава образующихся продуктов возгона от температуры (Т–х), с применением MIVM и SMIVM.
МЕТОДИКИ РАСЧЕТА
Летучесть (фугитивность) каждого компонента в газовой и жидкой фазах равны, когда система достигает равновесия. Соотношение общего равновесия для VLE может быть выражено следующим образом [10]:
(1)
$\phi _{i}^{ \wedge }({{y}_{i}}p) = \phi _{i}^{{{\text{sat}}}}({{x}_{i}}{{\gamma }_{i}}){\kern 1pt} {\text{exp}}\left[ {\frac{{V_{i}^{L}\left( {P - P_{i}^{{{\text{sat}}}}} \right)}}{{RT}}} \right],$При низком давлении (p ≤ 1330 Па), используемом в данном исследовании, коэффициент Пойнтинга ${\text{exp}}\left[ {\frac{{V_{i}^{L}(P - P_{i}^{{{\text{sat}}}})}}{{RT}}} \right]$ ≈ 1. В добавлении, газовая фаза может рассматриваться как идеальный газ и зависимостью фугитивности жидкой фазы от давления можно пренебречь. Уравнение (1) может быть выражено следующим образом:
(2)
${{y}_{{i~}}}p = {{x}_{i}}{{\gamma }_{i}}p_{i}^{{{\text{sat}}}}\,\,\left( {i = 1,2, \ldots .N} \right).$Если жидкая смесь идеальна, то по закону Рауля γi = 1. Для бинарного сплава i–j:
(4)
$p = р_{i}^{{{\text{sat}}}}{{\gamma }_{i}}{{x}_{i}} + р_{j}^{{{\text{sat}}}}{{\gamma }_{j}}{{x}_{j}} = р_{i}^{{{\text{sat}}}}{{\gamma }_{i}}{{x}_{i}} + р_{j}^{{{\text{sat}}}}{{\gamma }_{j}}\left( {1 - {{x}_{i}}} \right).$Из уравнений (2) и (4) можно выразить xi и уi , как:
(5)
$~{{x}_{i}} = \frac{{Р - P_{j}^{{{\text{sat}}}}{{\gamma }_{j}}}}{{P_{i}^{{{\text{sat}}}}{{\gamma }_{i}} - P_{j}^{{{\text{sat}}}}{{\gamma }_{j}}}},\,\,\,\,{{y}_{i}} = \frac{{P_{i}^{{{\text{sat}}}}{{\gamma }_{i}}{{x}_{i}}}}{Р}.$Модель MIVM считается одной из наиболее удобных и надежных [11–13]. Однако, до сих пор ее практическое применение было затруднено из-за сложного процесса расчета координационных чисел (Z) и отсутствия молярных объемов в жидком состоянии ($V_{i}^{L}$) некоторых компонентов (например, С, Ta, V2O5, Cu2S, CaSiO3). Упрощение MIVM достигнуто путем придания обоим Zi и Zj значений, равных 10, и заменой молярного объема i-компонента в жидком состоянии на его молярный объем в твердом состоянии (Vi) [14, 15].
При расчете VLE коэффициент активности компонента в жидкой фазе является существенным параметром. Согласно MIVM, молярный избыток энергии Гиббса $G_{m}^{E}$ жидкой смеси i–j можно представить, как [16, 17]:
(6)
$\frac{{G_{m}^{E}}}{{RT}} = {{x}_{i}}\ln \left( {\frac{{{{V}_{{mi}}}}}{{{{x}_{i}}{{V}_{{mi}}} + {{x}_{j}}{{V}_{{mj}}}{{B}_{{ji}}}}}} \right) + {{x}_{j}}\ln \left( {\frac{{{{V}_{{mj}}}}}{{{{x}_{j}}{{V}_{{mj}}} + {{x}_{i}}{{V}_{{mi}}}{{B}_{{ij}}}}}} \right) - \frac{{{{x}_{i}}{{x}_{j}}}}{2}\left( {\frac{{{{Z}_{i}}{{B}_{{ji}}}{\text{ln}}{{B}_{{ji}}}}}{{{{x}_{i}} + {{x}_{j}}{{B}_{{ji}}}}} + \frac{{{{Z}_{j}}{{B}_{{ij}}}{\text{ln}}{{B}_{{ij}}}}}{{{{x}_{j}} + {{x}_{i}}{{B}_{{ij}}}}}} \right),$Значения Bij и Bji из уравнения (6) определяются выражениями:
(7)
${{B}_{{ij}}} = {\text{ехр}}\left[ { - \left( {\frac{{{{\varepsilon }_{{ij}}} - {{\varepsilon }_{{jj}}}}}{{kT}}} \right)} \right],\,\,\,\,{{B}_{{ji}}} = {\text{ехр}}\left[ { - \left( {\frac{{{{\varepsilon }_{{ji}}} - {{\varepsilon }_{{ii}}}}}{{kT}}} \right)} \right],$Координационное число определяли следующим образом [18]:
(8)
${{Z}_{i}} = \frac{{4\sqrt {2\pi } }}{3}\left( {\frac{{r_{{mi}}^{3} - r_{{oi}}^{3}}}{{{{r}_{{mi}}} - {{r}_{{oi}}}}}} \right){{\rho }_{i}}{{r}_{{mi}}}{\text{exp}}\left( {\frac{{\Delta {{H}_{{mi}}}\left( {{{T}_{{mi}}} - T} \right)}}{{{{Z}_{c}}RT{{T}_{{mi}}}}}} \right),$Для бинарной смеси i–j, с помощью термодинамического соотношения ($\partial $$G_{m}^{E}$/$\partial $xi)T,p,xj ≠ i, коэффициенты активности i- и j-компонентов могут быть получены из уравнения (6), соответственно, как:
(9)
$\begin{gathered} {\text{ln}}{{\gamma }_{i}} = \ln \left( {\frac{{{{V}_{{m,i}}}}}{{{{x}_{i}}{{V}_{{m,i}}} + {{x}_{j}}{{V}_{{m,j}}}{{B}_{{ji}}}}}} \right) + {{x}_{j}}\left( {\frac{{{{V}_{{m,j}}}{{B}_{{ji}}}}}{{{{x}_{i}}{{V}_{{m,i}}} + {{x}_{j}}{{V}_{{m,j}}}{{B}_{{ji}}}}} - \frac{{{{V}_{{m,i}}}{{B}_{{ij}}}}}{{{{x}_{j}}{{V}_{{m,j}}} + {{x}_{i}}{{V}_{{m,i}}}{{B}_{{ij}}}}}} \right) - \\ - \,\,\frac{{x_{j}^{2}}}{2}\left[ {\frac{{{{Z}_{i}}B_{{ji}}^{2}{\text{ln}}{{B}_{{ji}}}}}{{{{{({{x}_{i}} + {{x}_{j}}{{B}_{{ji}}})}}^{2}}}} + \frac{{{{Z}_{j}}B_{{ij}}^{2}{\text{ln}}{{B}_{{ij}}}}}{{{{{({{x}_{j}} + {{x}_{i}}{{B}_{{ij}}})}}^{2}}}}} \right], \\ \end{gathered} $(10)
$\begin{gathered} {\text{ln}}{{\gamma }_{j}} = \ln \left( {\frac{{{{V}_{{m,j}}}}}{{{{x}_{j}}{{V}_{{m,j}}} + {{x}_{i}}{{V}_{{m,i}}}{{B}_{{ij}}}}}} \right) + {{x}_{i}}\left( {\frac{{{{V}_{{m,i}}}{{B}_{{ij}}}}}{{{{x}_{j}}{{V}_{{m,j}}} + {{x}_{i}}{{V}_{{m,i}}}{{B}_{{ij}}}}} - \frac{{{{V}_{{m,j}}}{{B}_{{ji}}}}}{{{{x}_{i}}{{V}_{{m,i}}} + {{x}_{j}}{{V}_{{m,j}}}{{B}_{{ji}}}}}} \right) - \\ - \,\,\frac{{x_{i}^{2}}}{2}\left[ {\frac{{{{Z}_{j}}B_{{ij}}^{2}{\text{ln}}{{B}_{{ij}}}}}{{{{{({{x}_{j}} + {{x}_{i}}{{B}_{{ij}}})}}^{2}}}} + \frac{{{{Z}_{i}}B_{{ji}}^{2}{\text{ln}}{{B}_{{ji}}}}}{{{{{({{x}_{i}} + {{x}_{j}}{{B}_{{ji}}})}}^{2}}}}} \right]. \\ \end{gathered} $Значения Bij и Bji при любой температуре могут быть рассчитаны из уравнения (11) предполагая, что $ - \left( {\frac{{{{\varepsilon }_{{ij}}} - {{\varepsilon }_{{jj}}}}}{k}} \right)$ и $ - \left( {\frac{{{{\varepsilon }_{{ji}}} - {{\varepsilon }_{{ii}}}}}{k}} \right)$ в уравнении (7) не зависимы от температуры:
(11)
${{B}_{{ij\left( {\text{2}} \right)}}} = B_{{ij\left( {\text{1}} \right)}}^{{{{T({\text{1}})} \mathord{\left/ {\vphantom {{T({\text{1}})} {T\left( {\text{2}} \right)}}} \right. \kern-0em} {T\left( {\text{2}} \right)}}}},\,\,\,\,{{B}_{{ji\left( {\text{2}} \right)}}} = B_{{ji\left( {\text{1}} \right)}}^{{{{T\left( {\text{1}} \right)} \mathord{\left/ {\vphantom {{T\left( {\text{1}} \right)} {T\left( {\text{2}} \right)}}} \right. \kern-0em} {T\left( {\text{2}} \right)}}}}.$Координационное число Zi жидких металлов может быть рассчитано из уравнения (8), однако, это несколько сложнее, поскольку ряд параметров, включая молекулярные объемы для некоторых компонентов, отсутствует в литературе. Следовательно, упрощение MIVM необходимо для расширения области его применения, поскольку метод прогнозирования, включающий только некоторые параметры, является необходимым.
Фактически, в решеточной теории растворов Z имеет одно и то же постоянное значение между 6 и 12. Кроме того, Z ≈ 10 для типичных жидкостей в обычных условиях [11, 15, 17, 19]. Установлено, что разница между координационными числами компонентов незначительно влияет на точность прогнозирования MIVM [11]. Однако лучшие результаты получены, когда Z близко к 10. Таким образом, в целях упрощения MIVM значения Zi и Zj могут быть равны 10. Кроме того, молярный объем i-компонента в жидком состоянии Vmi может быть заменен его молярным объемом в твердом состоянии Vi [11, 12], поскольку разность плотностей для вещества между жидким и твердым состояниями небольшая, то уравнение (7) можно упростить:
(12)
$\frac{{G_{m}^{E}}}{{RT}} = {{x}_{i}}\ln \left( {\frac{{{{V}_{i}}}}{{{{x}_{i}}{{V}_{i}} + {{x}_{j}}{{V}_{j}}{{B}_{{ji}}}}}} \right) + {{x}_{j}}\ln \left( {\frac{{{{V}_{j}}}}{{{{x}_{j}}{{V}_{j}} + {{x}_{i}}{{V}_{i}}{{B}_{{ij}}}}}} \right) - 5{{x}_{i}}{{x}_{j}}\left( {\frac{{{{B}_{{ji}}}{\text{ln}}{{B}_{{ji}}}}}{{{{x}_{i}} + {{x}_{j}}{{B}_{{ji}}}}} + \frac{{{{B}_{{ij}}}{\text{ln}}{{B}_{{ij}}}}}{{{{x}_{j}} + {{x}_{i}}{{B}_{{ij}}}}}} \right).$Уравнения (9) и (10) также можно упростить до следующего вида:
(13)
$\begin{gathered} {\text{ln}}{{\gamma }_{i}} = 1 + \ln \left( {\frac{{{{V}_{i}}}}{{{{x}_{i}}{{V}_{i}} + {{x}_{j}}{{V}_{j}}{{B}_{{ji}}}}}} \right)--\left( {\frac{{{{x}_{i}}{{V}_{i}}}}{{{{x}_{i}}{{V}_{i}} + {{x}_{j}}{{V}_{j}}{{B}_{{ji}}}}} + \frac{{{{x}_{j}}{{V}_{i}}{{B}_{{ij}}}}}{{{{x}_{j}}{{V}_{j}} + {{x}_{i}}{{V}_{i}}{{B}_{{ij}}}}}} \right) - \\ - \,\,5x_{j}^{2}\left( {\frac{{B_{{ji}}^{2}{\text{ln}}{{B}_{{ji}}}}}{{{{{({{x}_{i}} + {{x}_{j}}{{B}_{{ji}}})}}^{2}}}} + \frac{{B_{{ij}}^{2}{\text{ln}}{{B}_{{ij}}}}}{{{{{({{x}_{j}} + {{x}_{i}}{{B}_{{ij}}})}}^{2}}}}} \right), \\ \end{gathered} $(14)
$\begin{gathered} {\text{ln}}{{\gamma }_{j}} = 1 + \ln \left( {\frac{{{{V}_{j}}}}{{{{x}_{j}}{{V}_{j}} + {{x}_{i}}{{V}_{i}}{{B}_{{ij}}}}}} \right)--\left( {\frac{{{{x}_{j}}{{V}_{j}}}}{{{{x}_{j}}{{V}_{j}} + {{x}_{i}}{{V}_{i}}{{B}_{{ij}}}}} + \frac{{{{x}_{i}}{{V}_{j}}{{B}_{{ji}}}}}{{{{x}_{i}}{{V}_{i}} + {{x}_{j}}{{V}_{j}}{{B}_{{ji}}}}}} \right) - \\ - \,\,5x_{i}^{2}\left( {\frac{{B_{{ij}}^{2}{\text{ln}}{{B}_{{ij}}}}}{{{{{({{x}_{j}} + {{x}_{i}}{{B}_{{ij}}})}}^{2}}}} + \frac{{B_{{ji}}^{2}{\text{ln}}{{B}_{{ji}}}}}{{{{{({{x}_{i}} + {{x}_{j}}{{B}_{{ji}}})}}^{2}}}}} \right). \\ \end{gathered} $Уравнения (13), (14), относящиеся к SMIVM, не содержат координационного числа чистого компонента, что делает эту модель более удобной, по сравнению с MIVM.
Давление насыщенных паров чистых компонентов, необходимое для расчета VLE, может быть получено следующим образом [3–5]:
где psat – давление насыщенных паров чистого компонента в Па; T – абсолютное значение температуры, К; коэффициенты A–D являются константами испарения [20].Сравнили значения содержания компонентов сплавов в жидкой и газовой фазах, полученных по моделям SMIVM и MIVM. Для этого были вычислены показания среднего относительного (${{S}_{i}}$) и среднего квадратичного отклонений ($S_{i}^{*}$):
(16)
${{S}_{i}} = \pm \frac{{100}}{n}\sum\limits_{i = 1}^n {\left| {\frac{{х{{{\left( у \right)}}_{{i,SMIVM}}} - х{{{\left( у \right)}}_{{i,MIVM}}}}}{{х{{{\left( у \right)}}_{{i,SMIVM}}}}}} \right|} \cdot 100\% ,$(17)
$S_{i}^{*} = \pm {{\left[ {\frac{1}{n}\sum\limits_{i = 1}^n {{{{\left[ {х{{{\left( у \right)}}_{{i,SMIVM}}} - х{{{\left( у \right)}}_{{i,MIVM}}}} \right]}}^{2}}} } \right]}^{{0.5}}},$РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исходные характеристики Zn–Ag сплава приведены в табл. 1.
Таблица 1.
Значения параметров $\gamma _{i}^{\infty },$ $\gamma _{j}^{\infty },$ ${{B}_{{ij}}},$ ${{B}_{{ji}}},$ ${{Z}_{i}},$ ${{Z}_{j}},$ $р_{i}^{*},$ $р_{j}^{*},$ Vm(i,j) сплава Zn–Ag
| i–j сплав | Т, К | ${{\gamma _{{{\text{Zn}}}}^{\infty }} \mathord{\left/ {\vphantom {{\gamma _{{{\text{Zn}}}}^{\infty }} {\gamma _{{{\text{Ag}}}}^{\infty }}}} \right. \kern-0em} {\gamma _{{{\text{Ag}}}}^{\infty }}}$ | В | Z | |||
|---|---|---|---|---|---|---|---|
| ${{B}_{{{\text{Zn}}{\kern 1pt} - {\kern 1pt} {\text{Ag}}}}}$ | ${{B}_{{{\text{Ag}}{\kern 1pt} - {\kern 1pt} {\text{Zn}}}}}$ | Zn | Ag | ||||
| Zn/Ag | 1300 | 1.03/1.53 | 0.5236 | 1.395 | 11.04 | 10.61 | |
| Металл | –А | –В | С | D | Vm = f(T), см3/моль | ||
| Zn | 6620 | 1.255 | – | 14.465 | 9.2[1 + 2.065 ·10–4(T – 273)] | ||
| Ag | 14 400 | 0.85 | – | 11.7 | 11.6[1 + 0.98 ·10–4(T – 234)] | ||
Цинк легко возгоняется (высокие значения $р_{{{\text{Zn}}}}^{*}$ = 5.8 · 102 – 3.1 · 104 Па) в отличие от серебра (низкие значения $р_{{{\text{Ag}}}}^{*}$ = 5.3 ⋅ 10–9–5.1 ⋅ 10–5 Па), которое концентрируется в жидкой фазе, что позволяет достаточно полно их разделить вакуумной дистилляцией (табл. 2). Возможность отделения Zn от Ag из их сплава вакуумной дистилляцией характеризуется коэффициентом разделения (β), для расчета которого используют коэффициенты активности (табл. 3, 4).
Таблица 2.
Рассчитанные давления паров Zn и Ag
| Т, К | $р_{{{\text{Zn}}}}^{*},$ Па | $р_{{{\text{Ag}}}}^{*},$ Па | ${{р_{{{\text{Zn}}}}^{*}} \mathord{\left/ {\vphantom {{р_{{{\text{Zn}}}}^{*}} {р_{{{\text{Ag}}}}^{*}}}} \right. \kern-0em} {р_{{{\text{Ag}}}}^{*}}}$ |
|---|---|---|---|
| 823 | 5.79 ·102 | 5.31 ·10–9 | 1.09 ·1011 |
| 923 | 3.73 ·103 | 3.79 ·10–7 | 9.84 ·109 |
| 1023 | 1.65 ·104 | 1.16 ·10–5 | 1.42 ·109 |
| 1073 | 3.10 · 104 | 5.05 ·10–5 | 6.14 ·108 |
Таблица 3.
Рассчитанные значения коэффициентов активности Zn и Ag в расплаве
| T, K | γ | xZn | ||||
|---|---|---|---|---|---|---|
| 0.1 | 0.3 | 0.5 | 0.7 | 0.9 | ||
| 823 | γZn γAg |
0.149 | 0.271 | 0.475 | 0.751 | 0.972 |
| 0.966 | 0.733 | 0.460 | 0.189 | 0.070 | ||
| 923 | 0.218 | 0.364 | 0.576 | 0.819 | 0.982 | |
| 0.981 | 0.824 | 0.558 | 0.307 | 0.180 | ||
| 1023 | 0.295 | 0.456 | 0.663 | 0.870 | 0.989 | |
| 0.984 | 0.859 | 0.643 | 0.430 | 0.333 | ||
| 1073 | 0.334 | 0.500 | 0.701 | 0.891 | 0.992 | |
| 0.986 | 0.874 | 0.681 | 0.490 | 0.418 | ||
Таблица 4.
Рассчитанные значения коэффициента разделения Zn и Ag (lg βZn)
| T, K | xZn | ||||
|---|---|---|---|---|---|
| 0.1 | 0.3 | 0.5 | 0.7 | 0.9 | |
| 823 | 10.2 | 10.6 | 11.1 | 11.6 | 12.2 |
| 923 | 9.34 | 9.64 | 10.0 | 10.4 | 10.7 |
| 1023 | 8.63 | 8.88 | 9.16 | 9.46 | 9.62 |
| 1073 | 8.32 | 8.55 | 8.80 | 9.05 | 9.16 |
Значения βZn > 1, поскольку cодержание Zn в газовой фазе больше, чем в жидкой (уZn $ \gg $ xZn). Цинк концентрируется в газовой фазе, а серебро – в кубовом остатке (xAg $ \gg $ уAg), что разделяет исходный сплав Zn–Ag на цинк и серебро.
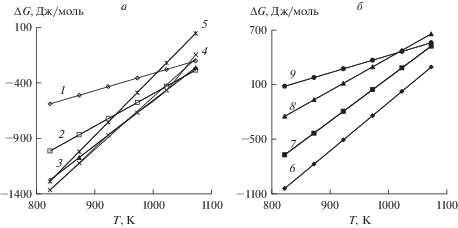
Коэффициент разделения цинка и серебра возрастает (lg βZn = 8.32–12.2) по мере снижения температуры процесса (1073–823 К) и доли серебра (xAg = 0.9–0.1) в составе бинарного сплава (рис. 1). Данные по количественному составу продуктов дистилляции представлены на рис. 2 и в табл. 5.
Рис. 1.
Значения lg βZn при вакуумной дистилляции бинарного сплава при Т, К: 823 (1); 873 (2); 923 (3); 973 (4); 1023 (5); 1073 (6).

Рис. 2.
Равновесная диаграмма “жидкость–газ” Zn–Ag сплава при T, К: 823 (1); 873 (2); 923 (3); 973 (4); 1023 (5); 1073 (6).

Таблица 5.
Рассчитанные значения уAg ⋅ 10–11 сплавa Zn–Ag
| T, K | xZn | ||||
|---|---|---|---|---|---|
| 0.01 | 0.03 | 0.05 | 0.07 | 0.09 | |
| 823 | 1.1 | 0.9 | 0.7 | 0.5 | 0.3 |
| 923 | 9.9 | 8.9 | 7.9 | 6.9 | 5.9 |
| 1023 | 80 | 75 | 70 | 65 | 60 |
| 1073 | 200 | 184 | 165 | 147 | 130 |
Цинк можно отделить от серебра возгонкой при температуре ≤550°С. Исходя из состава сплава (xAg) можно прогнозировать температуру, при которой количество возгоняемой примеси серебра в конденсированном цинке не будет превышать заданную величину: для xAg (ат. %/мас. %) равного 10/16.5 при 600°С значения уAg (ат. %/мас. %) составляют 24 ⋅ 10–12/39.6 ⋅ 10–12, а для 800°С – уAg (ат. %/мас. %) достигает 1300 ⋅ 10–12/ 2145 ⋅ 10–12. В этом случае, при увеличении температуры возгонки на 200°С содержание cеребра в конденсате цинке возрастает более, чем в 50 раз.
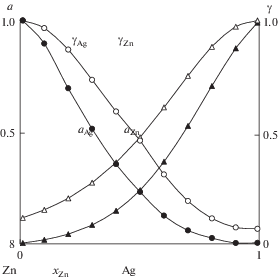
Активности Zn и Ag (aZn, aAg) в расплаве определены с использованием рассчитанных значений коэффициентов активности этих компонентов (γZn, γAg) (рис. 3, табл. 3) [19, 20].
Рис. 3.
Активности (а) и коэффициенты активности (γ) компонентов Zn–Ag сплава при температуре 823 К.
При построении “Т–х” диаграммы бинарной системы Zn–Ag для каждой фиксированной температуры подбирали состав сплава (хZn), при котором сумма парциальных давлений цинка и серебра уравнивала внешнее давление (табл. 6, рис. 4а) [21–26].
Таблица 6.
Рассчитанные значения Tliq, уAg Zn–Ag сплавa для “Т–х” диаграмм
| P, Па | xZn | 0.01 | 0.03 | 0.05 | 0.90 | 0.95 | 0.97 | 0.99 |
|---|---|---|---|---|---|---|---|---|
| 133 | Тliq,К | 1103 | 1027 | 993 | 764 | 761 | 760 | 759 |
| уAg | (85.2–3.2) ·10–8 | ≤ 6.2 ·10–15 | ||||||
| 13.3 | Тliq,К | 961 | 903 | 876 | 682 | 678 | 677 | 676 |
| уAg | (11.3–0.42) ·10–8 | ≤1 ·10–15 | ||||||
| 1.33 | Тliq,К | 852 | 806 | 785 | 615 | 612 | 611 | 610 |
| уAg | (15.3–0.56) ·10–9 | ≤1 ·10–16 | ||||||
Рис. 4.
Фазовые диаграммы “Т–х” (а) и “Р–х” Zn–Ag сплава при давлении, Па: 1.33 (1); 13.33 (2); 133.3 (3), и температуре, К: 873 (4); 973 (5); 1073 (6).

Установлено, что при увеличении глубины вакуума переход из жидкой в газовую фазу происходит в более узком диапазоне температур и способствует разделению Zn и Ag: для получения конденсата цинка при давлении 133 Па · с содержанием серебра не более 8.5 ⋅ 10–8 достаточно температуры ~1100 К. При давлении не более 13 Па и температуре 960 К количество серебра в жидкой фазе (xAg) больше, чем при 13 ≤ Р ≤ 133 Па и 960 ≤ Т ≤ 1103 К, что свидетельствует о благоприятном воздействии низкого остаточного давления в системе на эффективность возгонки цинка при заданной температуре.
Для кубового остатка серебра (xAg ≥ 0.99, xZn ≤ 0.01) по мере снижения давления в последовательности 133/13.3/1.33 Па температура дистилляции также уменьшается до значений 1103/961/852 К, соответственно. Неизменными при этом остаются составы продуктов возгонки, а именно: цинкового конденсата (уZn ≥ 0.99, уAg ≤ 0.01) и кубового остатка серебра (xAg ≥ 0.99, xZn ≤ 0.01). При увеличении содержания цинка в сплаве (xZn) в пределах 0.01–0.99) и по мере снижения давления от 133 до 13.3 Па исходная температура возгонки металлов из состава сплава закономерно снижается от 759 до 610 К, постепенно увеличиваясь по мере возгонки цинка и росте доли серебра в кубовом остатке.
Определены значения относительного (${{S}_{i}}~$ = 1.42%) и квадратичного ($S_{i}^{*}$ = 7.54 К) отклонений, между вычисленными и опытными значениями температур. Относительно невысокие абсолютные значения вычисленных средних отклонений свидетельствуют об адекватности модели процесса вакуумной дистилляции бинарного сплава в исследованных интервалах изменения давления (Р) и температуры (Т).
Расчет диаграмм “Р–х” подобен “Т–х” диаграммам (рис. 4б, табл. 7, 8).
Таблица 7.
Рассчитанные значения Рl ⋅ 103 (Па) Zn–Ag сплавa
| Т, К | xZn | ||||
|---|---|---|---|---|---|
| 0.1 | 0.3 | 0.5 | 0.7 | 0.9 | |
| 873 | 0.028 | 0.148 | 0.409 | 0.856 | 1.37 |
| 973 | 0.21 | 1.01 | 2.53 | 4.83 | 7.23 |
| 1073 | 1.04 | 4.66 | 10.9 | 19.4 | 27.7 |
Таблица 8.
Значения уZn, Pg (Па), γZn, γAg = 1.0 для “Р–х” диаграмм Zn–Ag сплава
| T, K | уZn | 0.1 | 0.3 | 0.5 | 0.7 | 0.9 |
|---|---|---|---|---|---|---|
| 873 | xZn ·10–11 | 3.5 | 13.5 | 31.5 | 73.5 | 284.0 |
| γZn | 0.104 | |||||
| Pg ·10–7 | 0.564 | 0.725 | 1.02 | 1.69 | 5.09 | |
| 973 | xZn ·10–10 | 1.23 | 4.75 | 11.1 | 25.8 | 99.2 |
| γZn | 0.255 | |||||
| Pg ·10–6 | 2.55 | 3.28 | 4.59 | 7.66 | 22.9 | |
| 1073 | xZn ·10–10 | 4.0 | 15.4 | 35.9 | 83.8 | 322 |
| γZn | 0.455 | |||||
| Pg ·10–5 | 5.62 | 7.23 | 10.1 | 16.9 | 50.6 | |
Значения γZn, γAg определены для серии величин хZn при заданной температуре системы, как и давлении насыщенных паров $р_{{{\text{Zn}}}}^{*}$ и $р_{{{\text{Ag}}}}^{*}$ (табл. 1). Затем рассчитаны значения давления (p) в системе для хZn,хAg, γZn, γAg, $р_{{{\text{Zn}}}}^{*},$ $р_{{{\text{Ag}}}}^{*},$ после чего определены величины уZn. Фазовая диаграмма “Р–х” отражает состав получаемых продуктов возгонки в зависимости от температуры и давления: кривые “Р–х” при 1073 K и давлении (0.5–5) ⋅ 10–4 Па свидетельствуют о высокой степени разделения возгона и остатка, а именно: содержание цинка в остатке xZn ≤ 3.22 ⋅ 10–8 при давлении Pg ≤ 5.06 ⋅ 10–4 Па. Данные “Р–х” диаграмм дополняют сведения “Т–х” диаграмм бинарного сплава.
Термодинамические параметры Zn–Ag сплава приведены в табл. 9 и на рис. 5. Энергия Гиббса $G_{m}^{E}$ для бинарной смеси Zn–Ag определяется процессом удерживания вещества в пограничном слое фаз при переходе “жидкость–газ”, который обусловлен соотношением компонентов в сплаве и температурой системы.
Таблица 9.
Рассчитанные значения $G_{m}^{E},$ $Н_{m}^{E},$ $S_{m}^{E}$ Zn–Ag сплавa
| T, K | $G_{m}^{E}$, кДж/моль | ||||
|---|---|---|---|---|---|
| xZn | |||||
| 0.1 | 0.3 | 0.5 | 0.7 | 0.9 | |
| 823 | –0.582 | –1.27 | –1.28 | –0.674 | 0.081 |
| 923 | –0.427 | –0.865 | –0.748 | –0.196 | 0.273 |
| 1023 | –0.272 | –0.459 | –0.212 | 0.283 | 0.464 |
| 1073 | –0.194 | –0.256 | 0.055 | 0.522 | 0.560 |
| $(Н_{m}^{E}$), кДж/моль | –1.86 | –4.61 | –5.72 | –4.61 | –1.53 |
| $S_{m}^{E}$, Дж/моль ·К | 1.57 | 4.06 | 5.38 | 4.78 | 1.92 |
Величина энтальпии пограничного слоя $\left( {H_{m}^{E}} \right)$ определяется энергией Гиббса и теплотой образования поверхности $\left( {TS_{m}^{E}} \right),$ где $S_{m}^{E}$ – энтропия. Значения $H_{m}^{E}$ < 0 свидетельствуют об экзотермическом процессе дистилляции компонентов Zn–Ag сплава. Небольшие значения $G_{m}^{E}~$ ≤ 1.52 кДж/моль отражают слабое взаимодействие между атомами цинка и серебра в жидком сплаве, что на два порядка меньше энергии межатомного взаимодействия в твердой фазе [27–29].
ЗАКЛЮЧЕНИЕ
1. Для температур 823–1073 К рассчитаны давления насыщенного пара для цинка ($p_{{{\text{Zn}}}}^{*}$ = 5.8 ⋅ 102–3.1 ⋅ 104 Па) и серебра ($p_{{{\text{Ag}}}}^{*}$ = 5.3 ⋅ 10–9–5.1 ⋅ 10–5 Па). Цинк легко возгоняется вследствие высоких значений $p_{{{\text{Zn}}}}^{*}$ = 5.8 ⋅ 102–3.1 ⋅ 104 Па в отличие от серебра с низкими значениями $p_{{{\text{Ag}}}}^{*}$ = 5.3 ⋅ 10–9–5.1 ⋅ 10–5 Па, которое концентрируется в жидкой фазе, что позволяет достаточно полно их разделить вакуумной дистилляцией.
2. Исходя из состава сплава (xAg) можно прогнозировать температуру, при которой количество возгоняемой примеси серебра в конденсированном цинке (уAg) не будет превышать заданную величину, например: для xAg (ат. %) = 10 при 600°С значение уAg (ат. %) = = 24 ⋅ 10–12; при возрастании температуры до 800°С величина уAg (ат. %) = 13 ⋅ 10–10, изменяется в большую сторону, практически, на два порядка.
3. Для пограничного слоя “жидкость–газ” системы Zn–Ag вычислены термодинамические функции, кДж/моль: $G_{m}^{E}$ = 0.08–1.36; $ - Н_{m}^{E}$ = 1.53–5.72; $~S_{m}^{E}$ = (1.57–5.38) ⋅ ⋅ 10–3 К–1.
4. Равновесные диаграммы “Т–х” и “Р–х” для системы Zn–Ag можно использовать, в частности, на предварительных этапах проектирования опытно-промышленного оборудования для вакуумной дистилляции, а также для обоснования выбора диапазонов температуры и давления в системе с целью получения продуктов возгонки необходимого состава, минимизируя количество установочных опытов.
Список литературы
Chen W.M., Yang B., Chai L., Min X., Dai Y., Zhang C. Vacuum distillation refining of crude lithium (I) // Transactions of Nonferrous Metals Society of China. 2001. 11. № 6. P. 937–941.
Kong X.-f., Yang B., Xiong H., Kong L.-x. Thermodynamics of removing impurities from crude lead by vacuum distillation refining // Transactions of Nonferrous Metals Society of China. 2014. 24. № 6. P. 1946–1950.
Barbin N., Terentiev D., Alexeev S., Barbina T. // Computational Materials Science. 2013. 66. P. 28–33. https://doi.org/10.1016/j.commatsci.2012.06.013
Dai Y.N. Vacuum distillation and separation of Pb–Sn alloy // Nonferrous Metal. 1977. 9. P. 24–30.
Dai Y.N. Vacuum distillation of Pb–Sn alloy // Nonferrous Metal. 1980. 32. P. 73–79.
Dai Y.N., He A.P. Vacuum distillation of lead-tin alloy // J. Kunming Inst. Technol. 1989. 14. P. 16–27.
Volodin V.N., Isakova R.A., Khrapunov V.E. Liquid-vapour phase equilibrium in metal systems and parameters of vacuum distillation processes forecasting // Non-ferrous Metals. 2011. № 1. P. 38–42.
Морачевский А.Г., Смирнова Н.А., Пиотровская Е.М. Термодинамика равновесия жидкость–пар. Ленинград: Химия, 1989.
Volodin V.N., Khrapunov V.E., Burabaeva N.M., Marki I.A. // Russian J. Non-Ferrous Metals. 2010. 51. № 3. P. 205–211. https://doi.org/10.3103/S1067821210030028
Zhang Y., Deng J., Jiang W., Mei Q., Liu D. Application of vacuum distillation in refining crude lead // Vacuum. 2018. 148. P. 140–148.
Deng J., Zhang Y., Jiang W., Mei Q., Liu D. Harmless, industrial vacuum-distillation treatment of noble lead // Vacuum. 2018. 149. P. 306–312.
Ding J.C., Zhang T.F., Mane R.S., Kim K.-H., Kang M.C., Zou C.W., Wang Q.M. Low-temperature deposition of nanocrystalline Al2O3 films by ion source-assisted magnetron sputtering // Vacuum. 2018. 149. P. 284–290.
Chen S., Fu D., Luo H., Wang Y., Teng J., Zhang H. Hot workability of PM 8009Al/Al2O3 particle-reinforced composite characterized using processing maps // Vacuum. 2018. 149. P. 297–305.
Gerold V., ed. Materials science and technology: a comprehensive treatment. 1. Structure of solids. Weinheim. VCH. 1993.
Afanasieva I.A., Bobkov V.V., Gritsyna V.V., Logachev Yu. E., Okseniuk I.I., Skrypnyk A.A., Shevchenko D.I. On excited particle formation in crossed E × H fields // Vacuum. 2018. 149. P. 124–128.
Shi M., Zhu C., Wei M., He Z., Lu M. Dy3+-, Tb3+-, and Eu3+-activated NaCa4(BO3)3 phosphors for lighting based on near ultraviolet light emitting diodes // Vacuum. 2018. 149. P. 343–349.
Королев А.А., Краюхин С.А., Мальцев Г.И. Равновесные системы “газ–жидкость” для сплава Sb–Ag при вакуумной дистилляции // Обработка металлов (технология, оборудование, инструменты). 2017. 4. № 77. С. 68–83.
Королев А.А., Мальцев Г.И., Тимофеев К.Л., Лобанов В.Г. // Обработка металлов (технология, оборудование, инструменты). 2018. № 1. С. 6–21. https://doi.org/10.17212/1994-6309-2018-20.1-6-21
Chakraborty M., Bhattacharyya S. Air-annealed growth and characterization of Cd1– xZnxTe thin films grown from CdTe/ZnTe/CdTe multi-stacks // Vacuum. 2018. 149. P. 156–167.
Liang L., Dachun L., Heli W., Kaihua L., Juhai D., Wenlong J. Removal of chloride impurities from titanium sponge by vacuum distillation // Vacuum. 2018. 152. P. 166–172.
Trigueiro J., Bundaleski N., Teodoro O.M.N.D. Monitoring dynamics of different processes on rutile TiO2(110) surface by following work function change // Vacuum. 2018. 152. P. 327–329.
Deng L., Lu S., Tang B., Lin Y. Effect of Si on thermal stability of Nb–22.5Cr alloy // Vacuum. 2018. 152. P. 312–318.
Wang L., Guo P., Zhao P., Kong L., Tian Z. Thermodynamic and experimental study of C-S system and C–S–Mo system // Vacuum. 2018. 152. P. 330–336.
Baránková H., Bardos L., Silins K., Bardos A. Reactive deposition of TiN films by magnetron with magnetized hollow cathode enhanced target // Vacuum. 2018. 152. P. 123–127.
Zamchiy A.O., Baranov E.A., Merkulova I.E., Volodin V.A., Sharafutdinov M.R., Khmel S.Ya. Effect of annealing in oxidizing atmosphere on optical and structural properties of silicon suboxide thin films obtained by gas-jet electron beam plasma chemical vapor deposition method // Vacuum. 2018. 152. P. 319–326.
Hu S.P., Hu T.Y., Lei Y.Z., Song X.G., Liu D., Cao J., Tang D.Y. Microstructural evolution and mechanical properties of vacuum brazed Ti2AlNb alloy and Ti60 alloy with Cu75Pt filler metal // Vacuum. 2018. 152. P. 340–346. 27.
Королев А.А., Краюхин С.А., Мальцев Г.И. // Вестник ЮУрГУ. Серия “Металлургия”. 2017. 17. № 2. С. 22–33. https://doi.org/10.14529/met170203
Королев А.А., Краюхин С.А., Мальцев Г.И. // Вестник ПНИПУ. Машиностроение, материаловедение. 2017. 19. № 3. С. 75–99. https://doi.org/15593/2224-9877/2017.3.05
Королев А.А., Краюхин С.А., Мальцев Г.И.Фазовые равновесия для Pb–Zn–Аg сплава при вакуумной дистилляции // Расплавы. 2017. № 5. С. 435–450.
Дополнительные материалы отсутствуют.