Растительные ресурсы, 2019, T. 55, № 2, стр. 246-258
Продуктивность и физиолого-биохимические свойства Menyanthes trifoliata в условиях среднетаежной подзоны Республики Коми
И. Г. Захожий 1, *, С. П. Маслова 1, Г. Н. Табаленкова 1, О. В. Дымова 1
1 Институт биологии Коми НЦ УрО РАН
г. Сыктывкар, Россия
* E-mail: zakhozhiy@ib.komisc.ru
Поступила в редакцию 02.07.2018
После доработки 10.09.2018
Принята к публикации 31.10.2018
Аннотация
Представлены данные сравнительного изучения продуктивности и физиолого-биохимических свойств Menyanthes trifoliata L. в условиях подзоны средней тайги Республики Коми. Растения, произрастающие в условиях низинного болота, накапливали 325 г/м2 фитомассы, около 50% которой приходилось на корневища. Продуктивность растений, обитающих на топяных участках мезоолиготрофного болота, была вдвое ниже. Растения из разных ценопопуляций не имели достоверных различий по содержанию хлорофиллов (a + b) (6–7 мг/г сухой массы) и суммы каротиноидов (около 1.4 мг/г сухой массы), характеризовались высокой активностью фотосинтетического аппарата. Выявлено высокое содержание растворимых углеводов в листьях и корневищах M. trifoliata – 180–400 мг/г сухой массы. Растения низинного болота накапливали на 25–30% меньше сахаров, чем растения мезоолиготрофного болота. Листья растений M. trifoliata из разных ценопопуляций характеризовались значительным содержанием биологически активных соединений – полифенолов (36–43 мг/г), флавоноидов (35 мг/г) и иридоидов (17–21 мг/г в расчете на сухую массу). Концентрация полифенолов в корневищах составляла около 9–11 мг/г, иридоидов 25–29 мг/г сухого растительного материала. Установлено, что растения низинного болота отличались более высоким содержанием азота, фосфора и калия, чем растения мезоолиготрофного болота. Показана значительная аккумуляция железа и марганца растениями эвтрофного болота, что может быть обусловлено высокой доступностью растворимых форм данных элементов, поступающих с грунтовыми водами к корневой системе.
Важную роль в поддержании биологического разнообразия, формировании запасов и потоков углерода в условиях таежных экосистем играют болота, площадь которых составляет 10% всей территории Республики Коми [1]. Зачастую доминантами травянистых сообществ болот в условиях среднетаежной подзоны являются прибрежно-водные гигрогелофиты Comarum palustre L. и Menyanthes trifoliata L. Эти растения могут формировать чистые заросли с обилием до 90% за счет способности к вегетативному размножению с помощью эпигеогенных корневищ [2]. Нами были проведены сравнительные исследования морфофизиологических и биохимических характеристик растений Comarum palustre в условиях средней и крайне-северной тайги [3]. Выявлено значительное уменьшение размеров, снижение биомассы растений, формирование компактных клонов и усиление геофильности корневищ при продвижении на Север.
Вахта трехлистная (Menyanthes trifoliata L.) – прибрежно-водное растение, гигрогелофит из сем. Menyanthaceae [2]. Это бореальный евроазиатский вид, встречается в таежной и тундровой зоне на водоемах, болотах, заболоченных лугах и болотистых лесах [4]. M. trifoliata является лекарственным растением, широко применяется в народной и официальной медицине, включена в фармакопею [5]. Настой из листьев используют в качестве средства, возбуждающего аппетит, способствующего усилению желудочной секреции и улучшению пищеварения. К веществам, обуславливающим фармакологическое действие препаратов на основе M. trifoliata, относят горечи (иридоидные гликозиды, секоиридоиды и их производные), фенольные соединения (флавоноиды, фенольные кислоты, танины).
Сведения о содержании биологически активных веществ в растениях M. trifoliata, произрастающих в условиях Севера, влиянии почвенных и климатических факторов на их накопление единичны [6, 7]. Это обуславливает актуальность проведения исследований, направленных на количественное определение вторичных метаболитов фенольной и терпеноидной природы. Более многочисленны данные литературы о биологии, структурных и функциональных свойствах растений M. trifoliata на европейском северо-востоке. Изучены эколого-физиологические особенности M. trifoliata в условиях северной Карелии [8–10], исследован минеральный состав листьев растений [11]. Приводятся данные о структурных и физиологических свойствах Menyanthes trifoliata [12], продуктивности ценопопуляций данного вида в различных типах растительных сообществ на севере [10, 13–15].
Изучение структурно-функциональных свойств растений M. trifoliata, произрастающих в болотных экосистемах бореальных лесов, важно с позиций их вклада в формирование потоков углерода и круговороте биогенных элементов в условиях естественной динамики почвенно-растительного покрова болот и при изменениях, связанных с воздействием климатических факторов.
Целью наших исследований была сравнительная оценка продуктивности, физиологической активности и биохимического состава растений M. trifoliata, произрастающих в условиях низинного и мезоолиготрофного болот в среднетаежной подзоне Республики Коми.
МАТЕРИАЛ И МЕТОДЫ
Исследования проводили в подзоне средней тайги Республики Коми. Климат района умеренно континентальный, характеризуется сравнительно длинной холодной снежной зимой и умеренно теплым коротким летом. Вегетационный период составляет в среднем 100 дней, а средняя температура самого теплого месяца июля около +17 °С, самого холодного месяца января – –16 °С, среднегодовое количество осадков 700 мм (База данных “Центр по гидрометеорологии и мониторингу окружающей среды Республики Коми”).
Изучали две ценопопуляции Menyanthes trifoliata. Растения первой ценопопуляции произрастали на низинном ключевом хвощово-вахтовом гипновом болоте. В травянистом ярусе доминируют Menyanthes trifoliata (40–45%) и Equisetum fluviatile (30–35%). Менее обильны Poa palustris, Epilobium palustre, Galium palustre, G. uliginosum, Stellaria crassifolia, Rumex acetosa, Saxifraga hirculus. Деревья представлены отдельностоящими Betula pubescens, кустарники представлены Salix phylicifolia и S. pyrolifolia. Напочвенный покров образован гипновыми мхами с проективным покрытием 10%.
Вторая ценопопуляция растений M. trifoliata была локализована на мезоолиготрофном болоте. Отбор образцов проводили на топяных участках в мезотрофных и мезоевтрофных фитоценозах с проективным покрытием вахты не менее 30%. Кроме M. trifoliata в травянисто-кустарничковом ярусе отмечены Scheuchzeria palustris, Carex limosa, Eriophorum vaginatum, E. gracile, Carex rostrata, Equisetum fluviatile, Comarum palustre, Eriophorum gracile, Carex chordorrhiza, Pedicularis palustris. Обилие видов значительно варьирует в зависимости от экологических условий. Моховый покров образован сфагновыми мхами с примесью гипновых [1].
Образцы воды, отобранные на топяных участках мезоолиготрофного болота, имели кислую реакцию (pH 3.8), низкое содержание Ca (2.2 мг/дм3) и Mg (0.8 мг/дм3), и относительно высокое содержание Al и Cu (84 и 8 мг/дм3 соответственно). Минеральные формы азота представлены аммонием (N-NH4 – 0.076 мг/дм3) и нитритами (менее 0.001 мг/дм3), содержание фосфора – около 0.01 мг/дм3. Вода из низинного болота имела близкую к нейтральной реакцию (pH 6.9), сравнительно высокую жесткость (2.12 ммоль/дм3), обусловленную присутствием кальция (29 мг/дм3) и магния (7.8 мг/дм3), содержание ${\text{HCO}}_{3}^{ - }$ – 147 мг/дм3. Минеральный азот представлен нитратной (N-NO3 – 0.036 мг/дм3) и нитритной (N-NO2 – 0.13 мг/дм3) формами, содержание фосфора P-PO4 – 0.02 мг/дм3.
В период цветения (июль) оценивали продуктивность растений M. trifoliata на площадках 1 м2 в 10-кратной повторности в каждой ценопопуляции. Для этого растения выкапывали, отмывали, разделяли на органы, высушивали до постоянной массы при 80 °С и взвешивали.
Оценку функциональной активности фотосинтетического аппарата растений проводили на основании данных индуцированной флуоресценции хлорофилла, полученных с помощью портативного флуориметра РАМ-2100 (Walz, Германия), в лабораторных условиях при температуре 20 °С. Зависимость скорости транспорта электронов (ETR) в электрон-транспортной цепи (ЭТЦ) фотосистемы 2 (ФС2) от освещенности получали, экспонируя листья сначала при минимальной фотосинтетически активной радиации (ФАР), затем интенсивность ФАР ступенчато повышали до максимального уровня 1800 мкмоль/м2 с. Методики расчета ETR и описания световой зависимости скорости транспорта электронов в ЭТЦ ФС2 описаны нами ранее [16].
Содержание хлорофиллов и каротиноидов определяли в ацетоновых экстрактах растительного материала спектрофотометрически [17]. Растительные образцы для других биохимических анализов фиксировали в жидком азоте и подвергали лиофильной сушке. Определение содержания углеводов выполняли спектрофотометрическим методом по колориметрированию избытка щелочного раствора гексацианоферрата (III) калия после реакции с редуцирующими сахарами. Количественный анализ растворимых фенольных соединений и флавоноидов проводили спектрофотометрическим методом [18, 19]. При построении градуировочной зависимости в качестве стандарта применяли галловую кислоту и катехин для суммы фенолов и флавоноидов соответственно. Содержание фенолов выражали в эквивалентах галловой кислоты (GAE), флавоноидов – в эквивалентах катехина (CE), в пересчете на единицу сухой массы растительного материала. Количественный анализ ироидоидов осуществляли спектрофотометрически, после получения соответствующих гидроксамовых кислот в реакции со щелочным раствором гидроксиламина и хлоридом железа III [20]. Содержание суммы иридоидов выражали в эквивалентах герпагида ацетата (EHA) в пересчете на единицу сухой массы растительного материала. Антирадикальную активность метанольных экстрактов растительных образцов проводили с применением спектрофотометрии стабильного свободного радикала 2,2-дифенил-1-пикрилгидразила (ДФПГ) в соответствии с [21]. На основании полученных данных рассчитывали EC50 – величину “эффективного содержания” исследуемого образца, которая необходима для уменьшения количества свободных радикалов ДФПГ в 2 раза. Спектрофотометрические измерения выполняли на сканирующем спектрофотометре UV-1700 (Shimadzu, Япония).
Анализ элементного состава растений выполняли с применением метода оптической эмиссионной спектроскопии с индуктивно связанной плазмой на приборе Spectro Ciros CCD (SPECTRO Analytical Instruments, Германия) после минерализации проб 65%-ной HNO3 в присутствии H2O2. Содержание азота и углерода оценивали методом газовой хроматографии с применением специализированного элементного CHNS-O анализатора в ЦКП “Хроматография” Института биологии Коми НЦ УрО РАН.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В период цветения растения M. trifoliata, обитающие на низинном болоте формировали 173 ± 65 г/м2 надземной фитомассы (листья, черешки листьев, соцветия и цветоносы) и 152 ± 94 г/м2 плагиотропных побегов (корневищ) в расчете на воздушно-сухой материал. Общая продуктивность растений составляла 325 ± 138 г/м2 (рис. 1). Продуктивность растений, произрастающих на топяных участках мезоолиготрофного болота, была значительно ниже и составляла 62 ± 15 г/м2 надземной фитомассы и 72 ± 35 г/м2 плагиотропных побегов. Существенный вклад (47–54%) корневищ в общую фитомассу у растений из разных ценопопуляциий указывает на значительную аллокацию ассимилированного углерода и элементов минерального питания в подземных органах. Анализ данных литературы показывает, что накопление биомассы листьев M. trifoliata варьирует в широких пределах – от 25 до 110 г сухой массы/м2 в разных климатических зонах России [22, 23]. Следовательно, в изученных нами ценопопуляциях растения M. trifoliata характеризуются сравнительно высокими показателями накопления надземной фитомассы.
Рис. 1.
Продуктивность Menyanthes trifoliata в условиях низинного (а) и мезоолиготрофного (b) болот. По горизонтали – часть растения: 1 – надземная часть растения, 2 – корневища, 3 – целое растение; по вертикали – сухая фитомасса, г/м2. Fig. 1. Productivity of Menyanthes trifoliata growing in the rich fen (а) and in the meso-oligotrophic peatland (b). X-axis – plant parts: 1 – above-ground part, 2 – rhizomes, 3 – whole plant; y-axis – dry phytomass, g/m2.
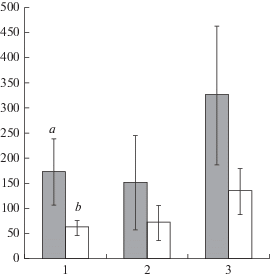
Продуктивность растений тесно связана с интенсивностью фотосинтеза и сопряженных процессов. Содержание фотосинтетических пигментов в листьях рассматривают как один из показателей физиологического состояния растений. Сравнительное исследование пигментного комплекса M. trifoliata не выявило достоверных различий содержания зеленых (хлорофиллов) и желтых (каротиноидов) пигментов в листьях растений разных ценопопуляций. Концентрация хлорофиллов (a + b) составляла в среднем 6–7 мг/г сухой массы, каротиноидов – 1.3–1.5 мг/г сухой массы (табл. 1). Полученные значения близки к средним показателям содержания хлорофиллов и каротиноидов в листьях типичных представителей прибрежно-водных видов макрофитов в условиях среднетаежной подзоны [24]. Доля хлорофилла в составе светособирающего комплекса составляла 57%, что характерно для растений светолюбивого типа.
Таблица 1.
Физиолого-биохимическая характеристика листьев Menyanthes trifoliata Table 1. Physiological and biochemical characteristics of Menyanthes trifoliata leaves
| Параметр Parameter |
Низинное болото Rich fen |
Мезоолиготорофное болото Meso-oligotrophic peatland |
|---|---|---|
| Общий азот, мг/г Total nitrogen content, mg/g DW |
33.0 ± 4.0 | 30.0 ± 3.0 |
| Содержание хлорофилла a, мг/г сухой массы Chlorophyll a content, mg/g DW |
4.58 ± 0.69 | 5.30 ± 0.79 |
| Содержание хлорофилла b, мг/г сухой массы Chlorophyll b content, mg/g DW |
1.60 ± 0.32 | 1.86 ± 0.37 |
| Содержание каротиноидов, мг/г сухой массы Carotenoids, mg/g DW |
1.34 ± 0.20 | 1.45 ± 0.22 |
| Отношение Хл/Кар Chl/Car ratio |
4.6 ± 0.1 | 4.9 ± 0.5 |
| Доля Хл в составе ССК,% Chlorophyll in light-harvesting complex, % |
57 | 57 |
| Максимальная скорость транспорта электронов в ЭТЦ ФС2 (ETRmax), мкмоль/(м2 с) Maximum electron transport rate through photosystem II (ETRmax), µmol m–2 s–1 |
165 ± 4 | 172 ± 5 |
| Интенсивность светового потока при
насыщении ETR (ФАРнас), мкмоль/(м2 с) Saturating photosynthetically active photon flux density (PPFDsat), µmol m–2 s–1 |
998 | 1055 |
Для выявления функциональной активности ассимиляционных органов M. trifoliata была изучена световая зависимость скорости транспорта электронов (ETR) в электрон-транспортной цепи фотосистемы 2 (ФС2) хлоропластов листьев. Величина ETRmax отражает максимальную интенсивность электронного транспорта в ФС2, сопряженную с ассимиляцией углекислого газа и некоторых других процессов, которые поддерживают электронный транспорт, но не связаны с фиксацией CO2 (фотодыхание, ассимиляция нитратов, реакция Мелера). Считается, что в отсутствии стресса существует линейная взаимосвязь между величиной ETR и интенсивностью ассимиляции углекислоты [25]. В процессе изучения фотохимической активности ФС2 листьев M. trifoliata нами не выявлено различий в величине данной характеристики у растений разных ценопопуляций. Величина ETRmax у растений низинного и мезоолиготрофного болот составляла около 170 мкмоль/(м2с), а насыщение фотохимической активности достигалось при уровне потока ФАР (ФАРsat) равном 1000 мкмоль/(м2с). Полученные данные свидетельствуют о формировании пигментного комплекса листьев в благоприятных световых условиях и высокой функциональной активности фотосинтетического аппарата.
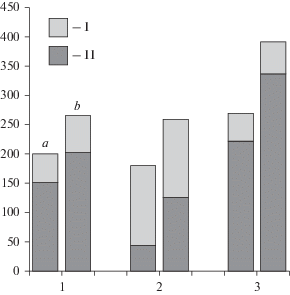
Углеводы, синтезируемые растениями в процессе фотосинтеза, являются исходным материалом для пластического и энергетического обмена. Выявлено, что органы растений M. trifoliata обоих ценопопуляций характеризовались высоким накоплением (от 182 до 392 мг/г сухой массы) растворимых углеводов (рис. 2). Следует отметить, что корневища превосходили листья по содержанию сахаров. В общем пуле углеводов листьев и корневищ преобладали олигосахариды, в черешках листьев – моносахара. Выявлено меньшее содержание сахаров в органах растений низинного болота по сравнению с данными показателями для растений мезоолиготрофного болота. Это может быть связано с большими затратами органического субстрата и энергии на формирование листьев и разрастание плагиотропных побегов (корневищ) растениями в более благоприятных условиях минерального питания на эвтрофном болоте по сравнению с растениями мезоолиготрофного болота.
Рис. 2.
Содержание растворимых углеводов (I – моносахариды; II – олигосахариды) в органах растений Menyanthes trifoliata на низинном (а) и мезоолиготорофном (b) болотах. По горизонтали – часть растения: 1 – листья, 2 – черешки, 3 – корневища; по вертикали – содержание растворимых углеводов, мг/г сухой массы. Fig. 2. Content of soluble carbohydrates (I – monosaccharides; II – oligosaccharides) in Menyanthes trifoliata plant organs in the rich fen (а) and the meso-oligotrophic peatland (b). X-axis – plant parts: 1 – leaves, 2 – petioles, 3 – rhizomes; y-axis – content of soluble carbohydrates, mg/g DW.
Поглощение и транспорт растениями химических элементов зависит от генотипических особенностей вида и, в значительной степени, модулируется условиями среды. Растения M. trifoliata, обитающие на низинном болоте, характеризовались большим, по сравнению с растениями мезоолиготрофного болота, содержанием азота, фосфора и калия (табл. 2). Сравнительно высокая аккумуляция железа и марганца растениями эвтрофного болота (табл. 2) может быть обусловлена повышенным содержанием подвижных форм данных элементов в корнеобитаемом слое. Для таежной зоны Европейского Северо-Востока России железо и марганец являются типоморфными элементами. Грунтовые воды, играющие ключевую роль в питании низинных болот, обогащены соединениями железа и марганца, что способствует аккумуляции этих металлов в болотных низинных почвах и их доступности растениям.
Таблица 2.
Элементный состав фитомассы Menyanthes trifoliata Table 2. Mineral composition of Menyanthes trifoliata dry phytomass
| Элемент Nutrient |
Орган Organs | ||
|---|---|---|---|
| Листья Leaves |
Черешки Petioles |
Корневища Rhizomes |
|
| Макроэлементы, мг/г Macronutrients, mg/g |
|||
| C | $\frac{{443 \pm 16}}{{448 \pm 16{\text{*}}}}$ | $\frac{{415 \pm 14}}{{427 \pm 15}}$ | $\frac{{430 \pm 15}}{{448 \pm 16}}$ |
| N | $\frac{{33.0 \pm 4.0}}{{30.0 \pm 3.0}}$ | $\frac{{17.7 \pm 2.0}}{{18.3 \pm 2.0}}$ | $\frac{{7.8 \pm 1.0}}{{5.1 \pm 1.0}}$ |
| P | $\frac{{5.8 \pm 1.7}}{{3.5 \pm 1.0}}$ | $\frac{{6.8 \pm 2.0}}{{3.8 \pm 1.1}}$ | $\frac{{2.9 \pm 0.9}}{{0.7 \pm 0.2}}$ |
| К | $\frac{{24.0 \pm 9.0}}{{21.0\quad \pm {\text{ }}8.0}}$ | $\frac{{45.0 \pm 18.0}}{{33.0 \pm 13.0}}$ | $\frac{{15.0 \pm 6.0}}{{6.4 \pm 2.5}}$ |
| Ca | $\frac{{5.2 \pm 1.6}}{{5.9 \pm 1.8}}$ | $\frac{{3.4 \pm 1.0}}{{3.0 \pm 0.9}}$ | $\frac{{3.4 \pm 1.0}}{{3.3 \pm 1.0}}$ |
| Mg | $\frac{{2.7 \pm 0.8}}{{3.3 \pm 1.0}}$ | $\frac{{2.9 \pm 0.9}}{{2.6 \pm 0.8}}$ | $\frac{{2.5 \pm 0.8}}{{1.8 \pm 0.5}}$ |
| Микроэлементы, мг/кг Micronutrients, mg/kg |
|||
| Na | $\frac{{560 \pm 220}}{{540 \pm 220}}$ | $\frac{{730 \pm 290\quad}}{{900 \pm 300}}$ | $\frac{{1300 \pm 500}}{{1000 \pm 400}}$ |
| Cu | $\frac{{1.28 \pm 0.26}}{{1.90 \pm 0.40}}$ | $\frac{{1.12 \pm 0.22}}{{1.90 \pm 0.40}}$ | $\frac{{0.30 \pm 0.06}}{{0.53 \pm 0.11}}$ |
| Zn | $\frac{{52 \pm 10}}{{63 \pm 13}}\quad$ | $\frac{{53 \pm 11}}{{60 \pm 12}}$ | $\frac{{58 \pm 12}}{{79 \pm 16}}$ |
| Mn | $\frac{{300 \pm 90}}{{140 \pm 40}}$ | $\frac{{140 \pm 40}}{{72 \pm 22}}$ | $\frac{{170 \pm 50}}{{84 \pm 25}}$ |
| Fe | $\frac{{680 \pm 190}}{{74 \pm 21}}$ | $\frac{{1100 \pm 300}}{{90 \pm 25}}$ | $\frac{{5200 \pm 1400}}{{120 \pm 30}}$ |
| Al | $\frac{{16 \pm 4}}{{13 \pm 3}}$ | $\frac{{30 \pm 8}}{{15 \pm 4}}$ | $\frac{{10 \pm 3}}{{41 \pm 11}}$ |
| B | $\frac{{18 \pm 5}}{{13 \pm 4}}$ | $\frac{{24 \pm 7}}{{17 \pm 5}}$ | $\frac{{31 \pm 9}}{{17 \pm 5}}$ |
Сравнительная оценка распределения химических элементов по органам растений показала, что надземная часть (листья и черешки) превосходили корневища по содержанию N, P, K, Mg и Cu и уступала по накоплению Na и Fe. Черешки характеризовались более высоким содержанием P, K, Na, Fe, Al и B по сравнению с листьями. Полученные результаты согласуются с данными литературы по минеральному составу растений M. trifoliata [11, 26, 27].
Отмершие листья M. trifoliata характеризуются высокими темпами разложения и высвобождения из них элементов минерального питания. В зависимости от почвенных условий время, необходимое для 50%-ного разложения растительного вещества M. trifoliata, составляет от 8–50 дней [28] до нескольких месяцев [29]. Процесс разложения растительных остатков M. trifoliata сопряжен с быстрым выносом из мортмассы углерода, азота и зольных элементов.
Расчеты, основанные на данных о продуктивности растений и их элементном составе, показывают, что за счет формирования надземной фитомассы растения M. trifoliata способны ежегодно вовлекать в круговорот от 19 до 57 кг азота, 2–10 кг фосфора и 13–41 кг калия в расчете на один гектар зарослей. Запасы азота в фитомассе корневищ составляют 3.7–11.9 кг; фосфора – 0.5–4.4 кг; калия – 4.6–22.9 кг в расчете на гектар зарослей. Полученные данные свидетельствуют о существенной роли M. trifoliata в круговороте биогенных элементов эвтрофных и мезоолиготрофных болот с высоким обилием данного вида в составе растительного покрова.
Важным показателем при оценке качества растительного сырья M. trifoliata является содержание иридоидов и фенольных соединений. Суммарное содержание иридоидов в листях M. trifoliata составляет около 16 мг/г [30], флавоноидов – 36 мг/г, фенолкарбоновых кислот – около 23 мг/г сухой массы [31].
Наши исследования выявили существенные отличия органов растений M. trifoliata по содержанию биологически активных соединений. Листья значительно превосходили соцветия и черешки по накоплению флавоноидов (около 35 мг/г сухой массы) и суммы фенольных соединений (36–43 мг/г сухой массы) (табл. 3). Корневища практически в 4 раза уступали листьям по содержанию полифенолов. Органы растений по величине общего пула полифенолов и флавоноидов образуют следующий ряд: листья > > соцветия > черешки ≈ корневища.
Таблица 3.
Суммарное содержание фенолов, флавоноидов, иридоидов и антирадикальная активность фитомассы Menyanthes trifoliata, мг/г сухой массы Table 3. Total polyphenols, flavonoids and iridoid contents and antiradical activity of Menyanthes trifoliata phytomass, mg/g DW
| Орган | Сумма фенолов Total polyphenols |
Флавоноиды Flavonoids |
Иридоиды Iridoids |
EC50, мг сухой массы/г ДФПГ EC50, mg DW/g DPPH |
|---|---|---|---|---|
| Низинное болото The rich fen |
||||
| Листья Leaves |
42.7 ± 1.0 | 36.2 ± 1.8 | 20.9 ± 0.8 | 2847 ± 381 |
| Соцветия Inflorescences |
26.2 ± 0.5 | 21.1 ± 0.5 | 7.8 ± 0.7 | 5388 ± 47 |
| Черешки Petioles |
8.1 ± 0.2 | 7.7 ± 0.1 | 7.9 ± 1.0 | 16 670 ± 67 |
| Корневища Rhizomes |
11.3 ± 0.6 | 9.3 ± 0.1 | 28.7 ± 0.1 | 11 919 ± 504 |
| Мезоолиготрофное болото The meso-oligotrophic peatland |
||||
| Листья Leaves |
36.4 ± 0.6 | 35.0 ± 0.1 | 17.1 ± 0.6 | 2914 ± 85 |
| Соцветия Inflorescences |
32.0 ± 0.6 | 26.7 ± 0.9 | 11.9 ± 2.2 | 3898 ± 71 |
| Черешки Petioles |
12.8 ± 0.2 | 15.1 ± 1.0 | 10.9 ± 1.0 | 7312 ± 106 |
| Корневища Rhizomes |
9.4 ± 0.3 | 8.8 ± 0.1 | 25.0 ± 1.0 | 12 837 ± 556 |
Растительные полифенолы обладают выраженными антиоксидантными и антирадикальными свойствами. Исследование антирадикальной активности метанольных экстрактов M. trifoliata в тесте с ДФПГ показали, что наибольшей способностью ингибирования радикалов обладают спиртовые извлечения из листьев и соцветий (табл. 3), что является следствием большего содержания в них полифенолов. Антирадикальная активность метанольных экстрактов листьев M. trifoliata составляла примерно 2900 мг сухой массы/г ДФПГ, что сопоставимо с ранее полученным величинами (1600–3200 мг сухой массы/г ДФПГ) для растительного сырья Comarum palustre [32].
Наибольшим содержанием суммы иридоидов, до 30 мг/г сухой массы, характеризовались корневища растений M. trifoliata. Листья накапливали 17–21 мг/г сухой массы, соцветия и черешки листьев – не более 12 мг иридоидов в расчете на грамм сухой массы. Представленные данные свидетельствуют о том, что растения, обитающие на территории среднетаежной подзоны Республики Коми, не уступают по накоплению иридоидов растениям из других регионов [7, 30].
Сравнительный анализ показал, что растения M. trifoliata, обитающие в благоприятных для роста условиях на низинном болоте, характеризовались более высоким накоплением полифенолов и иридоидов в листьях и корневищах (табл. 3). Следовательно, наиболее перспективными биотопами для заготовки растительного сырья M. trifoliata в среднетаежной подзоны Республики Коми являются низинные (эвтотрофные) болота.
ЗАКЛЮЧЕНИЕ
Проведено сравнительное изучение продуктивности и физиолого-биохимических свойств Menyanthes trifoliata в условиях подзоны средней тайги Республики Коми. В период цветения растения низинного болота накапливали 325 г/м2 фитомассы, 47% которой приходилось на корневища. Продуктивность растений, обитающих на топяных участках мезоолиготрофного болота, была вдвое ниже. Растения из разных ценопопуляций характеризовались сравнительно высокой активностью фотосинтетического аппарата и не имели достоверных различий по содержанию (в расчете на сухую массу) суммы хлорофиллов (6–7 мг/г) и каротиноидов (около 1.4 мг/г). Показано сравнительно высокое содержание растворимых углеводов в органах растений M. trifoliata, около 180–400 мг/г сухой массы. Растения низинного болота накапливали на 25–30% меньше сахаров, чем растения, обитающие на мезоолиготрофном болоте. Это может быть связано с большими затратами веществ энерго-пластического обмена на формирование листьев и разрастание плагиотропных побегов (корневищ) у растений, обитающих на эвтрофном болоте, по сравнению с растениями мезоолиготрофного болота. Выявлено значительное накопление биологически активных соединений в листьях растений M. trifoliata: содержание полифенолов (в расчете на сухую массу) составляло около 40 мг/г, флавоноидов – 35 мг/г, иридоидов – около 20 мг/г. Корневища характеризовались более высоким содержанием иридоидов (25–29 мг/г), а величина пула полифенолов была в 4 раза меньше, чем в листьях. Растения низинного болота по накоплению биологически активных веществ фенольной и терпеноидной природы в листьях и корневищах превосходили растения мезоолиготрофного болота. Установлены особенности минерального состава органов растений M. trifoliata, произрастающих на болотах с разным типом водного питания. Растения низинного болота, характеризовались более высоким содержанием азота, фосфора и калия. Показана значительная аккумуляция железа и марганца растениями низинного болота. По содержанию железа (5200 мг/кг сухой массы) корневища растений эвтрофного болота более чем в 40 раз превосходили растения мезоолиготрофного болота. В целом, полученные нами данные о продуктивности и элементном составе M. trifoliata свидетельствуют о существенном вкладе вида в общий запас растительного вещества, и в круговорот биогенных элементов эвтотрофных и мезоолиготрофных болотных систем на Севере.
Список литературы
Углерод в лесных и болотных экосистемах особо охраняемых природных территории Республики Коми. 2014. Сыктывкар. 202 с. https://ib.komisc.ru/rus/book-2014/1399-uglerod-v-lesnykh-i-bolotnykh-ekosistemakh-osobo-okhranyaemykh-prirodnykh-territorii-respubliki-komi
Вишницкая О.Н. 2009. Биоморфология некоторых сплавинообразующих гигрогелофитов: Автореф. дис. … канд. биол. наук. Сыктывкар. 19 с. http://www.dissercat.com/content/biomorfologiya-nekotorykh-splavinoobrazuyushchikh-gigrogelofitov
Маслова С.П., Табаленкова Г.Н., Бабак Т.В. 2010. Морфофизиологические и биохимические характеристики Comarum palustre L. на Севере. – Изв. Самарского НЦ РАН. Т.12 (1–3): 760–764. http://www.ssc.smr.ru/media/journals/izvestia/2010/2010_1_760_764.pdf
Мартыненко В.А. 1977. Сем. Menyanthaceae. – В кн.: Флора Северо-Востока Европейской части СССР. Т.IV. Л. С. 63–64.
Государственная фармакопея СССР. XI изд. Вып. 2: Общие методы анализа. Лекарственное растительное сырье. 1990. М. С. 262–264. http://www.fptl.ru/biblioteka/farmacop/gf11-2.pdf
Максимова Т.А., Баранова И.И., Юдина В.Ф. 1980. Сезонное развитие вахты трехлистной и динамика содержания горьких гликозидов, аскорбиновой кислоты и дубильных веществ в ее листьях. – Раст. ресурсы. 16(4): 559–566.
Martz A., Turunen M., Julkunen-Tiitto R., Lakkala K., Sutinen M. 2009. Effect of the temperature and the exclusion of UVB radiation on the phenolics and iridoids in Menyanthes trifoliata L. leaves in the subarctic. – Environmental Pollution. 157(12): 3471–3478. https://doi.org/https://doi.org/10.1016/j.envpol.2009.06.022
Потаевич Е.В., Кузнецов О.Л. 1982. Эколого-физиологические особенности болотных растений. – В кн.: Эколого-биологические особенности и продуктивность растений болот. Петрозаводск. С. 163–187.
Потаевич Е.В., Кучко Л.А. 1979. К физиологии вахты трехлистной. – В кн.: Экология, продуктивность и биохимический состав лекарственных и ягодных растений лесов и болот Карелии. Петрозаводск. С. 104–114.
Юдина В.Ф. 1997. Состояние изученности лекарственных и ягодных растений болот Карелии. – Раст. ресурсы. 33(4): 109–115.
Холопцева Н.П., Юдина В.Ф., Королева Л.Ф. 1988. Минеральный состав листьев Menyanthes trifoliata L. (Карельская АССР). – Раст. ресурсы. 24 (2): 237–241.
Маслова С.П., Табаленкова Г.Н., Канев В.А. 2017 Физиолого-биохимическая характеристика Menyanthes trifoliata (Menyanthaceae) в условиях средней тайги (окрестности г. Сыктывкар). – Раст. ресурсы. 53 (1): 59–69.
Максимова Т.А. 1979. Эколого-фитоценотическая характеристика вахты трехлистной как компонента фитоценозов болот северной Карелии. – В кн.: Экология, продуктивность и биохимический состав лекарственных и ягодных растений лесов и болот Карелии. Петрозаводск. С. 83–104.
Максимова Т.А. 1982. Урожайность вахты трехлистной на болотах Карелии. – В кн.: Комплексные исследования растительности болот Карелии. Петрозаводск. С. 119–134.
Мартыненко В.А., Груздев Б.И., Котелина Н.С. 1994. Недревесные растительные ресурсы Республики Коми. Сыктывкар. 32 с.
Rozentsvet O., Kosobryukhov A., Zakhozhiy I., Tabalenkova G., Nesterov V., Bogdanova E. 2017. Photosynthetic parameters and redox homeostasis of Artemisia santonica L. under conditions of Elton region. – Plant Physiol. Biochem. 118: 385–393. https://doi.org/https://doi.org/10.1016/j.plaphy.2017.07.005
Методика измерений массовой доли пигментов спектрофотометрическим методом (фиксация и экстракция диметилкетоном). Cвидетельство об аттестации методики измерений № 88-17641-077-01.00076-2014. 2014. Сыктывкар. 24 с.
Pekal A., Pyrzynska K. 2014. Valuation of aluminium complexation reaction for flavonoid content assay. – Food Analytical Methods. 7(9): 1776–1782. https://doi.org/https://doi.org/10.1007/s12161-014-9814-x
Singleton V.L., Rossi J.A. 1965. Colorimetry of total phenolics with hosphomolybdic-phosphotungstic acid reagents. – American Journal of Enology and Viticulture. 16 (3): 144–158. http://www.ajevonline.org/content/16/3/144
Шаменкова Н.В. 2005. Усовершенствование определения иридоидов в траве пустырника. – Фармация. 5: 15–19.
Molyneux P. 2004. The use of the stable free radical diphenylpicrylhydrazyl (DPPH) for estimating antioxidant activity. – Songklanakarin J. Sci. Technol. 26(2): 211–219. http://rdo.psu.ac.th/sjstweb/journal/26-2/07-DPPH.pdf
Фетисов А.А., Дмитриев С.В. 1990. Запасы дикорастущих лекарственных растений в западных районах Московской области. – Раст. ресурсы. 26(1): 47–51.
Шутов В.В., Миронов К.А., Письмеров А.В., Задорожный А.М., Лебедев В.П., Смирнов А.Н. 1992. Запасы сырья некоторых дикорастущих лекарственных растений в центральных районах Костромской области. – Раст. ресурсы. 28(1): 41–50.
Дымова О.В., Далькэ И.В. 2016. Фотосинтетические пигменты и СО2-газообмен водных макрофитов в подзоне средней тайги. – Известия Коми научного центра УрО РАН. 1 (25): 37–44. http://www.izvestia.komisc.ru/archive/i25_ann.files/dymova.pdf
Корнеев Д.Ю. 2002. Информационные возможности метода индукции флуоресценции хлорофилла. Киев. 188 с. http://www.oocities.org/photosynthesis_kiev/Kornyeyev_book.pdf
Сосорова С.Б., Меркушева М.Г., Убугунов Л.Л. 2012. Микроэлементный состав некоторых видов растений в окрестностях озера Котокельское (Западное Забайкалье). – Раст. ресурсы. 48 (3): 403–414.
Haraguchi A. 2004. Seasonal changes in redox properties of peat, nutrition and phenology of Menyanthes trifoliata L. in a floating peat mat in Mizorogaike Pond, central Japan. – Aquatic Ecology. 38 (3): 351–357. https://doi.org/https://doi.org/10.1023/B:AECO.0000035171.00202.5c
Kufel L., Kufel I., Krolikowska J. 2004. The effect of lake water characteristics on decomposition of aquatic macrophytes. – Polish Journal of Ecology. 52(3): 261–273. https://miiz.waw.pl/pliki/article/ar52_3_02
Головацкая Е.А., Никонова Л.Г. 2013. Разложение растительных остатков в торфяных почвах олиготрофных болот. – Вестник Томского государственного университета. Биология. 3(23): 137–151. http://journals.tsu.ru/biology/&journal_page=archive&id=926&article_id=29928
Жогова А.А., Самылина И.А., Эллер К.И. 2013. Изучение иридоидов в листьях вахты трехлистной. – Фармация. 6: 17–20. https://pharmaciyajournal.ru/en/pharm-2013-06-05
Ivanisova E., Krajcovic T., Tokar M., Drab S., Kantor A., Kacaniova M. 2017. Potential of wild plants as a source of bioactive compounds. – Scientific Papers: Animal Science & Biotechnologies. 50(1): 109–114. http://www.spasb.ro/index.php/spasb/article/view/2338
Захожий И.Г., Маслова С.П., Табаленкова Г.Н. 2012. Компонентный состав и урожайность Comarum palustre (Rosaceae) в условиях Республики Коми. – Раст. ресурсы. 48 (1): 71–78.
Дополнительные материалы отсутствуют.
Инструменты
Растительные ресурсы


