Теплофизика высоких температур, 2019, T. 57, № 6, стр. 857-862
(PVT)-данные и фазовое равновесие системы ионная жидкость–н-гексан при высоких температурах и давлениях
И. М. Абдулагатов 1, 2, С. М. Расулов 2, *, И. А. Исаев 2, С. М. Оракова 2
1 ФГБОУ ВО Дагестанский государственный университет
г. Махачкала, Россия
2 ФГБУН Институт физики им. Х.И. Амирханова ДНЦ РАН
г. Махачкала, Россия
* E-mail: suleimanr1@rambler.ru
Поступила в редакцию 21.03.2019
После доработки 14.06.2019
Принята к публикации 19.06.2019
Аннотация
Выполнены исследования (PVT)-данных на пьезометре постоянного объема и фазовых равновесий бинарной системы н-гексан–ионная жидкость (10%) в области температур 300–575 К и давлений до 16 МПа. Получены линии фазового равновесия жидкость–жидкость, жидкость–газ и критические параметры исследованной системы.
ВВЕДЕНИЕ
Среди электролитических систем в настоящее время большое внимание уделяют исследованию ионных жидкостей, которые имеют молекулярно-ионную природу с большой ионной составляющей. Научные исследования во многих странах мира направлены на реализацию новых процессов с применением альтернативных растворителей, удовлетворяющих принципам “зеленой химии”. К числу таких растворителей относятся ионные жидкости. Широкое применение в рефрактометрии, в качестве электрохимических сенсоров, в катализе и в органическом синтезе, в электрохимии и в других областях требует изучения физико-химических свойств этих веществ и их растворов с другими веществами, в том числе и с углеводородами. На сегодняшний день в литературе [1–12] представлено мало информации по этим вопросам и имеющиеся данные противоречивы.
ЭКСПЕРИМЕНТАЛЬНАЯ УСТАНОВКА И РЕЗУЛЬТАТЫ
Исследование (PVT)-данных 10% смеси ионной жидкости (1-этил-3-метилимидазолия бис(трифторметилсульфонил)имид) и н-гексана. Измерения выполнены на пьезометре постоянного объема [13] по 10 изохорам в температурной области 300–575 К при давлениях до 16 МПа и в пределах плотности 65.4–663.4 кг/м3. Ранее пьезометр использовался для измерения (PVTx)-данных чистого 1-бутанола и бинарных смесей H2O + н-C5H12 и H2O + н-C6H14 в широком интервале температур и давлений, включающих критические и сверхкритические области [14–19]. Описание установки приведено, например, в [14]. Для настоящих исследований измерение давления осуществлялось мембранным датчиком давления вместо грузопоршневого манометра МП-600. Датчик давления СДВ-А-16,00-4-20мА-0322С-0605-2-код с погрешностью измерения ±0.15% устанавливался на одном конце пьезометра, на другом запорный вентиль, который служил для откачки и заполнения пьезометра.
Давление в объеме пьезометра регистрировалось датчиком давления с точностью ±0.15%. Объем пьезометра, определяемый калибровкой по воде, составлял 24.410 ± 0.025 см3 при ~20°С. Для учета изменения объема пьезометра в зависимости от температуры и давления вносились поправки. Пьезометр заполнялся под вакуумом через вентиль на торце пьезометра. Запорный вентиль имеет два автономных выхода для получения в пьезометре вакуума и заправки его жидкостью через капилляры из нержавеющей стали. Вакуумный выход соединялся с насосом, а капилляр для заправки, снабженный пробкой, опускался в пикнометр с исследуемой жидкостью. Изначально выход для заправки был закрыт и система откачивалась вакуумным насосом. Далее вакуумный выход закрывался и открывался выход для заправки. При этом раствор полностью перетекал из пикнометра в пьезометр. Компоненты смеси взвешивались на аналитических весах с погрешностью не более 0.5 мг. Для подготовки смеси были использованы ионная жидкость (1-этил-3-метилимидазолия бис(трифторметилсульфонил)имид) чистотой 99% и н-гексан марки х. ч.
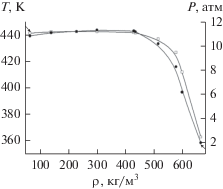
Результаты измерений представлены на рис. 1 и в табл. 1. В нормальном состоянии эти жидкости не смешиваются. Ионные жидкости имеют очень низкое давление насыщенных паров и практически не влияют на давление паров чистого н-гексана. На исследованных изохорах обнаруживаются два излома, соответствующие фазовым переходам. До первого перехода все изохоры совпадают с изохорами чистого н-гексана. Первый переход, можно предположить, соответствует растворению ионной жидкости в н-гексане (переход жидкость–жидкость) и одновременному разложению ионной жидкости. Такой вывод следует из того факта, что повторные измерения Р−Т-данных этой области не совпадают с первоначальными измерениями, образуя гистерезис (рис. 2, 3), и после первого перехода цвет разделившейся меньшей части жидкости приобретает коричневый оттенок. Параметры при повторном измерении смещаются в сторону уменьшения давления относительно давления первоначальных измерений. Следовательно, в системе происходят необратимые процессы. Для проверки проведен эксперимент с визуальным наблюдением. В термостатирующий сосуд высокого давления с оптическими окнами под вакуумом заправлялся н-гексан, в середине н-гексана помещалась тарелочка из нержавеющей стали с ионной жидкостью. Температура системы контролировалась регулятором температуры и измерялась термометром сопротивления ПТС-10. Температура менялась от комнатной до значений выше температуры первого фазового перехода. Наблюдения показали, что в области первого перехода ионная жидкость выделяет пузырки, происходит образование каких-то волокон, цепочек внутри ионной жидкости, и она меняет цвет на коричневый. Однако растворения ионной жидкости в н-гексане не происходит. Следовательно, первый переход не соответствует переходу жидкость–жидкость, а является результатом разложения ионной жидкости. Разложившаяся ионная жидкость остается как балласт в н-гексане в виде растворенных в нем продуктов разложения и продолжает оставаться в таком виде и после перехода н-гексана в пар.
Рис. 1.
P−T-зависимость для системы н-гексан–ионная жидкость по изохорам: 1 − ρ = 65.4 кг/м3, 2 − 139.75, 3 − 228.7, 4 − 300.2, 5 − 429.3, 6 − 514.5, 7 − 576.9, 8 − 598.3, 9 − 663.4.

Таблица 1.
P−T-данные системы н-гексан–ионная жидкость по изохорам
| Р, атм | T, К | P, атм | T, К | P, атм | T, К | P, атм | T, К | P, атм | T, К | Р, атм | T, К | P, атм | T, К | P, атм | T, К | P, атм | T, К |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ρ = 65.4 кг/м3 | ρ = 164 кг/м3 | ρ = 229 кг/м3 | ρ = 300 кг/м3 | ρ = 429 кг/м3 | ρ = 515 кг/м3 | ρ = 577.7 кг/м3 | ρ = 598 кг/м3 | ρ = 663 кг/м3 | |||||||||
| 0.27 | 307.62 | 0.28 | 309.00 | 0.20 | 300.02 | 0.26 | 304.35 | 0.12 | 291.70 | 0.27 | 316.85 | 0.27 | 308.03 | 0.25 | 303.16 | 0.16 | 295.06 |
| 0.37 | 314.62 | 0.51 | 322.23 | 0.30 | 310.43 | 0.28 | 309.51 | 0.42 | 315.33 | 0.68 | 332.60 | 0.55 | 324.29 | 0.50 | 322.03 | 1.38 | 353.58 |
| 0.55 | 323.86 | 0.71 | 334.72 | 0.54 | 323.73 | 0.54 | 323.85 | 0.59 | 325.58 | 1.05 | 345.96 | 0.76 | 335.72 | 0.78 | 337.21 | 1.58 | 357.29 |
| 0.76 | 336.00 | 1.07 | 346.62 | 0.83 | 337.81 | 0.70 | 334.10 | 0.82 | 341.13 | 1.76 | 360.17 | 1.92 | 363.15 | 0.99 | 343.64 | 1.72 | 359.44 |
| 1.16 | 349.15 | 1.88 | 361.15 | 1.30 | 350.33 | 1.12 | 347.67 | 1.53 | 356.59 | 2.46 | 373.28 | 2.81 | 377.35 | 1.29 | 351.49 | 1.92 | 362.69 |
| 1.83 | 361.27 | 2.55 | 374.47 | 2.05 | 364.05 | 1.76 | 359.99 | 1.80 | 361.02 | 3.60 | 386.78 | 3.80 | 389.67 | 1.59 | 357.15 | 1.94 | 362.71 |
| 2.55 | 374.42 | 3.50 | 385.85 | 2.80 | 376.97 | 2.38 | 370.95 | 2.17 | 367.42 | 5.28 | 404.16 | 5.15 | 402.92 | 1.95 | 363.87 | 4.85 | 364.07 |
| 3.53 | 386.72 | 4.85 | 400.13 | 4.11 | 393.50 | 3.43 | 385.23 | 2.18 | 368.08 | 6.35 | 412.62 | 6.53 | 415.61 | 2.31 | 369.65 | 13.21 | 365.72 |
| 4.77 | 399.27 | 5.96 | 410.51 | 6.48 | 412.92 | 4.61 | 398.65 | 3.20 | 382.71 | 6.67 | 416.70 | 7.55 | 423.01 | 2.66 | 376.59 | 13.90 | 365.86 |
| 6.23 | 412.76 | 7.37 | 422.40 | 8.25 | 426.25 | 5.89 | 410.20 | 4.10 | 393.02 | 7.22 | 420.71 | 7.82 | 424.71 | 3.65 | 386.96 | 20.65 | 367.29 |
| 7.50 | 422.41 | 7.55 | 423.20 | 8.80 | 429.43 | 7.50 | 421.92 | 5.50 | 406.55 | 7.81 | 424.55 | 8.35 | 427.17 | 5.00 | 403.93 | 35.25 | 370.35 |
| 8.40 | 429.63 | 7.76 | 424.42 | 9.61 | 434.11 | 8.60 | 429.15 | 6.71 | 417.55 | 8.50 | 428.17 | 8.68 | 428.15 | 5.21 | 414.13 | 47.83 | 372.91 |
| 9.25 | 435.46 | 7.80 | 424.79 | 10.60 | 437.00 | 9.11 | 431.34 | 9.40 | 432.42 | 10.02 | 436.12 | 9.65 | 431.29 | 5.75 | 418.00 | 62.07 | 375.98 |
| 9.80 | 438.41 | 8.31 | 426.94 | 11.21 | 441.68 | 9.95 | 435.75 | 9.72 | 434.84 | 10.50 | 438.62 | 14.34 | 433.40 | 6.15 | 411.13 | 74.60 | 378.50 |
| 10.81 | 440.28 | 9.10 | 431.03 | 11.42 | 443.32 | 10.34 | 437.68 | 10.21 | 436.64 | 10.90 | 440.21 | 21.50 | 435.91 | 6.45 | 413.66 | 87.41 | 381.01 |
| 11.60 | 450.28 | 9.12 | 431.03 | 12.10 | 446.36 | 10.72 | 440.81 | 10.71 | 439.33 | 11.51 | 442.83 | 28.37 | 438.31 | 6.70 | 414.13 | 96.10 | 382.83 |
| 13.85 | 462.90 | 9.40 | 434.56 | 13.19 | 451.83 | 11.23 | 443.53 | 11.19 | 441.56 | 11.99 | 445.60 | 34.73 | 441.06 | 6.81 | 414.62 | 117.25 | 386.77 |
| 14.45 | 464.25 | 10.02 | 439.73 | 14.60 | 456.89 | 11.94 | 445.15 | 11.81 | 444.84 | 12.52 | 447.96 | 43.65 | 444.15 | 7.31 | 419.15 | 145.61 | 393.19 |
| 15.04 | 467.60 | 10.11 | 435.97 | 15.79 | 462.33 | 12.30 | 446.73 | 12.40 | 447.16 | 13.20 | 451.36 | 61.25 | 450.30 | 7.50 | 418.00 | ||
| 15.43 | 474.15 | 11.25 | 443.50 | 16.60 | 465.65 | 13.00 | 450.41 | 13.21 | 451.61 | 14.20 | 455.49 | 101.80 | 466.34 | 7.49 | 417.65 | ||
| 16.60 | 485.15 | 11.37 | 447.90 | 17.27 | 468.43 | 13.45 | 452.45 | 14.11 | 454.77 | 15.00 | 458.16 | 146.19 | 479.96 | 10.12 | 419.95 | ||
| 17.78 | 497.15 | 12.05 | 448.83 | 17.75 | 469.90 | 14.40 | 455.93 | 14.61 | 457.29 | 15.65 | 461.53 | 166.20 | 486.67 | 15.78 | 420.03 | ||
| 18.80 | 508.11 | 13.10 | 453.86 | 18.43 | 472.66 | 15.25 | 459.46 | 16.10 | 463.19 | 16.30 | 463.66 | 15.90 | 420.64 | ||||
| 19.12 | 510.26 | 13.80 | 460.09 | 18.90 | 474.31 | 16.25 | 463.35 | 17.20 | 467.26 | 16.56 | 464.92 | 23.45 | 422.12 | ||||
| 19.70 | 521.86 | 14.75 | 461.75 | 19.82 | 478.27 | 17.06 | 466.63 | 18.25 | 471.62 | 17.60 | 467.94 | 31.81 | 425.00 | ||||
| 20.65 | 533.92 | 16.23 | 468.01 | 20.25 | 478.96 | 18.30 | 470.31 | 17.00 | 466.31 | 18.20 | 471.13 | 37.80 | 426.76 | ||||
| 21.49 | 541.51 | 16.80 | 471.71 | 21.10 | 481.62 | 19.08 | 473.42 | 17.65 | 468.19 | 20.01 | 473.61 | 40.26 | 427.65 | ||||
| 22.45 | 555.68 | 17.27 | 474.65 | 22.11 | 484.87 | 20.37 | 476.82 | 18.25 | 471.49 | 28.02 | 477.92 | 46.60 | 429.63 | ||||
| 23.20 | 566.17 | 17.91 | 478.46 | 24.41 | 489.11 | 20.85 | 479.92 | 19.20 | 474.50 | 45.93 | 488.67 | 57.40 | 433.00 | ||||
| 19.60 | 485.35 | 25.05 | 493.72 | 21.71 | 482.25 | 20.59 | 479.22 | 68.65 | 500.95 | 75.79 | 438.40 | ||||||
| 19.62 | 485.87 | 26.65 | 498.15 | 22.36 | 483.75 | 21.37 | 481.82 | 88.70 | 511.55 | 95.19 | 445.00 | ||||||
| 22.41 | 495.95 | 27.00 | 501.53 | 23.11 | 485.94 | 22.21 | 484.82 | 111.57 | 524.18 | 113.00 | 450.84 | ||||||
| 25.31 | 503.17 | 29.81 | 505.83 | 24.14 | 488.74 | 23.30 | 487.16 | 163.10 | 548.25 | 148.42 | 461.56 | ||||||
| 26.03 | 508.06 | 33.60 | 517.75 | 25.06 | 491.82 | 24.30 | 489.40 | ||||||||||
| 28.65 | 519.19 | 37.45 | 528.07 | 25.95 | 493.80 | 24.91 | 491.41 | ||||||||||
| 29.60 | 525.52 | 41.35 | 538.65 | 26.81 | 496.86 | 25.65 | 493.77 | ||||||||||
| 33.04 | 547.70 | 45.20 | 550.60 | 27.72 | 498.61 | 26.62 | 496.80 | ||||||||||
| 34.91 | 563.91 | 28.70 | 501.06 | 27.60 | 498.45 | ||||||||||||
| 37.89 | 586.33 | 29.74 | 504.17 | 29.55 | 500.83 | ||||||||||||
| 41.75 | 607.91 | 30.89 | 506.77 | 31.65 | 503.27 | ||||||||||||
| 31.60 | 509.00 | 33.90 | 505.88 | ||||||||||||||
| 34.48 | 514.09 | 41.85 | 513.62 | ||||||||||||||
| 37.13 | 519.47 | 48.51 | 519.50 | ||||||||||||||
| 41.20 | 529.55 | 61.15 | 529.74 | ||||||||||||||
| 48.14 | 541.17 | 88.62 | 555.63 | ||||||||||||||
Рис. 2.
Первоначальная и повторная изохоры системы н-гексан–ионная жидкость в области первого фазового перехода при ρ = 65.4 кг/м3.

Рис. 3.
Первоначальная и повторная изохоры системы н-гексан–ионная жидкость в области первого фазового перехода при ρ = 139.75 кг/м3.

Линии первого фазового перехода в Т−ρ- и Р−ρ-диаграммах приведены на рис. 4. Второй переход соответствует фазовому переходу жидкость–газ. При повторном измерении области второго фазового перехода различия между данными измерений не обнаружено, обе группы данных совпадают в пределах погрешности измерения. Это указывает на то, что при переходе жидкость–газ необратимые процессы не происходят. После первого перехода вплоть до перехода жидкость–газ изохоры незначительно смещены друг относительно друга, но практически имеют вид кривых для простых жидкостей.
Линии фазового перехода жидкость–газ приведены на рис. 5, параметры перехода по изохорам даны в табл. 2. Параметры перехода жидкость–газ этой системы, определенные методом прямолинейного диаметра, равны Тк = 510.25 К, Рк = 3.222 МПа и ρк = 346 кг/м3. Для чистого н-гексана критические параметры равны соответственно Тк = 507.82 К, Рк = 3.044 МПа и ρк = = 233.19 кг/м3. Как видно, добавление ионной жидкости вызывает незначительное увеличение критических температуры и давления и значительное увеличение критической плотности.
Таблица 2.
Параметры фазового равновесия при первом и втором переходах системы н-гексан–ионная жидкость
| ρ, кг/м3 | Первый переход | Второй переход | ||
|---|---|---|---|---|
| T, К | P, атм | T, К | P, атм | |
| 65.4 | 440.8 | 10.75 | 468.65 | 14.82 |
| 139 | 441.75 | 11.02 | 470.27 | 16.75 |
| 229 | 441.9 | 11.12 | 489.1 | 24.40 |
| 300 | 441.9 | 11.24 | 505.65 | 30.72 |
| 429 | 441.15 | 11.16 | 500.66 | 28.52 |
| 434.7 | 440.95 | 11.10 | 499.07 | 27.85 |
| 515 | 438.19 | 10.81 | 470.65 | 18.21 |
| 577 | 426.4 | 8.22 | 426.4 | 8.22 |
| 598 | 411.66 | 6.13 | 411.66 | 6.13 |
| 663 | 363.14 | 1.97 | 363.14 | 1.97 |
ЗАКЛЮЧЕНИЕ
На основе результатов экспериментальных исследований показано, что в изученной системе по изохорам имеются два фазовых перехода. Первый переход связан с разложением ионной жидкости и растворением продуктов разложения в н-гексане, а второй − с фазовым переходом жидкость–газ. Определены параметры фазовых переходов, линии фазового равновесия и критические параметры исследованной системы. Критические температура и давление незначительно выше, чем у чистого н-гексана, а критические плотности различаются значительно. Данные эксперимента могут быть использованы в процессах катализа и органического синтеза, в процессе синтеза высокомолекулярных соединений.
Список литературы
Kenta Fujii, Yasufumi Soejima, Yasuhiro Kyoshoin, Shuhei Fukuda, Ryo Kanzaki, Yasuhiro Umebayashi, Toshio Yamaguchi, Shin-ichi Ishiguro, Toshiyuki Takamuku. Liquid Structure of Room-temperature Ionic Liquid, 1-ethyl-3-methylimidazolium bis(trifluoromethanesulfonyl)imide // J. Phys. Chem. B. 2008. V. 112. № 14. P. 4329.
Gahlmann A. Ionic Liquids for Electrochemical Applications // Aldrich Chemfiles. 2005. V. 5(6). P. 10.
Van-Oanh Nquyen-Thi, Houriez C., Roussean B. Viscosity of the 1-ethyl-3-methylimidazolium bis(trifluiromethylsulfonyl)imide Ionic Liquid from Equilibrium and Nonequilibrium Molecular Dynamics // Phys. Chem.-Chem. Phys. 2010. V. 12. № 4. P. 930.
Safarov J., El-Awady W.A., Shahverdiyev A., Hassel E. Thermodynamic Properties of 1-ethyl-3-methylimi-dazolium bis(trifluiromethylsulfonyl)imide // J. Chem. Eng. Data. 2011. V. 56. № 1. P. 106.
Andreas H., Lehmann J.K., Wertz Ch. Thermodynamic Properties Containing Ionic Liquids. 3.Liquid-liquid Equilibria of Binary Mixtures 1-ethyl-3-methylimida-zolium bis(trifluiromethylsulfonyl)imide with Propanon-1-ol, Butan-1-ol, and Pentan-1-ol // J. Chem. Eng. Data. 2003. V. A107. № 42. P. 8872.
Kelkar M.S., Maginn E.J. Effect of Temperature and Water Content of the Shear Viscosity of the Ionic Liquid 1-ethyl-3-methylimidazolium bis(trifluiromethylsulfonyl)imide as Studied by Atomistic Simulations // J. Phys. Chem. B. 2007. V. 111. № 18. P. 4867.
Kato R., Krummen M., Gmehling J. Measurement and Correlation of Vapor-liquid Equilibria and Excess Enthalpies of Binary Systems Containing Ionic Liquids and Hydrocarbons // Fluid Phase Equilib. 2004. V. 224. P. 47.
Shamsipur M., Brigi A.-A.M., Teyouri M., Pourmortazavi S.M., Irandoust M. Physical and Electrochemical Properties of Ionic Liquids 1-ethyl-3-methylimadasolium Tetrafluoborate, 1-buthyl-3-methylimadasolium Fluoromethanesulfonate and 1-buthyl-1-mrthylpyrrolidinium bis(trifluoromethylsulfonyl)imide // J. Mol. Liquids. 2010. V. 157. P. 43.
Шведене Н.В., Чернышев Д.В., Плетнев И.В. Ионные жидкости в электрохимических cенсорах // Рос. хим. журн. 2008. № 2. С. 80.
Ngo H.L., LeCompte K., Hargens L. Thermal Properties of Imidazolium Ionic Liquids // Thermochem. Acta. 2000. V. 357–358. P. 97.
Khupse N.D., Kumas A. Ionic Liquids: New Materials with Wide Applications // Ind. J. Chem. 2010. V. 49A. P. 635.
Musial M., Zarebski M., Dzida M., Safarov J., Zarebski E., Hassel E. High Pressure Speed of Sound and Related Properties of 1-ethyl-3-methylimadazolium Methanesulfonate // J. Mol. Liquids. 2019. V. 276. P. 885.
Расулов С.М., Хамидов М.М. Установка для одновременного измерения давления, температуры, объема и вязкости жидкостей и газов // ПТЭ. 1999. № 1. С. 148.
Rasulov S.M., Abdulagatov I.M. PVTx Measurements of Water–n-pentane Mixtures in the Critical and Supercritical Regions // J. Chem. Eng. Data. 2010. V. 55. P. 3247.
Rasulov S.M., Radzhabova L.M., Abdulagatov I.M., Stepanov G.V. Experimental Study of the PVT and CvVT Properties of n-butanol in the Critical Region // Fluid Phase Equuilib. 2013. V. 337. P. 323.
Orakova S.M., Rasulov S.M., Abdulagatov I.M. Experimental Study of the PVTx Relationship, L–L–V and L–V Phase Boundary of n-hexane + Water Mixtures near the Upper and Lower Critical Lines // Phys. Chem. Liquids. 2014. V. 52. P. 130.
Orakova S.M., Rasulov S.M., Abdulagatov I.M. Experimental Study of the Isomorphism behavior of Weakly (CVX) and Strongly (CPX, KTX) Singular Properties of 0.082n-Hexane + 0.918water Mixtures near the Upper Critical Point // J. Mol. Liquids. 2013. V. 187. P. 7.
Расулов С.М., Оракова С.М., Абдулагатов И.М. Термодинамические и структурные свойства смеси н-гексан–вода вблизи критической точки чистого растворителя // ТВТ. 2015. Т. 53. № 4. С. 524.
Расулов С.М., Оракова С.М., Исаев И.А. Термические свойства и фазовые диаграммы водно-углеводородных систем // ТВТ. 2016. Т. 54. № 2. С. 223.
Дополнительные материалы отсутствуют.
Инструменты
Теплофизика высоких температур