Теоретические основы химической технологии, 2019, T. 53, № 2, стр. 152-159
Характеристики паровоздушной газификации углеродного топлива в фильтрационном режиме при повышенном давлении
С. В. Глазов 1, *, Е. В. Полианчик 1
1 Институт проблем химической физики РАН
Черноголовка, Россия
* E-mail: glazov@icp.ac.ru
Поступила в редакцию 29.06.2016
После доработки 07.08.2018
Принята к публикации 28.06.2018
Аннотация
Представлены результаты расчетов стационарного режима фильтрационного горения смесей углерода с твердым негорючим материалом в противотоке газообразного окислителя (паровоздушная смесь) в предположении термодинамически равновесного состава газообразных продуктов и самосогласованной с ним температуре горения. Рассмотрено влияние давления в реакторе на температуру горения и состав газообразных продуктов. Показано, что повышение давления приводит к повышению температуры, уменьшению выхода водорода и снижению чувствительности режима горения к содержанию водяного пара в окислителе.
ВВЕДЕНИЕ
Технологии на основе так называемого прямого процесса газификации, в которых используются встречные потоки твердого горючего и газообразного окислителя, являются наиболее выгодными с точки зрения преобразования энергетического потенциала топлива в теплотворную способность газа [1]. В частности, “сверхадиабатические” режимы фильтрационного горения (ФГ) рассматриваются в качестве основы для создания перспективных методов переработки горючих отходов и получения энергии из низкосортных топлив [2, 3]. Промышленные процессы газификации часто реализуют при повышенном давлении, способствующем увеличению скорости и полноты химических превращений и, следовательно, позволяющем значительно уменьшить габариты реакторов [4]. Влияние повышенного давления на характеристики фильтрационного горения углеродного топлива неоднозначно. С одной стороны, как было упомянуто, повышение давления позволяет увеличить скорость протекания химических реакций, уменьшить линейные скорости газовых потоков и увеличить удельную производительность реакторов. Но, с другой стороны, целевым продуктом газификации углеродного топлива, как правило, является газ с максимально возможным количеством водорода и монооксида углерода, и повышение давления (в соответствии с принципом Ле-Шателье) будет снижать их выход. Кроме того, неизбежно возрастает стоимость аппаратного оформления процесса. Следовательно, целесообразность повышения давления в процессах газификации не так очевидна. Отсюда следует важность учета давления при оптимизации подобных процессов.
При сравнительно малых скоростях подачи газа-окислителя (т.е. медленном распространении фронта горения) и при высоких температурах химические реакции можно считать быстрыми, и лимитирующим процессом становится поступление реагентов в зону химических реакций. При этом реализуются режимы с полным расходованием реагентов, в которых кинетические параметры системы перестают входить в определяющие соотношения [5], что довольно часто реализуется в “сверхадиабатических” режимах ФГ [3, 6]. Известно, что в этом случае вместо кинетических данных можно использовать условие термодинамического равновесия в продуктах при температуре горения, что практикуется для оценок параметров газификации [4]. Модель фильтрационного горения углеродных систем в приближении термодинамически равновесного состава продуктов, самосогласованного с температурой горения, была представлена в наших предыдущих работах [7, 8]. В процитированных работах приведены результаты расчета режимов ФГ смесей углерода с твердым химически инертным материалом (инертом) при фильтрации кислородно-азотных смесей различной концентрации, рассмотрено влияние добавки эндотермических окислителей (диоксид углерода и водяной пар). В настоящей работе в общих рамках подхода, развитого в работах [7, 8], рассматривается влияние давления в реакторе на температуру и состав газообразных продуктов при фильтрационном горении углеродных топлив в “сверхадиабатических” режимах ФГ.
ОПИСАНИЕ МОДЕЛИ
Предложенная в [7, 8] математическая модель позволяет рассчитать концентрации продуктов и температуру горения при газификации твердого топлива (смеси углерода с твердым инертным негорючим материалом) в режиме фильтрационного горения в противотоке кислородсодержащего газа для заданных состава твердого топлива (отношения углерод/инерт), давления и состава газообразного окислителя без использования данных о детальном кинетическом механизме реакций окисления. Модель базируется на следующих основных допущениях:
– реакция протекает в узкой зоне горения, ширина зон теплообмена много меньше размеров реактора;
– в зоне горения происходит полное расходование углерода и кислорода;
– состав продуктов горения отвечает химическому равновесию газов над поверхностью углерода при температуре горения;
– линейная скорость газового потока невелика, что позволяет пренебречь кинетической энергией газа по сравнению с тепловой и химической;
– теплопотери через стенки реактора отсутствуют.
Указанное приближение позволяет выявить качественные закономерности процесса и провести оценку влияния на режимы газификации от состава твердого топлива, состава газообразного окислителя и давления.
Область применимости модели ограничивается стехиометрическими режимами [5, 7], в которых скорость химических реакций достаточно высока, а скорости подачи компонентов достаточно малы для того, чтобы химическое превращение реагентов успевало завершиться, и термодинамически равновесный состав продуктов успевал установиться в сравнительно узкой зоне реакции. Границы области применимости подробно рассмотрены в опубликованной ранее работе [7]. В дальнейшем рассмотрении состав газообразных продуктов ограничивается набором следующих компонентов: азот, монооксид и диоксид углерода, водород, метан и водяной пар. Будем считать, что остальные компоненты присутствуют в столь незначительных количествах, что не могут оказать существенного влияния на результаты. Как было показано ранее [8], в рассматриваемых условиях равновесная концентрация других возможных продуктов пренебрежимо мала. Как следует из рассмотрения в [7, 8], общее давление в реакторе является независимым управляющим параметром, однако расчеты влияния давления на режимы процесса выполнены не были. В настоящей работе мы рассматриваем это влияние.
В замкнутую систему уравнений [8] входит уравнение сохранения энергии, которое в сделанных предположениях имеет вид сохранения энтальпии во фронте горения для нормальной структуры зоны горения
(1)
$\begin{gathered} {{x}_{0}}{{H}_{x}}({{T}_{b}}) + {{n}_{0}}{{H}_{n}}({{T}_{b}}) + {{w}_{0}}{{H}_{w}}({{T}_{b}}) + \\ + \,\,a{{H}_{a}}({{T}_{0}}) + {{c}_{0}}{{H}_{c}}({{T}_{0}}) = n{{H}_{n}}({{T}_{0}}) + \\ + \,\,m{{H}_{m}}({{T}_{0}}) + d{{H}_{d}}({{T}_{0}}) + e{{H}_{e}}({{T}_{0}}) + \\ + \,\,h{{H}_{h}}({{T}_{0}}) + w{{H}_{w}}({{T}_{0}}) + a{{H}_{a}}({{T}_{b}}), \\ \end{gathered} $а для инверсной
В систему уравнений также входят условия поэлементного сохранения в зоне реакции:
(5)
${\text{а з о т а }}\quad\quad\quad\quad\quad\quad\quad\,\,\,\,\,\,\,\,\,\,{{n}_{0}} = {\text{ }}n,$Использованное в модели приближение идеального газа предполагает, что заданное полное давление является суммой парциальных давлений компонентов. Условие термодинамического равновесия в продуктах горения, записанное через константы диссоциации и давление насыщенных паров углерода [8], дает три независимых замыкающих уравнения, которые можно привести к виду
где κ1(T), κ2(T) и κ3(T) – функции только температуры, выражающиеся через константы диссоциации как(11)
${{\kappa }_{2}}(T) = \frac{{{{K}_{m}}(T){{K}_{e}}(T)}}{{{{K}_{w}}(T){{K}_{h}}(T)P_{{\text{C}}}^{2}(T)}},$(12)
${{\kappa }_{3}}(T) = \frac{{{{{\left[ {{{K}_{h}}(T)} \right]}}^{2}}{{P}_{{\text{C}}}}(T)}}{{{{K}_{e}}(T)}}.$Получение аналитического решения системы уравнений (1)–(9) для температуры и состава продуктов при заданном составе реагентов затруднительно, но расчет для каждого конкретного значения управляющих параметров можно провести с помощью стандартных численных методов. Проведенное в [8] сопоставление результатов расчетов равновесного состава газообразных продуктов по вышеописанной модели с результатами расчетов по стандартной программе термодинамических равновесий показало, что приближение (7)–(9) позволяет с достаточной точностью рассчитать равновесный состав газообразных продуктов.
Представленные ниже расчеты проведены для случаев, когда твердое топливо представляет собой смесь углерода с инертом. В расчетах использовали значения термодинамических функций (энтальпии, константы диссоциации), опубликованные в [9]. Термодинамические свойства углерода полагали соответствующими свойствам графита, а для инерта использованы характеристики Al2O3. В качестве газообразного окислителя рассматривается смесь воздуха (21 об. % O2, 79 об. % N2) с водяным паром. Доля углерода в топливе и доля пара в газообразном окислителе, а также давление – управляющие параметры, значения которых варьировали в ходе расчетов.
РЕЗУЛЬТАТЫ РАСЧЕТОВ
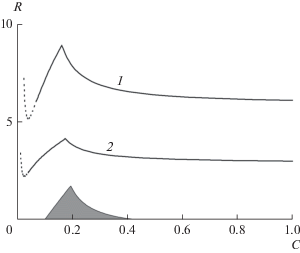
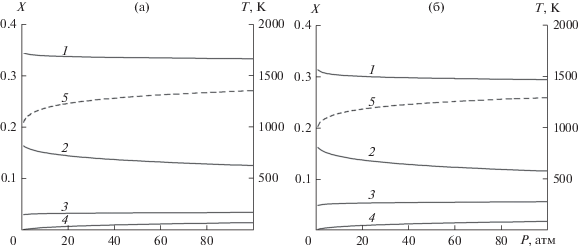
На рис. 1а представлены зависимости температуры горения и объемных долей газообразных продуктов от давления при мольном отношении пар/кислород в газообразном окислителе R = = [H2O]/[O2] = 1.5 и при содержании углерода в топливе 40 мас. % (при этом реализуется инверсная структура фронта горения). Аналогичные зависимости для состава с нормальной тепловой структурой фронта (содержание углерода 12 мас. %) представлены на рис. 1б. При определенном составе реагентов (т.е. при заданных содержании углерода в топливе и отношении пар/кислород в газообразном окислителе) повышение давления в реакторе приводит к увеличению температуры горения, а также к снижению концентрации водорода и монооксида углерода в газообразных продуктах.
Рис. 1.
Зависимость объемных долей газообразных продуктов (сплошные линии, 1 – CO, 2 – H2, 3 – CO2, 4 – CH4) и температуры горения (пунктирная линия 5) от давления при отношении пар/кислород R = 1.5 и содержании углерода 40 (а) и 12 мас. % (б).
Общую картину влияния давления на температуру наглядно показывает изменение положения изолиний на диаграмме исходных составов (рис. 2), где по оси абсцисс – состав твердого топлива (массовая доля углерода в смеси), а по оси ординат – состав газа-окислителя (мольное отношение пар/кислород R = [H2O]/[O2] при фиксированном объемном отношении кислород/азот = 21/79). Характеристики, рассчитанные для конкретного исходного состава реагентов, соответствуют определенной точке на этой диаграмме. Характеристики, представленные на рис. 1а и 1б, соответствуют точкам А и B на рис. 2.
Рис. 2.
Расчетные изолинии температуры горения (1 – 1000 К; 2 – 1200; 3 –1500; 4 – 2000 К) на диаграмме составов для различных значений давления: (а) – 1, (б) – 20, (в) – 100 атм.
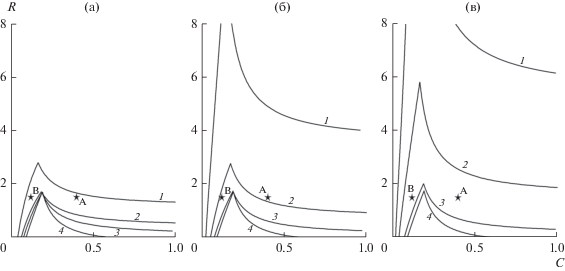
На диаграмме видно, что при повышении давления происходит увеличение температуры горения, причем существенно более сильное для параметрической области, где температуры горения невысоки. Изолинии высокой температуры почти не реагируют на повышение давления: сдвиг изолиний Tb = 2000 K (кривые 4) при повышении давления от 1 до 100 атм незаметен в масштабе рис. 2, в то время как изолинии для Tb = 1000 K (кривые 1) сдвигаются значительно. Такой сдвиг изолиний вверх в практическом смысле означает, что увеличение количества пара в газе-окислителе будет существенно слабее влиять на температуру горения.
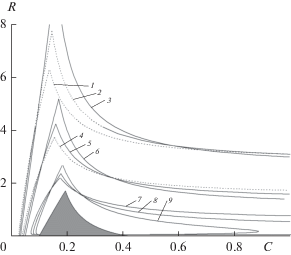
Что касается состава продукт-газа, в первую очередь рассмотрим изменение содержаний монооксида углерода и водорода, поскольку это два основных компонента целевого продукта (синтез-газа). Результаты расчетов показывают, что при повышении общего давления содержание водорода в продукт-газе довольно резко уменьшается, причем особенно резко в области невысоких (меньше 1200 К) температур. На рис. 3 представлены изолинии 15 (а), 12 (б) и 10% (в) объемного содержания водорода в продукт-газе для различных давлений. Состав продукт-газа рассматриваем за вычетом содержащейся в нем воды (сухой газ). Затемненный треугольник в нижней части диаграммы составов соответствует режимам со слишком высокой температурой горения (выше 2300 K), которые не могут быть реализованы даже с использованием в качестве инерта такого огнеупорного материала, как окись алюминия. Пунктиром соответствующие изолинии показаны в области составов, для которых расчетная температура ниже 1000 К (ср. с рис. 2). В этой параметрической области достижение термодинамического равновесия в продуктах труднодостижимо в реальных практических применениях. Конкретное значение граничной температуры выбрано нами произвольно.
Рис. 3.
Расчетные изолинии 15 (а), 12 (б) и 10 об. % (в) содержания водорода в продуктах для различных значений давления: 1 – 1, 2 – 10, 3 – 20, 4 – 25, 5 – 30, 6 – 35, 7 – 50, 8 – 100 атм.
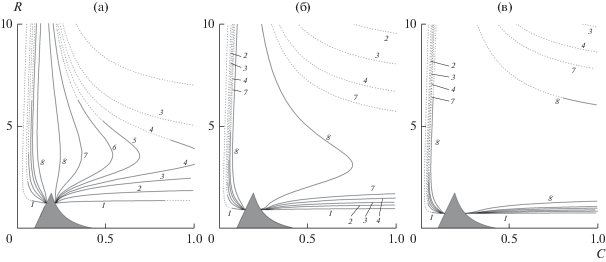
На рис. 3а видно, что при атмосферном давлении область высокого (15 об. % и более) содержания водорода охватывает весьма широкое поле составов (область содержания углерода, ограниченная слева и справа двумя ветвями линии 1), а при 100 атм эта область значительно сужается (область, ограниченная линиями 6). Это свидетельствует о том, что такой концентрации водорода можно достичь лишь в узком диапазоне содержания углерода. Похожая картина наблюдается и для изолиний, соответствующих другим значениям содержания водорода. На рис. 3б представлены изолинии 12% содержания водорода. В этом случае область тоже сужается, но не столь значительно и 12% содержание водорода можно получить при более широком варьировании содержания углерода в топливе. Еще шире параметрическая область, в которой достижимо 10% содержание водорода (рис. 3в).
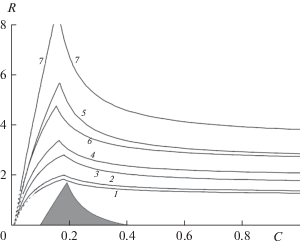
Содержание монооксида углерода в продуктах изменяется не столь значительно и не однозначно. На рис. 4 приведены расчетные изолинии 15, 25 и 35 об. % содержания CO для давлений 1, 10 и 100 атм. Как и на предыдущем рисунке, затемненный треугольник в нижней части соответствует режимам со слишком высокой температурой (выше 2300 K), а в областях низкой температуры (ниже 1000 К) расчетные изолинии показаны пунктиром. Линии, соответствующие определенному содержанию CO, группируются в пучок. В центральных областях поля составов (области, близкие к “линии инверсии”, где температура горения максимальна) увеличение давления приводит к увеличению концентрации CO в продуктах, а в краевых областях (далеко от линии инверсии) – наоборот.
Рис. 4.
Расчетные изолинии 15 (1, 2 и 3), 25 (4, 5 и 6) и 35 об. % (7, 8 и 9) содержания CO в продуктах для различных значений давления: 1, 4 и 7 – 1; 2, 5 и 8 – 10; 3, 6 и 9 – 100 атм.
Как отмечалось в работе [8], при низком давлении (1 атм) водород и монооксид углерода являются основными горючими компонентами продукт-газа, определяющими его теплотворную способность. Однако при увеличении давления содержание метана становится достаточно высоким, чтобы стал значимым его вклад в теплоту сгорания продукт-газа. На рис. 5 представлены изолинии 10 и 5 об. % содержания метана в продуктах для давления 100 атм. При 5% содержании метана его вклад в общую теплоту сгорания газа составляет уже не менее 25–30%. Для давлений 1 и 10 атм равновесное содержание метана в продуктах выше 5 об. % достигается лишь в области температур горения ниже 1000 К.
Если дальнейшее использование газообразных продуктов подразумевает сжигание с получением тепловой энергии, то увеличение содержания метана можно считать положительным фактором, а в случае использования продуктов для химического синтеза (синтез-газ) увеличение содержания метана является нежелательным.
Расчетные значения теплоты сгорания продукт-газа представлены на рис. 6. Сходный характер имеют изолинии химического КПД газификации, определяемого как отношение энтальпии окисления газообразных продуктов к энтальпии окисления исходного углерода (рис. 7). На рис. 6 и 7, кроме высокотемпературной области (затемненный треугольник в нижней части рисунков, соответствующий температуре выше 2300 К), затемнены области низких температур (ниже 1000 К). Как видно из сравнения диаграмм, с повышением давления эти низкотемпературные области сдвигаются в сторону большего количества пара в газообразном окислителе.
Рис. 6.
Расчетные изолинии теплоты сгорания продукт-газа для давления 1 (а), 10 (б) и 100 (в) атм: 1 – 100, 2 – 110, 3 – 120, 4 – 130, 5 – 150 кДж/моль.
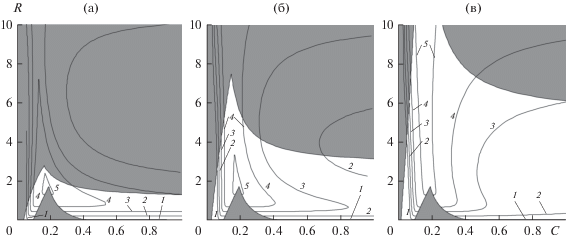
Рис. 7.
Расчетные изолинии КПД газификации для давления 1 (а), 10 (б) и 100 (в) атм: 1 – 80, 2 – 85, 3 – 90, 4 – 95, 5 – 99%.
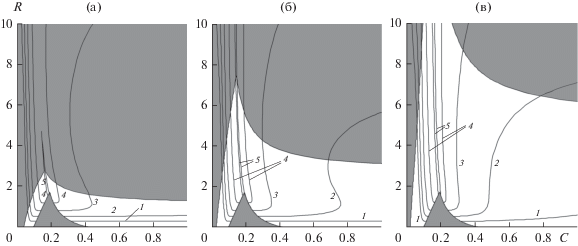
Максимальная теплота сгорания газа (и высокий КПД газификации) достигаются в области небольших содержаний углерода (15–30 мас. %) и при умеренной концентрации пара в подаваемой паровоздушной смеси. При повышении давления эта область немного сужается по доле углерода, но расширяется в сторону высокого содержания пара за счет увеличения количества метана в продуктах.
В том случае, когда газообразные продукты планируется использовать в качестве химического сырья для синтеза, например, углеводородов по методу Фишера–Тропша, важна такая характеристика, как отношение [H2]/[CO] в продуктах. Расчетные значения этой характеристики продукт-газа представлены на рис. 8. Видно, что чем выше давление, тем больше пара требуется для достижения того же значения этого отношения в продуктах. Практически важные значения отношения ([H2]/[CO] = 1 и [H2]/[CO] = 2) при атмосферном давлении оказываются недостижимыми во всей параметрической области режимов с температурой горения от 1000 до 2300 К. Достижимые значения отношения [H2]/[CO] растут с ростом давления. При давлении 10 атм значение этого отношения может достигать единицы, но для получения газа с характерным отношением [H2]/[CO] = 2 даже повышения давления до 100 атм будет недостаточно. При этом увеличение содержания метана в составе продукт-газа делает его малопригодным сырьем для синтеза углеводородов.
Рис. 8.
Расчетные изолинии отношения [H2]/[CO] при различном давлении: 1 – [H2]/[CO] = 0.5, P = 1; 2 – [H2]/[CO] = 0.5, P = 10 атм; 3 – [H2]/[CO] = 0.5, P = = 100 атм; 4 – [H2]/[CO] = 0.75, P = 10 атм; 5 – [H2]/[CO] = 0.75, P = 100 атм; 6 – [H2]/[CO] = 1.0, P = 10 атм; 7 – [H2]/[CO] = 1.0, P = 100 атм.
ЗАКЛЮЧЕНИЕ
Представленные результаты показывают, что повышение давления при газификации углеродных систем в режиме фильтрационного горения существенно сказывается на температуре и составе продуктов. Повышение давления приводит к возрастанию температуры горения и значительному снижению содержания водорода в продуктах газификации. При использовании продуктов газификации в энергетических целях снижение содержания водорода при повышении давления в некоторой степени компенсируется увеличением содержания метана. Показано, что в отличие от газификации, проводимой при низком (атмосферном) давлении, когда содержание пара в газообразном окислителе является хорошим управляющим параметром для контроля температуры, при повышенном давлении этот параметр управления теряет свою эффективность.
Следует помнить, что представленная расчетная модель подразумевает высокую скорость химических реакций и быстрое установление термодинамического равновесия в продуктах сгорания, что является довольно строгим ограничением области ее применимости. Тем не менее представленные результаты могут быть полезными для предварительной оценки режимов газификации углеродных систем и направления оптимизации режимов ФГ для конкретных практических задач.
Работа выполнена по теме Государственного задания № 01201361842 и при частичной поддержке Программы фундаментальных исследований Президиума РАН № 18 “Фундаментальные аспекты химии углеродной энергетики” и Программы фундаментальных исследований Президиума РАН № 31п “Фундаментальные исследования процессов горения и взрыва”.
ОБОЗНАЧЕНИЯ
| a, c, d, e, h, n, m, w, x | удельные мольные расходы инертного материала, углерода, диоксида углерода, метана, водорода, азота, монооксида углерода, водяного пара и кислорода соответственно, моль/(с м2) |
| C | массовая доля углерода в смеси углерода с твердым негорючим материалом |
| Hi =Hi(T) | энтальпия i-го компонента, кДж/моль |
| Ki=Ki(T) | константы диссоциации i-го компонента, Па, Па2, Па4 |
| P | абсолютное значение давления, Па |
| PC = PC(T) | равновесное давление паров над поверхностью углерода, Па; |
| pi | парциальное давление i-го газового компонента, Па |
| Q | суммарный тепловой эффект химических реакций, кДж/(с м2) |
| R | мольное отношение пар/кислород в газообразном окислителе |
| Т0 | температура окружающей среды, К |
| Tb | температура горения, К |
| X | объемная доля компонента в смеси газов |
| κ1(T), κ2(T), κ3(T) | безразмерные функции равновесия |
ИНДЕКСЫ
Список литературы
Канторович Б.В. Основы теории горения и газификации твердого топлива. М.: АН СССР, 1958.
Manelis G.B., Glazov S.V., Lempert D.B., Salgansky E.A. Filtration combustion of solid fuel in countercurrent reactors // Russ. Chem. Bull. 2011. V. 60. № 7. P. 1301. [Манелис Г.Б., Глазов С.В., Лемперт Д.Б., Салганский Е.А. Фильтрационное горение твердого топлива в противоточных реакторах // Изв. АН. Сер. хим. 2011. № 7. С. 21.]
Zaichenko A.Y., Zhirnov A.A., Manelis G.B., Polianchik E.V., Zholudev A.F. Filtration combustion of carbon in a non-one-dimensional solid flow // Theor. Found. Chem. Eng. V. 44. № 1. P. 30. [Зайченко А.Ю., Жирнов А.А., Манелис Г.Б., Полианчик Е.В., Жолудев А.Ф. Фильтрационное горение углерода при неодномерном течении твердой фазы // Теорет. основы хим. технологии. 2010. Т. 44. № 1. С. 31.]
Higman C., van der Burgt M. Gasification. Amsterdam: Elsevier, 2003.
Schult D.A., Matkowsky B.J., Volpert V.A., Fernandez-Pello A.C. Forced forward smolder combustion // Combust. Flame. 1996. V. 104. P. 1.
Salgansky E.A., Kislov V.M., Glazov S.V., Zholudev A.F., Manelis G.B. Filtration combustion of a carbon-inert material system in the regime with superadiabatic heating // Combust., Explos., Shock Waves. 2008. V. 44. № 3. P. 273. [Салганский Е.А., Кислов В.М., Глазов С.В., Жолудев А.Ф., Манелис Г.Б. Фильтрационное горение смеси углерод–инертный материал в режиме со сверхадиабатическим разогревом // Физика горения и взрыва. 2008. Т. 44. № 3. С. 30.]
Polianczyk E.V., Glazov S.V. Model for filtration combustion of carbon: Approximation of a thermodynamically equilibrium composition of combustion products // Combust., Explos., Shock Waves. 2014. V. 50. № 3. P. 251. [Полианчик Е.В., Глазов С.В. Модель горения углерода в фильтрационном режиме в приближении термодинамически равновесного состава продуктов // Физика горения и взрыва. 2014. Т. 50. № 3. С. 9.]
Glazov S.V., Polianczyk E.V. Filtration combustion of carbon in the presence of endothermic oxidizers // Combust., Explos., Shock Waves. 2015. V. 51. № 5. P. 540. [Глазов С.В., Полианчик Е.В. Фильтрационное горение углерода в присутствии эндотермических окислителей // Физика горения и взрыва. 2015. Т. 51. № 5. С. 34.]
Термодинамические свойства индивидуальных веществ. Справочное издание в четырех томах / Под ред. Глушко В.П., Гуревич Л.В. 3-е изд. М.: Наука, 1981.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии