Теоретические основы химической технологии, 2019, T. 53, № 4, стр. 452-457
Межфазное распределение тиофена, толуола и о-ксилола в экстракционной системе гексан–полимер–вода
Ю. А. Заходяева 1, 2, *, В. О. Соловьев 2, И. В. Зиновьева 2, Д. Г. Рудаков 1, А. В. Тимошенко 1, А. А. Вошкин 1, 2
1 МИРЭА – Российский технологический университет
Москва, Россия
2 Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
* E-mail: yz@igic.ras.ru
Поступила в редакцию 20.03.2019
После доработки 21.03.2019
Принята к публикации 27.03.2019
Аннотация
Выполнено экспериментальное и теоретическое исследование процессов экстракционного выделения серосодержащих и ароматических соединений из легких углеводородов с использованием водорастворимых полимеров. В ходе экспериментальных исследований изучена экстракция тиофена, толуола и о-ксилола из н-гексана в экстракционных системах на основе полиэтиленгликолей с различной молекулярной массой, полипропиленгликоля 425 и поливинилпирролидона 3500. Посредством математического моделирования получены зависимости коэффициентов распределения толуола и о-ксилола от содержания полимера при использовании экстракционной системы на основе полиэтиленгликоля 400. Полученные результаты могут быть в дальнейшем использованы при разработке новых экстракционных процессов очистки легких углеводородных фракций от серосодержащих и ароматических соединений.
ВВЕДЕНИЕ
В последние годы все более важной экологической проблемой становится загрязнение атмосферного воздуха, одним из основных источников которого являются соединения серы, образующиеся при сжигании серосодержащего топлива [1, 2]. В результате сжигания топлива образуются оксиды серы SOx, которые приводят к образованию кислотных дождей и разрушению озонового слоя. Кроме того, они приводят к снижению каталитической активности автомобильных катализаторов и являются ингибиторами катализаторов, обеспечивающих очистку выбросов от соединений углерода и азота в атмосферу [1].
Очистка жидкого топлива от серосодержащих и ароматических соединений является важной и достаточно трудной задачей в нефтеперерабатывающей промышленности и представляет собой актуальную научную проблему. Строгое ограничение на выбросы SOx в атмосферу связано с введением новых стандартов по содержанию серы в топливе, так в США с 2010 г. не более 15 ppm, в Европе с 2009 г. не более 10 ppm [1, 2].
В настоящее время для решения задач выделения серосодержащих соединений из топлив используют процессы гидроочистки [3], сорбции [4, 5], экстракции [2, 6–11], окисления [1, 12, 13]. Ведется интенсивная работа по развитию существующих и разработке новых методов десульфуризации жидких топлив.
Особую актуальность для решения задач извлечения, разделения и очистки органических веществ приобретают экстракционные методы [14–18], которые реализуются в более мягких условиях. В том числе жидкостная экстракция применяется для десульфуризации жидких топлив. Наиболее используемыми экстрагентами являются сульфолан, диметилформамид, диметилсульфоксид, ацетонитрил, 1-метил-2-пирролидон и др. [7]. Однако одним из основных недостатков этих реагентов является их токсичность, летучесть и пожароопасность. Поэтому разработка простого, эффективного и в то же время экологически безопасного метода обессеривания различных видов топлив становится актуальной задачей. Одним из решений данной проблемы является применение ионных жидкостей. Исследованиям в этом направлении посвящено большое количество публикаций [6–8]. Их анализ показывает, что ионные жидкости определенного состава проявляют высокую селективность по отношению к конкретным серосодержащим соединениям. Однако их практическое применение в настоящее время пока еще сдерживается высокой стоимостью и сложностью синтеза.
Еще одним из решений данной проблемы является применение водорастворимых полимеров (полиэтиленгликолей), которые имеют очень низкое давление паров, высокую температуру кипения, низкую вязкость и токсичность [2, 10, 11, 19]. Экстракционные системы на их основе используются для извлечения ряда металлов, в том числе редкоземельных [20], в процессах утилизации химических источников тока [21–23]. Кроме того, такие системы широко применяются при извлечении органических веществ [18], в биотехнологических процессах [24, 25] и в производстве фармацевтических препаратов [26, 27].
Известен ряд работ [2, 10, 11], в которых используют полиэтиленгликоли для извлечения тиофена и его производных из модельных топлив.
В настоящей работе исследованы процессы экстракционного выделения тиофена, а также толуола и о-ксилола из модельных растворов легких углеводородных фракций на примере н-гексана с использованием водорастворимых полимеров различной природы.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
При проведении экспериментальных исследований были использованы следующие реактивы: тиофен (Biochem Chemopharma, ≥99.0%), н-гексан (квалификация “х. ч.”), толуол (квалификация “х. ч.”), о-ксилол (квалификация “х. ч.”), полиэтиленгликоль 400 (Clariant), полиэтиленгликоль 1500 (Fluka), полипропиленгликоль 425 (Acros Organics), поливинилпирролидон 3500 (Acros Organics, ≥99%). Все реактивы были использованы без дополнительной очистки.
Исходный раствор, моделирующий легкие углеводородные фракции, готовили растворением тиофена (0.05 мас. %), толуола (1 мас. %) и о-ксилола (0.4 мас. %) в гексане. Раствор экстрагента готовили растворением точной навески полимера, взвешенной на аналитических весах (AND HR-100AZ), в дистиллированной воде.
Для исследования экстракционных равновесий использовали градуированные пробирки и делительные воронки с пришлифованными пробками. Экстракцию проводили смешиванием равных объемов органической фазы, содержащей тиофен (толуол или о-ксилол) в гексане, и раствора полимера, далее смесь перемешивали в течение 1 ч в термостатированном шейкере Enviro-Genie (Scientific Industries, Inc.) при температуре 25°С и скорости вращения 30 об/мин для установления равновесия. Далее смесь центрифугировали в течение 10 мин при 2500 об/мин (центрифуга CM-6MT, SIA ELMI), измеряли объемы фаз. Затем фазы разделяли и определяли содержание компонентов в системе. Количественное определение тиофена, толуола и о-ксилола в исходном растворе и в органической фазе после экстракции определяли методом спектрофотометрии (спектрофотометр Cary-60, Agilent) при длинах волн 228, 257 и 262 нм соответственно. В качестве раствора сравнения использовали гексан. Концентрацию тиофена, толуола и о-ксилола в полимерной фазе определяли по разности между его концентрацией в исходном растворе и в органической фазе после экстракции.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Экспериментально и теоретически изучено межфазное распределение тиофена, толуола и о-ксилола в экстракционных системах на основе полиэтиленгликолей с различной молекулярной массой, полипропиленгликоля 425 и поливинилпирролидона 3500.
На рис. 1 представлены результаты исследований зависимости коэффициента распределения тиофена от содержания полиэтиленгликоля 400, полиэтиленгликоля 1500, поливинилпирролидона 3500 и полипропиленгликоля 425. Полученные экспериментальные данные показывают, что с увеличением концентрации полимера в системах наблюдается общая тенденция к возрастанию коэффициентов распределения тиофена. В области концентраций полимера более 80% наблюдается экспоненциальный рост для систем с полиэтиленгликолем 400 и полипропиленгликолем 425.
Рис. 1.
Зависимость коэффициента распределения тиофена от содержания различных полимеров в системе: 1 – полиэтиленгликоль 400, 2 – полиэтиленгликоль 1500, 3 – поливинилпирролидон 3500, 4 – полипропиленгликоль 425.
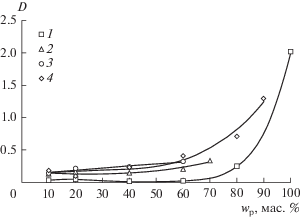
Следует отметить, что применение для экстракции 100%-ного полипропиленгликоля 425 невозможно, поскольку в этом случае гетерогенная система не образуется. В этом случае использование водного раствора полимера обеспечивает возможность экстракционного извлечения тиофена. Экстракционные системы на основе поливинилпирролидона 3500, несмотря на удовлетворительные значения коэффициентов распределения, нельзя рассматривать как подходящие для извлечения тиофена, поскольку увеличение содержания полимера более 60% приводит к образованию гетерогенной системы, обладающей физико-химическими свойствами, препятствующими проведению экстракционного извлечения. Очевидно, что перспективными для извлечения тиофена, наряду с системой с полиэтиленгликолем 400, можно рассматривать системы с полипропиленгликолем 425 и полиэтиленгликолем 1500.
Изучено извлечение толуола и о-ксилола из гексана с использованием полипропиленгликоля 425. На рис. 2 приведены экспериментальные зависимости коэффициента распределения толуола от концентрации полипропиленгликоля 425.
Рис. 2.
Зависимость коэффициента распределения толуола от содержания полипропиленгликоля 425 при извлечении из гексана.
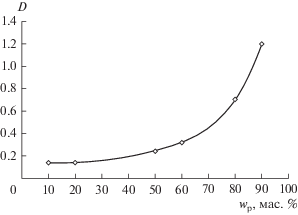
Полученная зависимость имеет экспоненциальный характер, при содержании полимера более 70% может быть обеспечено удовлетворительное извлечение толуола в полимерную фазу. Экстракционная система с концентрацией полипропиленгликоля 425 90% является перспективной для выделения толуола из гексана (коэффициент распределения более 1).
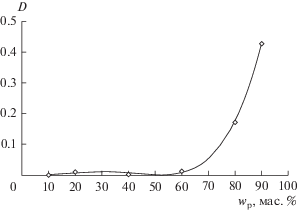
На рис. 3 представлена зависимость коэффициента распределения о-ксилола от содержания полипропиленгликоля 425. Результаты показывают, что экстракционная система с содержанием полимера менее 60% не экстрагирует о-ксилол из гексана в значимых количествах (коэффициент распределения ~0), что может быть востребовано в случае необходимости селективного извлечения ароматических соединений из углеводородных фракций. Повышение концентрации полимера до 90% обеспечивает удовлетворительное извлечение о-ксилола в полимерную фазу.
Рис. 3.
Зависимость коэффициента распределения о-ксилола от содержания полипропиленгликоля 425 при извлечении из гексана.
Таким образом, проведенные экспериментальные исследования показали возможность применения водных растворов рассматриваемых полимеров для извлечения серосодержащих и ароматических соединений из гексана.
Для поиска, разработки и оценки эффективности внедрения тех или иных технологических решений важным этапом является математическое моделирование химико-технологических процессов. Однако математическое моделирование фазового равновесия в многокомпонентных многофазных (с числом жидких фаз, равным двум и более) системах представляет собой достаточно сложную задачу [28]. Нами проведено математическое моделирование процесса экстракции исследуемых компонентов в программном комплексе Aspen Plus v.10. Для описания фазового равновесия была использована специализированная модель POLYUF, которая также является модификацией стандартной групповой модели UNIFAC и ориентирована на описание фазового равновесия в системах с полимерами. Молекулярные групповые параметры (R и Q) представлены в табл. 1. Бинарные групповые параметры уравнения POLYUF представлены в табл. 2.
Таблица 1.
Молекулярные групповые параметры (R и Q), где Ar – атом углерода в бензольном кольце
| Группа i/j | CH2 | CH2O | CH3 | ArCH | ArCCH3 | H2O |
|---|---|---|---|---|---|---|
| Q | 0.54 | 0.78 | 0.848 | 0.4 | 0.968 | 1.4 |
| R | 0.6744 | 0.9183 | 0.9011 | 0.5313 | 1.2663 | 0.92 |
Таблица 2.
Групповые параметры бинарного взаимодействия уравнения POLYUF, где Ar – атом углерода в бензольном кольце
| Группа i/j | CH2 | CH2O | CH3 | ArCH | ArCCH3 | H2O |
|---|---|---|---|---|---|---|
| CH2 | 0 | 251.5 | 0 | 61.13 | 76.5 | 1318 |
| CH2O | 83.36 | 0 | 83.36 | 52.13 | 65.69 | –314.7 |
| CH3 | 0 | 251.5 | 0 | 61.13 | 76.5 | 1318 |
| ArCH | –11.12 | 32.14 | –11.12 | 0 | 167 | 903.8 |
| ArCCH3 | –69.7 | 213.1 | –69.7 | –146.8 | 0 | 5695 |
| H2O | 300 | 540.5 | 300 | 362.3 | 377.6 | 0 |
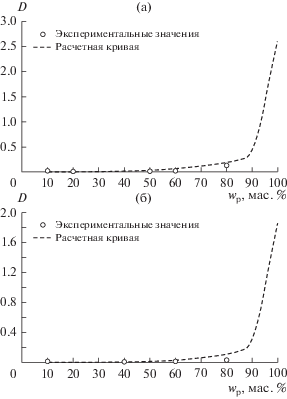
Математическое моделирование проводили на примере извлечения толуола и о-ксилола из гексана с использованием полиэтиленгликоля 400. Моделирование проводили для следующих условий процесса: температура 25°C, давление 100 кПа. Объемное соотношение фаз 1 : 1. Расчет проводили при варьировании концентрации полимера от 0 до 100 мас. %. Рассчитаны значения коэффициентов распределения толуола и о-ксилола в зависимости от концентрации полимера в экстракционной системе. Результаты представлены на рис. 4. Как видно, расчетные зависимости, полученные с использованием модели POLYUF, качественно описывают экспериментальные данные. Из рис. 4 видно, что при уменьшении концентрации полиэтиленгликоля 400 ниже 80% наблюдается резкое снижение извлечения толуола и о-ксилола из гексана, что связано с уменьшением растворимости компонентов в полимерной фазе. Наибольшее извлечение толуола и о-ксилола наблюдается из безводного полимера.
Рис. 4.
Экспериментальная и расчетная зависимости коэффициента распределения толуола (а) и о-ксилола (б) от содержания полиэтиленгликоля 400 при извлечении из гексана.
Результаты математического моделирования могут быть использованы в дальнейшем при поиске перспективных экстракционных систем для очистки легких углеводородных фракций от серосодержащих и ароматических соединений, а также для сокращения числа трудоемких экспериментальных исследований.
ЗАКЛЮЧЕНИЕ
В настоящей работе проведено экспериментальное и теоретическое исследование процессов экстракционного извлечения тиофена, толуола и о-ксилола из н-гексана в экстракционных системах на основе полиэтиленгликолей с различной молекулярной массой, полипропиленгликоля 425 и поливинилпирролидона 3500. Установлено, что наиболее перспективными для извлечения тиофена, толуола и о-ксилола из гексана являются экстракционные системы на основе полипропиленгликоля 425 с концентрацией полимера более 80%. Математическое моделирование процесса извлечения толуола и о-ксилола из гексана показало, что характер зависимости коэффициента распределения извлекаемого компонента от концентрации полимера с использованием модели POLYUF соответствует экспериментальным данным. Полученные результаты могут быть в дальнейшем использованы при разработке новых экстракционных процессов очистки легких углеводородных фракций от серосодержащих и ароматических соединений.
Исследование выполнено за счет гранта Российского научного фонда (проект № 17-73-10486).
ОБОЗНАЧЕНИЯ
ИНДЕКСЫ
Список литературы
Krolikowski M., Lipinska A. Separation of thiophene, or benzothiophene from model fuel using glycols. Liquid–liquid phase equilibria and oxidative desulfurization study // Fluid Phase Equilibria. 2019. V. 482. P. 11.
Kianpour E., Azizian S. Polyethylene glycol as a green solvent for effective extractive desulfurization of liquid fuel at ambient conditions // Fuel. 2014. V. 137. P. 36.
Jaf Z.N., Altarawneh M., Miran H.A., Jiang Z.T., Dlugogorski B.Z. Hydrodesulfurization of thiophene over γ-Mo2N catalyst // Molecular Catalysis. 2018. V. 459. P. 21.
Dehghan R., Anbia M. Zeolites for adsorptive desulfurization from fuels: A review // Fuel Processing Technology. 2017. V. 167. P. 99.
Zhang X.F., Wang Z., Feng Y., et al. Adsorptive desulfurization from the model fuels by functionalized UiO-66(Zr) // Fuel. 2018. V. 234. P. 256.
Ibrahim M.H., Hayyan M., Hashim M.A., Hayyan A. The role of ionic liquids in desulfurization of fuels: A review // Renewable and Sustainable Energy Reviews. 2017. V. 76. P. 1534.
Zhao K., Cheng Y., Liu H., et al. Extractive desulfurization of dibenzothiophene by a mixed extractant of N,N-dimethylacetamide, N,N-dimethylformamide and tetramethylene sulfone: Optimization by Box-Behnken design // RSC Advances. 2015. V. 5. № 81. P. 66013.
Song Z., Yu D., Zeng Q., et al. Effect of water on extractive desulfurization of fuel oils using ionic liquids: A COSMO-RS and experimental study // Chinese J. Chemical Engineering. 2017. V. 25. № 2. P. 159.
Nicolae M., Oprea F., Fendu E. Dipropylene glycol as a solvent for the extraction of aromatic hydrocarbons. Analysis and evaluation of the solvency properties and simulation of the extraction processes // Chemical Engineering Research and Design. 2015. V. 104. P. 287.
Gao J., Zhu S., Dai Y., Xiong C., Li C., Yang W., Jiang X. Performance and mechanism for extractive desulfurization of fuel oil using modified polyethylene glycol // Fuel. 2018. V. 233. P. 704.
Bhutto A.W., Abro R., Gao S., Abbas T., Chen X., Yu G. Oxidative desulfurization of fuel oils using ionic liquids: A review // J. Taiwan Institute of Chemical Engineers. 2016. V. 62. P. 84.
Lima F., Gouvenaux J., Branco L.C., Silvestre A.J.D., Marrucho I.M. Towards a sulfur clean fuel: Deep extraction of thiophene and dibenzothiophene using polyethylene glycol-based deep eutectic solvents // Fuel. 2018. V. 234. P. 414.
Chen Y., Song H., Meng H., et al. Polyethylene glycol oligomers as green and efficient extractant for extractive catalytic oxidative desulfurization of diesel // Fuel Processing Technology. 2017. V. 158. P. 20.
Zakhodyaeva Yu.A., Voshkin A.A., Belova V.V., Khol’kin A.I. Extraction of monocarboxylic acids with binary extracting agents based on amines and quaternary ammonium bases // Theor. Found. Chem. Eng. 2011. V. 45. № 5. P. 739.
Kholkin A.I., Belova V.V., Zakhodyaeva Y.A., Voshkin A.A. Solvent extraction of weak acids in binary extractant systems // Separation Science and Technology. 2013. V. 48. № 9. P. 1417.
Zakhodyaeva Yu.A., Voshkin A.A., Belova V.V., Khol’kin A.I. Extraction of monocarboxylic acids by trioctylmethylammonium di(2-ethylhexyl)phosphate // Theor. Found. Chem. Eng. 2012. V. 46. № 4. P. 413.
Khol’kin A.I., Zakhodyaeva Yu.A., Voshkin A.A., Belova V.V. Interphase distribution of weak acids in systems with binary extractants // Theor. Found. Chem. Eng. 2013. V. 47. № 4. P. 453.
Voshkin A.A., Zakhodyaeva Yu.A., Zinov’eva I.V., Shkinev V.M. Interphase distribution of aromatic acids in the polyethylene glycol–sodium sulfate–water system // Theor. Found. Chem. Eng. 2018. V. 52. № 5. P. 890.
Zakhodyaeva Y.A., Rudakov D.G., Solov’ev V.O., Voshkin A.A., Timoshenko A.V. Liquid-liquid equilibrium of aqueous two-phase system composed of poly(ethylene oxide) 1500 and sodium nitrate // J. Chemical and Engineering Data. 2019. V. 64. № 3. P. 1250.
de Oliveira W.C.M., Rodrigues G.D., Mageste A.B., de Lemos L.R. Green selective recovery of lanthanum from Ni-MH battery leachate using aqueous two-phase systems // Chemical Engineering Journal. 2017. V. 322. P. 346.
Zakhodyaeva Yu.A., Izyumova K.V., Solov’eva M.S., Voshkin A.A. Extraction separation of the components of leach liquors of batteries // Theor. Found. Chem. Eng. 2017. V. 51. № 5. P. 883.
Valadares A., Valadares C.F., de Lemos L.R., Mageste A.B., Rodrigues G.D. Separation of cobalt and nickel in leach solutions of spent nickel-metal hydride batteries using aqueous two-phase systems (ATPS) // Hydrometallurgy. 2018. V. 181. P. 180.
Leite D.S., Carvalho P.L.G., de Lemos L.R., Mageste A.B., Rodrigues G.D. Hydrometallurgical separation of copper and cobalt from lithium-ion batteries using aqueous two-phase systems // Hydrometallurgy. 2017. V. 169. P. 245.
Phong W.N., Show P.L., Chow Y.H., Ling T.C. Recovery of biotechnological products using aqueous two phase systems // J. Bioscience and Bioengineering. 2018. V. 126. № 3. P. 273.
Wu X., Li G., Yang H., Zhou H. Study on extraction and separation of butyric acid from clostridium tyrobutyricum fermentation broth in PEG/Na2SO4 aqueous two-phase system // Fluid Phase Equilibria. 2015. V. 403. P. 36.
Sampaio D.A., Mafra L.I., Yamamoto C.I., et al. Aqueous two-phase (polyethylene glycol + sodium sulphate) system for caffeine extraction: Equilibrium diagrams and partitioning study // J. Chem. Thermodyn. 2016. V. 98. P. 86.
Nadar S.S., Pawar R.G., Rathod V.K. Recent advances in enzyme extraction strategies: A comprehensive review // International J. Biological Macromolecules. 2017. V. 101. P. 931.
Frolkova A.V., Akishina A.A., Frolkova A.K. Multicomponent systems with three-phase splitting region // Fine Chemical Technologies. 2016. V. 11. № 6. P. 15.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии


