Теоретические основы химической технологии, 2020, T. 54, № 2, стр. 185-191
Способ получения биогенного кремнезема
Т. П. Щербакова a, *, И. Н. Васенева a
a Институт химии Коми научного центра УрО РАН
Сыктывкар, Россия
* E-mail: Sher.taty@mail.ru
Поступила в редакцию 30.10.2018
После доработки 15.10.2019
Принята к публикации 22.10.2019
Аннотация
Исследованы методы выделения и изолирования кремнезема, обеспечивающие энергоресурсосбережение, сокращение потерь и отходов растительного сырья, а также экологическую безопасность процессов. Методом окислительного озоления и щелочной экстракции получены образцы биогенного кремнезема (SiO2) c содержанием целевого компонента 76.4–99.9%. Физико-химическими методами определен качественный элементный состав и структурные характеристики полученных материалов.
ВВЕДЕНИЕ
Аморфный кремнезем и кремниевые комплексы являются многоцелевыми материалами и широко используются как модифицирующие наполнители в производстве резин, в полимерной, лакокрасочной и химической промышленности, а также в сельском хозяйстве и растениеводстве как регуляторы-стимуляторы роста растений. Лигноцеллюлозный компонент, являющийся доминирующим в растительной биомассе, используют во всех направлениях целлюлозной промышленности.
Анализ мирового рынка синтетического (осажденного и пирогенного) аморфного кремнезeма показывает наличие целого ряда технических наименований и торговых марок с характерными физико-химическими параметрами, например “Аэросил”, “белая сажа” [1]. Тем не менее получение пирогенного кремнезeма (содержание основного вещества SiO2 99.5% и выше) требует больших энергозатрат и защитных мер по взрывобезопасности. Осаждённый кремнезём (содержание SiO2 варьирует в диапазоне 60.0–90.0%) получают, как правило, из жидкого стекла (Na2SiO3), что в техническом плане немного проще и безопаснее [2]. Способ получения определяет свойства конечного продукта: размер и форму частиц, наличие или отсутствие пор, свойства поверхности [1].
Биогенный кремнезем – один из источников аморфной модификации, синтезируется растениями в своих вегетативных частях в связанном состоянии с растительными компонентами. Кремнийсодержащие растительные материалы, в основном травянистого происхождения, древесные растения концентрируют кремниевые соединения в определенных вегетативных частях (в основном в листьях, хвойной зелени).
Перспективность биогенного кремнезема и способы его выделения из растительной массы рассмотрены в работах [3–12]. Российскими специалистами разработаны способы получения высокочистого (до 99.99%) аморфного диоксида кремния из рисовой шелухи с выходом до 22.0 мас. % [1, 3, 5].
Основной задачей исследования является повышение полноты использования растительного сырья. Целью исследования являлось получение аморфного кремнезема с высоким содержанием основного вещества как целевого продукта.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объектами исследования являлись растительные полимеры: рисовая шелуха и хвощ лесной. Компонентный состав растительных образцов исследован согласно методикам, представленным в монографии [13]. Содержание лигнина определяли сернокислотным методом в модификации Комарова, содержание целлюлозы – методом Кюршнера (экстракцией растительного образца азотно-спиртовой смесью). Для определения валового содержания кремнезема применяли метод сплавления со щелочами [14].
Исследуемые объекты (с вариацией предварительной подготовки: измельчение, экстракция раствором кислоты, экстракция раствором гидроксида натрия) подвергали озолению в муфельной печи в токе воздуха. Образцы массой 0.2–0.3 г нагревали от 25 до 600–1000°С со скоростью 8°С/мин в динамической атмосфере воздуха со скоростью потока 5 л/мин.
Образцы подвергали экстракции водой и/или 0.1 н. раствором соляной кислоты при температуре 90°С в течение 60 мин с последующей фильтрацией и сушкой [6, 7].
Образцы подвергали экстракции 2.5 н. раствором гидроксида натрия при температуре 90°С в течение 60 мин с получением экстракта щелочерастворимых компонентов растительной матрицы (кремнезема, лигнина, пектиновых веществ, гемицеллюлоз) и твердым остатком (целлюлозы).
Микрофотографии образцов были получены с помощью сканирующего электронного микроскопа Tescan Vega III SBU (фирма Tescan, Чехия). Качественный элементный состав определяли с помощью рентгеновского энергодисперсионного микроанализатора AZTECENERGY/X-ACT TESCANVEGA 3 SBU.
Характеристики пористой структуры (удельную площадь поверхности Sуд, суммарный объем пор VΣ, диаметр пор dпор) определяли с помощью прибора NOVAStationA. Площадь удельной поверхности согласно методу БЭТ рассчитывали по изотерме тепловой сорбции азота.
Рентгеноструктурный анализ проводили с помощью рентгеновского дифрактометра SHIMADZU XRD-6000 (фирма SHIMADZU, Япония).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Источники биогенного кремнезема рисовая шелуха (РШ) и хвощ лесной (ХЛ) характеризуются определенным компонентным составом (табл. 1) и содержанием кремнезема (табл. 2). Основной состав биомассы представлен целлюлозой, полисахаридами и лигнином, с которыми кремний образует комплексы [15]. При этом содержание основных компонентов в растительных образцах широко варьируется.
Таблица 1.
Компонентный состав исследуемых образцов
| Биомасса | Сash, мас. % | СL, мас. % | СPS, мас. % | Сcell, мас. % |
|---|---|---|---|---|
| РШ | 21.0 ± 1.0 | 41.0 ± 1.0 | 8.0 ± 1.2 | 38.5 ± 0.5 |
| ХЛ | 8.2 ± 0.6 | 7.0 ± 0.4 | 54.0 ± 0.6 | 20.0 ± 0.5 |
Таблица 2.
Характеристика образцов на содержание кремнезема
| Биомасса | Сash, мас. % | SiO2 в золе, мас. % | SiO2 в образце, мас. % |
|---|---|---|---|
| РШ | 21.0 ± 1.0 | 83.0 | 16.9 ± 0.5 |
| ХЛ | 8.2 ± 0.6 | 86.0 | 7.3 ± 0.3 |
Технологические характеристики полученных кремнеземов представлены в табл. 3. Выделение кремнезема из растительной массы проводили методом озоления и методом осаждения. При окислительном озолении происходит выгорание органического вещества, до 80% растительных компонентов, имеющих технологическое значение (углеводный комплекс, ароматическая часть), переходит в категорию отходов. Зольный остаток преимущественно состоит из кремнезема.
Таблица 3.
Технологические характеристики полученных кремнеземов
| Образец | Функциональная схема | Технологическая характеристика | |||
|---|---|---|---|---|---|
| ρРС, г/см3 | ВОЗ, % | ${{C}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}$, % | ρз, г/см3 | ||
| РШ1 | Озоление | 0.1003 | 20.00 | 86.0 | 0.1319 |
| РШ2 | Озоление | 0.1200 | 19.68 | 99.8 | 0.2140 |
| ХЛ1 | Экстракция кислотой → озоление | 0.0900 | 8.80 | 83.0 | 0.1500 |
| ХЛ2 | Экстракция кислотой → озоление | 0.0990 | 8.60 | 99.5 | 0.1642 |
| РШ3 | Щелочная экстракция → осаждение | 0.1005 | 16.40 | 76.4 | 0.1640 |
| РШ4 | Экстракция кислотой → щелочная экстракция → осаждение | 0.1200 | 21.4 | 98.6 | 0.2515 |
Степень чистоты кремнеземов зависит от предварительной подготовки растительной биомассы. В результате озоления исходной растительной массы РШ1 получен кремнезем с содержанием основного вещества (SiO2) – 86.0%, а ХЛ1 – 83.0%.
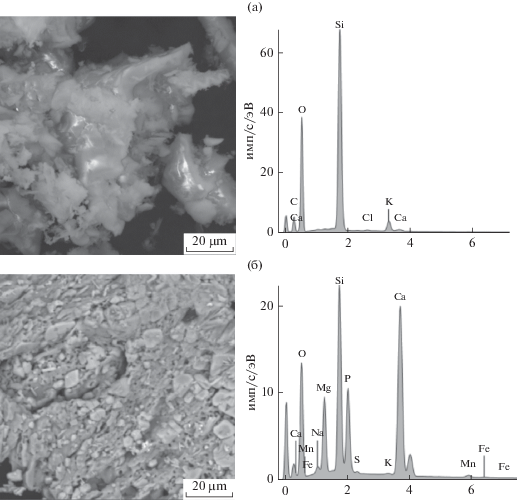
На рис. 1 представлены результаты сканирующей электронной микроскопии (СЭМ) и энергодисперсионного анализа (ЭДА) образцов кремнезема (РШ, ХЛ1).
Исследования морфологической структуры полученных кремнеземов показали, что частицы кремнезема образуют аморфные глобулы (РШ1) или чашуйки, собранные в агломераты (ХЛ1).
Степень чистоты полученных образцов анализировали посредством ЭДА (рис. 1). Показано наличие в озоле сопутствующих минеральных компонентов, которое также в зависимости от вида растительной массы широко варьируется.
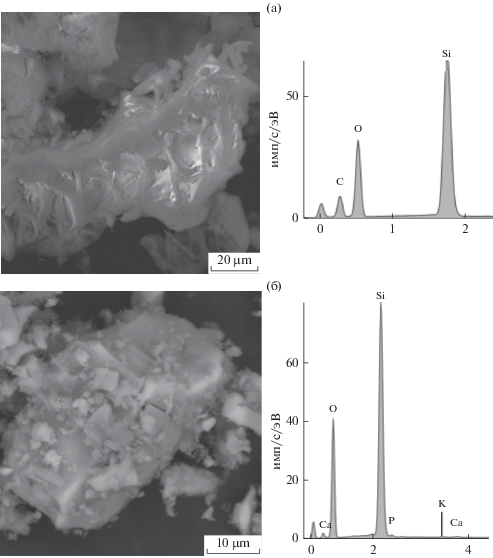
Экстракция биомассы растворами минеральных кислот позволяет удалить из лигноцеллюлозной матрицы все растворимые минеральные компоненты кроме кремния и получить в процессе озоления аморфный кремнезем с чистотой до 99.9% [3, 5] (рис. 2).
Учитывая физико-химические характеристики кремнезема, при выделении его из минерального или растительного сырья широко применяют методы щелочной экстракции. В литературе описаны способы выделения кремнезема из растительных материалов с минимизированием количества потерь биомассы и выделением определенных органо-кремниевых комплексов (лигно-кремниевых, кремниево-полисахаридных) как целевых продуктов и как прекурсоров для получения микро- и нанодисперсного кремнезема высокой степени чистоты [3, 5, 16].
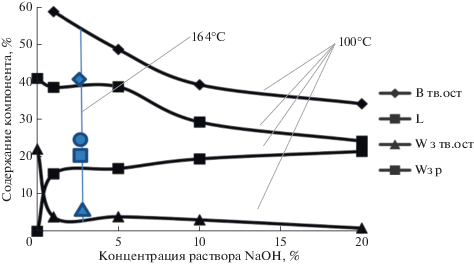
Исследована зависимость степени обескремнивания растительного материала от концентрации экстрагента (гидроксида натрия) в пределах от 1 до 20% и температурная зависимость процесса (табл. 4, рис. 3).
Таблица 4.
Физико-химические характеристики процесса обескремнивания биомассы
| СNaOH, % | tэкстр, °С | Втв. ост, % | СL, % | ωз тв. ост, % | ωз р, % | ρ, г/см3 | Содержание, % | Силикатный модуль n | |
|---|---|---|---|---|---|---|---|---|---|
| SiO2 | Na2O | ||||||||
| 1 | 100 | 58.86 | 38.60 | 3.85 | 15.4 | 1.0116 | 3.54 | 2.95 | 1.20 |
| 5 | 100 | 48.74 | 38.74 | 3.89 | 16.8 | 1.0430 | 10.04 | 19.16 | 0.52 |
| 10 | 100 | 39.28 | 29.28 | 3.06 | 19.4 | 1.0523 | 10.04 | 35.26 | 0.58 |
| 20 | 100 | 34.16 | 24.16 | 0.83 | 21.4 | 1.1120 | 11.32 | 85.10 | 0.28 |
| 2.5 | 164 | 39.15 | 16.00 | 0.12 | 22.0 | – | 24.23 | 14.45 | 1.7 |
Показано, что при температуре 100°С – ниже кипения раствора щелочи (1–20%) полного выделения кремнезема не происходит. При автоклавном выщелачивании – при температуре выше температуры кипения используемых растворов (164°С, 6 атм) установлено практически полное выщелачивание кремния из растительного материала, а также выщелачивание полисахаридов и лигнинных веществ. Так, массовая доля золы (при автоклавном выщелачивании рисовой шелухи) составляет 22.0% с содержанием целевого компонента (SiO2) – 74.0%, что в пересчете на сухой исходный материал составляет 16.28%.
Качественный состав растворов щелочных силикатов определяют по силикатному модулю, по содержанию SiO2 или М2О, или содержанию твердого вещества (SiO2 и М2О) (по озолу). В данных технологических параметрах получены низкомодульные силикаты натрия.
Выход остатка биомассы составляет 58.8 → → 48.7 → 39.3 → 34.2% соответственно для концентрации раствора NaOH 1 → 5 → 10 → 20%. Повышение температуры экстракции до 164°С позволяет добиться предельной степени обескремнивания и делигнификации при снижении концентрации экстрагента до 2.5%. Остаточное содержание лигнинных веществ в твердых остатках исследуемых образцов составляет 38.6 → → 38.74 → 29.28 → 24.16% соответственно (рис. 3, табл. 4). Следовательно, при заявленных технологических параметрах в раствор переходит 0.8 → → 0.7 → 10.3 → 15.2% лигнинных веществ. При интенсификации процесса (164°С, 6 атм) в течение 60 мин при концентрации экстрагента 2.5% в раствор переходит 25.0% лигнинных веществ.
Предварительное кислотное выщелачивание позволяет повысить степень чистоты кремнезема до 98.6%. На рис. 4 представлены результаты СЭМ и ЭДА кремнезема (РШ4).
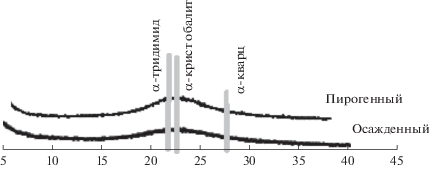
Рентгенограммы исследованных образцов характеризуются широким размытым максимумом в районе главного экстремума (пик α-кристобалита) 2θ = 20–26, что свидетельствует об аморфном состоянии образцов (рис. 5).
Полученные кремнеземы характеризуются удельной поверхностью 240–260 м2/г, общим объемом пор 44 см3/г, средним радиусом пор 8.29 Å.
Таким образом, методом окислительного озоления получены образцы биогенного кремнезема из рисовой шелухи с содержанием целевого компонента 86.1–99.8%, из хвоща лесного – 83.0–99.5%. При этом ~80% биомассы переходит в категорию потерь. Методом щелочной экстракции получены образцы биогенного кремнезема из рисовой шелухи с содержанием целевого компонента 74.0–98.6% и техническая целлюлоза с выходом 52.6%, которая характеризуется содержанием кремния – 1.4–2.3%.
ЗАКЛЮЧЕНИЕ
В настоящей работе предложен способ комплексной переработки кремнеземсодержащей растительной массы с получением аморфного кремнезема с высоким содержанием основного вещества и сохранением лигно-углеводного комплекса.
Работа выполнена с использованием оборудования ЦКП “Химия” Института химии Коми НЦ УрО РАН.
ОБОЗНАЧЕНИЯ
Список литературы
Обзор рынка диоксида кремния (белая сажа и аэросил) в СНГ. М.: Инфомайн, 2017.
Холомейдик А.Н. Получение, состав и свойства кремний- и углеродсодержащих продуктов переработки плодовых оболочек риса. Дис. … канд. хим. наук. Владивосток: Институт химии Дальневосточного отделения Российской академии наук, 2016.
Земнухова Л.А., Федорищева Г.А., Егоров А.Г., Сергиенко В.И. Исследование условий получения, состава примесей и свойств аморфного диоксида кремния из отходов производства риса // Журн. прикл. хим. 2005. Т. 78. Вып. 2. С. 324.
Воронков М.Г., Зельчан Г.И., Лукевиц Э.Я. Кремний и жизнь. Биохимия, фармакология и токсикология соединений кремния. Рига: Зинатне, 1978.
Земнухова Л.А., Виноградов В.В., Былков А.А., Виноградов Д.В. Способ получения высокочистых аморфных диоксида кремния и углерода из рисовой шелухи. Патент 2144498 РФ. 2000.
Земнухова Л.А., Юдаков А.А., Сергиенко В.И. Способ переработки кремнийсодержащего растительного сырья и установка для его осуществления. Патент 2245300 РФ. 2005.
Зюбин Л.В. Способ получения из рисовой шелухи аморфного диоксида кремния. Патент 2307070 РФ. 2007.
Земнухова Л.А., Хохряков А.А. Способ комплексной переработки рисовой шелухи и соломы. Патент 2533459 РФ. 2014.
Хизриева И.Х., Алиев З.М., Айдемирова З.О. Способ получения геля кремниевой кислоты. Патент 2525087 РФ. 2014.
Виноградов В.В., Виноградова Е.П. Способ переработки рисовой шелухи. Патент 2436730 РФ. 2011.
Земнухова Л.А., Федорищева Г.А. Способ получения диоксида кремния. Патент 2394764 РФ. 2010.
Габдуллин А.Н., Никоненко Е.А., Катышев С.Ф., Вайтнер В.В., Молодых А.С., Байкова Л.А., Косарева М.А. Способ получения высокодисперсного диоксида кремния. Патент 2593861 РФ. 2016.
Оболенская А.В., Ельницкая З.П., Леонович А.А. Лабораторные работы по химии древесины и целлюлозы. М.: Экология, 1991.
ГОСТ 13997.3-84 Изделия огнеупорные. Методы испытаний. Часть 2: материалы и изделия огнеупорные цирконийсодержащие. Методы определения двуокиси кремния. 2004.
Колесников М.П. Формы кремния в растениях // Усп. биол. хим. 2001. Т. 41. С. 301.
Виноградов В.В., Былков А.А. Способ подготовки рисовой шелухи для получения высокочистого диоксида кремния. Патент 2161124 РФ. 2000.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии