Теоретические основы химической технологии, 2020, T. 54, № 3, стр. 345-353
Синтез наноразмерного порошка бемита (AlООН) при низких температурах гидротермальной обработки
И. В. Козерожец a, *, Г. П. Панасюк a, Е. А. Семенов a, Н. П. Симоненко a, Л. А. Азарова a, В. Н. Белан a
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
* E-mail: irina135714@yandex.ru
Поступила в редакцию 06.12.2019
После доработки 21.01.2020
Принята к публикации 24.01.2020
Аннотация
Разработан способ синтеза наноразмерного порошка бемита при низких температурах гидротермальной обработки в 1.5 мас. % растворе НСl при 150 и 170°C и в воде при 80, 100 и 130°C. Определены оптимальные параметры гидротермальной обработки. Установлены этапы превращения γ-Аl2О3 в бемит (АlООН); подтверждено, что процесс является твердофазным (топохимическим). Исследованы физические и технологические свойства синтезированного нанопорошка бемита; установлено, что независимо от температуры гидротермальной обработки синтезированный бемит обладает схожими свойствами.
ВВЕДЕНИЕ
Гидротермальная обработка является широко распространенным промышленным способом синтеза порошков оксидов и гидроксидов металлов с заданными свойствами за счет варьирования параметров обработки [1–9]. В работах [10–19] представлены экспериментальные исследования влияния рН среды на форму и размеры частиц, в частности на форму и размеры частиц бемита [20, 21]. Так, при обработке в среде с рН > 7 формируются частицы бемита пластинчатой формы, при обработке в среде с рН < 7 – частицы бемита игольчатой формы, а при рН 7 – изометрические частицы бемита. Однако, согласно работам [22–24], независимо от рН среды, превращение прекурсор–бемит является твердофазным (топохимическим). Превращение микронных частиц оксидов и гидроксидов алюминия в бемит наиболее оптимально осуществляется при температуре гидротермальной обработке 200°C [25]. При гидротермальной обработке микронных частиц γ-Аl2О3 в 1.5 мас. % растворе НСl минимальной температурой, позволяющей получить технологический результат в 100% превращения бемита, является 180°C. Ниже этой температуры процесс идет очень медленно, что не позволяет получать бемит в промышленном масштабе [25]. Максимальная температура гидротермальной обработки в 220°C приводит к формированию крупных частиц бемита с плохо сформированной структурой, что не отвечает требованиям современной промышленности. Актуальность проблемы синтеза бемита со строго заданными физическими (размер, форма частиц, насыпная плотность, удельная площадь поверхности, теплопроводность, электропроводность, микротвердость и др.) и технологическими (абразивная способность, температура спекаемости и т.д.) свойствами определяется его широким применением. Бемит (АlООН) является прекурсором для получения различных чистых и легированных оксидов алюминия, сложных оксидов (в частности, алюмомагниевой шпинели [26]); является универсальным наполнителем в пластмассы, резину, полимеры, бумагу; может использоваться как огнезащитный материал, компонент масел; для производства керамики [27–30]; как сорбент широкого назначения [31–33]; в производстве лакокрасочных материалов и в ряде других важных областях. Особенно следует отметить использование бемита в процессах водоочистки [31, 32].
В связи с развитием современной промышленности формируются новые требования к исходному сырью, в частности к форме и размерам частиц бемита, а также к увеличению КПД производств за счет снижения энергозатрат производства бемита. Это возможно при использовании в качестве прекурсора для синтеза бемита наноразмерных частиц.
Данная работа направлена на исследование возможности превращения нанопорошка γ-Аl2О3 в бемит (АlООН) при низких температурах гидротермальной обработки в 1.5 мас. % растворе НСl при 150 и 170°C, в воде при 80, 100 и 130°C, а также на исследование физических и технологических свойств синтезированного при разных температурах обработки бемита.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе в качестве прекурсора использовался нанопорошок γ-Al2O3, синтезированный по технологии, описанной в статье [34]. Обработка нанопорошка γ-Al2O3 осуществлялась в автоклавах объемом 25 см3 в тефлоновом вкладыше в воде при температурах 80, 100 и 130°C и в 1.5 мас. % растворе НСl при температурах 150 и 170°C. Коэффициент заполнения автоклава 35%. Автоклавы охлаждались проточной водой, после разгерметизации образцы бемита извлекались из вкладышей, промывались дистиллированной водой и высушивались при 100°C. Обработка нанопорошка γ-Al2O3 в растворе кислоты обусловлена тем, что, согласно работам [29], возможные примеси, содержащиеся в γ-Al2O3, остаются в маточном растворе, таким образом, достигается дополнительная очистка конечного продукта – бемита. Использование тефлонового вкладыша позволяет избежать загрязнения синтезированного бемита примесями, возникающими за счет коррозии стенок контейнера. Синтезированный бемит исследовался методами: РФА на дифрактометре Bruker D8 Advance; СЭМ на приборе САМSCAN-S2; ПЭМ на приборе Jem-1011; ИК-спектроскопией на ИК-Фурье спектрометре Nexus “Nicolett”; ДСК на приборе SDT Q600; низкотемпературной адсорбцией азота с использованием анализатора АТХ-06. Насыпная плотность измерялась согласно ГОСТ 19440-94. Теплопроводность измерялась на приборе ИТП-МГ4 “Зонд” СКБ.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исходный порошок γ-Al2O3 с размером частиц 10–40 нм является монофазным образцом, удельная площадь поверхности которого 190 м2/г, коэффициент теплопроводности 0.02 Вт/(м К), насыпная плотность 0.015 г/см3 [34].
Выбор температур гидротермальной обработки наноразмерного порошка γ-Al2O3 в 1.5 мас. % растворе НСl и в воде определялся задачами промышленности по уменьшению энергозатрат при производстве бемита. Так, в настоящее время в промышленности реализован способ получения бемита при гидротермальной обработке микронных частиц прекурсора в автоклаве в различных средах, при этом 100% выход бемита возможен только при обработке в автоклаве от 180°C [24]. Таким образом, в работе экспериментально подобран ряд температур, позволяющий снизить энергозатраты при производстве порошка бемита.
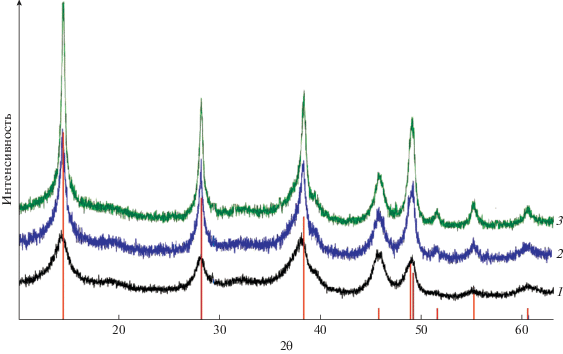
Гидротермальная обработка наноразмерного порошка γ-Al2O3 в 1.5 мас. % растворе НСl при изотермической выдержке при 170°C проводилась в течение 24 ч (рис. 1). При этом появление рефлекса бемита, относящегося к межплоскостному расстоянию d020 = 6.13 Å, было зафиксировано уже после 4 ч обработки (рис. 1–5), что свидетельствует о высокой реакционной способности наноразмерных частиц γ-Al2O3, так как для микронных частиц γ-Al2O3 без введения дополнительных активаторов превращение в таких условиях не характерно. Полностью превращение прекурсор–бемит осуществлялось за 12 ч обработки. Изотермическая выдержка при 170°C в течение 24 ч позволила получить наноразмерный порошок бемита (рис. 2) с хорошо сформированной структурой, что подтверждают узкие рефлексы на дифрактограммах.
Рис. 1.
Дифрактограммы наноразмерного порошка γ-Аl2O3 (1) и образцов, полученных при его гидротермальной обработке при 170°C в 1.5 мас. % растворе HCl в течение 1 ч (2) /γ-Аl2O3/; 2 ч (3) /γ-Аl2O3/; 3 ч (4) /γ-Аl2O3/; 4 ч (5) /γ-Аl2O3 и АlООН/; 6 ч (6) /γ-Аl2O3 и АlООН/; 8 ч (7) /γ-Аl2O3 и АlООН/; 9 ч (8) /γ-Аl2O3 и АlООН/; 10 ч (9) /γ-Аl2O3 и АlООН/; 12 ч (10) /АlООН/;14 ч (11) /АlООН/; 16 ч (12) /АlООН/; 18 ч (13) /АlООН/; 20 ч (14) /АlООН/; 24 ч (15) /АlООН/.
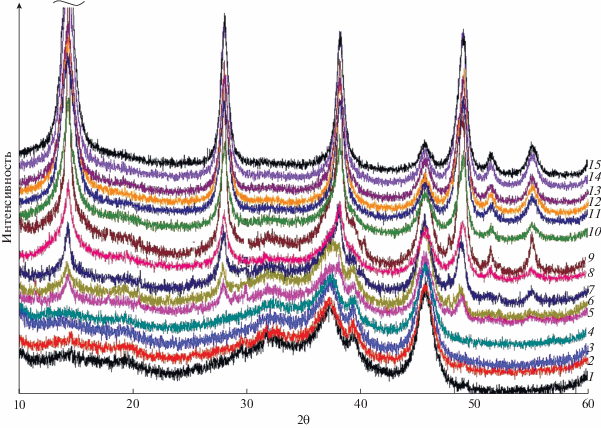
Рис. 2.
СЭМ (а, б), ПЭМ (в, г) – изображения бемита, полученного при гидротермальной обработке наноразмерного порошка γ-Аl2O3 в 1.5 мас. % растворе НСl при 170°C в течение 12 ч.

Рис. 3.
ИК-спектры поглощения исходного наноразмерного порошка γ-Аl2O3 (1) и подвергнутого гидротермальной обработке в 1.5 мас. % растворе НСl при 170°C в течение 1 ч (2) /γ-Аl2O3/; 4 ч (3) /γ-Аl2O3 и АlООН/; 5 ч (4) /γ-Аl2O3 и АlООН/; 6 ч (5) /γ-Аl2O3 и АlООН/; 8 ч (6) /γ-Аl2O3 и АlООН/; 12 ч (7) /АlООН/.
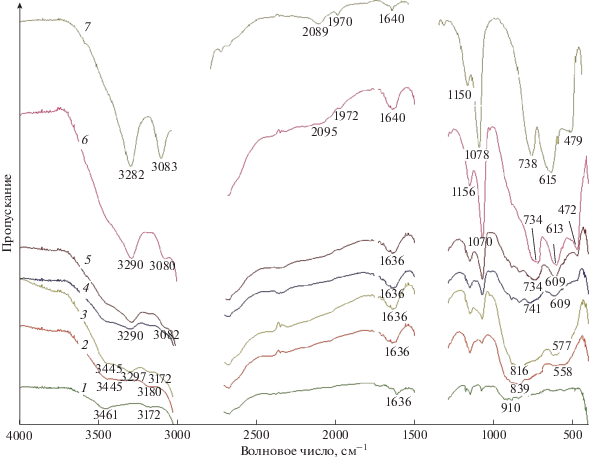
Рис. 4.
Дифрактограммы образцов, полученных при обработке γ-Аl2O3 при 150°C в 1.5% растворе HCl в течение 8 ч (1) /γ-Аl2O3 и АlООН/; 12 ч (2) /γ-Аl2O3 и АlООН/; 16 ч (3) /γ-Аl2O3 и АlООН/; 20 ч (4) /γ-Аl2O3 и АlООН/; 24 ч (5) /γ-Аl2O3 и АlООН/; 36 ч (6) /АlООН/; 60 ч (7) /АlООН/; 96 ч (8) /АlООН/.
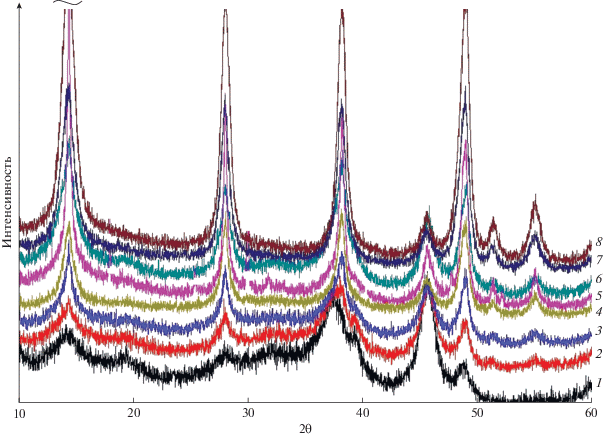
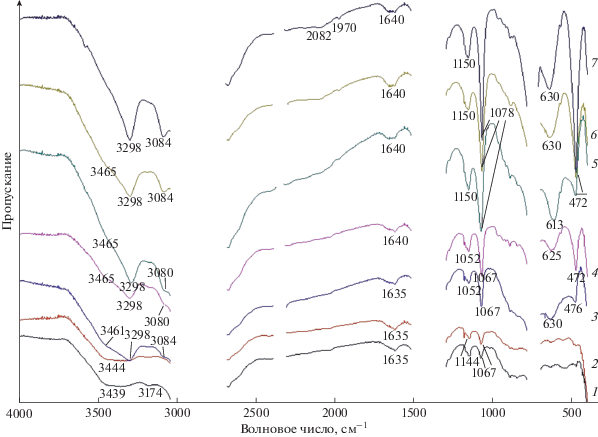
Рис. 5.
ИК-спектры поглощения образцов, полученных после обработки γ-Аl2O3 при 150°C в 1.5% растворе HCl в течение 8 ч (1) /γ-Аl2O3 и АlООН/; 12 ч (2) /γ-Аl2O3 и АlООН/; 16 ч (3) /γ-Аl2O3 и АlООН/; 20 ч (4) /γ-Аl2O3 и АlООН/; 24 ч (5) /γ-Аl2O3 и АlООН/; 36 ч (6) /АlООН/; 60 ч (7) /АlООН/.
Данные ИК-спектроскопии подтверждают результаты РФА и фиксируют при гидротермальной обработке наноразмерного порошка γ-Al2O3 в 1.5 мас. % растворе НСl при 170°C в течение 12 ч полосы, характерные для бемита (рис. 3–7): 3282 и 3083 см–1, относящиеся к валентным колебаниям OH-групп бемита; 1150 и 1078 см–1, соответствующие деформационным колебаниям связи as Al–OH и s Al–OH; 738 и 615 см–1, соответствующие симметричным (s Al–O) и асимметричным (as Al–O) деформационным колебаниям связи алюминий–кислород (Al–O), полоса при 479 см–1, соответствующая валентным (as Al–O) колебаниям связи Al–O [12–14, 25].
Рис. 6.
СЭМ (а), ПЭМ (б) – изображения бемита, полученного при гидротермальной обработке наноразмерного порошка γ-Аl2O3 в 1.5 мас. % растворе НСl при 150°C в течение 36 ч.

Рис. 7.
Дифрактограммы образцов, полученных при обработке наноразмерного порошка γ-Аl2O3 в воде при 80°C в течение 96 ч (1) /γ-Аl2O3 и АlООН/, при 100°C в течение 80 ч (2) /γ-Аl2O3 и АlООН/, при 130°C в течение 24 ч (3) /γ-Аl2O3 и АlООН/.
На рис. 2 представлены СЭМ и ПЭМ бемита, синтезированного при гидротермальной обработке порошка γ-Al2O3 в 1.5 мас. % растворе НСl при 170°C в течение 24 ч. Согласно микрофотографиям, бемит представляет собой крупные агломераты со средним размером порядка 3 мкм, состоящие из наноразмерных частиц со средним размером порядка 20 нм, что подтверждается расчетом по дифрактограмме по формуле Дебая–Шеррера (средний размер частиц 43 ± 5 нм).
Физические и технологические свойства бемита, синтезированного при гидротермальной обработке порошка γ-Al2O3 в 1.5 мас. % растворе НСl при 170°C в течение 12 ч, представлены в табл. 1.
Таблица 1.
Свойства наноразмерного порошка бемита, полученного при гидротермальной обработке нанопорошка γ-Al2O3 в 1.5 мас. % растворе НСl при 150 и 170°C
| Характеристика | Температура обработки, °C | |
|---|---|---|
| 170 | 150 | |
| Диапазон размера частиц, нм | 10–40 | 10–40 |
| Теплопроводность, Вт/(м К) | 0.02 | 0.02 |
| Удельная площадь поверхности, м2/г | 67.45 | 66.34 |
| Размер пор, нм | 1.89 | 1.89 |
| Удельный объем пор, см3/г | 0.033 | 0.030 |
| Время полного превращения, ч | 12 | 36 |
Гидротермальная обработка нанопорошка γ-Al2O3 в 1.5 мас. % растворе НСl при 150°C также позволила получить бемит при изотермической выдержке в течение 36 ч (рис. 4–6). При этом первый рефлекс бемита формируется за 8 ч обработки. Формирование структуры частиц бемита с узкими рефлексами на дифрактограмме достигается при обработке в течение 96 ч.
Данные ИК-спектроскопии подтверждают результаты РФА. Для бемита, полученного при обработке γ-Al2O3 в 1.5 мас. % растворе НСl при 150°C в течение 36 ч (рис. 5 и 6), фиксируются все те же полосы, что и для бемита, полученного при обработке γ-Al2O3 при 170°C в течение 24 ч (рис. 3–7).
Результаты исследования методами СЭМ и ПЭМ подтверждают наноразмерность частиц синтезированного бемита, полученного при обработке γ-Al2O3 в 1.5 мас. % растворе НСl при 150°C в течение 36 ч (рис. 6). При этом бемит также представляет собой агломераты с размером до 10 мкм, состоящие из наноразмерных частиц с размером порядка 20 нм, что подтверждается расчетом по формуле Дебая–Шеррера (средний размер частиц 15 ± 5 нм).
Физические и технологические свойства бемита, синтезированного при гидротермальной обработке порошка γ-Al2O3 в 1.5 мас. % растворе НСl при 150°C в течение 36 ч, представлены в табл. 1.
Гидротермальная обработка нанопорошка γ-Al2O3 в 1.5 мас. % растворе НСl при температурах ниже 150°C не позволила получить частицы бемита с 100% выходом за временной промежуток, удовлетворяющий современную промышленность.
В ходе экспериментов зафиксировано частичное превращение нанопорошка γ-Al2O3 в бемит при температурах гидротермальной обработки в воде 80 (τ = 96 ч), 100 (τ = 80 ч) и 130°C (τ = 24 ч), что указывает на высокую реакционную способность γ-Al2O3 (рис. 7). Однако полученные образцы, согласно дифрактограммам, представляют собой смесь фаз бемита и γ-Al2O3, что не позволяет реализовать данный экспериментальный результат в промышленности.
Согласно представленным в табл. 1 результатам синтезированный наноразмерный порошок бемита, независимо от температуры синтеза, обладает схожими свойствами. Размер частиц колеблется в диапазоне 10–40 нм; теплопроводность при комнатной температуре 0.02–0.025 Вт/(м К); удельная площадь поверхности изменяется в диапазоне от 65.32 до 67.45 м2/г и удельный объем пор в диапазоне от 0.030 до 0.033 см3/г; размер пор независимо от температуры синтеза бемита равен 1.9 нм.
Рассмотренные выше свойства позволяют рекомендовать синтезированный порошок бемита: в качестве сорбента для сточных вод промышленных предприятий; в качестве добавки к краскам, лакам, бетону для повышения теплоизоляционных свойств; в качестве более реакционно-способного материала по сравнению с частицами бемита микронного размера; в качестве добавки при создании огнезащитных материалов с рабочей температурой до 800°C; в качестве промежуточной фазы для синтеза наноразмерного порошка α-Al2O3, а значит, и для создания различных видов керамики, в том числе и как исходное сырье для синтеза лейкосапфира; в качестве прекурсора для синтеза алюмомагниевой шпинели и т.д.
ЗАКЛЮЧЕНИЕ
Исследовано превращение наноразмерного порошка γ-Al2O3 при гидротермальной обработке при низких температурах в воде при 80 (τ = 96 ч), 100 (τ = 80 ч) и 130°C (τ = 24 ч) и в 1.5 мас. % растворе НСl при 150 (τ = 36 ч) и 170°C (τ = 12 ч). Выявлен схожий механизм превращений в разных средах: твердофазный (топохимический). Показано, что переход γ-Al2O3–бемит при обработке при 170°C осуществляется за 12 ч обработки, а при 150°C – за 36 ч. Установлено, что независимо от температуры гидротермальной обработки синтезирован бемит со схожими свойствами. Предложены возможные области применения синтезированного нанопорошка бемита.
Работа выполнена в рамках государственного задания ИОНХ РАН в области фундаментальных научных исследований.
ОБОЗНАЧЕНИЯ
Список литературы
Oh M.-H., Nho J.-S., Cho S.-B. et al. Novel method to control the size of well-crystalline ceria particles by hydrothermal method // Mater. Chem. Phys. 2010. V. 124. № 1. P. 134. https://doi.org/10.1016/j.matchemphys.2010.06.004
Quan Y., Fang D., Zhang X. et al. Synthesis and characterization of gallium oxide nanowires via a hydrothermal method // Mater. Chem. Phys. 2010. V. 121. № 1–2. P. 142. https://doi.org/10.1016/j.matchemphys.2010.01.009
Shan H.-Y., Li J., Li S. et al. Epitaxial ZnO films grown on ZnO-buffered c-plane sapphire substrates by hydrothermal method // Appl. Surf. Sci. 2010. V. 256. № 22. P. 6743. https://doi.org/10.1016/j.apsusc.2010.04.083
Kim S.-J., Kim H.-H., Kwon J.-B. et al. Novel fabrication of various size ZnO nanorods using hydrothermal method // Microelectron. Eng. 2010. V. 87. № 5–8. P. 1534. https://doi.org/10.1016/j.mee.2009.11.033
Chen Z., He X. Low-temperature preparation of nanoplated bismuth titanate microspheres by a sol–gel-hydrothermal method // J. Alloys Compd. 2010. V. 497 № 1–2. P. 312. https://doi.org/10.1016/j.jallcom.2010.03.053
Ding M., Zhao D., Yao B. et al. The p-type ZnO film realized by a hydrothermal treatment method // Appl. Phys. Lett. 2011. V. 98. № 6. Article number 062102. https://doi.org/10.1063/1.3549304
Sreekantan S., Wei L.C. Study on the formation and photocatalytic activity of titanate nanotubes synthesized via hydrothermal method // J. Alloys Compd. 2010. V. 490. № 1–2. P. 436. https://doi.org/10.1016/j.jallcom.2009.10.030
Liu R., Yang W.D., Chueng H.J. Preparation and Visible-Light Photocatalytic Activity of TiO2 Nanotubes from a Hydrothermal Method // Adv. Mater. Res. 2011. V. 197–198. P. 786. https://doi.org/10.4028/www.scientific.net/amr.197-198.786
Kometani N., Teranishi T. Preparation of size-controlled silver nanoparticles by the hydrothermal method // Phys. Status Solidi C. 2010. V. 7. № 11–12. P. 2644. https://doi.org/10.1002/pssc.200983783
Manikandan V., Jayanthi P., Priyadharsan A. et al. Green synthesis of pH-responsive Al2O3 nanoparticles: Application to rapid removal of nitrate ions with enhanced antibacterial activity // J. Photochem. Photobiol., A. 2019. V. 371. P. 205. https://doi.org/10.1016/j.jphotochem.2018.11.009
Ribut S.H., Abdullah C.A.C., Mustafa M. et al. Influence of pH variations on zinc oxide nanoparticles and their antibacterial activity // Mater. Res. Express. 2019. V. 6. № 2. Article number 025016. https://doi.org/10.1088/2053-1591/aaecbc
Mohanraj V., Jayaprakash R., Chandrasekaran J. et al. Influence of pH on particle size, band-gap and activation energy of CdS nanoparticles synthesized at constant frequency ultrasonic wave irradiation // Mater. Sci. Semicond. Process. 2017. V. 66. P. 131. https://doi.org/10.1016/j.mssp.2017.04.006
Tang Z., Kwon H., Yi M.Y. et al. Role of Halide Ions for Controlling Morphology of Copper Nanocrystals in Aqueous Solution // ChemistrySelect. 2017. V. 2. № 17. P. 4655. https://doi.org/10.1002/slct.201701173
Wan Y.Y., Zhou X.P. Formation mechanism of hafnium oxide nanoparticles by a hydrothermal route // RSC Adv. 2017. V. 7. № 13. P. 7763. https://doi.org/10.1039/c6ra26663k
Mestanza S.N.M., Ribeiro A.O., De Souza Ribeiro C.S. et al. Study of the influence of dynamics variables on the growth of silica nanoparticles // Inorg. Nano-Met. Chem. 2017. V. 47. № 6. P. 824. https://doi.org/10.1080/15533174.2016.1212226
Podlogar M., Recnik A., Yilmazoglu G. et al. The role of hydrothermal pathways in the evolution of the morphology of ZnO crystals // Ceram. Int. 2016. V. 42. № 14. P. 15358. https://doi.org/10.1016/j.ceramint.2016.06.181
Egorova S.R., Bekmukhamedov G.E., Mukhamed’ya-rova A.N. et al. On the nature of phase conversions and transformations in porous system in hydrothermal processing of χ-Al2O3 into boehmite // Russ. J. Appl. Chem. 2016. V. 89. № 5. P. 703. https://doi.org/10.1134/S1070427216050049
Akiba H., Ichiji M., Nagao H. et al. Effect of Seeding and pH Conditions on the Size and Shape of Au Nanoparticles in Reduction Crystallization // Chem. Eng. Technol. 2015. V. 38. № 6. P. 1068. https://doi.org/10.1002/ceat.201400671
Hai C.X., Zhang L.J., Zhou Y. et al. Phase Transformation and Morphology Evolution Characteristics of Hydrothermally Prepared Boehmite Particles // J. Inorg. Organomet. Polym. Mater. 2018. V. 28. № 3. P. 643. https://doi.org/10.1007/s10904-017-0756-9
Padilla I., Lopez-Andres S., Lopez-Delgado A. Effects of Different Raw Materials in the Synthesis of Boehmite and γ- and α-Alumina // J. Chem. 2019. Article number 5353490. https://doi.org/10.1155/2016/5353490
Panasyuk G.P., Kozerozhets I.V., Semenov E.A. et al. Mechanism of Phase Transformations of γ-Al2O3 and Al(OH)3 into Boehmite (AlOOH) during Hydrothermal Treatment // Inorg. Mater. 2019. V. 55. № 9. P. 929 https://doi.org/10.1134/S0020168519090139
Panasyuk G.P., Belan V.N., Voroshilov I.L. et al. The study of hydrargillite and γ-alumina conversion process in boehmite in different hydrothermal media // Theor. Found. Chem. Eng. 2013. V. 47. № 4. P. 415. https://doi.org/10.1134/S0040579513040143
Panasyuk G.P., Belan V.N., Voroshilov I.L. et al. Hydrargillite → boehmite transformation // Inorg. Mater. 2010. V. 46. № 7. P. 747. https://doi.org/10.1134/S0020168510070113
Панасюк Г.П., Семенов Е.А., Козерожец И.В., Азарова Л.А., Ворошилов И.Л., Белан В.Н., Першиков С.А. Способ получения наполнителей для строительных материалов. Патент PФ 2625388. 2015.
Panasyuk G.P., Kozerozhets I.V., Danchevskaya M.N. et al. A New Method for Synthesis of Fine Crystalline Magnesium Aluminate Spinel // Dokl. Chem. 2019. V. 487. № 2. P. 218. https://doi.org/10.1134/S0012500819080019
Panasyuk G.P., Azarova L.A., Belan V.N. et al. Preparation of Fine-Grained Corundum Powders with Given Properties: Crystal Size and Habit Control // Theor. Found. Chem. Eng. 2018. V. 52. № 5. P. 879. https://doi.org/10.1134/S0040579518050202
Panasyuk G.P., Semenov E.A., Kozerozhets I.V. et al. Production of High-Flexural-Strength Corundum Ceramics // Dokl. Chem. 2019. V. 485. № 2. P. 116. https://doi.org/10.1134/S0012500819040049
Panasyuk G.P., Semenov E.A., Kozerozhets I.V. et al. A New Method of Synthesis of Nanosized Boehmite (AlOOH) Powders with a Low Impurity Content // Dokl. Chem. 2018. V. 483. P. 272. https://doi.org/10.1134/S0012500818110022
Chen Y.G., Huo W.L., Zhang X.Y. et al. Ultrahigh-strength alumina ceramic foams via gelation of foamed boehmite sol // J. Am. Ceram. Soc. 2019. V. 102. № 9. P. 5503. https://doi.org/10.1111/jace.16378
Kamari M., Shafiee S., Salimi F. et al. Comparison of modified boehmite nanoplatelets and nanowires for dye removal from aqueous solution // Desalin. Water Treat. 2019. V. 161. P. 304. https://doi.org/10.5004/dwt.2019.24295
Rajamani M., Rajendrakumar K. Chitosan-boehmite desiccant composite as a promising adsorbent towards heavy metal removal // J. Environ. Manage. 2019. V. 244. P. 257. https://doi.org/10.1016/j.jenvman.2019.05.056
Dubey S.P., Dwivedi A.D., Sillanpaa M. et al. Adsorption of As(V) by boehmite and alumina of different morphologies prepared under hydrothermal conditions // Chemosphere. 2017. V. 169. P. 99. https://doi.org/10.1016/j.chemosphere.2016.11.052
Panasyuk G.P., Kozerozhets I.V., Semenov E.A. et al. A New Method for Producing a Nanosized γ-Al2O3 Powder // Russ. J. Inorg. Chem. 2018. V. 63. № 10. P. 1303. [Панасюк Г.П., Козерожец И.В., Семенов Е.А. и др. // Журн. неорг. хим. 2018. Т. 63. № 10. С. 1286.]https://doi.org/10.1134/S0036023618100157
Panasyuk G.P., Kozerozhets I.V., Voroshilov I.L. et al. The thermodynamic properties and role of water contained in dispersed oxides in precursor-boehmite conversion, based on the example of aluminum hydroxide and oxide under hydrothermal conditions in different environments // Russ. J. Phys. Chem. A. 2015. V. 89. № 4. P. 592. https://doi.org/10.1134/S0036024415040196
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии


