Теоретические основы химической технологии, 2021, T. 55, № 2, стр. 216-223
Экстракция Pt(IV) и Pd(II) из солянокислых растворов полипропиленгликолем 425
Ю. А. Заходяева a, *, И. В. Зиновьева a
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
* E-mail: yz@igic.ras.ru
Поступила в редакцию 23.11.2020
После доработки 27.11.2020
Принята к публикации 04.12.2020
Аннотация
Впервые предложена экологически безопасная экстракционная система на основе полипропиленгликоля 425 и хлорида натрия для экстракции Pt(IV) и Pd(II) из разбавленных солянокислых растворов. Проведено исследование влияния исходной концентрации металла, кислотности среды, температуры, концентрации HCl и содержания хлорида натрия в системе на межфазное распределение ионов платиновых металлов. Установлен механизм экстракции исследуемых ионов металлов. Показано, что предложенная экстракционная система потенциально может быть использована для разделения платины и палладия.
ВВЕДЕНИЕ
Стремительный технический прогресс, интенсивный маркетинг и реклама и, как следствие, увеличение потребительского спроса привели к образованию большого количества отходов электронного и электротехнического оборудования. К 2021 г. прогнозируется накопление более 50 млн тонн электронного оборудования и товаров, не пригодных для целевого использования, которое требует незамедлительных решений в вопросе их переработки [1]. В отходах электроники содержится разнообразный состав органических и неорганических соединений, содержание которых зависит от типа производителя и цели использования. К примеру, являясь незаменимым компонентом электронных устройств, печатные платы отличаются довольно широким элементным составом, причем содержание некоторых драгоценных и цветных металлов (например, Au, Pt, Pd, Cu и др.) в них может быть выше, чем в минеральных ресурсах [2].
Электронная промышленность использует значительное количество драгоценных, в том числе платиновых, металлов ввиду их высокой химической стабильности, электропроводности и коррозионной стойкости для изготовления контактных материалов, гальванических покрытий. При соответствующей переработке электронные отходы могут оказаться значимым вторичным сырьем таких элементов. Металлы платиновой группы выщелачивают из компонентов электронных устройств с использованием пероксида водорода, азотной, серной, соляной кислот и их смесей. Дальнейшее селективное извлечение ценных компонентов из водных кислых растворов реализуется жидкостной экстракцией, мембранным разделением, хроматографией, осаждением и другими методами [3–5].
Современные методы жидкостной экстракции позволяют успешно решать вопросы гидрометаллургической переработки драгоценных металлов. Анализ литературных данных показал, что наибольший интерес представляет извлечение платины(IV) и ее отделение от родственных металлов [6]. Так как элементы платиновой группы способны образовывать комплексные соединения с разнообразными лигандами (аква-, гидроксо-, аквагидроксокомплексы и др. [4]) для их извлечения из водных растворов предложен широкий круг экстрагентов: Aliquat 336, Alamine 336, Lix 84I, Cyanex 923, PC 88A, трибутилфосфат, три-н-октиламин, фосфиноксиды, сульфоксиды, бинарные экстрагенты и др. [7–12]. Cyanex 301 позволяет проводить эффективное извлечение Pd(II) из хлоридных растворов в диапазоне концентраций HCl 0.5–9 моль/л вследствие прочного взаимодействия металла с экстрагентом, в то время как экстракция Pt(IV) протекает со степенью извлечения менее 10%, что позволяет достигать высокой степени разделения Pd(II) и Pt(IV). Однако недостатком использования фосфорсодержащих органических кислот в качестве экстрагентов является сложность процесса реэкстракции металлов из органической фазы.
В настоящее время активно развивается направление жидкостной экстракции без использования органических растворителей [13–16]. Экстракционные системы на основе водорастворимых полимеров позволяют обеспечивать экологическую безопасность в процессах выделения и разделения веществ [17–19]. Двухфазные водные системы хорошо изучены для задач выделения из водных растворов органических и неорганических соединений [20–22]. В ряде работ предложены технологические схемы выделения и разделения ионов металлов из растворов выщелачивания различных типов химических источников тока [23, 24].
Во многих работах предложен наиболее вероятный механизм экстракции исследуемых металлов (Fe(III), Tl(III), Au(III), Cr(IV) и др.) в полимерную фазу в двухфазных водных системах [25–28]. Металлы хорошо экстрагируется в полимерную фазу в виде анионных комплексов (напр., хлоридных, роданидных). Au(III), находясь в форме стабильного хлоридного комплекса [AuCl4]–, количественно экстрагируется в полимерную фазу в системе полиэтиленгликоль 1500 – сульфат аммония – вода в присутствии хлорид-ионов [28]. Известно, что в технологических растворах при высоких концентрациях Cl– (>0.1 моль/л) преобладают анионные неакватированные хлорокомплексы Pt(IV) и Pd(II). Поэтому двухфазные водные системы представляют собой потенциально перспективные экстракционные системы для извлечения платиновых металлов из водных сред.
Ранее межфазное распределение ионов платиновых металлов в двухфазных водных системах на основе полипропиленгликоля не изучалось. Таким образом, настоящая работа посвящена экспериментальному исследованию экстракции Pt(IV) и Pd(II) из разбавленных солянокислых растворов с использованием системы полипропиленгликоль 425–хлорид натрия–вода.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для приготовления двухфазной водной системы использовали полипропиленгликоль со средней молекулярной массой 425 г/моль (Acros Organics) и хлорид натрия квалификации “х. ч.”. В большинстве экспериментов использовали систему состава полипропиленгликоль 425 (30 мас. %)–хлорид натрия (8 мас. %)–вода за исключением экспериментов, в которых было исследовано влияние содержания хлорида натрия на эффективность экстракции платины(IV) и палладия(II).
Для изучения экстракции исследуемых металлов в качестве исходных водных растворов использовали соли комплексных кислот металлов состава H2[PtCl6] и H2[PdCl4] с концентрациями 0.005 и 0.0094 моль/л соответственно.
Экспериментальное исследование экстракционных равновесий проводили при температуре 25°С и атмосферном давлении в градуированных центрифужных пробирках с использованием термостатированного шейкера Enviro-Genie (Scientific Industries, Inc.) при скорости вращения 45 об./мин. Время контакта фаз, необходимое для установления экстракционного равновесия, определено предварительно и составило 30 мин. Образцы центрифугировали при 2500 об./мин в течение 10 мин до полного расслоения фаз. Определяли объемы полимерной и солевой фаз, значение рН солевой фазы и концентрацию ионов металла.
Количественное определение ионов металлов в исходном растворе и равновесных фазах после экстракции осуществляли спектрофотометрическим методом по известным методикам [29], основанным на комплексообразовании в видимой области спектра при длинах волн 403 и 407 нм для платины(IV) и палладия(II) соответственно относительно воды в стеклянных кюветах с длиной оптического пути 10 мм; измерение оптической плотности проводили на приборе ПЭ-5400УФ (ООО “Экросхим”).
Спектры поглощения в области длин волн от 190 до 1000 нм записывали на приборе Cary-60 (Agilent Tech.) в кварцевой кювете толщиной 1 мм относительно воды.
Кислотность среды создавали с использованием серной кислоты и гидроксида натрия и контролировали рН-метром Starter 5000 (OHAUS) с комбинированным электродом, калиброванным по буферам, имеющим значения рН 1.68, 4.01, 7.00, 10.01 (при 25°С).
Все представленные эксперименты проводились не менее трех раз и обработаны методом математической статистики.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
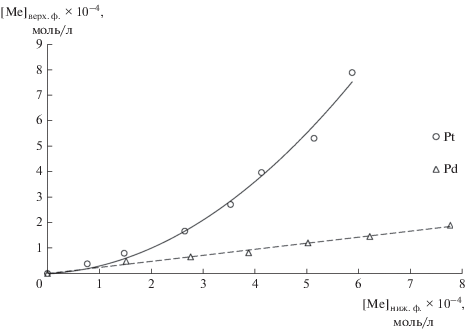
В качестве альтернативной экологически безопасной экстракционной системы для извлечения Pt(IV) и Pd(II) из разбавленных водных растворов нами была предложена экстракционная система на основе полипропиленгликоля 425 и хлорида натрия. В солянокислых растворах в зависимости от концентрации хлорид-ионов, протона и металла могут образовываться комплексы различного состава [30]. Для оценки влияния исходной концентрации платиновых металлов на коэффициент распределения была построена изотерма экстракции для платины(IV) и палладия(II) в диапазоне концентраций от 1 × 10–4 до 1 × 10–3 моль/л (рис. 1). На рис. 1 в случае экстракции Pt(IV) наблюдается зависимость экспоненциального характера, где коэффициент распределения платины с увеличением исходной концентрации увеличивается с 0.49 до 1.34. Такая форма кривой указывает на возможность эффективного разделения Pt(IV) и Pd(II) в области высоких концентраций в предложенной системе. Межфазное распределение палладия в исследуемой двухфазной водной системе сопровождается постоянством коэффициента распределения во всем диапазоне концентраций металла (D ≈ 0.24), что видно исходя из линейной зависимости изотермы экстракции.
Рис. 1.
Изотермы экстракции Pt(IV) и Pd(II) в системе ППГ 425 (30 мас. %)–NaCl (8 мас. %)–H2O: [Me]исх = 1 × 10–4 моль/л.
Электронные спектры поглощения равновесных фаз после экстракции металлов могут дать понимание о механизме экстракции Pt(IV) и Pd(II) в предложенной экстракционной системе. Исходя из полученных спектров поглощения (рис. 2а), платина(IV) и палладий(II) в солевой и полимерной фазе находятся в виде анионных хлорокомплексов [PtCl6]2– и [PdCl4]2–, что подтверждается наличием максимумов поглощения при 262 нм для платины; 223 и 281 нм для палладия [31].
Рис. 2.
Электронные спектры поглощения полимерной и солевой фаз после экстракции Pt(IV) и Pd(II) системе ППГ 425 (30 мас. %)–NaCl (8 мас. %)–H2O: (а) – [Me]исх = 1 × 10–4; (б) – [Me]исх = 1 × 10–3 моль/л.
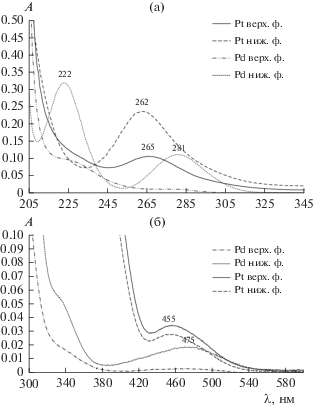
На рис. 2б представленные спектры поглощения платины и палладия в видимой области, на которых широкие полосы, соответствующие d–d-переходам, подтверждают нахождение платиновых металлов также в форме анионных хлорокомплексов.
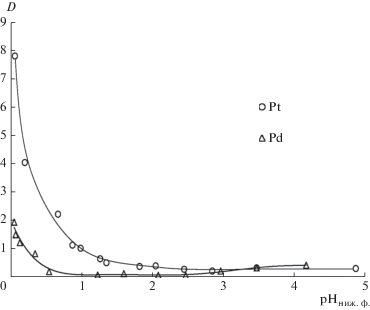
Кислотность среды имеет определяющее влияние на экстракцию ионов платиновых металлов. Изучено влияние значений рН солевой фазы на экстракцию Pt(IV) и Pd(II) в исследуемой системе в диапазоне от 0 до 5. Как видно, с уменьшением значений рН в системе достигается повышение эффективности экстракции исследуемых ионов металлов. Введение дополнительного протона приводит к повышению протонирования полимера, что способствует экстракции анионных комплексов Pt(IV) и Pd(II).
Рис. 3.
Зависимость коэффициента распределения Pt(IV) и Pd(II) от равновесных значений рН солевой фазы в системе ППГ 425 (30 мас. %)–NaCl (8 мас. %)–H2O в присутствии H2SO4: [Me]исх = 1 × 10–4 моль/л.
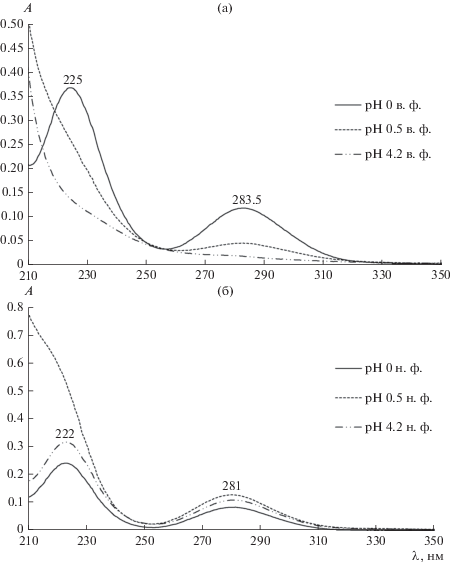
Экстракция ионов благородных металлов, присутствующих в водных растворах в виде анионных, нейтральных или катионных комплексов, может характеризоваться образованием координационно-сольватированных соединений разной степени прочности. К примеру, возможна сольватация протонов минеральных кислот сульфоксидами и последующее электростатическое взаимодействие сульфоксикатиона с анионными комплексами металла [32]. Диаграммы Пурбе для систем Pd–Cl–H2O и Pt–Cl–H2O показывают, что при стандартных окислительно-восстановительных потенциалах термодинамически устойчивыми комплексами исследуемых ионов металлов являются анионные формы [PdCl4]2– и [PtCl6]2– в широком диапазоне рН [4]. Для установления механизма экстракции исследуемых металлов в системе ППГ 425–NaCl–H2O фотометрическим методом были определены составы экстрагируемых форм платины и палладия. На рис. 4 и 5 представлены электронные спектры поглощения Pt(IV) и Pd(II) в равновесных полимерной и солевой фазах при различных значениях рН в диапазоне от 0 до 5. Из полученных спектральных данных видно, что при рН < 5 в обеих фазах платиновые металлы преимущественно существуют в форме анионных хлорокомплексов гексахлороплатинат- и тетрахлоропалладат-ионов. К тому же при уменьшении значений рН равновесной солевой фазы наблюдается значительное увеличение доли данных комплексов в полимерной фазе.
Рис. 4.
Электронные спектры поглощения полимерной (а) и солевой (б) фаз после экстракции Pt(IV) в системе ППГ 425 (30 мас. %)–NaCl (8 мас. %)–H2O с разными значениями рН.
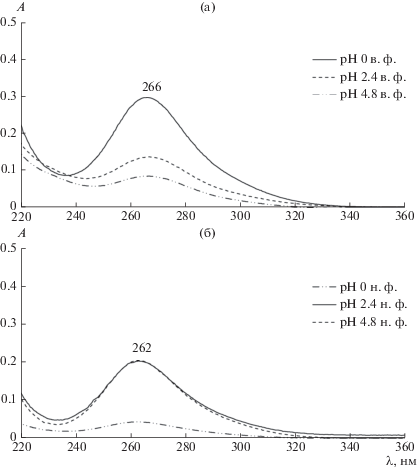
Рис. 5.
Электронные спектры поглощения полимерной (а) и солевой (б) фаз после экстракции Pd(II) в системе ППГ 425 (30 мас. %)–NaCl (8 мас. %)–H2O с разными значениями рН.
На основании полученных данных предложен механизм экстракции платиновых металлов в исследуемой двухфазной водной системе. Распределение хлорокомплексных кислот платиновых металлов в системе ППГ 425–NaCl–H2O может быть представлено следующими уравнениями:
(1)
$H_{{\left( {{\text{ниж}}{\text{.ф}}{\text{.}}} \right)}}^{ + } + {\text{ПП}}{{{\text{Г}}}_{{\left( {{\text{верх}}{\text{.ф}}{\text{.}}} \right)}}} \leftrightarrow \left[ {{\text{ППГ}}Н} \right]_{{\left( {{\text{верх}}{\text{.ф}}{\text{.}}} \right)}}^{ + },$(2)
$\begin{gathered} \left[ {{\text{MeC}}{{{\text{l}}}_{х}}} \right]_{{\left( {{\text{ниж}}{\text{.ф}}{\text{.}}} \right)}}^{{{\text{2}} - }} + {\text{ 2}}\left[ {{\text{ППГ}}Н} \right]_{{{\text{(верх}}{\text{.ф}}{\text{.)}}}}^{ + } \leftrightarrow \\ \leftrightarrow {{\left[ {{\text{MeCl}}_{х}^{{{\text{2}} - }} \cdot {\text{2ППГ}}{{H}^{ + }}} \right]}_{{\left( {{\text{верх}}{\text{.ф}}{\text{.}}} \right)}}}. \\ \end{gathered} $Схожий механизм экстракции ионов Cr(IV) и Fe(III) в двухфазных водных системах был установлен в ранее опубликованных работах [25, 26].
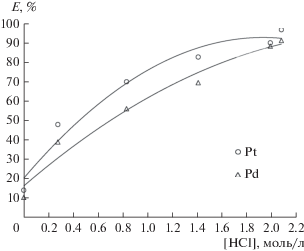
В гидрометаллургических процессах металлы платиновой группы содержатся в солянокислых растворах выщелачивания, где содержание HCl может варьироваться в зависимости от условий процесса. К тому же концентрация ионов Cl– является определяющим фактором в образовании преобладающих форм хлорокомплексов платины в растворе [33]. На рис. 6 представлена зависимость степени извлечения платины(IV) и палладия(II) от исходной концентрации HCl в диапазоне от 0 до 2 моль/л в системе ППГ 425–NaCl–H2O, дальнейшее увеличение концентрации кислоты в двухфазной водной системе приводит к ее гомогенизации. Из рис. 6 видно, что увеличение содержания HCl приводит к возрастанию степени извлечения ионов платины и палладия. Максимальный коэффициент распределения достигается при концентрации HCl ~2 моль/л. Похожий эффект наблюдался в работе [34] по извлечению исследуемых металлов, где в качестве экстрагента выступал Cyanex 921.
Рис. 6.
Зависимость степени извлечения Pt(IV) и Pd(II) от содержания соляной кислоты в системе ППГ 425 (30 мас. %)–NaCl (8 мас. %)–H2O: [Me]исх = = 1 × 10–4 моль/л.
Изучено влияние исходной концентрации хлорида натрия в системе ППГ 425 (30 мас. %)–NaCl–H2O на межфазное распределение исследуемых металлов. На рис. 7 представлены зависимости количественных характеристик экстракции платины и палладия от содержания NaCl в системе в диапазоне от 6 до 17 мас. %. Из полученных данных видно, что с увеличением содержания NaCl в двухфазной водной системе происходит снижение эффективности экстракции Pd(II) практически до 0, а в случае Pt(IV) наблюдается обратное поведение. Наиболее устойчивой формой Pd в хлоридных растворах является [PdCl4]2–, однако при низких концентрациях Cl– могут образовываться также комплексы состава [Pd(H2O)nCl4 – n]2 – n.
Рис. 7.
Зависимость коэффициента распределения Pt(IV) и Pd(II) от содержания хлорида натрия в системе ППГ 425 (30 мас. %)–NaCl–H2O: [Me]исх = 1 × 10–4 моль/л.
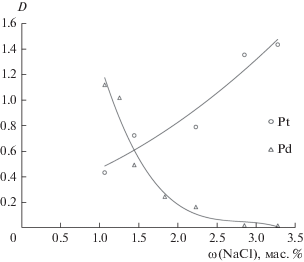
Коэффициент разделения Pt(IV) и Pd(II) в системе состава ППГ 425 (30 мас. %)–NaCl (17 мас. %)–H2O равен 71.5. Такая экстракционная система потенциально может использоваться для задач разделения платины(IV) и палладия(II).
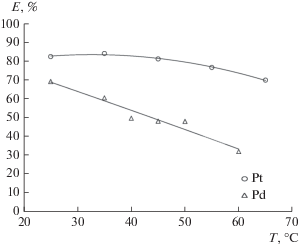
В ходе исследования были получены экспериментальные зависимости степени извлечения Pt(IV) и Pd(II) от температуры в диапазоне от 25 до 65°C (рис. 8). Как видно из рисунка, обе кривые имеют тенденцию к снижению степени извлечения при повышении температуры. Это говорит о том, что процесс экстракции металлов в системе ППГ 425–NaCl–H2O является экзотермическим. Высокая эффективность экстракции при нормальных условиях показывает преимущество предложенного метода извлечения платины(IV) и палладия(II) из солянокислых растворов.
ЗАКЛЮЧЕНИЕ
В ходе проведенных исследований изучено межфазное распределение Pt(IV) и Pd(II) в экологически безопасной экстракционной системе полипропиленгликоль 425–хлорид натрия–вода. Рассмотрено влияние параметров системы и условий проведения процесса на экстракцию исследуемых металлов. Установлен механизм извлечения Pt(IV) и Pd(II). Предложенная экстракционная система потенциально может быть использована для селективного извлечения Pt(IV) и Pd(II) из разбавленных солянокислых растворов без применения дополнительных реагентов.
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 18-29-24170.
Список литературы
Huang Y.-F., Pan M.-W., Lo S.-L. Hydrometallurgical metal recovery from waste printed circuit boards pretreated by microwave pyrolysis // Resour., Conserv. Recycl. 2020. V. 163. Article 105090.
Li H., Eksteen J., Oraby E. Hydrometallurgical recovery of metals from waste printed circuit boards (WPCBs): Current status and perspectives – A review // Resour., Conserv. Recycl. 2018. V. 139. P. 122.
Islam A., Ahmed T., Awual M. R., Rahman A., Sultana M., Aziz A.A., Monir M.U., Teo S.H., Hasan, M. Advances in sustainable approaches to recover metals from e-waste-A review // J. Cleaner Prod. 2019. V. 244. Article 118815.
Lee J., Kurniawan, Hong H.-J., Chung K.W., Kim S. Separation of platinum, palladium and rhodium from aqueous solutions using ion exchange resin: A review // Sep. Purif. Technol. 2020. V. 246. Article 116896.
Resina M., Fontàs C., Palet C., Muñoz M. Selective transport of platinum(IV) and palladium(II) through hybrid and activated composite membranes containing Aliquat 336 // Desalination. 2006. V. 200. № 1–3. P. 100.
Sun P.P., Lee M.S. Separation of Pt(IV) and Pd(II) from the loaded Alamine 336 by stripping // Hydrometallurgy. 2011. V. 109. № 1–2. P. 181.
Aly M.I., Masry B.A., Daoud J.A. Liquid-liquid extraction of platinum (IV) from acidic nitrate medium using a commercial trialkylphosphine oxide in kerosene // Sep. Sci. Technol. 2020. https://doi.org/10.1080/01496395.2020.1838542
Elizalde M., Menoyo B., Ocio A., Rúa M. del S. Palladium(II) extraction from nitric acid solutions by LIX 34 // J. Chem. Technol. Biotechnol. 2014. V. 89. № 6. P. 884.
Jha M.K., Gupta D., Lee J., Kumar V., Jeong J. Solvent extraction of platinum using amine based extractants in different solutions: A review // Hydrometallurgy. 2014. V. 142. P. 60.
Nguyen T.H., Sonu C.H., Lee M.S. Separation of platinum(IV) and palladium(II) from concentrated hydrochloric acid solutions by mixtures of amines with neutral extractants // J. Ind. Eng. Chem. (Amsterdam, Neth.). 2015. V. 32. P. 238.
Belova V.V., Khol’kin A.I. Zhidkova T.I. Extraction of platinum-group metals from chloride solutions by salts of quaternary ammonium bases and binary extractants // Theor. Found. Chem. Eng. 2007. V. 41. P. 743.
Voshkin A.A., Belova V.V., Zhilov V.I., Zhidkova T.I., Brenno Yu.Yu., Khol’kin A.I. Extraction of metal salts with trioctylmethylammonium di(2-ethylhexyl) dithiophosphate // Russ. J. Inorg. Chem. 2004. V. 49. № 8. P. 1278.
Rodrigues G.D., da Silva M.do C.H., da Silva L.H.M., Paggioli F.J., Minim L.A., Reis Coimbra J.S. dos. Liquid–liquid extraction of metal ions without use of organic solvent // Sep. Purif. Technol. 2008. V. 62. № 3. P. 687.
Zakhodyaeva Y.A., Zinov’eva I.V., Tokar E.S., Voshkin A.A. Complex extraction of metals in an aqueous two-phase system based on poly(ethylene oxide) 1500 and sodium nitrate // Molecules. 2019. V. 24. № 22. P. 4078.
Fedorova M.I., Zakhodyaeva Y.A., Zinov’eva I.V., Voshkin A.A. Recovery of rare-earth elements from nitrate solutions using polyethylene glycol 1500 // Russ. Chem. Bull. 2020. V. 69. № 7. P. 1344.
Da Silveira Leite D., Luis Gutierrez Carvalho P., Ramos Almeida M., Rodrigues de Lemos L., Barbosa Mageste A., Dias Rodrigues G. Extraction of yttrium from fluorescent lamps employing multivariate optimization in aqueous two-phase systems // Sep. Purif. Technol. V. 242. Article 116791.
Zakhodyaeva Y.A., Rudakov D.G., Solov’ev V.O., Voshkin A.A., Timoshenko A.V. Liquid–liquid equilibrium of aqueous two-phase system composed of poly(ethylene oxide) 1500 and sodium nitrate // J. Chem. Eng. Data. 2019. V. 64. № 3. P. 1250.
Zakhodyaeva Y.A., Rudakov D.G., Solov’ev V.O., Voshkin A.A., Timoshenko A.V. Liquid–liquid equilibrium in an extraction system based on polyvinylpyrrolidone-3500 and sodium nitrate // Theor. Found. Chem. Eng. 2019. V. 53. № 2. P. 159.
Rodrigues Barreto C.L., de Sousa Castro S., Cardozo de Souza Júnior E., Veloso C.M., Alcântara Veríssimo L.A., Sampaio V.S., Gandolfi O.R.R., da Costa Ilheu Fontan R., Neves I.C.O., Ferreira Bonomo R.C. Liquid–liquid equilibrium data and thermodynamic modeling for aqueous two-phase system PEG 1500 + sodium sulfate + + water at different temperatures // J. Chem. Eng. Data. 2019. V. 64. № 2. P. 810.
Zinov’eva I.V., Zakhodyaeva Y.A., Voshkin A.A. Extraction of monocarboxylic acids from diluted solutions with polyethylene glycol // Theor. Found. Chem. Eng. 2019. V. 53. № 6. P. 871.
Fedorova M.I., Levina A.V., Zakhodyaeva Y.A., Voshkin A.A. Interphase Distribution of V(IV) in the Polyethylene Glycol 1500–Sodium Nitrate–Water System // Theor. Found. Chem. Eng. 2020. V. 54. №4. P. 604.
Zinov’eva I.V., Zakhodyaeva Y.A., Voshkin A.A. Interphase distribution of caffeine and coumarin in extraction systems with polyethylene glycol and sodium sulfate // Theor. Found. Chem. Eng. 2019. V. 53. № 6. P. 996.
De Oliveira W.C.M., Rodrigues G.D., Mageste A.B., de Lemos L.R. Green selective recovery of lanthanum from Ni-MH battery leachate using aqueous two-phase systems // Chem. Eng. J. 2017. V. 322. P. 346.
Zakhodyaeva Y.A., Izyumova K.V., Solov’eva M.S., Voshkin A.A. Extraction separation of the components of leach liquors of batteries // Theor. Found. Chem. Eng. 2017. V. 51. № 5. P. 883.
Xie K., Huang K., Yang L., Yu P., Liu H. Three-liquid-phase extraction: a new approach for simultaneous enrichment and separation of Cr(III) and Cr(VI) // Ind. Eng. Chem. Res. 2011. V. 50. № 22. P. 12767.
Zakhodyaeva Y.A., Zinov’eva I.V., Voshkin A.A. Extraction of iron(III) chloride complexes using the polypropylene glycol 425–NaCl–H2O System // Theor. Found. Chem. Eng. 2019. V. 53. № 5. P. 735.
Huang Y., Chen D., Kong L., Su M., Chen Y. Aqueous two-phase (polyethylene glycol(400) + ammonia sulfate) system for thallium extraction: Process optimization, structural characterization, and mechanism exploration // Sep. Purif. Technol. 2019. V. 235. Article 115740.
Bulgariu L., Bulgariu D. Extraction of gold(III) from chloride media in aqueous polyethylene glycol-based two-phase system // Sep. Purif. Technol. 2011. V. 80. № 3. P. 620.
Марченко З. Методы спектрофотометрии в УФ и видимой областях в неорганическом анализе. М.: БИНОМ. Лаборатория знаний, 2007.
Аналитическая химия элементов. Платиновые металлы / Под ред. Алимарина И.П. М.: Наука, 1972.
Le Roux C.J., Kriek R.J. A detailed spectrophotometric investigation of the complexation of palladium(II) with chloride and bromide // Hydrometallurgy. 2017. V. 169. P. 447.
Чекушин В.С., Борбат В.Ф. Экстракция благородных металлов сульфидами и сульфоксидами. М.: Наука, 1984.
Nikoloski A.N., Ang K.-L. Review of the application of ion exchange resins for the recovery of platinum-group metals from hydrochloric acid solutions // Miner. Process. Extr. Metall. Rev. 2013. V. 35. № 6. P. 369.
Mhaske A.A., Dhadke P.M. Extraction separation studies of Rh, Pt and Pd using Cyanex 921 in toluene–a possible application to recovery from spent catalysts // Hydrometallurgy. 2001. V. 61. № 2. P. 143.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии