Теоретические основы химической технологии, 2021, T. 55, № 3, стр. 286-290
Повышение эффективности электромембранных процессов на участке электрохимического кадмирования
С. С. Кругликов a, *, Е. А. Архипов a, Д. А. Жирухин a, К. Н. Смирнов a, Т. А. Ваграмян a, В. А. Колесников a, Е. А. Филатова a
a Российский химико-технологический университет им. Д.И. Менделеева
Москва, Россия
* E-mail: skruglikov@mail.ru
Поступила в редакцию 20.01.2021
После доработки 25.01.2021
Принята к публикации 25.01.2021
Аннотация
На пилотной установке определены основные параметры электромембранного процесса извлечения ионов кадмия из сульфатно-аммонийного электролита кадмирования с высокими эксплуатационными характеристиками и ванны промывки кадмированных деталей в непроточной воде (ванны улавливания). Показано, что степень извлечения в стационарных условиях составляет около 99%, что соответствует значениям, полученным с другими сульфатно-аммонийными электролитами кадмирования, и позволяет рекомендовать исследуемый электролит для использования в промышленности.
ВВЕДЕНИЕ
В последние годы наблюдается постепенная замена традиционных реагентных технологий обезвреживания отработанных технологических растворов и очистки сточных вод гальванических производств новыми безреагентными и безотходными процессами, которые обеспечивают практически 100% извлечение металлов из технологических растворов [1–37 ]. Среди таких безреагентных технологий наиболее широкое применение в промышленности получил электромембранный процесс извлечения ионов кадмия из промывной воды [38–42]. На участках кадмирования из цианидных электролитов степень извлечения ионов кадмия превышает 99.9% [38–41].
При использовании электролитов кадмирования, содержащих соли аммония, образование аммиакатных комплексов исключает возможность очистки сточных вод с помощью традиционной реагентной технологии. В то же время наблюдается тенденция замены цианидных электролитов сульфатно-аммонийными, не уступающими цианидным по рассеивающей и кроющей способности и пригодными для кадмирования высокопрочных сталей [42–44]. Это означает, что при использовании новых сульфатно-аммонийных электролитов необходимо обеспечить максимальную степень удаления ионов кадмия из промывных вод и отработанных растворов еще на участке кадмирования, чтобы после соединения с другими сточными водами цеха можно было обеспечить выполнение требований по ПДК для кадмия за счет эффекта разбавления.
Задача данного исследования – определение на пилотной установке параметров электромембранного процесса, обеспечивающих максимальную степень извлечения ионов кадмия из сульфатно-аммонийного электролита и промывной воды в ванне улавливания – ванне с непроточной водой.
ТЕОРЕТИЧЕСКИЙ АНАЛИЗ
Процессы, используемые на участке электрохимического кадмирования, можно разделить на две группы на основе характера взаимосвязи между основными параметрами процесса и его производительностью:
(А) Процессы, скорость которых контролируется скоростью миграционного и диффузионного переноса ионов определенного вида через мембрану.
(Б) Процессы, скорость которых не зависит от переноса каких-либо ионов через мембрану.
Во всех технологических растворах, используемых на участках электрохимического кадмирования, молярная концентрация ионов кадмия составляет небольшую долю суммарной концентрации всех катионов, что означает невысокие значения числа переноса для ионов кадмия и, соответственно, низкую скорость их извлечения при относительно высоких энергозатратах для всех процессов, относящихся к группе А.
В группу А входят процессы регенерации хроматных растворов пассивирования кадмиевых покрытий и растворов снятия кадмиевых покрытий с бракованных деталей и с подвесок, а также процессы извлечения ионов кадмия из промывной воды после этих операций. Скорость извлечения ионов кадмия из сульфатно-аммонийного электролита кадмирования и промывной воды после этой операции не зависит от переноса каких-либо ионов через мембрану, а контролируется условиями конкуренции двух независимых электрохимических реакций – катодного восстановления ионов гидроксония и ионов кадмия. Восстановление ионов гидроксония повышает pH в прикатодной зоне раствора, и в присутствии ионов аммония это приводит к росту концентрации молекул аммиака.
Последние образуют с ионами кадмия комплексы, потенциал восстановления которых смещается в отрицательном направлении. Таким образом, необходимо, с одной стороны, предотвратить чрезмерное подкисление католита, ускоряющее разряд ионов гидроксония, а с другой – не создавать условий для связывания ионов кадмия в аммиакатные комплексы. Наряду с эффектами комплексообразования на кинетику процесса катодного разряда ионов кадмия оказывает влияние процесс массопереноса, который при рабочих режимах электролиза может играть решающую роль
В отношении состава анолита основным требованием является присутствие свободной серной кислоты, обеспечивающее стабильную работу свинцового анода.
Баланс основных катодных и анодных процессов в ваннах улавливания – это преимущественно разряд молекул воды на аноде и на катоде:
Участки кадмирования, как правило, работают в одну смену, поэтому изменения pH католита в рабочую смену компенсируются диффузией ионов гидроксила в анолит в нерабочие смены. Кроме того, постоянный занос ионов аммония в католит придает ему буферные свойства, а также предотвращает гидролиз соли кадмия благодаря образованию растворимых аммиакатных комплексов.
Последний эффект, очевидно, будет смещать потенциал осаждения кадмия в отрицательном направлении, т.е. способствовать снижению выхода по току кадмия.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Все эксперименты проводили на пилотной установке, параметры которой (за исключением объема катодной камеры) были соизмеримы с параметрами ванны улавливания на участке кадмирования:
объем анодной камеры – 2 л (в цехе – 4 л);
площадь мембраны МК-40Л – 3 дм2 (в цехе – 4 дм2);
объем катодной камеры – 5 л (в цехе – 50–200 л);
анод – свинцовый, площадью 2.2 дм2 (в цехе – 1–2 дм2);
катод – сталь 08КП – 8 шт. с рабочей поверхностью каждого 2–16 дм2 (в цехе – один катод 10–20 дм2).
Концентрацию ионов кадмия в растворе определяли титриметрическим и атомно-абсорбционным методами. Измерения выполнены на оборудовании Центра коллективного пользования им. Д.И. Менделеева.
Состав электролита кадмирования:
3CdSO4 ⋅ 8H2O – 50 г/л (Cdмет – 22 г/л),
(NH4)2SO4 – 220 г/л,
Добавка ЦКН-04 – 10 мл/л.
Анолит – раствор серной кислоты – 10 г/л (выбор такого состава анолита для промышленных установок обеспечивает устойчивую работу свинцового анода).
Электролиз проводили как в режиме стабилизации pH католита (pH 8), так и без корректировки, когда величина pH католита постепенно уменьшалась за счет диффузии ионов водорода из анолита во время межсменных перерывов.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
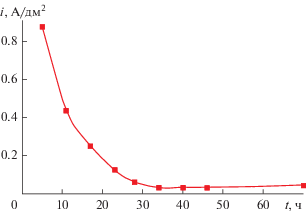
В первой серии экспериментов (рис. 1) был изучен процесс полного извлечения кадмия из электролита вышеуказанного состава. Необходимость такой операции возникает при загрязнении электролита примесями, очистка от которых технически затруднительна или нецелесообразна экономически. В процессе электролиза постепенно снижали катодную плотность тока (рис. 2), что позволило, с одной стороны, существенно интенсифицировать процесс на начальных стадиях, а с другой – исключить бесполезный расход электроэнергии на электролиз воды на последующих стадиях.
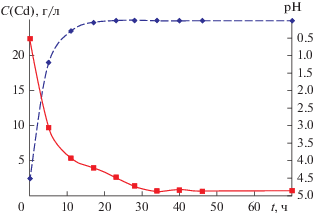
Рис. 1.
Зависимость концентрации кадмия в растворе католита от времени электролиза. Пунктирная линия отображает изменение рН католита по мере протекания электролиза.
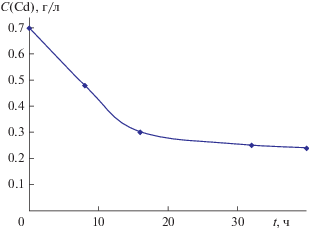
Во второй серии экспериментов воспроизведены условия электролиза, соответствующие режиму работы ванны улавливания. В первую очередь это относится к величине рH католита, которую поддерживали на уровне 8. При электролизе катодная плотность тока составляла 0.7 А/дм2 и во времени не изменялась. На рис. 3 показано изменение концентрации ионов кадмия в процессе электролиза. Стационарное значение концентрации ионов кадмия в ванне улавливания около 0.2 г/л означает снижение выноса кадмия на очистные сооружения в 100 раз. Этот показатель практически совпадает со значениями, измеренными в аналогичных ваннах улавливания на нескольких промышленных предприятиях, использующих электролиты кадмирования, близкого химического состава [42–44].
Рис. 3.
Зависимость концентрации кадмия в растворе католита, соответствующего составу промывной воды в ванне улавливания, от времени электролиза.
Поскольку выделившийся на катоде металлический кадмий можно полностью вернуть в производственный цикл анодным растворением кадмиевого осадка путем периодического завешивания катода на анодную штангу в ванне кадмирования, данная технология позволяет построить безотходный замкнутый технологический цикл по отношению к высокотоксичным ионам кадмия. При необходимости можно снизить вынос ионов кадмия на очистные сооружения еще на порядок, введя уже практикуемое в гальванических цехах опрыскивание водой подвесок, выгружаемых из ванны улавливания.
ЗАКЛЮЧЕНИЕ
Успешные результаты экспериментальной проверки применимости электромембранной технологии для утилизации отработанного электролита нового состава и извлечения ионов кадмия из ванн улавливания после операции кадмирования в этом электролите позволяют рекомендовать его как вполне приемлемый в отношении экологической безопасности.
ОБОЗНАЧЕНИЯ
Список литературы
Kruglikov S.S. The Use of electrochemical Modules (IEMs) in Plating Industry // Proc. NASF SUR/FIN`2006 Conference Milwaukee, USA. 18–21 Sept. 2006. P. 432.
Yurchuk T.Y., Bergmann H., Kruglikov S.S. Verfahren der elektrochemischen Umweltschutztechnik am Beischpiel der Regenerierung chromathaltiger Baeder der Galvanotechnik // Chem. Ing. Tech. 1997. V. 69. № 9. P. 43.
Paidar M., Fateev V., Bouzek K. Membrane electrolysis–history, current status and perspective // Electrochim. Acta. 2016. V. 209. P. 737.
Chen G. Electrochemical technologies in wastewater treatment // Sep. Purif. Technol. 2004. V. 38. P. 11.
Steathamann H., Grabovski A., Eigenberger B. Electromembrane processes, efficient and versatile tools in a sustainable industrial development // Desalination. 2006. V. 199. P. 1.
Varentsov V.K., Koshev A.N., Sukhov I.F. Mathematical modeling and experimental studies of the joint electrodeposition of gold and silver from sulfuric acid-thiourea solutions on flow-through 3D electrodes taking into account its nonstationary state // Theor. Found. Chem. Eng. 2018. V. 52. P. 495. [Варенцов В.К., Кошев А.Н., Сухов И.Ф. Процессы совместного осаждения золота и серебра из сернокислых растворов на проточном электроде // Теор. осн. хим. технол. 2018. Т. 52. С. 391.]
Желонкина Е.А., Шишкина С.В., Михайлова И.Ю., Ананченко Б.А. Исследование электродиализа раствора хлорида меди при сверхпредельных токах // Мембр. мембр. технол. 2017. Т. 7. № 3. С. 330. [Zhelonkina E.A., Shishkina S.V., Mihailova I.Yu., Ananc-henko B.A. Study of electrodialysis of a copper chloride solution at overlimiting currents // Pet. Chem. 2017. V. 57. № 11. P. 947.]
Marder L., Bernardes A.M., Ferreira J.Z. Cadmium electroplating wastewater treatment using a laboratory-scale electrodialysis system // Sep. Purif. Technol. 2004. V. 37. P. 247.
Первов А.Г., Андрианов А.П., Горбунова Т.П., Багдасарян А.С. Мембранные технологии в решении экологических проблем // Мембр. мембр. технол. 2011. Т. 1. № 2. С. 83. [Perov A.G., Adrianov A.P., Gorbunova T.P., Bagdasaryan A.S. Membrane technologies in solving environmental problems // Pet. Chem. 2011. V. 1. № 2. P. 83.]
Koshev A.N., Varentsov V.K. Mathematical modeling of operation of a reactor with flow-through electrodes at limiting diffusion current under non-steady-state conditions // Theor. Found. Chem. Eng. 2018. V. 52. P. 779. [Кошев А.Н., Варенцов В.К. Математическое моделирование работы реактора с проточными трехмерными электродами в режиме предельного диффузионного тока в условиях нестационарности // Теор. осн. хим. технол. 2018. Т. 52. С. 497.]
Koshev A.N., Varentsov V.K. Mathematical modeling of effective systems of reactors with flow-through 3D electrodes // Theor. Found. Chem. Eng. 2018. V. 52. № 1. P. 87. [Кошев А.Н., Варенцов В.К. Математическое моделирование эффективных систем реакторов с проточными трехмерными электродами // Теор. осн. хим. технол. 2018. Т. 52. № 1. С. 93.]
Landaburu Aguirre J., Pongracz E., Keiski R.L. Separation of cadmium and copper from phosphorus rich synthetic water by micellar enhanced ultrafiltration // Sep. Purif. Technol. 2011. V. 81. P. 41.
Vasudevan S., Lakshmi J. Effect of alternating and direct current in electrocoagulation process on the removal of cadmium from water – a novel approach // Sep. Purif. Technol. 2011. V. 80. P. 643.
Singh V., Panley S., Singh S.K., Sanghi R. Removal of cadmium from aqueous solutions by adsorption using poly(acrylamide) modified guar gum-silica nanocomposites // Sep. Purif. Technol. 2009. V. 67. P. 251.
Cay S., Uyanik A., Ozasik A. Single and binary component adsorption of copper(II) and cadmium(II) from aqueous solutions using tea industry waste // Sep. Purif. Technol. 2004. V. 38. P. 273.
Zhai Y., Wei X., Zeng G., Zhang D., Chu K. Study of adsorbent derived from sewage sludge for the removal of Cd2+, Ni2+ in aqueous solutions // Sep. Purif. Technol. 2004. V. 38. P. 191.
Reddy B.R., Priya D.N., Park K.H. Separation and recovery of cadmium(II), cobalt(II), and nickel(II) from sulfate leach liquors of spent Ni-Cd batteries using phosphorous based extractants // Sep. Purif. Technol. 2006. V. 50. P. 161.
Abbasn I.A., Al-Amer A.M., Laoui T., Atieh M.A. Heavy metals removal by advanced carbon nanotubes: Critical review of adsorption application // Sep. Purif. Technol. 2016. V. 157. P. 141.
Okieimen F.E., Sokbaike C.E., Ebhoaye J.E. Removal of cadmium and copper ions from aqueous solution with cellulose graft polymers // Sep. Purif. Technol. 2005. V. 44. P. 85.
Shenashen M.A., Elshehi E.A., Sherif A. ElSafty, Khairy M. Visual monitoring and removal of divalent copper, cadmium, and mercury ions from the water by using mesoporous cubic Ia3d aluminosilica sensors // Sep. Purif. Technol. 2013. V. 116. P. 73.
Densili A., Garipcan B., Karabakan A., Sai R., Patir S. Metal-complexing ligand methacryloylamidocysteine containing polymer beads for Cd(II) removal // Sep. Purif. Technol. 2003. V. 30. P. 3.
Salehi E., Madaleni S.S., Heidari F. Dynamic adsorption of Ni(II) and Cd(II) ions from water using 8-hydroxyquinoline ligand immobilized PVDF membrane isotherms, thermodynamix and kinetics // Sep. Purif. Technol. 2012. V. 94. P. 18.
Fiol N., Escusa I.V., Martinez M., Miralles N., Seratols J. Sorption of Pb(II), Ni(II), Cu(II), Cd(II) from aqueous solution by olive stone waste // Sep. Purif. Technol. 2006. V. 59. P. 132.
Al Hamouz O.C.S., Estatie M., Saleh T.A. Removal of cadmium ions from wastewater by dithiocarbamate functionalized pyrrole based terpolymers // Sep. Purif. Technol. 2017. V. 177. P. 101.
Jiha M.K., Gupta D., Choubey P.K., Kumar V., Lee J.-Ch. Solvent extraction of copper, zinc, cadmium, and nickel from sulfate solution in mixer settler unit (MSU) // Sep. Purif. Technol. 2014. V. 122. P. 119.
Mauchauffee S., Meux E., Schneider M. Selective precipitation of cadmium from nickel cadmium sulfate solutions using sodium deconate // Sep. Purif. Technol. 2008. V. 62. P. 394.
Ghaeabaghi M., Irannajad M., Azadmehr A.R. Leaching behavior of cadmium from hazardous waste // Sep. Purif. Technol. 2012. V. 86. P. 9.
Mahandra H., Singh R., Gupta B. Liquid-liquid extraction studies on Zn(II) and Cd(II) using phosponium ionic liquid (Cyphos IL 104) and recovery of zinc from zinc plating mud // Sep. Purif. Technol. 2017. V. 177. P. 281.
Sharma R.K., Puri A., Monga Y., Adholeya A. Newly modified silica-based magnetically-driven nano-adsorbent: A sustainable and versatile platform for effient and selective recovery of cadmium from water and fly-ash ameliorated soil // Sep. Purif. Technol. 2014. V. 127. P. 121.
Segund J.O.D.V., Salazar-Banda G.R., Feitoza A.C.O., Vilar E.O., Cavalcanti E.B. Cadmium and lead removal from aqueous synthetic waste utilizing Chemelec electrochemical reactor: Study of the operating conditions // Sep. Purif. Technol. 2012. V. 88. P. 1107.
Yaftian M.R., Zamani A.A., Parinejad M., Shams E. Ion-pair extraction of cadmium complex anions from hydrochloric acid media using oxonium dicyclohexyl-18-crown-6-complex // Sep. Purif. Technol. 2005. V. 42. P. 175.
Svecova L., Spanelova M., Kubal M., Guibal E. Cadmium, lead, and mercury biosorption on waste fungal biomass issued from fermentation industry. I. Equilibrium studies // Sep. Purif. Technol. 2006. V. 52. P. 142.
Некрасова Н.Е., Кругликова Е.С., Тележкина А.В., Капустин Е.С., Кравченко Д.В. Применение анода Ti/IrO2 – SnO2/PbO2 в растворе пассивирования кадмия // Гальванотех. обраб. поверхн. 2017. Т. 25. № 4. С. 4.
Kruglikov S.S. Application of Electromembrane Processes in Chromium Electroplating Technology // Pet. Chem. 2016. V. 56. № 10. P. 976. [Кругликов С.С. Применение электромембранных процессов в технологии электрохимического хромирования // Мембр. мембр. технол. 2016. Т. 6. № 3. С. 305.]
Кругликов С.С., Тележкина А.В., Капустин Е.С., Кравченко Д.В. Анодные материалы для электролиза хроматно-нитратных растворов // Гальванотех. обраб. поверхн. 2017. Т. 25. № 3. С. 37.
Kruglikov S.S., Kolesnikov V.A., Nekrasova N.E., Gubin A.F. Regeneration of Chromium Electroplating Electrolytes by the Application of Electromembrane Processes // Theor. Found. Chem. Eng. 2018. V. 52. № 5. P. 800. [Кругликов С.С., Колесников В.А., Некрасова Н.Е., Губин А.Ф. Регенерация электролитов хромирования с помощью электромембранных процессов // Теор. осн. хим. технол. 2018. Т. 52. № 5. С. 519.]
Кругликов С.С. Применение электромембранных процессов для стабилизации и регулирования состава раствора в электролизерах // Гальванотех. обраб. поверхн. 2018. Т. 26. № 2. С. 41.
Кругликов С.С., Кочергин Л.И., Белкина Л.Н., Яшина О.А. Опыт промышленной эксплуатации погружных электрохимических модулей в ваннах улавливания после операции кадмирования и хромирования // Гальванотех. обраб. поверхн. 2005. Т. 13. № 1. С. 69.
Kruglikov S.S., Sirotkin V.I. Removal of Cadmium and Cyanide Ions from Rinse Water in Plating Shops // Proc. AEFS SUR/FIN`2006 Conference. Milwaukee, 2006. P. 474.
Кругликов С.С., Сироткин В.И., Воробьева М.А., Тогузов Б.М. Об эффективности использования ПЭМ в ваннах улавливания после операции кадмирования. Опыт московских предприятий // Гальванотех. обраб. поверхн. 2009. Т. 17. № 4. С. 48.
Kruglikov S.S., Nekrasova N. E., Kuznetsov V.V., Filatova E.A. An electromembrane process for cadmium recovery from dilute cadmium electroplating dragout solutions // Membr. Membr. Technol. 2019. V. 1. № 2. P. 120. [Кругликов С.С., Некрасова Н.Е., Кузнецов В.В., Филатова Е.А. Электромембранный метод извлечения кадмия из разбавленных растворов ванн улавливания после электрохимического кадмирования // Мембр. мембр. технол. 2019. Т. 9. № 2. С. 146.
Архипов Е.А., Григорян Н.С., Шувалов Д.А., Жирухин Д.А., Смирнов К.Н., Ваграмян Т.А. Универсальная добавка для кислых электролитов кадмирования // Гальванотех. обраб. поверхн. 2018. Т. 26. № 4. С. 21.
Смирнов К.Н., Архипов Е.А., Кравченко Д.В. Добавки для сульфатно-аммонийного электролита кадмирования. Практика применения // Гальванотех. обраб. поверхн. 2016. Т. 24. № 2. С. 35.
Архипов Е.А., Смирнов К.Н., Жирухин Д.А., Володин И.А., Калинкина А.А., Ваграмян Т.А. Способ электроосаждения защитных кадмиевых покрытий (варианты). Пат. 2644639 РФ. 2018.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии