Теоретические основы химической технологии, 2021, T. 55, № 3, стр. 299-308
Глубокий эвтектический растворитель на основе хлорида холина и сульфосалициловой кислоты: свойства и применение
И. В. Зиновьева a, А. Я. Федоров a, Н. А. Милевский a, Ю. А. Заходяева a, *, А. А. Вошкин a
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
* E-mail: yz@igic.ras.ru
Поступила в редакцию 01.02.2021
После доработки 04.02.2021
Принята к публикации 08.02.2021
Аннотация
Представлены результаты исследования физических свойств глубокого эвтектического растворителя на основе хлорида холина и сульфосалициловой кислоты. Построена фазовая диаграмма для данной двухкомпонентной смеси, впервые изучены зависимости ее плотности и показателя преломления от температуры. Рассчитана молекулярная рефракция для исследуемого глубокого эвтектического растворителя. Оценена возможность его применения в качестве экстрагента для извлечения ионов металлов в системе твердое–жидкость.
ВВЕДЕНИЕ
Современные тенденции применения принципов зеленой химии в химической технологии мотивируют исследователей разрабатывать и использовать новые подходы для замены традиционных органических растворителей, которые обладают высокой летучестью, токсичны и взрывоопасны. Одними из таких являются глубокие эвтектические растворители, представляющие собой жидкую при комнатной температуре смесь, образованную из двух или более твердых компонентов. Переход из твердого состояния в жидкое становится возможным благодаря нековалентным взаимодействиям между донором и акцептором водородных связей [1, 2]. Глубокие эвтектические растворители характеризуются более низкой температурой плавления, чем у образующих его индивидуальных компонентов. Их преимущества состоят в том, что в состав зачастую входят нетоксичные, легкодоступные, дешевые соединения, а также отсутствует необходимость использования воды для их синтеза и применения.
В 2007 г. Эббот с соавторами [3] определили несколько типов глубоких эвтектических растворителей: I тип образован солью четвертичного аммониевого основания и хлоридом металла (Zn, Al, Fe, Ga), II тип – солью четвертичного аммониевого основания и гидратом хлорида металла (Cr, Co, Cu, Ni), III тип – солью четвертичного аммониевого основания и органическим соединением с –CONH2, –COOH, –OH группами, IV тип состоит из хлорида металла (например, ZnCl2), смешанного с различными донорами водородных связей, такими как мочевина, этиленгликоль, ацетамид и другими [4]. Тип V, являющийся относительно новым, представляет собой смесь неионных, молекулярных акцепторов и доноров водородной связи [5].
В качестве доноров водородных связей могут выступать органические кислоты (щавелевая, лимонная, молочная, левулиновая и др.), полимеры (например, полипропиленгликоль), полиолы (глицерин, этиленгликоль) и другие [6]. Среди акцепторов чаще всего применяют хлорид холина, бромид тетрабутиламмония и др. [7, 8].
Физические (плотность, вязкость) и электрохимические свойства глубоких эвтектических растворителей играют ключевую роль как в научных исследованиях, так и в промышленных применениях [9]. На свойства глубоких эвтектических растворителей и их температурную зависимость влияют молекулярные характеристики, природа доноров и акцепторов водородной связи, соотношение компонентов. Зачастую плотность большинства глубоких эвтектических растворителей находится в диапазоне от 1.0 до 1.35 г/см3 при 25°С. В работе [10] авторы определили плотности глубоких эвтектических растворителей на основе хлорида бензилалкиламмония, где в качестве доноров использовали ряд гликолей и глицерин. Результаты исследования показали, что глубокий эвтектический растворитель на основе этиленгликоля имеет более низкую плотность по сравнению с таковым на основе глицерина. Увеличение числа –ОН групп в молекуле донора водородной связи приводит к образованию большего количества водородных связей, тем самым уменьшая свободный объем в смеси. К сожалению, вязкость глубоких эвтектических растворителей при нормальных условиях имеет высокие значения, что делает их применение затруднительным. Например, вязкость эталина (хлорид холина–этиленгликоль) составляет 52 сП при 20°С по сравнению с 1 сП для воды при той же температуре. Поэтому понимание этого свойства жидкой смеси особенно важно в изучении глубоких эвтектических растворителей. Однако, варьируя состав или соотношение компонентов, можно изменять их свойства в зависимости от конкретного применения.
Глубокие эвтектические растворители нашли применение в аналитической химии (электрохимия, хроматография, адсорбция и др.) [11], биотехнологии [2], и катализе [12]. Их внедрение в различные производственные процессы, такие как десульфуризация [13] и производство биодизеля [14], оправдано не только с экономической, но и экологической точек зрения. В последнее время в химии и технологии экстракции жидкость–жидкость активно разрабатываются экстрагенты на основе ионных жидкостей [15–19], водорастворимых полимеров [20–25] и глубоких эвтектических растворителей [26, 27]. В экстракции твердое–жидкость происходит смещение направлений исследований в сторону зеленой химии. К примеру, традиционные методы извлечения металлов из электронных отходов неселективны, подразумевают использование минеральных кислот и последующие экономические затраты на регенерацию реагентов и обезвреживание сточных вод. Замена этих методов на подходы с использованием глубоких эвтектических растворителей позволяет избежать перечисленных проблем [28, 29]. Переработка отработанных химических источников тока, таких как Ni-MH, Li-ion и др., представляет собой важный технологический процесс, эффективность которого можно повысить, применяя глубокие эвтектические растворители на этапе выщелачивания [30, 31]. В последние годы глубокие эвтектические растворители были предложены в качестве альтернативных реагентов для растворения оксидов металлов [32, 33]. В частности, установлено, что глубокие эвтектические растворители на основе хлорида холина могут растворять широкий круг оксидов металлов, а эффективность в значительной степени зависит от свойств используемого донора водородной связи [34].
Целью настоящей работы является изучение физических свойств глубокого эвтектического растворителя на основе холина хлорида и сульфосалициловой кислоты и оценка возможности его применения в качестве экстрагента для извлечения ионов металлов в гетерогенной системе твердое–жидкость.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реактивы. Хлорид холина (Acros Organics, чистота 99%), салициловая и сульфосалициловая кислоты квалификации “хч” были использованы без дополнительной очистки. Оксид железа(III), оксид меди(II) и оксид иттрия(III) использовали со степенью чистоты >99%.
Определение эвтектической точки. Фазовая диаграмма для смеси донора и акцептора была построена на примере предложенной ранее методики [35]. Для этого нами были приготовлены смеси на основе хлорида холина и сульфосалициловой кислоты в соотношениях: 1 : 9, 1 : 4, 3 : 7, 2 : 3, 1 : 1, 3 : 2, 7 : 3, 4 : 1, 9 : 1. Взвешенные на аналитических весах AND HR-100AZ (Япония) реагенты помещали в стеклянные виалы объемом 10 мл. Для образования глубоких эвтектических растворителей виалы помещали в термостатированную глицериновую баню при температуре 90°С и перемешивали при 1250 об/мин в течение 2 ч на магнитной мешалке IKA C-MAG HS 4 (Германия). После приготовления всех составов температуру медленно снижали с шагом 0.5°С и наблюдали за кристаллизацией в объеме бинарной смеси. При появлении первого кристалла фиксировали температуру. На основе полученных данных построили фазовую диаграмму, по которой определили состав точки эвтектики.
Измерение физических свойств. Исследование зависимости показателя преломления (nD) глубоких эвтектических растворителей от температуры в диапазоне от 20 до 60°С проводили с помощью рефрактометра Anton Paar Abbemat 3200 (Австрия). Измерение плотности (ρ) синтезированных образцов в диапазоне от 20 до 80°С проводили на цифровом плотномере Anton Paar DMA 4500 M Chemicals (Австрия). Оценку вязкости осуществляли с использованием вискозиметра Anton Paar Lovis 2000 M/ME (Австрия).
Характеризация глубокого эвтектического растворителя. Спектры ядерного магнитного резонанса были записаны в дейтерированых растворителях (D2О для хлорида холина и сульфосалициловой кислоты и (D3С)2SO для глубокого эвтектического растворителя на их основе) на спектрометре Bruker Fourier 300 HD (Швейцария) с рабочей частотой 300 МГц при температуре 25°С. Инфракрасные спектры были записаны на приборе Shimadzu IRTracer-100 c приставкой НПВО MIRacle-10 (Япония) при температуре 25°С.
Растворение оксидов металлов в предложенном глубоком эвтектическом растворителе. Исследование растворения оксидов металлов (Fe2O3, CuO, Y2O3) проводили путем добавления к навескe оксида металла точного объемa глубокого эвтектического растворителя (массовое соотношение твердой фазы к жидкой составляло 1 : 50) в стеклянных виалах объемом 5 мл при температуре 80°С и постоянном перемешивании 1250 об/мин. Время установления равновесия составляет 120 мин. Концентрацию металла в жидкой фазе определяли спектрофотометрическим методом с использованием 4-(2-пиридилазо)резорцина, образующего комплексы с ионами меди(II), которые поглощают в видимой области спектра при длине волны 494 нм. Содержание Fe(III) в жидкой фазе определяли методом спектрофотометрии в видимой области при длине волны 420 нм с использованием в качестве индикатора сульфосалициловой кислоты относительно холостых растворов. Измерение оптической плотности проводили на приборе ПЭ-5400 УФ Экросхим (Россия). В определении иттрия(III) применяли метод комплексонометрического титрования комплексоном III, используя в качестве индикатора ксиленоловый оранжевый при рН 5.5–6.
Представленные экспериментальные данные являются результатом серии экспериментов и обработаны методами математической статистики.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Была проведена серия синтезов смесей с различным исходным соотношением акцептора и доноров водородных связей (рис. 1). Для синтеза были выбраны следующие соотношения – 3 : 2, 1 : 1, 1 : 2 (хлорид холина :сульфосалициловая кислота); 1 : 1, 1 : 2 (хлорид холина:салициловая кислота). Заметим, что наиболее перспективными с точки зрения практического использования стали смеси температура приготовления которых меньше 90°С, а температура кристаллизации меньше 10°С. Таким требованиям соответствует смесь акцептора и донора водородной связи следующего состава: хлорид холина:сульфосалициловая кислота, которая ранее была упомянута в литературных источниках, но не была изучена подробно [12]. Более того, с экономической точки зрения, хлорид холина является наиболее конкурентоспособным среди исследованных акцепторов.
Рис. 1.
Этапы синтеза глубокого эвтектического растворителя на основе хлорида холина и сульфосалициловой кислоты: слева – смесь двух твердых компонентов; справа – жидкая гомогенная смесь.

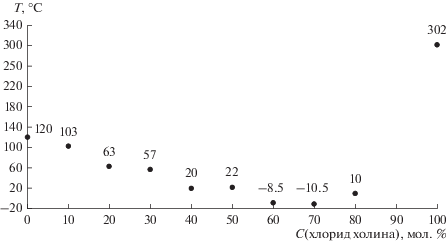
Точка эвтектики является основной определяющей характеристикой глубокого эвтектического растворителя, в которой наблюдается самая низкая температура кристаллизации. На рис. 2 представлены температуры кристаллизации исследуемых смесей хлорида холина и сульфосалициловой кислоты при разном содержании акцепторов. На основе фазовой диаграммы было выявлено соотношение акцептора и донора водородных связей, при котором смесь находится в точке эвтектики со значением –10.5°С – (7 : 3). Видно, что температура кристаллизации эвтектической смеси значительно ниже, чем у их отдельных компонентов – 120°С (сульфосалициловая кислота), 302°С (хлорид холина). Отметим, что исследуемый глубокий эвтектический растворитель может находиться в стабильном жидком состоянии при комнатной температуре в широком диапазоне составов.
Рис. 2.
Зависимость температуры кристаллизации смеси хлорида холина и сульфосалициловой кислоты от соотношения акцептора и донора водородных связей.
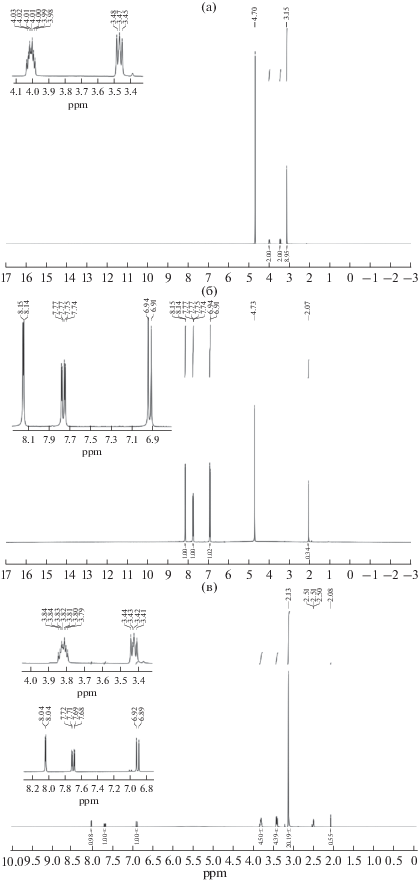
Из литературных данных известно, что глубокие эвтектические растворители на основе хлорида холина и органических кислот образованы межмолекулярными водородными связями [12]. Для подтверждения механизма образования глубокого эвтектического растворителя использовали методы ИК и ЯМР спектроскопии. Приведенные на рис. 3 спектры ЯМР подтверждают чистоту исходных компонентов (а и б). На ЯМР-спектре глубокого эвтектического растворителя (в) без изменения мультиплетности сохраняются характерные сигналы хлорида холина, представленные на спектре а, и сульфосалициловой кислоты, представленные на спектре б, что подтверждает отсутствие образования новых веществ.
Рис. 3.
ЯМР-спектры хлорида холина (а), сульфосалициловой кислоты (б) и глубокого эвтектического растворителя на их основе (в).
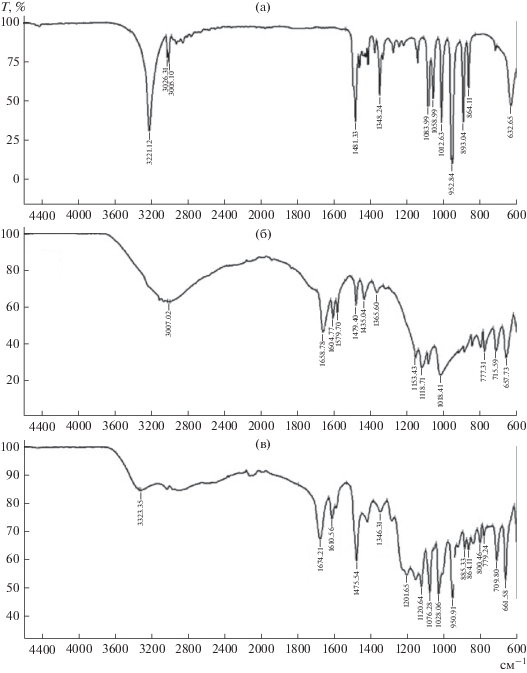
На рис. 4 приведены ИК-спектры исходных веществ и синтезированного глубокого эвтектического растворителя, сравнение которых указывает на образование водородной связи между карбоксильной группой сульфосалициловой кислоты и анионом хлора в молекуле хлорида холина. Характерный сдвиг уширенного сигнала ОН-группы с 3007 на 3323 см–1 связан с изменением энергии связи О–Н ввиду образования водородной связи. При этом характерные сигналы углеродных скелетов исходных молекул сохраняются, что подтверждает отсутствие образования новых ковалентных связей.
Рис. 4.
ИК-спектры хлорида холина (а), сульфосалициловой кислоты (б) и глубокого эвтектического растворителя на их основе (в).
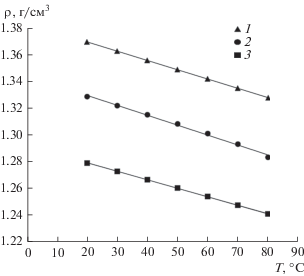
Плотность является ключевым показателем, который может предоставить информацию о межмолекулярных взаимодействиях в глубоких эвтектических растворителях [9]. В некоторых случаях соотношение акцепторa и донорa позволяет варьировать значение плотности смеси. Зависимость плотности исследуемого глубокого эвтектического растворителя при разных соотношениях компонентов от температуры представлена на рис. 5. Полученные результаты показывают, что для всех смесей значения плотности линейно уменьшаются с увеличением температуры. Такой характер зависимости наблюдается для большинства ранее исследуемых глубоких эвтектических растворителей [36, 37]. При этом плотность глубокого эвтектического растворителя возрастает с увеличением мольного соотношения сульфосалициловой кислоты. Это объясняется тем, что повышение концентрации сульфосалициловой кислоты приводит к увеличению количества функциональных групп, которые способствуют образованию большего количества водородных связей, что предположительно уменьшает свободное пространство в объеме смеси [9].
Рис. 5.
Зависимость плотности глубокого эвтектического растворителя хлорид холина : сульфосалициловая кислота от температуры для разных соотношений акцепторов и доноров водородных связей: 1 – 2 : 3; 2 – 1 : 1; 3 – 3 : 2.
Одним из важных физических свойств глубоких эвтектических растворителей, которое необходимо изучить для оценки их применения в технологических процессах, является вязкость. Проведенная нами оценка вязкости глубокого эвтектического растворителя на основе сульфосалициловой кислоты показала, что он может быть использован как экстрагент. При температурах от 50 до 80°С вязкость глубокого эвтектического растворителя находится в диапазоне 100–300 сП, что является приемлемым для их применения в технологических процессах на используемом в настоящее время оборудовании.
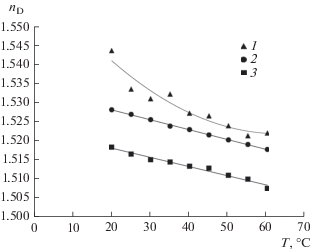
Изучена зависимость показателя преломления глубокого эвтектического растворителя на основе хлорида холина и сульфосалициловой кислоты от температуры (рис. 6). Видно, что для всех изученных составов показатели преломления снижаются с повышением температуры. Похожий эффект наблюдается для ранее изученных глубоких эвтектических растворителей [38].
Рис. 6.
Зависимость показателя преломления глубокого эвтектического растворителя хлорид холина:сульфосалициловая кислота от температуры для разных соотношений акцепторов и доноров водородных связей: 1 – 2 : 3; 2 – 1 : 1; 3 – 3 : 2.
Показатель преломления можно использовать для изучения электрических свойств глубоких эвтектических растворителей [9]. В исследовании [39] экспериментально полученные значения показателя преломления глубоких эвтектических растворителей на основе L-пролина и бетаина были использованы для расчета молекулярной рефракции Rm по уравнению Лорентц–Лоренца:
где V – молярный объем смеси, рассчитанный по формуле где MDES – молярная масса глубокого эвтектического растворителя и ρ – плотность глубокого эвтектического растворителя.Во многих моделях жидкого состояния предполагается наличие пустот между молекулами, характеризуемое свободным молярным объемом (Fm), значение которого необходимо для расчетов растворимости газов в рассматриваемой жидкости. Вышеупомянутые параметры необходимы для оценки растворимости газов в растворителях [40]. Проведен расчет молекулярной рефракции изученного глубокого эвтектического растворителя для разных соотношений акцепторов и доноров водородных связей (табл. 1).
Таблица 1.
Молекулярная рефракция глубокого эвтектического растворителя хлорид холина–сульфосалициловая кислота
| Соотношение акцептора и донора водородных связей | T, °С | Rm, мл/моль |
|---|---|---|
| 2 : 3 | 60 | 212.24 |
| 50 | 211.79 | |
| 40 | 211.83 | |
| 30 | 212.03 | |
| 20 | 215.13 | |
| 1 : 1 | 60 | 83.21 |
| 50 | 83.09 | |
| 40 | 83.01 | |
| 30 | 82.93 | |
| 20 | 82.85 | |
| 3 : 2 | 60 | 203.13 |
| 50 | 203.25 | |
| 40 | 203.05 | |
| 30 | 202.63 | |
| 20 | 202.72 |
Установлено, что значения Rm исследуемого глубокого эвтектического растворителя не зависят от температуры в диапазоне от 20 до 60°С, следовательно, поляризуемость не зависит от температуры, но зависит от соотношения компонентов, что коррелирует с зависимостью показателя преломления от состава глубокого эвтектического растворителя.
Исходя из экспериментально полученных данных о физических свойствах глубокого эвтектического растворителя на основе хлорида холина и сульфосалициловой кислоты для проведения экспериментальных исследований экстракции ионов переходных металлов в гетерогенных системах твердое–жидкость, нами было выбрано мольное соотношение акцептора и донора водородной связи, равное 3 : 2. В качестве модельных объектов были выбраны наиболее часто используемые представители разных групп металлов (цветные, редкоземельные и др.), которые входят в состав компонентов электронных устройств, активно применяемых в настоящее время [41].
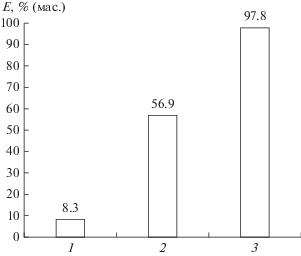
Исходя из полученных результатов, представленных на рис. 7, видно, что предложенный глубокий эвтектический растворитель в качестве экстрагента проявляет высокие селективные свойства. Так, оценка эффективности растворения оксидов металлов показала, что он потенциально может быть использован для разделения различных групп металлов в процессе выщелачивания. Однако необходимы дальнейшие исследования экстракционной возможности предложенного глубокого эвтектического растворителя на примере широкого ряда металлов.
ЗАКЛЮЧЕНИЕ
В рамках данной работы был найден и изучен эвтектический состав смеси хлорида холина и сульфосалициловой кислоты с температурой кристаллизации равной –10.5°С. Спектральными методами подтверждено наличие водородных связей в данной системе, что объясняет механизм образования глубокого эвтектического растворителя. Впервые для данного глубокого эвтектического растворителя были получены такие важные физические характеристики как плотность, вязкость и показатель преломления, измеренные в зависимости от температуры. Рассчитана молекулярная рефракция при различных температурах и соотношении акцептора и донора водородных связей. Полученные результаты по растворению оксидов металлов с использованием изученного глубокого эвтектического растворителя показали потенциальную возможность его использования в качестве селективного экстрагента.
Исследование выполнено при финансовой поддержке Российского научного фонда (проект № 20-13-00387).
ОБОЗНАЧЕНИЯ
Список литературы
Abbott A.P., Capper G., Davies D.L., Rasheed R.K., Tambyrajah V. Novel solvent properties of choline chloride/urea mixtures // Chem. Commun. 2003. V. 1. P. 70.
Zhang H., Wang Y., Zhou Y., Xu K., Li N., Wen Q., Yang Q. Aqueous biphasic systems containing PEG-based deep eutectic solvents for high-performance partitioning of RNA // Talanta. 2017. V. 170. P. 266.
Abbott A.P., Barron J.C., Ryder K.S., Wilson D. Eutectic-based ionic liquids with metal-containing anions and cations // Chem. – Eur. J. 2007. V. 13. № 22. P. 6495.
Zhang Q., De Oliveira Vigier K., Royer S., Jérôme F. Deep eutectic solvents: syntheses, properties and applications // Chem. Soc. Rev. 2012. V. 41. № 21. P. 7108.
Abranches D.O., Martins M.A., Silva L.P., Schaeffer N., Pinho S.P., Coutinho J.A. Phenolic hydrogen bond donors in the formation of non-ionic deep eutectic solvents: the quest for type V DES // Chem. Commun. 2019. V. 55. P. 10253.
New generation green solvents for separation and preconcentration of organic and inorganic species / Eds. Soylak M., Yilmaz E. Amsterdam: Elsevier, 2020.
Wang M., Tan Q., Liu L., Li J. A low-toxicity and high-efficiency deep eutectic solvent for the separation of aluminum foil and cathode materials from spent lithium-ion batteries // J. Hazard. Mater. 2019. V. 380. Article 120846.
Ijardar S.P. Deep eutectic solvents composed of tetrabutylammonium bromide and PEG: Density, speed of sound and viscosity as a function of temperature // J. Chem. Thermodyn. 2020. V. 140. Article 105897.
Hansen B.B., Spittle S., Chen B., Poe D., Zhang Y., Klein J.M., Horton A., Adhikari L., Zelovich T., Doher-ty B.W., Gurkan B., Maginn E.J., Ragauskas A., Dadmun M., Zawodzinski T.A., Baker G.A., Tuckerman M.E., Savinell R.F., Sangoro, J.R. Deep eutectic solvents: a review of fundamentals and applications // Chem. Rev. 2020 (in press).
Basaiahgari A., Panda S., Gardas R.L. Effect of ethylene, diethylene, and triethylene glycols and glycerol on the physicochemical properties and phase behavior of benzyltrimethyl and benzyltributylammonium chloride based deep eutectic solvents at 283.15−343.15 K // J. Chem. Eng. Data. 2018. V. 63. P. 2613.
Shishov A., Pochivalov A., Nugbienyo L., Andruch V., Bulatov A. Deep eutectic solvents are not only effective extractants // TrAC Trends Anal. Chem. 2020. V. 129. P. 115956.
Qin H., Hu X., Wang J., Cheng H., Chen L., Qi Z. Overview of acidic deep eutectic solvents on synthesis, properties and applications // Green Energy Environ. 2020. V. 5. P. 8.
Li J., Xiao H., Tang X., Zhou M. Green carboxylic acid-based deep eutectic solvents as solvents for extractive desulfurization // Energy Fuels. 2016. V. 30. № 7. P. 5411.
Zhao H., Baker G.A. Ionic liquids and deep eutectic solvents for biodiesel synthesis: a review // J. Chem. Technol. Biotechnol. 2012. V. 88. № 1. P. 3.
Voshkin A.A., Belova V.V., Zakhodyaeva Y.A. Iron Extraction with Di(2-Ethylhexyl)dithiophosphoric Acid and a Binary Extractant Based on It // Russ. J. Inorg. Chem. 2018. V. 63. № 3. P. 387. [Вошкин А.А., Белова В.В., Заходяева Ю.А. Экстракция железа ди(2-этилгексил)дитиофосфорной кислотой и бинарным экстрагентом на ее основе // Журн. неорг. хим. 2018. Т. 63. № 3. С. 387.]
Zakhodyaeva Y.A., Voshkin A.A., Belova V.V. Khol’kin A.I. Extraction of monocarboxylic acids by trioctylmethylammonium di(2-ethylhexyl)phosphate // Theor. Found. Chem. Eng. 2012. V. 46. P. 413. [Заходяева Ю.А., Вошкин А.А., Белова В.В, Холькин А.И. Экстракция монокарбоновых кислот ди(2-этилгексил)фосфатом триоктилметиламмония // Хим. технол. 2010. Т. 11 № 10. С. 605.]
Belova V.V., Egorova N.S., Voshkin A.A., Khol’kin A.I. Extraction of rare earth metals, uranium, and thorium from nitrate solutions by binary extractants // Theor. Found. Chem. Eng. 2015. V. 49. № 4. P. 545. [Белова В.В., Егорова Н.С., Вошкин А.А., Холькин А.И. Экстракция редкоземельных металлов, урана и тория из нитратных растворов бинарными экстрагентами // Хим. технол. 2014. Т. 15. № 2. С. 106.]
Belova V.V., Voshkin A.A., Egorova N.S., Kholkin A.I. Solvent extraction of rare earth metals from nitrate solutions with di(2,4,4-trimethylpentyl)phosphinate of methyltrioctylammonium // J. Mol. Liq. 2012. V. 172. P. 144.
Belova V.V., Voshkin A.A., Kholkin A.I., Payrtman A.K. Solvent extraction of some lanthanides from chloride and nitrate solutions by binary extractants // Hydrometallurgy. 2009. V. 97. № 3–4. P. 198.
Zakhodyaeva Y.A., Izyumova K.V., Solov’eva M.S., Voshkin A.A. Extraction separation of the components of leach liquors of batteries // Theor. Found. Chem. Eng. 2017. V. 51. № 5. P. 883. [Заходяева Ю.А., Изюмова К.В., Соловьева М.С., Вошкин А.А. Экстракционное разделение компонентов растворов выщелачивания элементов питания // Хим. технол. 2016. Т. 17. № 12. С. 569.]
Zakhodyaeva Y.A., Zinov’eva I.V., Tokar E.S., Voshkin A.A. Complex Extraction of Metals in an Aqueous Two-Phase System Based on Poly(Ethylene Oxide) 1500 and Sodium Nitrate // Molecules. 2019. V. 24 № 22. P. 4078.
Fedorova M.I., Zakhodyaeva Y.A., Zinov’eva I.V., Voshkin A.A. Recovery of rare-earth elements from nitrate solutions using polyethylene glycol 1500 // Russ. Chem. Bull. 2020. V. 69. № 7. P. 1344. [Федорова М.И., Заходяева Ю.А., Зиновьева И.В., Вошкин А.А. Извлечение легких редкоземельных элементов из нитратных растворов с использованием полиэтиленгликоля-1500 // Изв. Акад. наук. Сер. хим. 2020. № 7. С.1344.]
Zinov’eva I.V., Zakhodyaeva Y.A., Voshkin A.A. Data on the extraction of benzoic, salicylic and sulfosalicylic acids from dilute solutions using PEG-based aqueous two-phase systems // Data Brief. 2020. V. 28. Article 105033.
Zinov’eva I.V., Zakhodyaeva Y.A., Voshkin A.A. Interphase Distribution of Caffeine and Coumarin in Extraction Systems with Polyethylene Glycol and Sodium Sulfate // Theor. Found. Chem. Eng. 2019. V. 53. № 6. P. 996. [Зиновьева И.В., Заходяева Ю.А., Вошкин А.А. Межфазное распределение кофеина и кумарина в экстракционных системах с полиэтиленгликолем и сульфатом натрия // Теор. осн. хим. технол. 2019. Т. 53. № 6. С. 647.]
Voshkin A.A., Zakhodyaeva Yu.A., Zinov’eva I.V. “Green” extractants in the recovery processes of non-ferrous metal ions from technological solutions // IV Congress “Fundamental research and applied developing of recycling and utilization processes of technogenic formations”. KnE Social Sciences, 2020. P. 1.
Gilmore M., McCourt E., Connolly F., Nockemann P., Swadzba-Kwasny,M., Holbrey J.D. Hydrophobic deep eutectic solvents incorporating trioctylphosphine oxide: Advanced liquid Extractants // ACS Sustainable Chem. Eng. 2018. V. 6. № 12. P. 17323.
Shuainan N., Jia S., Hepeng Zh., Zhiyuan Z., Hailan Zh., Xiaoqi S. A cleaner strategy for comprehensive recovery of waste SmCo magnets based on deep eutectic solvents // Chem. Eng. J. 2021. Article 128602 (in press).
Rodriguez Rodriguez N., Machiels L., Onghena B., Spooren J., Binnemans, K. Selective recovery of zinc from goethite residue in the zinc industry using deep-eutectic solvents // RSC Adv. 2020. V. 10. № 12. P. 7328.
Zürner P., Frisch G. Leaching and selective extraction of indium and tin from zinc flue dust using an oxalic acid based deep eutectic solvent // ACS Sustainable Chem. Eng. 2019. V. 7. № 5. P. 5300.
Landa-Castro M., Aldana-González J., Montes de Oca-Yemha M.G., Romero-Romo M., Arce-Estrada E.M., Palomar-Pardavé M. Ni–Co alloy electrodeposition from the cathode powder of Ni-MH spent batteries leached with a deep eutectic solvent (reline) // J. Alloys Comp. 2020. V. 830. Article 154650.
Peeters N., Binnemans K., Riaño S. Solvometallurgical recovery of cobalt from lithium-ion battery cathode materials using deep-eutectic solvents // Green Chem. 2020. V. 22. P. 4210.
Chen W., Jiang J., Lan X., Zhao X., Mou H., Mu T. A strategy for dissolution and separation of rare earth oxides by novel Brønsted acidic deep eutectic solvents // Green Chem. 2019. V. 21. P. 4748.
Rodriguez Rodriguez N., Machiels L. Binnemans K. p-Toluenesulfonic Acid-based Deep-Eutectic Solvents for Solubilizing Metal Oxides // ACS Sustainable Chem. Eng. 2019. V. 7. № 4. P. 3940.
Damilano G., Laitinen A., Willberg-Keyriläinen P., Lavonen T., Häkkinen R., Dehaen W., Binnemans K., Kuutti, L. Effects of thiol substitution in deep-eutectic solvents (DESs) as solvents for metal oxides // RSC Adv. 2020. V. 10. № 39. P. 23484.
Taysun M.B., Sert E., Atalay F.S. Physical properties of benzyl tri-methyl ammonium chloride based deep eutectic solvents and employment as catalyst // J. Mol. Liq. V. 223. P. 845.
Shafie M.H., Yusof R., Gan C.-Y. Synthesis of citric acid monohydrate-choline chloride based deep eutectic solvents (DES) and characterization of their physicochemical properties // J. Mol. Liq. 2019. V. 288. Article 111081.
Florindo C., Oliveira F.S., Rebelo L.P.N., Fernandes A.M., Marrucho I.M. Insights into the Synthesis and Properties of Deep Eutectic Solvents Based on Cholinium Chloride and Carboxylic Acids // ACS Sustainable Chem. Eng. 2014. V. 2. № 10. P. 2416.
Omar K.A., Sadeghi R. Novel benzilic acid-based deep-eutectic-solvents: Preparation and physicochemical properties determination // Fluid Phase Equilib. 2020. V. 522. Article 112752.
Sánchez P.B., González B., Salgado J., José Parajó J., Domínguez Á. Physical properties of seven deep eutectic solvents based on L-proline or betaine // J. Chem. Thermodyn. 2019. V. 131. P. 517.
Basaiahgari A., Panda S., Gardas R.L. Acoustic, volumetric, transport, optical and rheological properties of Benzyltripropylammonium based Deep Eutectic Solvents // Fluid Phase Equilib. 2017. V. 448. P. 41.
Liu C., Lin J., Cao H., Zhang Y., Sun Z. Recycling of spent lithium-ion batteries in view of lithium recovery: A critical review // J. Cleaner Prod. 2019. V. 228. P. 801.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии