Теоретические основы химической технологии, 2023, T. 57, № 4, стр. 433-444
Ректификационное разделение промышленной смеси изобутилацетат–уксусная кислота–изоамилацетат
А. В. Полковниченко a, *, Т. В. Челюскина b, **
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
b МИРЭА – Российский технологический университет
(Институт тонких химических технологий имени М.В. Ломоносова)
Москва, Россия
* E-mail: anzakhlevniy@rambler.ru
** E-mail: chelyuskina@mirea.ru
Поступила в редакцию 15.05.2023
После доработки 01.06.2023
Принята к публикации 06.06.2023
- EDN: VGCJLH
- DOI: 10.31857/S0040357123040097
Аннотация
Рассмотрен процесс ректификационного разделения промышленной смеси изобутилацетат (ИБА)–уксусная кислота (УК)–изоамилацетат (ИАА), являющейся продуктом переработки многотоннажного отхода спиртовой промышленности. Предложены варианты принципиальной технологической схемы разделения (ПТСР) и определены параметры работы ректификационных колонн, обеспечивающие выделение ИАА и ИБА чистотой не менее 99.5 мол.% из промышленной смеси ИБА–УК–ИАА. ПТСР включает комплекс экстрактивной ректификации с использованием сульфолана (СФ). Проведена собственная оценка параметров бинарного взаимодействия модели NRTL-HOC для систем ИБА–УК, ИБА–ИАА, ИБА–СФ, УК–СФ. Для регрессии параметров получены новые экспериментальные данные о фазовом равновесии жидкость–пар в системах ИБА–СФ и УК–СФ при 200 мм рт. ст.
1. ВВЕДЕНИЕ
Промышленная смесь изобутилацетат (ИБА)–уксусная кислота (УК)–изоамилацетат (ИАА) является продуктом переработки многотоннажного отхода спиртовой промышленности, а именно: сивушных масел [1, 2]. Сивушные масла выступают в качестве прекурсора высокоэффективных компонентов смесевых растворителей повышенного качества с низкой себестоимостью и высоким выходом продукта [1]. Эти масла представляют собой смесь одноатомных насыщенных спиртов C3—C9, из которых главным компонентом является изоамиловый спирт [2]; в состав также входят изобутиловый спирт и изопропиловый спирт, в незначительных количествах высшие спирты, а также алифатические альдегиды, жирные кислоты и фурфурол. Целевым компонентом переработки сивушных масел выступает ИАА, в качестве дополнительного товарного продукта – ИБА. В связи с этим, практическая значимость разработки процесса разделения промышленной смеси ИБА–УК–ИАА очевидна. Компоненты смеси ИБА–УК–ИАА используются в пищевой промышленности; в виде душистых эссенций; в качестве растворителей лакокрасочных материалов, ацетил- и нитроцеллюлозы; для экстрагирования; для получения БАДов и лекарственных препаратов.
Одним из наиболее высокопроизводительных в основном органическом синтезе является процесс ректификации. Он же наиболее энергоемкий метод разделения. Синтез энергосберегающих схем разделения смесей сложной физико-химической природы требует комплексного подхода как на теоретическом, так и на прикладном уровне. Основной задачей в данном случае является снятие ограничений физико-химического характера, накладываемых на процесс ректификационного разделения бинарных и многокомпонентных смесей, в том числе биазеотропных [3]. Указанные ограничения можно преодолеть несколькими методами, включая методы азеотропной и экстрактивной ректификации [4–12]. Другой подход базируется на направленном изменении технологических параметров процесса (приводящем к преобразованию структур диаграмм фазового равновесия) c целью coздания наибoлее благoприятных уcлoвий ректификационного разделения.
Экспериментальное исследование процесса ректификации ввиду большого количества рабочих параметров – довольно продолжительная и дорогостоящая процедура. В свою очередь, моделирование с использованием современных программных комплексов позволяет прогнозировать данные и оптимизировать рабочие параметры процесса [13]. При этом, необходимым этапом является получение данных о фазовых равновесиях и построение адекватных математических моделей.
Целью настоящей работы является расчет процесса ректификационного разделения промышленной смеси ИБА–УК–ИАА на чистые компоненты и определение рабочих параметров ректификационных колонн, обеспечивающих получение целевых продуктов требуемого качества с наименьшими энергетическими затратами.
2. МАТЕРИАЛЫ И МЕТОДЫ
Расчет процесса ректификационного разделения смеси ИБА–УК–ИАА проводили в программном комплексе Aspen Plus®. Процесс разделения был ориентирован на достижение чистоты целевых продуктов – ИАА и ИБА – не менее 99.5 мол %. Для расчета и подбора режима работы ректификационных и экстрактивных колонн использовали модуль Sensitivity. Варьировали высоту колонны (Nтт), уровень подачи потока питания (NF) и разделяющего агента (NРА), флегмовое число (R). Физикохимические свойства чистых компонентов представлены в табл. 1.
При моделировании парожидкостного равновесия (ПЖР) изучаемых систем давление насыщенных паров рассчитывали по расширенному уравнению Антуана:
(1)
$\begin{array}{*{20}{c}} {\ln {{p}_{i}} = {{C}_{{1i}}} + \frac{{{{C}_{{2i}}}}}{{T + {{C}_{{3i}}}}} + {{C}_{{4i}}}T + {{C}_{{5i}}}\ln T + {{C}_{{6i}}}{{T}^{{{{C}_{{7i}}}}}},} \end{array}$Таблица 2.
Коэффициенты расширенного уравнения Антуанаa
| i | С1i | C2i | C3i | С4i | С5i | С6i | С7i |
|---|---|---|---|---|---|---|---|
| ИБА | 67.4172 | –6944.3 | 0 | 0 | –7.298 | 3.7892 × 10–6 | 2 |
| УК | 48.3772 | –6304.5 | 0 | 0 | –4.2985 | 8.8865 × 10–18 | 6 |
| ИАА | 94.6652 | –8876.8 | 0 | 0 | –11.075 | 2.4723 × 10–17 | 6 |
| СФ | 145.767 | –13283.0 | 0 | 0 | –19.429 | 0.013441 | 1 |
Для описания отклонения от идеального поведения жидкой фазы в системе ИБА-УК-ИАА использовали уравнение Non-Random Two-Liquid (NRTL) [14], рекомендованное авторами [15, 16] для биазеотропных систем. В программном комплексе Aspen Plus® уравнение NRTL приведено в следующем виде:
(2)
$\begin{array}{*{20}{c}} \begin{gathered} \ln {{\gamma }_{i}} = \frac{{\sum\limits_j {{{x}_{j}}{{\tau }_{{ji}}}{{G}_{{ji}}}} }}{{\sum\limits_k {{{x}_{k}}{{G}_{{ki}}}} }} + \\ + \,\,\sum\limits_j {\frac{{{{x}_{j}}{{G}_{{ij}}}}}{{\sum\limits_k {{{x}_{k}}{{G}_{{kj}}}} }}} \left( {{{\tau }_{{ij}}} - \frac{{\sum\limits_m {{{x}_{m}}{{\tau }_{{mj}}}{{G}_{{mj}}}} }}{{\sum\limits_k {{{x}_{k}}{{G}_{{kj}}}} }}} \right), \\ \end{gathered} \end{array}$Система ИБА–УК–ИАА включает бинарную составляющую ИБА–УК, которая при атмосферном давлении характеризуется наличием двух азеотропов, а при пониженном давлении – значениями коэффициента относительной летучести компонентов близкими к единице. Разделение азеотропных смесей или смесей с близкой летучестью компонентов с применением только последовательно соединенных колонн невозможно в силу физико-химических ограничений [4, 18]. Здесь необходимо применение специальных методов разделения [4, 11, 12]. В настоящей работе для разделения бинарной составляющей ИБА–УК предложен процесс экстрактивной ректификации, который является наиболее эффективным способом разделения смесей сложной физико-химической природы [16, 19–21], характеризуется существенно меньшими энергетическими затратами по сравнению с азеотропной ректификацией и разделением, основанным на варьировании давления [22, 23].
Одним из основных факторов, влияющих на качество выделяемых в процессе экстрактивной ректификации продуктов, является подбор эффективного разделяющего агента (РА). Список легкокипящих и тяжелокипящих разделяющих агентов сформирован в работе [15] на основании данных работ [24–26]. В качестве потенциального РА в настоящей работе рассмотрен сульфолан (СФ). Использованию СФ в качестве тяжелокипящего экстрактивного агента посвящена серия работ [27–30]. Этот РА зарекомендовал себя как весьма эффективный [31].
Для оценки параметров бинарного взаимодействия уравнения NRTL были получены собственные экспериментальные данные о ПЖР в бинарных системах ИБА–СФ и УК–СФ. Согласно информации, приведенной в работе [31], сульфолан разлагается при температуре выше 230°С. В связи с этим эксперимент проводили при пониженном давлении (200 мм рт. ст.). Чистота реактивов, используемых в настоящей работе, приведена в табл. 3.
Таблица 3.
Сведения об используемых веществах
| Вещество | Артикул | Производитель | Чистота ГХa (масс. д.) |
Содержание воды КФb (масс. д.) |
|---|---|---|---|---|
| ИБА | CAS-No 110-19-0 | GmBh | >0.990 | ≤0.0005 |
| УК | ГОСТ 61-75(х. ч.) | ООО “Русский Химик” | >0.998 | <0.0002 |
| СФ | CAS-No 126-33-0 | Merck KGaA | >0.990 | <0.0020 |
Экспериментальные данные о ПЖР в исследуемых системах были получены по методике, подробно описанной в работе [32], на эбулиометре Свентославского, снабженном насосом Коттреля (рис. 1).
Рис. 1.
Модифицированный эбулиометр Свентославского. 1 – кипятильник; 2 – трубка Коттреля; 3 – гильза термометра; 4 – обратный холодильник; 5 – счетчик капель; 6 – сборник пробы парового конденсата; 7–8 – вентили для отбора проб парового конденсата и жидкости; 9 – обмотка электрообогрева.
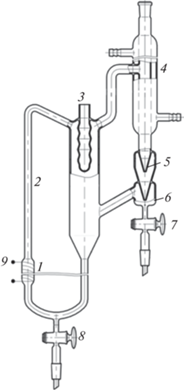
Контроль давления осуществляли с помощью вакууметра “VACUU⋅VIE extended” с точностью ±2 мм рт. ст. Равновесную температуру измеряли ртутным термометром TL-4 0…50–105, 0…100–155 и 0…150–205 с точностью ±0.1°С. Масса навесок измерялась на аналитических весах Mass Comparator MC-1000 с точностью ±0.0005 г. Пробы анализировали рефрактометрическим методом на приборе ИРФ-454 Б2М при 30°С, диапазон показателей преломления $n_{D}^{{30}}$ от 1.2 до 1.7 с точностью измерения 1 × 10–4. Значение температуры при измерении показателя преломления обусловлено температурой плавления сульфолана Тп = 27.4°С [31].
3. РАСЧЕТНО-ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Оценка параметров бинарного взаимодействия модели NRTL-HOC
Для расчета принципиальной технологической схемы разделения (ПТСР) необходимы параметры бинарного взаимодействия модели NRTL-HOC для бинарных составляющих смесей, образованных разделяемыми компонентами, в том числе с разделяющим агентом.
Исследованию ПЖР в системе ИБА–УК посвящен ряд экспериментальных [33–35] и расчетных работ [36–38]. Система является биазеотропной при атмосферном давлении, а при пониженном давлении характеризуется близкими температурами кипения и малой разницей между составами равновесных фаз. В технологически приемлемом диапазоне давлений система претерпевает изменения, включающие стадию образования внутреннего тангенциального азеотропа [4, 39], который является элементом эволюции биазеотропии при изменении давления (температуры).
В настоящей работе проведена собственная оценка параметров бинарного взаимодействия модели NRTL-HOC для моделирования ПЖР в системе ИБА-УК при двух значениях давления. Для 200 мм рт. ст. оценка параметров проведена по набору экспериментальных данных о ПЖР при 80°С (полный массив данных) [34]. Для 760 мм рт. ст. оценка параметров проведена одновременно по 3 наборам экспериментальных данных [34]: по экспериментальным данным о ПЖР при 117°С (полный массив данных); по характеристикам азеотропов и чистых компонентов; по характеристикам азеотропов.
Для бинарной составляющей ИБА–ИАА параметры бинарного взаимодействия оценены из экспериментальных данных работы [40]. Для бинарной составляющей УК–ИАА параметры бинарного взаимодействия взяты из работы [41].
Экспериментальные данные о ПЖР для систем ИБА–СФ и УК–СФ в литературе отсутствуют. В работе [38] оценку параметров бинарного взаимодействия модели NRTL-HOC проводили одновременно по двум наборам данных о ПЖР при 200 и 760 мм рт. ст., полученных с использованием модели UNIFAC-HOC. Расчет ПЖР показал, что системы зеотропны в указанном диапазоне давлений. Так как критерием адекватности математических моделей служит их корреляция с экспериментом, в настоящей работе для оценки параметров бинарного взаимодействия модели NRTL-HOC были получены собственные экспериментальные данные о ПЖР в системах ИБА–СФ и УК–СФ.
Параметры бинарного взаимодействия модели NRTL-HOC, используемые в настоящей работе для расчета ПЖР, представлены в табл. 4. Там же представлены данные о среднеквадратичном отклонении между моделью и экспериментальными данными.
Таблица 4.
Параметры бинарного взаимодействия модели NRTL-HOC
| Диапазон P, мм рт. ст. |
760 | 200 | 200–760 | 200–760 | 200–760 | 200–760 |
| Компонент i | ИБА | ИБА | УК | ИБА | ИБА | УК |
| Компонент j | УК | УК | ИАА | ИАА | СФ | СФ |
| Источник | Оценка из эксп. [34] | Оценка из эксп. [34] | Взято из работы [41] | Оценка из эксп. [40] | Оценка из эксп. табл. 5 | Оценка из эксп. табл. 6 |
| T | °C | °C | °C | °C | °C | °C |
| $а$ij | 0 | 0 | –0.6992 | 0 | –5.6085 | –4.72697 |
| $а$ji | 0 | 0 | 0.0741 | 0 | 2.12732 | –1.20441 |
| bij | 138.908 | 367.921 | 74.071 | 522.666 | 2385.46 | 1956.9 |
| bji | 85.2141 | –105.598 | 440.982 | –356.456 | –500.047 | –515.036 |
| cij | 0.3 | 0.3 | 0.3 | 0.3 | 0.3 | 0.3 |
| eij | 0 | 0 | 0 | 0 | 0 | 0.394509 |
| eji | 0 | 0 | 0 | 0 | 0 | 0.181541 |
| RMSD (T/P) | 0.7 кПа | 0.1 кПа | – | 0.2°C | 0.4°C | 2.8°C |
| RMSD (y), мол. д. | 0.0041 | 0.0059 | – | 0.0126 | 0.0019 | 0.0121 |
Из данных табл. 4 следует, что модели удовлетворительно описывают экспериментальные данные.
Определение парожидкостного равновесия в системах ИБА–СФ и УК–СФ
Для определения составов парового конденсата (yi) и жидкой фазы (xi) для систем ИБА-СФ и УК-СФ были построены зависимости показателя преломления $n_{D}^{{30}}$ от состава xi (рис. 2).
Рис. 2.
Зависимость показателя преломления от состава $n_{D}^{{30}} = f\left( {{{x}_{1}}} \right)$ для системы: (а) ИБА (1)–СФ (2); (б) УК (1)–СФ (2).
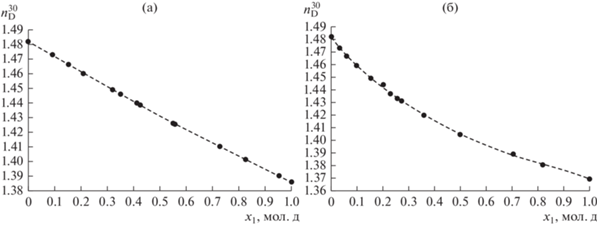
Экспериментальные данные по фазовому равновесию жидкость–пар в бинарных системах ИБА–СФ и УК–СФ приведены в табл. 5 и табл. 6, соответственно.
Таблица 5.
Данные о ПЖР в системе ИБА (1)–СФ (2) при 200 мм рт. ст.
| x1, мол. д. | Эксперимент | NRTL-HOC | ||
|---|---|---|---|---|
| T, °C | y1, мол. д. | T, °C | y1, мол. д. | |
| 0.0921 | 118.3 | 0.9901 | 118.2 | 0.9858 |
| 0.1611 | 102.6 | 0.9948 | 101.7 | 0.9944 |
| 0.2321 | 93.7 | 0.9995 | 94.2 | 0.9965 |
| 0.2476 | 92.4 | 0.9984 | 93.1 | 0.9968 |
| 0.3051 | 90.2 | 0.9995 | 90.0 | 0.9974 |
| 0.3475 | 88.6 | 0.9995 | 88.4 | 0.9977 |
| 0.3545 | 88.4 | 0.9953 | 88.1 | 0.9977 |
| 0.3754 | 87.6 | 0.9995 | 87.5 | 0.9979 |
| 0.5007 | 85.1 | 0.9997 | 85.0 | 0.9983 |
| 0.5937 | 83.7 | 0.9995 | 83.7 | 0.9985 |
| 0.6077 | 83.3 | 0.9997 | 83.5 | 0.9985 |
| 0.7079 | 82.1 | 0.9998 | 82.3 | 0.9987 |
| 0.8160 | 80.4 | 0.9999 | 80.8 | 0.9990 |
| 0.9291 | 78.1 | 0.9999 | 78.8 | 0.9995 |
Таблица 6.
Данные о ПЖР в системе УК (1)–СФ (2) при 200 мм рт. ст.
| x1, мол. д. | Эксперимент | NRTL-HOC | ||
|---|---|---|---|---|
| T, °C | y1, мол. д. | T, °C | y1, мол. д. | |
| 0.0490 | 197.7 | 0.7236 | 193.9 | 0.6917 |
| 0.1317 | 164.5 | 0.9095 | 163.2 | 0.9116 |
| 0.2276 | 138.5 | 0.9616 | 142.5 | 0.9694 |
| 0.3737 | 119.5 | 0.9764 | 121.2 | 0.9921 |
| 0.4611 | 110.0 | 0.9876 | 111.5 | 0.9962 |
| 0.5675 | 99.5 | 0.9932 | 101.6 | 0.9984 |
| 0.6694 | 92.8 | 0.9962 | 94.0 | 0.9993 |
| 0.7827 | 85.0 | 0.9966 | 87.6 | 0.9997 |
| 0.8909 | 80.1 | 0.9962 | 83.3 | 0.9999 |
| 0.9430 | 77.5 | 0.9967 | 81.5 | 0.9999 |
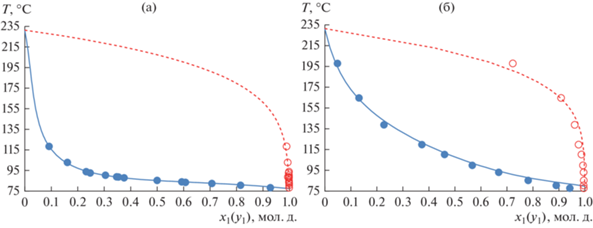
Корреляция экспериментальных данных о ПЖР в системах ИБА–СФ (табл. 5) и УК–СФ (табл. 6) с данными, рассчитанными по модели NRTL-HOC (табл. 5, табл. 6), представлена на рис. 3.
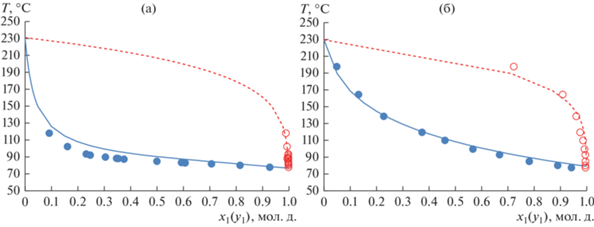
Здесь следует отметить, что в случае отсутствия эксперимента для оценки параметров бинарного взаимодействия уравнений локальных составов допустимо использование данных, полученных по модели UNIFAC [16]. В этом случае использование групповой модели UNIFAC обосновано обширной базой данных о взаимодействии между функциональными группами рассматриваемых классов соединений [42]. Так, например, с использованием математического моделирования по уравнению UNIFAC-HOC впервые была получена информация о ПЖР и о наличии биазеотропии в системе ИБА–УК [33], а авторами работы [38] модель UNIFAC-HOC была использована для прогнозирования ПЖР в системах ИБА–СФ и УК–СФ. На рис. 4 приведены экспериментальные и рассчитанные данные о ПЖР в системах ИБА–СФ (табл. 5) и УК–СФ (табл. 6).
Из рис. 4 видно, что результаты натурного и вычислительного экспериментов согласованы. Таким образом, на основании проведенного исследования проиллюстрирована возможность применения моделей группового взаимодействия для прогнозирования термодинамических свойств и фазового равновесия некоторых полярных смесей с участием сульфолана.
Ректификация смеси ИБА–УК–ИАА
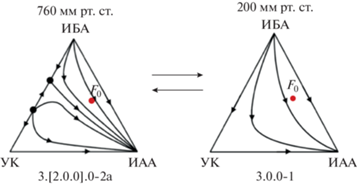
Структуры диаграмм фазового равновесия (СДФР) системы ИБА–УК–ИАА при значениях давления 760 мм рт. ст. (класс 3.[2.0.0].0-2а [38, 43]), когда система биазеотропна, и при 200 мм рт. ст. (класс 3.0.0-1 [44]), когда система зеотропна, представлены на рис. 5; отмечен состав потока питания F0, который приближен к промышленному (xИБА = 0.45; xУК = 0.10; xИАА = 0.45 мол. д. [2, 45]). При указанных значениях давления в системе отсутствуют тройные азеотропы. Результаты расчета ректификационной колонны при 760 и 200 мм рт. ст. (составы потоков (x); величины потоков питания (F0), кубового продукта (W), дистиллята (D); нагрузка на кипятильник (Qreb)) представлены в табл. 7.
Таблица 7.
Параметры работы ректификационной колонны смеси ИБА–УК–ИАА. Нумерация тарелок ведется с верха колонны.
| P, мм рт. ст. |
Nтт | NF | R | F0, кмоль/ч |
D, кмоль/ч |
W, кмоль/ч |
xF, мол. д. |
xD, мол. д. |
xW, мол. д. |
Qreb, кВт |
|
|---|---|---|---|---|---|---|---|---|---|---|---|
| 760 | TF= 126.89°C; TD = 117.49°C; TW = 141.65°C | ||||||||||
| 30 | 13 | 3.23 | 100 | 55 | 45 | ИБА | 0.45 | 0.8176 | 0.0007 | 2304.1 | |
| УК | 0.10 | 0.1783 | 0.0043 | ||||||||
| ИАА | 0.45 | 0.0041 | 0.9950 | ||||||||
| 200 | TF = 85.90°C; TD = 78.03°C; TW = 98.28°C | ||||||||||
| 30 | 12 | 2.62 | 100 | 55 | 45 | ИБА | 0.45 | 0.8179 | 0.0003 | 2072.6 | |
| УК | 0.10 | 0.1780 | 0.0047 | ||||||||
| ИАА | 0.45 | 0.0041 | 0.9950 | ||||||||
Из приведенных в табл. 7 данных следует, что требуемая чистота ИАА в кубе колонны достигнута. Сравнение затрат энергии на кипятильник ректификационных колонн показывает, что при пониженном давлении экономия составляет 10%.
Отметим, что в ходе процесса разделения в потоке дистиллята выделяется смесь ИБА и УК, имеющая промышленное значение. Помимо процессов этерификации, она встречается в технологии обезвоживания органических кислот [46, 47]. Целевым компонентом здесь выступает ИБА.
Анализ концентрационного симплекса трехкомпонентной системы ИБА–УК–СФ
С использованием оцененных параметров бинарного взаимодействия модели NRTL-HOC (табл. 4) проведено математическое моделирование ПЖР производной трехкомпонентной системы ИБА-УК-СФ и рассчитаны коэффициенты относительной летучести компонентов смеси ИБА–УК в присутствии СФ $\left( {\alpha _{{{\text{ИБА/УК}}}}^{{{\text{СФ}}}} = \frac{{{{y}_{{{\text{ИБА}}}}}{{x}_{{{\text{УК}}}}}}}{{{{x}_{{{\text{ИБА}}}}}{{y}_{{{\text{УК}}}}}}}} \right)$ при различных давлениях (рис. 6).
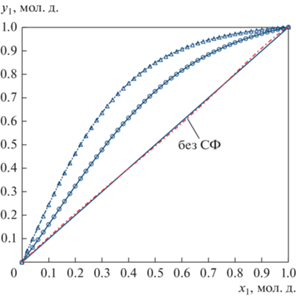
Рис. 6.
Ход линий постоянных значений коэффициента относительной летучести компонентов смеси ИБА–УК в присутствии СФ ($\alpha _{{{\text{ИБА/УК}}}}^{{{\text{СФ}}}}$) при различных давления: (а) – 760 мм рт. ст.; (б) – 200 мм рт. ст.
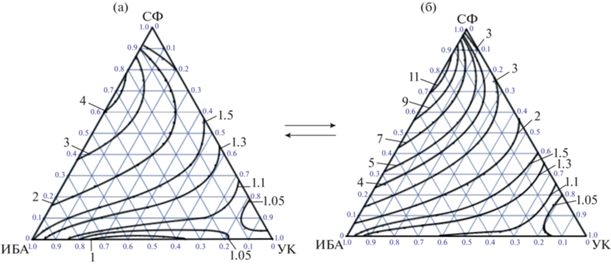
Из полученных результатов следует, что СФ увеличивает летучесть ИБА относительно УК (рис. 6), причем этот эффект проявляется в большей степени при 200 мм рт. ст., чем при атмосферном давлении. В качестве исходного состава взяты данные по потоку дистиллята из расчета на предыдущем этапе (табл. 7). На основании данных о величине коэффициента относительной летучести компонентов разделяемой смеси в присутствии сульфолана выбрано соотношение количеств РА и исходного питания – 2 : 1, которому отвечает максимальное значение $\alpha _{{{\text{ИБА/УК}}}}^{{{\text{СФ}}}}$. Преобразование фазовой диаграммы псевдобинарной системы ИБА–УК в присутствии сульфолана при атмосферном и пониженном давлении приведено на рис. 7.
Моделирование процесса экстрактивной ректификации смеси ИБА–УК
Принципиальная схема ЭР смеси ИБА–УК приведена на рис. 8. Были рассмотрены два варианта организации работы комплекса: 1 – когда колонна ЭР работает при атмосферном давлении; 2 – когда колонна ЭР работает при пониженном давлении 200 мм рт. ст. Отметим, что при атмосферном давлении при кипении чистый СФ разлагается, поэтому колонна регенерации РА в обоих комплексах работает при пониженном давлении 200 мм рт. ст.
Процесс разделения смеси ИБА–УК был ориентирован на достижение чистоты целевого компонента – ИБА – не менее 99.5 мол. %. В качестве исходного состава взяты данные по потоку дистиллята из расчета на предыдущем этапе (табл. 7). Результаты расчета комплекса ЭР представлены в табл. 8 и табл. 9.
Таблица 8.
Параметры работы комплекса экстрактивной ректификации смеси ИБА–УК с применением СФ в качестве РА (давление в колонне ЭР 760 мм рт. ст.)
| № колонны |
P, мм рт. ст. |
Nтт | NF | NСФ | R | F0, кмоль/ч |
СФ, кмоль/ч |
D, кмоль/ч |
W, кмоль/ч |
xF, мол. д. |
xD, мол. д. |
xW, мол. д. |
Qreb, кВт |
|
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 760 | TF = 117.49°C; TСФ = 115.00°C; TD = 116.53°C; TW = 232.48°C | ||||||||||||
| 30 | 17 | 4 | 0.5 | 55 | 110 | 45 | 120 | ИБА | 0.8176 | 0.9964 | 0.0011 | 1529.0 | ||
| УК | 0.1783 | 0.0025 | 0.0808 | |||||||||||
| ИАА | 0.0041 | 0.0011 | 0.0014 | |||||||||||
| СФ | 0 | 0 | 0.9167 | |||||||||||
| 2 | 200 | TF= 150°C; TD = 79.70°C; TW = 229.25°C | ||||||||||||
| 10 | 5 | – | 1.25 | 120 | 110 | 9.8 | 110.2 | ИБА | 0.0011 | 0.0139 | 0 | 678.4 | ||
| УК | 0.0808 | 0.9684 | 0.0018 | |||||||||||
| ИАА | 0.0014 | 0.0177 | 0 | |||||||||||
| СФ | 0.9167 | 0 | 0.9982 | |||||||||||
Таблица 9.
Параметры работы комплекса экстрактивной ректификации смеси ИБА–УК с применением СФ в качестве РА (давление в колонне ЭР 200 мм рт. ст.)
| № колонны |
P, мм рт. ст. |
Nтт | NF | NСФ | R | F0, кмоль/ч |
СФ, кмоль/ч |
D, кмоль/ч |
W, кмоль/ч |
xF, мол. д. |
xD, мол. д. |
xW, мол. д. |
Qreb, кВт | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 200 | TF = 78.03°C; TСФ = 75°C; TD = 77.14°C; TW = 177.72°C | ||||||||||||
| 20 | 15 | 4 | 0.2 | 55 | 110 | 45 | 120 | ИБА | 0.8179 | 0.9969 | 0.0010 | 1279.9 | ||
| УК | 0.1780 | 0.0001 | 0.0815 | |||||||||||
| ИАА | 0.0041 | 0.0030 | 0.0008 | |||||||||||
| СФ | 0 | 0 | 0.9167 | |||||||||||
| 2 | 200 | TF = 177.72°C; TD = 79.57°C; TW = 229.24°C | ||||||||||||
| 10 | 5 | – | 1.67 | 120 | 110 | 9.8 | 110.2 | ИБА | 0.0010 | 0.0128 | 0 | 505.2 | ||
| УК | 0.0815 | 0.9778 | 0.0018 | |||||||||||
| ИАА | 0.0008 | 0.0094 | 0 | |||||||||||
| СФ | 0.9167 | 0 | 0.9982 | |||||||||||
Из приведенных в табл. 8 и табл. 9 данных следует, что в обоих случаях удалось достичь требуемой чистоты ИБА в дистилляте колонны ЭР. В колонне регенерации РА в виде дистиллята получена уксусная кислота 2-го сорта, в виде кубового потока получен СФ чистотой выше 99.8 мол. %, что позволяет избежать накопления компонентов разделяемой смеси в схеме. Сравнивая затраты энергии на кипятильники колонн, установили, что при пониженном давлении (∑Qreb = 1785.1 кВт) разделение смеси энергетически более выгодно, чем при атмосферном давлении (∑Qreb = 2207.4 кВт); экономия составляет около 19%. Таким образом, процесс экстрактивной ректификации смеси ИБА–УК, энергетически более выгодно проводить при пониженном давлении.
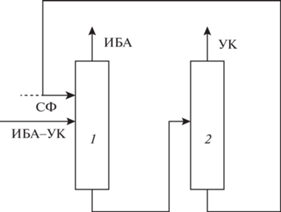
Принципиальная технологическая схема разделения смеси ИБА–УК–ИАА на чистые компоненты
ПТСР промышленной смеси ИБА–УК–ИАА на чистые компоненты приведена на рис. 9. Сравнение затрат энергии на работу кипятильников ректификационных колонн приведено в табл. 10.
Рис. 9.
ПТСР смеси ИБА–УК–ИАА на чистые компоненты, включающая комплекс ЭР. 1 – ректификационная колонна; 2 – колонна ЭР; 3 – колонна регенерации РА.
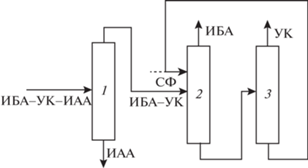
Таблица 10.
Затраты энергии на кипятильники ректификационных колонн
| № колонны на рис. 9 | 1 | 2 | 3 | ∑Q, кВт | ∆абс, кВт | % | |
|---|---|---|---|---|---|---|---|
| Вариант 1 | P, мм рт. ст. | 760 | 760 | 200 | 4511.5 | 653.8 | 14.5 |
| Qreb, кВт | 2304.1 | 1529.0 | 678.4 | ||||
| Вариант 2 | P, мм рт. ст. | 200 | 200 | 200 | 3857.7 | ||
| Qreb, кВт | 2072.6 | 1279.9 | 505.2 | ||||
Данные табл. 10 показывают, что понижение давления во всех ректификационных колоннах (вариант 2) позволило снизить общие энергозатраты на 14.5% по сравнению со схемой, работающей при 760 мм рт. ст. (вариант 1).
4. ЗАКЛЮЧЕНИЕ
Рассмотрен процесс ректификационного разделения промышленной смеси ИБА–УК–ИАА, являющейся продуктом переработки многотоннажного отхода спиртовой промышленности. Система включает бинарную составляющую ИБА–УК, также имеющую промышленное значение. Помимо процессов этерификации, она встречается в технологии обезвоживания органических кислот. Разделение смеси ИБА–УК обычной ректификацией практически невозможно и требует применения специальных методов. Для разделения этой смеси предложен процесс экстрактивной ректификации с использованием СФ.
Для расчета ПТСР проведена собственная оценка параметров модели NRTL-HOC для систем ИБА–УК, ИБА–ИАА, ИБА–СФ, УК–СФ. В работе получены новые экспериментальные данные о ПЖР в системах ИБА–СФ и УК–СФ при 200 мм рт. ст. Данные натурного эксперимента хорошо согласуются с полученными по модели UNIFAC-HOC. Сравнение результатов моделирования ПЖР в системах ИБА–СФ и УК–СФ при 200 мм рт. ст. по модели UNIFAC-HOC с данными натурного эксперимента иллюстрирует возможность применения моделей группового взаимодействия для прогнозирования термодинамических свойств и фазового равновесия некоторых полярных смесей с участием СФ.
В работе предложены варианты ПТСР и определены параметры работы ректификационных колонн, обеспечивающие выделение ИАА и ИБА чистотой более 99.5 мол. % из промышленной смеси ИБА–УК–ИАА. Проведение ректификационного разделения при пониженном давлении позволило снизить энергозатраты на выделение ИАА на 10%, ИБА на 19%, на полное разделение смеси ИБА–УК–ИАА на 14.5%.
Совокупность полученных результатов обладает прогностическими возможностями и вносит вклад в теоретические основы процессов ректификационного разделения смесей сложной физико-химической природы.
Экспериментальная часть работы выполнена при финансовой поддержке Минобрнауки России в рамках государственного задания ИОНХ РАН.
ОБОЗНАЧЕНИЯ
| ${{а}_{{ij}}}$,${{b}_{{ij}}}$,${{c}_{{ij}}}$,${{d}_{{ij}}}$,${{e}_{{ij}}}$,${{f}_{{ij}}}$ | коэффициенты бинарного взаимодействия уравнения NRTL |
| C1i–С7i | коэффициенты уравнения Антуана |
| D | дистиллят, кмоль |
| F | поток питания, кмоль |
| M | молекулярная масса, г/моль |
| NРА | номер тарелки подачи разделяющего агента |
| Nтт | число теоретических ступеней разделения |
| NF | номер тарелки подачи потока питания |
| nD | показатель преломления |
| Р | давление, мм рт. ст. (кПа) |
| pi | парциальное давление чистого компонента, мм рт. ст. |
| Q | энергетические затраты, кВт |
| R | флегмовое число |
| RMSD | среднеквадратичное отклонение |
| Т | температура, °С (К) |
| W | кубовый поток |
| x | состав потока, мол. д. |
| xi | концентрация компонента в жидкой фазе, мол. д. |
| yi | концентрация компонента в паровой фазе, мол. д. |
| α | коэффициент относительной летучести |
| γi | коэффициент активности |
| ∆ | изменение |
ИНДЕКСЫ
Список литературы
Пантелеев Е.В., Пантелеев П.Е., Пантелеева Г.В. Способ переработки сивушного масла. 2011. Патент № 2471769
Patidar P., Mahajani S.M. Esterification of Fusel Oil Using Reactive Distillation. Part II: Process Alternatives // Ind. Eng. Chem. Res. 2013. V. 52. P. 16637–16647
Комарова Л.В., Серафимов Л.А., Гарбер Ю.Н. Классификация диаграмм трехкомпонентных смесей, включающих биазеотропные составляющие // Журн. физической химии. 1974. Т. 48. С. 1391
Жаров В.Т., Серафимов Л.А. Физико-химические основы дистилляции и ректификации. Химия, Л. 1975
Gorak A., Schoenmakers H. Distillation: Operation and Applications, 1st ed. Elsevier, Amsterdam. 2014
Коган В.Б. Азеотропная и экстрактивная ректификация. Изд. 2-е, перераб. и доп. Химия, Л. 1971
Seader J.D., Henley E.J. Separation process principles. Wiley, New York. 1998
Doherty M.F., Malone M.F. Conceptual Design of Distillation Systems. McGraw-Hill, New York. 2001
Lei Z., Li C., Chen B. Extractive Distillation: A Review // Separation & Purification Reviews. 2003. V. 32. P. 121–213. https://doi.org/10.1081/SPM-120026627
Wankat P.C. Equilibrium Staged Separations. Prentice Hall, Englewood Cliffs, NJ. 1984
Фролкова А.К. Разделение азеотропных смесей. Физико-химические основы и технологические приемы. Гуманитар. изд. центр “Владос”, М. 2010
Тимофеев В.С., Серафимов Л.А., Тимошенко А.В. Принципы технологии основного органического и нефтехимического синтеза // Учебное пособие для вузов. Изд. 3-е, перераб. и доп. М.: Высшая школа, 2010. 407 с.
Muñoz R., Montón J.B., Burguet M.C., de la Torre J. Separation of isobutyl alcohol and isobutyl acetate by extractive distillation and pressure-swing distillation: Simulation and optimization // Sep. Purif. Technol. 2006. V. 50. P. 175–183. https://doi.org/10.1016/j.seppur.2005.11.022
Renon H., Prausnitz J.M. Local compositions in thermodynamic excess functions for liquid mixtures // AIChE J. 1968. V. 14. P. 135–144. https://doi.org/https://doi.org/10.1002/aic.690140124
Митюшкина И.А. Разделение бинарных биазеотропных смесей с использованием дополнительных веществ различной летучести / Дисс. … канд. техн. наук. МИТХТ, М. 2011
Челюскина Т.В. Теоретические основы ректификационного разделения биазеотропных смесей / Дисс. … докт. техн. наук. МИТХТ, М. 2011
Hayden J.G., O’Connell J.P. A generalized method for predicting secod virial coefficients // Industrial & Engineering Chemistry Process Design and Development. 1975. V. 14. P. 209
Серафимов Л.А. Теоретические принципы построения технологических смех ректификации неидеальных многокомпонентных смесей / Дисс. … докт. техн. наук. МИТХТ, М. 1968
Шутова Г.В. Физико-химические закономерности биазеотропии в бинарных системах / Дисс. … канд. хим. наук. МИТХТ, М. 1992
Серафимов Л.А., Фролкова А.К., Челюскина Т.В. Подбор экстрактивных агентов при разделении биазеотропных бинарных смесей экстрактивной ректификацией // Теоретические основы химической технологии. 2009. Т. 43. С. 648
Мягкова Т.О. Физико-химические основы разделения биазеотропных смесей / Дисс. … канд. техн. наук. МИТХТ, М. 2007
Meirelles A., Weiss S., Herfurth H. Ethanol dehydration by extractive distillation // Journal of Chemical Technology & Biotechnology. 1992. V. 53. P. 181
Клаузнер П.С., Рудаков Д.Г., Анохина Е.А., Тимошенко А.В. Применение комплекса с частично связанными тепловыми и материальными потоками и тепловых насосов в экстрактивной ректификации смеси аллило- вый спирт – аллилацетат с н-бутилпропионатом // Химия и технология органических веществ. 2020. № 4 (16). C. 42–56.
Павлов С.Ю. Выделение и очистка мономеров для синтетического каучука. Химия, Л. 1987
Зарецкий М.И. Комплексообразование бензола и галогенбензолов с органическими растворителями // Российский химический журн. 1998. Т. XLII. С. 9
Биттрих Г.Й., Гайле А.А., Лемпе Д., Проскуряков В.А., Семенов Л.В. Разделение углеводородов с использованием селективных растворителей. Химия, Л. 1987
Челюскина Т.В., Бедретдинов Ф.Н. Математическое моделирование экстрактивной ректификации смеси бутилбутират – масляная кислота // Теоретические основы химической технологии. 2016. Т. 50. С. 516
Бедретдинов Ф.Н., Челюскина Т.В. Исследование различных изомногообразий в четырехкомпонентных системах, содержащих биазеотропные бинарные составляющие // Тонкие химические технологии. 2018. Т. 13. № 1. C. 45–53.
Раева В.М., Громова О.В. Разделение смеси вода – муравьиная кислота – уксусная кислота в присутствии сульфолана // Тонкие химические технологии. 2019. Т. 14. № 4. C. 24–32.
Bedretdinov F., Chelyuskina T., Frolkova A. Modeling of vapor-liquid equilibrium and extractive rectifiction of butyl-propionate-propionic acid mixture // In: 10th International Conference on Distillation and Absorption. Germany. 2014. P. 928.
Гайле А.А., Сомов В.Е. Сульфолан. Получение и применение в качестве селективного растворителя. 2-е изд., испр. и доп. ХИМИЗДАТ, СПб. 2014
Иванов И.В., Лотхов В.А., Глебова Ю.А., Челюскина Т.В., Кулов Н.Н. Исследование фазового равновесия в системе бензол–гептан–N-метилпирролидон // Теоретические основы химической технологии. 2014. Т. 48. С. 363.
Christensen S.P., Olson J.D. Phase equilibria and multiple azeotropy of the acetic acid-isobutyl acetate system // Fluid Phase Equilib. 1992. V. 79. P. 187–199. https://doi.org/10.1016/0378-3812(92)85129-V
Burguet M.C., Montón J.B., Muñoz R., Wisniak J., Segura H. Polyazeotropy in Associating Systems: The 2-Methylpropyl Ethanoate + Ethanoic Acid System // J. Chem. Eng. Data. 1996. V. 41. p. 1191–1195. https://doi.org/10.1021/je960159k
Zhang C., Wan H., Xue L., Guan G. Investigation on isobaric vapor liquid equilibrium for acetic acid + water + (n-propyl acetate or iso-butyl acetate) // Fluid Phase Equilib. 2011. V. 305. P. 68–75. https://doi.org/10.1016/j.fluid.2011.03.006
Челюскина Т.В., Митюшкина И.А., Чернышова М.А., Фролкова А.К. Математическое моделирование эволюции биазеотропии в системе изобутилацетат – уксусная кислота // Вестник МИТХТ. 2011. Т. 6. С. 47.
Челюскина Т.В., Митюшкина И.А., Фролкова А.К., Чернышова М.А. Разделение биазеотропных смесей с использованием легколетучих дополнительных веществ // Химическая технология. 2011. Т. 12. С. 730.
Серафимов Л.А., Челюскина Т.В., Полковниченко А.В., Якушев Р.А. Анализ взаимных преобразований структур диаграмм трехкомпонентных систем путем образования бинарных внутренних тангенциальных азеотропов // Теоретические основы химической технологии. 2018. Т. 52. С. 636–648. https://doi.org/10.1134/S0040357118040061
Серафимов Л.А., Челюскина Т.В., Якушев Р.А. Термодинамико-топологический анализ образования внутренних тангенциальных азеотропов в бинарных двухфазных системах // Тонкие химические технологии. 2015. Т. 10. С. 41.
Sánchez C.A., Sánchez O.A., Orjuela A., Gil I.D., Rodríguez G. Vapor–Liquid Equilibrium for Binary Mixtures of Acetates in the Direct Esterification of Fusel Oil // J. Chem. Eng. Data. 2017. V. 62. P. 11–19. https://doi.org/10.1021/acs.jced.6b00221
Osorio-Viana W., Duque-Bernal M., Quintero-Arias J.D., Dobrosz-Gómez I., Fontalvo J., Gómez-García M.Á. Activity model and consistent thermodynamic features for acetic acid–isoamyl alcohol–isoamyl acetate–water reactive system // Fluid Phase Equilib. 2013. V. 345. P. 68–80. https://doi.org/10.1016/j.fluid.2013.02.006
Wittig R., Lohmann J., Gmehling J. Vapor-Liquid Equilibria by UNIFAC Group Contribution. 6. Revision and Extension // Ind. Eng. Chem. Res. 2003. V. 42. P. 183.
Челюскина Т.В., Полковниченко А.В., Модурова Д.Д. Расширение классификации трехкомпонентных систем, содержащих бинарные биазеотропные составляющие и не имеющих тройных азеотропов // Теоретические основы химической технологии. 2020. Т. 54. С. 738.
Серафимов Л.А. Термодинамико-топологический анализ диаграмм гетерогенного равновесия многокомпонентных смесей // Журн. физической химии. 2002. Т. 76. С. 1351.
Patidar P., Mahajani S.M. Esterification of fusel oil using reactive distillation – Part I: Reaction kinetics // Chemical Engineering J. 2012. V. 207–208. P. 377–387. https://doi.org/10.1016/j.cej.2012.06.139
Huang X. Modeling and Optimization of Acetic Acid Dehydration Process in Industrial Heterogeneous Azeotropic Distillation. PhD Thesis, East China University of Science and Technology, Shanghai 2014.
Gao H., Zhao F., Zhu L., Yang F., Wang Y., Li D. Dehydration of a Dilute Acetic Acid-Water Mixture via Batch Heteroazeotropic Distillation // Chem. Eng. Technol. 2021. V. 44. P. 477–487.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии