Теоретические основы химической технологии, 2023, T. 57, № 5, стр. 581-588
Анализ устойчивости химического процесса в проточном реакторе
А. А. Беляев a, *, А. В. Арутюнов a, b, В. С. Арутюнов a
a Федеральное государственное бюджетное учреждение науки Федеральный исследовательский центр
химической физики имени Н.Н. Семенова Российской академии наук
Москва, Россия
b Shenzhen MSU-BIT University
518172 Shenzhen, China
* E-mail: belyaevihf@yandex.ru
Поступила в редакцию 30.06.2023
После доработки 11.07.2023
Принята к публикации 23.07.2023
- EDN: MDHIJC
- DOI: 10.31857/S0040357123050044
Аннотация
Проведено исследование возможности возникновения колебательных режимов при протекании химического процесса в проточном реакторе с пространственной неоднородностью. Математическая модель динамики реактора учитывает процессы молекулярного и конвективного тепло- и массопереноса. Задача решается в одномерном приближении в условиях протекания одностадийной химической реакции. При условии равенства коэффициентов диффузии и температуропроводности получено аналитическое выражение для критерия устойчивости стационарного режима. Показана последовательность действий при определении критических условий устойчивости системы. Проведен ряд численных экспериментов проверки возникновения колебательных режимов при различных значениях параметров, отвечающих реальным условиям в реакторе.
ВВЕДЕНИЕ
Возникновение колебательных режимов в химических системах связано с критическими явлениями в химической кинетике, вызываемыми накоплением активных продуктов или тепла в реагирующей системе [1]. В проточных системах условия для возникновения термохимических колебаний более благоприятны по сравнению с замкнутыми системами, поскольку в реакторах такого типа потребление исходных веществ постоянно восполняется поступлением в реактор свежих реагентов. Такие явления наблюдались экспериментально, например, при парциальном окислении метана [2, 3]. Перспективы практического использования различных технологических процессов на основе окисления углеводородов делают необходимым анализ условий, приводящих к возникновению колебательных режимов, и их дальнейшей эволюции. Учитывая большое количество физико-химических параметров, описывающих такие системы, провести экспериментальное исследование всех их особенностей, как правило, невозможно. Однако при реализации таких процессов в промышленных условиях необходима уверенность, что случайные изменения параметров не приведут к переходу процесса в неустойчивый режим с неконтролируемым развитием событий. С другой стороны, не исключено, что именно при таких значениях параметров возможен более высокий выход целевых продуктов и, соответственно, более высокая эффективность процесса.
Поскольку реальные кинетические механизмы окисления и горения углеводородов содержат сотни элементарных реакций с участием десятков компонент, их анализ достаточно сложен. Поэтому в данной работе анализируется одностадийная химическая реакция 1-го порядка. Такой подход оправдан для исходных смесей реагентов стехиометрического состава, а также при значительном избытке одного из исходных реагентов или для реакций с участием только одного реагента [1].
Для подобного анализа удобна математическая модель проточного реактора идеального смешения, которая допускает возникновение автоколебаний [4, 5]. Модель реактора идеального смешения представляет собой сосредоточенную систему, поведение которой во всех точках пространства одинаково, а независимой переменной является только время. С использованием такой модели при компьютерном моделировании были получены колебательные режимы в процессе окисления метана [6, 7]. Однако предположение об однородности состава реакционной среды в результате быстрого перемешивания в реальных ситуациях выполняется далеко не всегда. При моделировании динамики реального проточного реактора желательно учитывать процессы молекулярного и конвективного тепло- и массопереноса, то есть переход к более общему и более реальному случаю пространственно распределенной системы [8]. Учет продольного перемешивания и конвективного переноса желателен и при моделировании биохимических процессов [9].
Задача данной работы – получить условие устойчивости стационарного режима для проточного реактора с пространственной неоднородностью. Для анализа устойчивости пространственно распределенной системы была реализована следующая последовательность действий: сначала анализируются стационарные решения сосредоточенной системы и находится положение неустойчивого равновесия, а затем полученное решение анализируется уже в рамках системы с пространственной неоднородностью [10].
МАТЕМАТИЧЕСКАЯ ФОРМУЛИРОВКА
Систему уравнений для реактора идеального смешения при одностадийной реакции можно представить в виде:
(1)
$\frac{{dx}}{{dt}} = - \alpha x\exp \left( { - \frac{\beta }{y}} \right) + \gamma \left( {{{x}_{0}} - x} \right) = F(x,y),$(2)
$\frac{{dy}}{{dt}} = \alpha \eta x\exp \left( { - \frac{\beta }{y}} \right) + \left( {\gamma + \kappa } \right)\left( {{{y}_{0}} - y} \right) = G(x,y),$Приведенные выше параметры связаны с теплофизическими и кинетическими характеристиками системы следующим образом:
Систему уравнений для проточного реактора в одномерном приближении и при учете пространственной неоднородности можно записать в виде [11]:
(3)
$\frac{{\partial x}}{{\partial t}} = F(x,y) + {{D}_{x}}\frac{{{{\partial }^{2}}x}}{{\partial {{r}^{2}}}} - v\frac{{\partial x}}{{\partial r}},$(4)
$\frac{{\partial y}}{{\partial t}} = G(x,y) + {{D}_{y}}\frac{{{{\partial }^{2}}y}}{{\partial {{r}^{2}}}} - v\frac{{\partial y}}{{\partial r}},$Граничные условия:
(6)
$r = L,\,\,\,\,\frac{{\partial x}}{{\partial r}} = 0,\,\,\,\,\frac{{\partial y}}{{\partial r}} = 0,$Далее будем предполагать, что Dx = Dy = D (число Le = 1). Для этого случая в Приложении описано получение критерия устойчивости стационарного решения системы (3)–(4) с краевыми условиями (5)–(6). Было показано, что решение системы устойчиво, если выполняется условие:
где ${{a}_{{11}}} = {{\left( {\frac{{\partial F}}{{\partial x}}} \right)}_{{x = {{x}_{s}},{\kern 1pt} y = {{y}_{s}}}}},\,\,{{a}_{{22}}} = {{\left( {\frac{{\partial G}}{{\partial y}}} \right)}_{{x = {{x}_{s}},{\kern 1pt} y = {{y}_{s}}}}}$, xs и ys – значения x и y, которые отвечают состоянию равновесия сосредоточенной системы (1)–(2), т.е. условиям F(xs, ys) = 0 и G(xs, ys) = 0. Эти же значения являются стационарным решением системы (3)–(4) с краевыми условиями (5)–(6). μ1 – корень трансцендентного уравнения(8)
$ - \frac{v}{{2D}}{\text{tg}}\left( {L\sqrt {\frac{{{{\mu }_{1}}}}{D}} } \right) = \sqrt {\frac{{{{\mu }_{1}}}}{D}} ,$Из (8) следует, что μ1 является функцией трех параметров, т.е. μ1(v, D, L). Зафиксировав два из них, можно найти критическое значение по третьему параметру.
На основе полученного критерия был проведен ряд численных экспериментов по анализу условий возникновения колебательных режимов в проточном реакторе.
ПРОВЕРКА СИСТЕМЫ НА УСТОЙЧИВОСТЬ
Для проведения исследования системы (3)–(4) с граничными условиями (5)–(6) на устойчивость нужно задаться конкретными значениями параметров. Известно, что во многих случаях учет неоднородности пространства благоприятствует установлению устойчивого равновесия [12]. Из формулы (7) видно, что это выполняется и в нашей задаче. Поэтому нас будет интересовать, как в условиях неустойчивого равновесия для сосредоточенной системы нарушение пространственной однородности позволяет избежать колебаний. Сначала найдем условия, при которых в сосредоточенной системе (1)–(2) возникнет колебательный режим. Примем следующие значения параметров: x0 = 0.26667, y0 = 0.583, α = 2.3 × 1015, β = 22.744, γ = 0.3057, η = 2.2482. Параметр κ, который отвечает за теплообмен между газом и стенкой реактора, будем варьировать от 1.23 до 2.46. Все выбранные значения параметров отвечают экспериментальным данным по окислению углеводородов в реакторе идеального смешения [5].
Приравняв F(x, y) и G(x, y) в системе (1)–(2) нулю, можно найти значения xs и ys, которые отвечают состоянию равновесия сосредоточенной системы. При варьировании параметра κ можно получить зависимость xs и ys от этого параметра и путем анализа состояния равновесия этих точек установить, когда положение равновесия неустойчиво, и возникнет колебательный режим.
Известно, что, изменяя условия теплоотвода, в реакторе идеального смешения можно получить как стационарный, так и колебательный режим [5, 7]. При этом в случае отсутствия теплоотвода или слабой его величине возникновение осцилляций температуры и концентрации невозможно. Но осцилляции не возникают и при очень сильной теплоотдаче.
Значение κ = 1.23 соответствует слабому теплоотводу. Анализ точки равновесия показывает, что получается устойчивый узел, а при расчете системы (1)–(2) видно, что решение выходит на равновесное значение. При κ = 1.48 точка равновесия становится устойчивым фокусом. При этом возникают небольшие колебания, но быстро затухают. При κ = 1.6 анализ показывает, что точка равновесия становится неустойчивым фокусом. При решении сосредоточенной системы в этом случае получается колебательный режим, а из фазового портрета системы видно, что возникает предельный цикл. Известно, что при превращении устойчивого фокуса в неустойчивый в результате изменения параметров системы рождается предельный цикл, охватывающий этот фокус [13]. Установить, при каком именно значении κ в интервале от 1.48 до 1.6 возникает бифуркация Андронова–Хопфа [14], целью данного исследования не является. При κ = 1.6 состояние неустойчивого равновесия характеризуется величинами: xs = 0.01539, ys = 0.673612, a11 = –5.30872, a22 = 6.75088.
В случае пространственно распределенной системы появляются параметры Dx, Dy, v, L. По-прежнему предполагая, что Dx = Dy = D, для оценки устойчивости режима нужно воспользоваться условием (7) с учетом (8). Зафиксировав постоянные значения двух из трех параметров D, v и L, можно по третьему параметру определить его критическое значение, при котором режим становится неустойчивым. Все последующие оценки будут проводиться при κ = 1.6.
Из (7) видно, что увеличение скорости газового потока v способствует возникновению устойчивого режима, в то время как усиление молекулярного переноса тепла и вещества D действует в противоположном направлении. Это вполне согласуется с физико-химическими особенностями процесса. Формула (7) не предназначена для оценок предельных случаев D и v. Однако понятно, что при очень больших значениях D мы снова возвращаемся к модели реактора идеального смешения, а при D = 0 получается модель реактора идеального вытеснения. Значение v = 0 не соответствует реальным условиям, поскольку описывает неподвижный газовый поток, а не проточный реактор. При больших значениях скорости газа возникает турбулизация среды, анализ последствий которой выходит за рамки рассматриваемой задачи.
Сложнее оценить влияние на устойчивость процесса длины реактора L. И при относительно высоких скоростях газового потока и при сравнительно небольших значениях D процесс устойчив при любой длине реактора. Однако в определенном диапазоне значений D и v с увеличением длины реактора режим может потерять устойчивость. Такая же ситуация может возникнуть и при очень малой длине реактора, которая, как правило, не соответствует реальным условиям.
Перепишем условие (7) в виде:
(9)
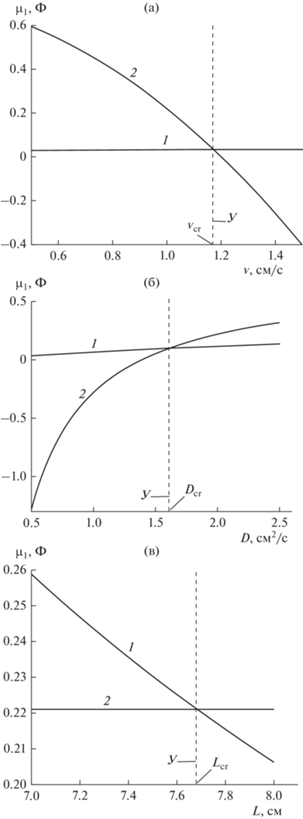
${{\mu }_{1}} \geqslant \Phi = \frac{{{{a}_{{11}}} + {{a}_{{22}}}}}{2} - \frac{{{{v}^{2}}}}{{4D}}.$На рис. 1 показано нахождение критических значений v (1а), D (1б) и L (1в) при фиксированных значениях двух других параметров, характеризующих пространственное распределение. На этом рисунке линией 1 обозначена зависимость от искомого параметра величины μ1, а линией 2 – поведение Φ. В той области, где линия 1 идет выше линии 2, режим устойчив и колебаний нет. Граница устойчивого режима обозначена пунктирной линией, и на оси абсцисс обозначены соответствующие критические значения параметров. Заметим, что на рис. 1в линия 2 идет строго параллельно оси абсцисс.
Рис. 1.
Нахождение критических значений при пересечении функций μ1 (1) и Φ (2) для: (а) скорости газа (vcr = 1.17 см/с) при D = 0.5 см2/c и L = 11 см; (б) молекулярного тепло- и массопереноса (Dcr = = 1.61 см2/c) при v = 2 см/с и L = 11 см; (в) длины реактора (Lcr = 7.68 см) при v = 2 см/с и D = 2 см2/c. У – область устойчивости.
Решение системы (3)–(4) с граничными условиями (5)–(6) с помощью численного расчета позволяет проверить, действительно ли при данных значениях параметров получается устойчивое или неустойчивое поведение системы. Это показано на рис. 2–4. Наглядный пример колебательного режима в реакторе представлен на рис. 2. Здесь представлено распределение концентрации (мольные доли) и безразмерной температуры вдоль пространственной координаты в разные моменты времени. Видно перемещение профилей концентрации и температуры в виде бегущей по длине реактора волны к входу в реактор, после чего все повторяется. На рис. 3 для тех же условий, что и на рис. 2, показано поведение во времени концентрации и температуры в точке при значении координаты, близкой к середине длины реактора. На рис. 4 представлен типичный пример выхода на стационар после начального возмущения. В таблице представлены некоторые примеры критического значения скорости газовой смеси vcr при фиксированных значениях D и L.
Рис. 2.
Распределения x (а) и y (б) вдоль оси реактора в разные моменты времени t (c): 20 (1), 25 (2), 30 (3), 35 (4), 40 (5), 45 (6). D = 0.5 см2/c, v = 0.5 см/c, L = 11 см.
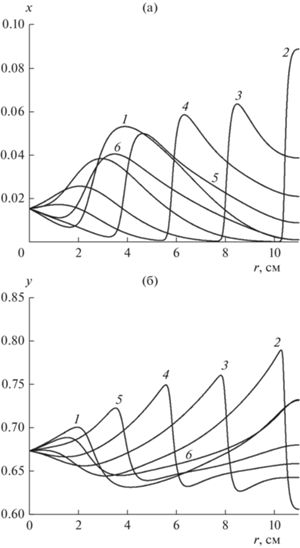
Рис. 3.
Поведение во времени x (а) и y (б) в точке при значении координаты r = 5 см. D = 0.5 см2/c, v = 0.5 см/c, L = 11 см.
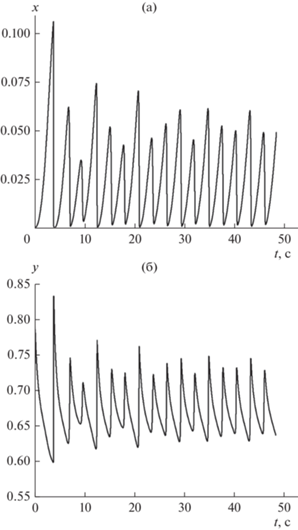
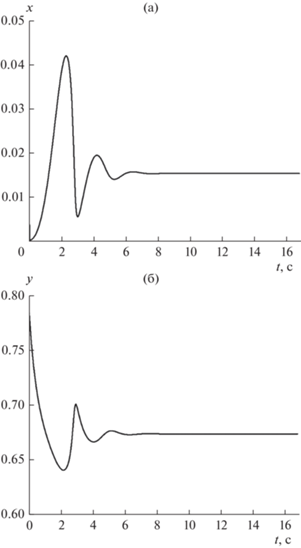
Рис. 4.
Поведение во времени x (а) и y (б) в точке при значении координаты r = 5 см. D = 0.5 см2/c, v = 2 см/c, L = 11 см.
В случае, когда Dx≠Dy, получить аналитическое выражение для условия устойчивости не представляется возможным. Однако результаты численного решения системы (3)–(4) показывают, что неравенство коэффициентов молекулярного тепло- и массопереноса является дестабилизирующим фактором, и область неустойчивого режима в этом случае расширяется. Выше отмечалось, что при Dx = Dy = D уменьшение D приводит к уменьшению vcr, но при Dx ≠ Dy ситуация будет иной. Например, пусть при Dx = Dy = D, тогда при определенном значении L получим критическое значение скорости $v_{{{\text{cr}}}}^{0}$. При Dx < Dy = D и том же значении L получим, что значение критической скорости ${{v}_{{{\text{cr}}}}} > v_{{{\text{cr}}}}^{0}$. Та же тенденция будет при Dy < Dx = D. Усиление тенденции к неустойчивости при неравенстве коэффициентов молекулярного тепло- и массопереноса обсуждалось в [5, 15].
ЗАКЛЮЧЕНИЕ
Получено аналитическое условие устойчивости работы химического реактора с одномерной пространственной неоднородностью. Для его получения предполагали, что коэффициенты диффузии и температуропроводности равны. Поскольку учет неоднородности пространства способствует установлению устойчивого равновесия, то сначала находились значения параметров, при которых в сосредоточенной системе (реактор идеального смешения) возникает колебательный режим, а затем осуществлялся анализ пространственно распределенной системы, отвечающей реальным условиям в реакторе. Для получения аналитического условия предполагалось, что коэффициенты диффузии и температуропроводности равны. Показано определение критических условий устойчивости системы и проверка поведения системы с помощью численного счета при разных значениях параметров.
Данную работу можно рассматривать лишь как первый шаг в исследовании устойчивости процессов химической конверсии углеводородов в реакторах с пространственной неоднородностью параметров. В работе лишь схематично рассмотрена ситуация существенного различия коэффициентов молекулярного тепло- и массопереноса. Между тем эта проблема заслуживает отдельного исследования. Анализ одностадийной химической реакции 1-го порядка очень удобен для параметрического исследования, но не всегда оправдан в реальных условиях, когда необходим учет более сложной кинетики химического процесса. Отметим также, что в задаче использовалось одномерное приближение, тогда как в ряде случаев необходимо рассматривать процессы диффузии и теплопроводности не только вдоль оси реактора, но и в поперечном направлении.
Авторы выражают искреннюю благодарность В.С. Посвянскому (ФИЦ ХФ РАН) за содержательное обсуждение и крайне полезные советы, которые во многом способствовали написанию этой статьи.
Список литературы
Франк-Каменецкий Д.А. Диффузия и теплопередача в химической кинетике. М.: Наука, 1987.
Yarlagadda P.S., Morton L.A., Hunter N.R., Gesser H.D. Temperature oscillations during the high-pressure partial oxidation of methane in a tubular flow reactor // Combustion and Flame. 1990. V. 79. № 2. P. 216.
Arutyunov V. Direct methane to methanol: Foundations and prospects of the process. Amsterdam: Elsevier B.V., 2014.
Вольтер Б.В., Сальников И.Е. Устойчивость режимов работы химических реакторов. М.: Химия, 1981.
Быков В.И., Цыбенова С.Б. Нелинейные модели химической кинетики. М.: КРАССАНД, 2011.
de Joannon M., Sabia P., Tregrossi A., Cavaliere A. Dynamic behavior of methane oxidation in premixed flow reactor // Combust. Sci. and Tech. 2004. V. 176. № 5–6. P. 769.
Arutyunov A.V., Belyaev A.A., Lidskii B.V., Nikitin A.V., Posvyanskii V.S., Arutyunov V.S. Thermokinetic oscillations in the partial oxidation of methane // Russian J. Phys. Chem. В. 2017. V. 11. № 3. P. 403. [Арутюнов А.В., Беляев А.А., Лидский Б.В., Никитин А.В., Посвянский В.С., Арутюнов В.С. Термокинетические колебания при парциальном окислении метана // Химическая физика. 2017. Т. 36. № 6. С. 3.]
Перлмуттер Д. Устойчивость химических реакторов (Перевод с англ.). Л.: Химия, 1976.
Aleksandrova L.Yu., Moshinskii A.I. Description of the operation of a biochemical reactor by a diffusion model // Theor. Found. Chem. Eng. 2022. V. 56. № 3. P. 265. [Александрова Л.Ю., Мошинский А.И. Описание работы биохимического реактора диффузионной моделью // Теор. основы хим. технологии. 2022. Т. 56. № 3. С. 273.]
Воробьев А.Х., Богданов А.В. Кинетика нелинейных химических систем. М.: хим. фак. МГУ им. Ломоносова, 2019.
Bykov V.I., Tsybenova S.B., Slin’ko M.G. The dynamics of a continuous tank of incomplete stirring // The Proc. the Russ. Acad. of Sci. 2001. V. 380. № 5. P. 649 [Быков В.И., Цыбенова С.Б., Слинько М.Г. Динамика проточного реактора неполного перемешивания // Докл. АН. 2001. Т. 380. № 5. С. 649.]
Романовский Ю.М., Васильев В.А., Яхно В.Г. Автоволновые процессы в распределенных кинетических системах // Успехи физ. Наук. 1979. Т. 128. № 4. С. 625.
Холодниок М., Клич А., Кубичек М., Марек М. Методы анализа нелинейных динамических моделей (Перевод с чешского). М.: Мир, 1991.
Арнольд В.И. Дополнительные главы теории обыкновенных дифференциальных уравнений. М.: Наука, 1978.
Колебания и бегущие волны в химических системах / Под ред. Филда Р., Бургер М. (пер. с англ.). М.: Мир, 1988.
Гельфанд И.М. Лекции по линейной алгебре. М.: Наука, 1971.
Тихонов А.Н., Самарский А.А. Уравнения математической физики. М.: Наука, 1977.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии


