Теоретические основы химической технологии, 2023, T. 57, № 6, стр. 720-730
Локализация паров иодида цезия на керамических блочно-ячеистых контактных элементах в окислительной среде
М. Д. Гаспарян a, *, В. Н. Грунский a, Ю. С. Мочалов b, Л. П. Суханов b, А. В. Титов a, С. В. Тищенко a, Е. О. Обухов a
a Российский химико-технологический университет им. Д.И. Менделеева
Москва, Россия
b Акционерное общество “Прорыв”
Москва, Россия
* E-mail: migas56@yandex.ru
Поступила в редакцию 17.08.2023
После доработки 24.09.2023
Принята к публикации 26.09.2023
- EDN: IHABNA
- DOI: 10.31857/S0040357123060064
Аннотация
Исследована эффективность раздельного улавливания оксида цезия и молекулярного иода, образующихся при окислительном термолизе иодида цезия, в процессе хемосорбции на керамических высокопористых блочно-ячеистых контактных элементах. Определена динамическая сорбционная емкость контактных элементов с нанесенным алюмосиликатным сорбционно-активным слоем и с активным слоем нитрата серебра по цезию и иоду соответственно. Разработанные контактные элементы рекомендуются для использования в системах локальной газоочистки высокотемпературных переделов переработки облученного ядерного топлива.
ВВЕДЕНИЕ
Цезий является самым значимым как в количественном отношении, так и в отношении активности и энерговыделения летучим продуктом деления (ЛПД), во многом определяющим условия длительного хранения и технологию переработки облученного ядерного топлива (ОЯТ) [1]. Современные технологии переработки смешанного оксидного или смешанного нитридного уран-плутониевого (СНУП) топлива реакторов на быстрых нейтронах предусматривают максимальное выделение и локализацию соединений цезия в головных процессах, например, при высокотемпературной обработке (ВТО) фрагментированного ОЯТ на пирохимическом переделе.
Суммарное содержание изотопов цезия, в том числе радиоактивных Cs-137, Cs-134, Cs-135 и стабильного Cs-133, составляет около 6.5 г на 1 кг СНУП ОЯТ с выгоранием 8% т.а. и послереакторной выдержкой 1 год. Наиболее эффективными и технологичными контактными элементами для локализации изотопов цезия в парогазовой фазе являются твердые хемосорбенты, улавливающие цезий в форме оксида с образованием его устойчивых алюмосиликатов. Кроме высокой эффективности улавливания, основное требование к таким материалам – максимальная сорбционная емкость и, соответственно, минимальное количество образующихся вторичных твердых радиоактивных отходов (ТРО).
Улавливанию оксида цезия, выделяющегося при термолизе его солей (нитрат, карбонат, силикат), твердыми пористыми неорганическими сорбентами в газовой фазе посвящено немало работ [2–4]. В ходе предыдущих наших исследований разработаны керамические фильтры-сорбенты для улавливания Cs2O, образующегося в воздушной среде из нитрата стабильного цезия-133 [5–7] при температурах выше 700°С. Основой этих контактных элементов (КЭ) являлись корундовые высокопористые ячеистые материалы (ВПЯМ), содержащие более 95% α-Al2O3 (наполнитель – электрокорунд марки F-360, основное связующее – глинозем ГН-1), на которые нанесен алюмосиликатный активный слой с массовым соотношением γ-Al2O3/SiO2 = = 30/70. Активный слой в процессе хемосорбции насыщается оксидом цезия практически полностью с образованием его устойчивых алюмосиликатов по реакциям:
(1)
$\begin{gathered} {\text{C}}{{{\text{s}}}_{{\text{2}}}}{\text{O}} + {\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{3}} + {\text{2Si}}{{{\text{O}}}_{2}} \to \\ \to 2{\text{CsAlSi}}{{{\text{O}}}_{4}}({\text{C}}{{{\text{s}}}_{{\text{2}}}}{\text{O}} \cdot {\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}} \cdot 2{\text{Si}}{{{\text{O}}}_{{\text{2}}}}), \\ \end{gathered} $(2)
$\begin{gathered} {\text{CsAlSi}}{{{\text{O}}}_{{\text{4}}}} + {\text{Si}}{{{\text{O}}}_{{\text{2}}}} \to \\ \to {\text{CsAlS}}{{{\text{i}}}_{{\text{2}}}}{{{\text{O}}}_{6}}({\text{C}}{{{\text{s}}}_{{\text{2}}}}{\text{O}} \cdot {\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{3}} \cdot 4{\text{Si}}{{{\text{O}}}_{2}}). \\ \end{gathered} $Продукт реакции (2) – поллуцит – является наиболее устойчивой и предпочтительной формой фиксации изотопов цезия. При высокой эффективности улавливания (>99%), сорбционная емкость в интервале температур 700–1000°С в статических условиях не превышает 0.2 г Cs2O/г КЭ.
В настоящей работе в качестве прекурсора оксида цезия использовался иодид цезия. Его выбор обусловлен данными из [8, 9], согласно которым при вскрытии твэлов после выдержки для переработки топлива, особенно с высоким выгоранием, радионуклиды цезия и йода выделяются преимущественно в виде термодинамически стабильного соединения CsI – продукта взаимодействия элементарных I и Cs внутри оболочки по реакции:
(3)
${\text{C}}{{{\text{s}}}_{{\left( {\text{г}} \right)}}} + {{{\text{I}}}_{{\left( {\text{г}} \right)}}} \leftrightarrow {\text{CsI}}.$Отсюда вытекает цель исследований – определение эффективности контактных элементов нового поколения на основе керамических ВПЯМ в процессе локализации CsI в условиях, приближенных к реальным условиям процессов переработки ОЯТ. В настоящей работе моделируются условия проведения операции ВТО в окислительной среде (Ar + O2, воздух) [10].
Существует ряд эффективных гранулированных сорбентов, разработанных для локализации иода в условиях эксплуатации АЭС [11] и способных улавливать аэрозоли иодида цезия, включающие радиоизотопы (137Cs131I) за счет физической адсорбции без разложения на атомарные цезий и иод.
Мы предлагаем технологическую схему локализации CsI, включающую его термолиз, селективное улавливание изотопов Cs и I и дальнейшую раздельную иммобилизацию КЭ, насыщенных цезием и иодом в процессе хемосорбции. Отметим, что в России твердые хемосорбенты цезия, в отличие от иодных сорбентов, специально не производятся и в системах газоочистки существующих в России технологий переработки ОЯТ [7, 12] не применяются.
В работе [7] показано, что благодаря своим уникальным структурно-физическим характеристикам, в первую очередь это чрезвычайно высокая внешняя доступная удельная объемная поверхность (до 4000 м2/м3) и общая пористость до 95%, КЭ на основе керамических ВПЯМ имеют емкость по улавливаемым в процессе хемосорбции различным ЛПД, в 1.5–2 раза превышающую емкость традиционных гранулированных КЭ. Их применение в составе локальных систем газоочистки (ЛСГО) на различных высокотемпературных переделах переработки ОЯТ позволит в такой же степени снизить количество вторичных ТРО.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез КЭ. Образцы контактных элементов, селективно улавливающих соединения цезия, синтезировались по известной технологии дублирования структуры ретикулированного пенополиуретана (ППУ) с плотностью пор 30 ppi [5, 7]. В качестве наполнителя керамического шликера использовали электрокорунд марки F-360, основным связующим служила полуфарфоровая литьевая масса (ПФЛ-1), содержащая ~20 мас. % Al2O3 и ~70% SiO2 [13]. После пропитки ППУ водным шликером и последующего высокотемпературного обжига в интервале температур 1180–1220°С на полученный керамический каркас из ВПЯМ методом мультислойной пропитки и термообработки наносился активный слой (АС) из аморфных γ-Al2O3 и SiO2, взятых в уже отмеченном оптимальном массовом соотношении 30/70, с общим содержанием 25–35 мас. %. Размеры синтезированных образцов КЭ составляли 35–50 (d) × × 50 (h) мм, средняя плотность 0.45–0.55 г/см3, открытая пористость 70–80%.
На рис. 1 показана ячеистая структура образца синтезированных ВПЯМ (а) и микроструктура участка перемычки ячейки (б). Средний размер ячейки (1.0–1.2 мм) соответствует плотности пор исходного ППУ. На поверхности перемычки выделяются зерна наполнителя исходного размера (20–25 мкм) и частицы связующего размером <5 мкм.
Замена связующего глинозема, применяемого в наших прежних работах, на массу ПФЛ-1 имела целью вовлечение в процесс хемосорбции оксида цезия, не только нанесенного АС, но и материала керамической основы, что должно было повысить сорбционную емкость КЭ. Такая же тенденция наблюдается в разрабатываемых южнокорейским институтом “KAERI” зольных фильтрах (fly-ash filters) аналогичного состава и структуры [2, 3], используемых для локализации цезия и рубидия в комплексной системе газоочистки головного процесса пирохимической технологии переработки ОЯТ легководных реакторов – высокотемпературной волоксидации [14]. Кроме того, использование массы ПФЛ-1 с низкой температурой обжига облегчает дальнейшую утилизацию отработавших КЭ по технологии остекловывания.
По аналогичной технологии синтезировались образцы КЭ с нанесенным на промежуточную активную подложку из γ-Al2O3 активным слоем AgNO3 в количестве 15–25 мас. %, показавшие в предыдущих исследованиях [15] высокую эффективность локализации соединений иода.
Определение эффективности локализации паров иодида цезия. CsI – кристаллическое вещество с температурой плавления 634°С и кипения 1280°С при 760 мм. рт. ст., при возгонке на воздухе частично диссоциирует с образованием молекулярного иода [16]. Давление паров в мм рт. ст.: 1 (737°C), 10 (872°C), 100 (1056°C) [17]. С учетом этих данных, а также на основании приведенных в различных источниках оптимальных температур процессов хемосорбции отдельно соединений цезия и иода, определяли режим проведения экспериментов. Оптимальной температурой улавливания Cs2O является 900°С [2, 5, 7, 14]. Для процесса хемосорбции иода в [18] предложена реакция:
(4)
$6{\text{AgN}}{{{\text{O}}}_{{\text{3}}}} + 3{{{\text{I}}}_{{\text{2}}}} \to 4{\text{AgI}} + 2{\text{AgI}}{{{\text{O}}}_{3}} + 6{\kern 1pt} {\text{N}}{{{\text{O}}}_{2}}{\kern 1pt} \uparrow {\kern 1pt} .$Оптимальная температура ее протекания составляет примерно 200°С [7, 14, 15, 18], поскольку нитрат серебра начинает разлагаться при температурах выше температуры кипения (210°С) по реакции:
(5)
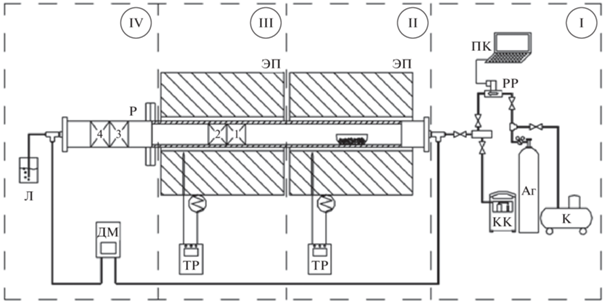
${\text{2AgN}}{{{\text{O}}}_{{\text{3}}}}~\,\, \to 2{\text{Ag}}~\,\, + {\text{ 2N}}{{{\text{O}}}_{2}}~\,\, + {{{\text{O}}}_{2}},$Исследование эффективности улавливания и сорбционной емкости контактных элементов проводили на сорбционно-каталитическом стенде (рис. 2), состоящем из 4-х блоков.
Блок подготовки газа-носителя (I) включает баллон с аргоном, концентратор кислорода (КК), воздушный компрессор (К) и регуляторы-расходомеры (РР). Стальной реактор (Р) размещен в следующих 3-х блоках. Два первых оснащены трубчатыми электропечами (ЭП) с терморегуляторами (ТР). Эта зона реактора футерована внутри корундовой трубкой. В блоке II происходит нагрев газа-носителя до температуры эксперимента (800–960°С) и испарение навески иодида цезия в корундовом тигле-лодочке. Далее пары CsI поступают в испытательный блок III, где в реакторе установлены 2 образца КЭ (№ 1 и 2) диаметром 35 мм с алюмосиликатным активным слоем (испытуемый и контрольный) для улавливания цезия. В зоне реактора, расположенной вне электропечей (блок IV) и охлаждаемой вентилятором до заданной температуры (180–220°С), установлены также 2 образца КЭ (№ 3 и 4) диаметром 50 мм с активным слоем AgNO3, предназначенные для улавливания I2. Наличие проскока иода качественно наблюдается по изменению цвета раствора крахмала в ловушке (Л), установленной на выходе из реактора. Дифманометр (ДМ) измеряет газодинамическое сопротивление КЭ и всей сборки.
Условия проведения испытаний и усредненные расчетные характеристики для проведенных серий экспериментов приведены в табл. 1.
Таблица 1.
Условия проведения и результаты экспериментов по улавливанию паров CsI: газ-носитель – (Ar + + 15% O2), τexp = 10 ч или воздух (τexp = 20 ч)*
| № эксп. |
№ обр. |
WG, л/ч |
texp, °С |
mCsI, г |
CCsI, г/л |
${{A}_{{{\text{C}}{{{\text{s}}}_{{\text{2}}}}{\text{O}}}}}$, г/г КЭ (г/г АС) |
ACsI, г/г КЭ |
AI2 г/г КЭ (г/г АС) |
η, % | ECsI, % |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 1 | 70 | 800 | 6.87 | 0.0098 | 0.12 (0.34) | 0.01 | – | 60.8 | 97.8 |
| 2 | 0.01 (0.06) | 0.01 | – | 9.0 | ||||||
| 3 | 200 | – | 0.01 | 0.07 (0.42) | 70.6 | |||||
| 4 | – | – | 0.01 (0.07) | 6.4 | ||||||
| 2 | 1 | 150 | 800 | 8.75 | 0.0058 | 0.13 (0.61) | 0.03 | – | 78.5 | 98.0 |
| 2 | 0.03 (0.13) | 0.01 | – | 23.3 | ||||||
| 3 | 200 | – | 0.01 | 0.10 (0.48) | 75.9 | |||||
| 4 | – | – | 0.03 (0.15) | 22.3 | ||||||
| 3 | 1 | 150 | 900 | 9.60 | 0.0064 | 0.14 (0.57) | 0.02 | – | 73.8 | 98.5 |
| 2 | 0.04 (0.16) | – | – | 23.7 | ||||||
| 3 | 200 | – | 0.01 | 0.08 (0.43) | 71.8 | |||||
| 4 | – | – | 0.01 (0.04) | 7.0 | ||||||
| 4 | 1 | 180 | 900 | 11.86 | 0.0066 | 0.19 (1.09) | – | – | 90.2 | 99.0 |
| 2 | 0.06 (0.38) | 0,01 | – | 30.6 | ||||||
| 3 | 200 | – | 0.01 | 0.10 (0.42) | 86.7 | |||||
| 4 | – | – | 0.02 (0.12) | 13.1 | ||||||
| 5 | 1 | 180 | 960 | 12.56 | 0.0069 | 0.20 (0.90) | – | – | 92.2 | 96.9 |
| 2 | 0.05(0.20) | – | – | 25.5 | ||||||
| 3 | 200 | – | – | 0.09 (0.40) | 82.5 | |||||
| 4 | – | – | 0.03 (0.14) | 21.0 | ||||||
| 6* | 1 | 150 | 960 | 20.16 | 0.0067 | 0.31 (0.99) | 0.01 | – | 126.5 | 99.2 |
| 2 | 0.11 (0.52) | – | – | 75.7 | ||||||
| 3 | 200 | – | – | 0.11 (0.60) | 97.8 | |||||
| 4 | – | – | 0.08 (0.38) | 68.8 |
Динамическая сорбционная емкость образца КЭ по Cs2O обозначена как ${{A}_{{{\text{C}}{{{\text{s}}}_{{\text{2}}}}{\text{O}}}}}$, ACsI– сорбционная емкость по CsI, AI2 – сорбционная емкость по I2, ECsI – суммарная эффективность улавливания CsI всеми образцами сборки. Степень использования активного слоя (η) определяется на основании прироста массы КЭ после окончания эксперимента, содержания в нем АС, а также количества и состава продуктов хемосорбции Cs2O и I2.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В среде аргонокислородной смеси или воздуха протекает реакция:
(6)
$4{\text{CsI}} + {{{\text{O}}}_{2}} = 2{\text{C}}{{{\text{s}}}_{{\text{2}}}}{\text{O}} + 2{{{\text{I}}}_{2}}.$Образовавшийся оксид цезия вступает в реакцию с алюмосиликатным активным слоем КЭ, установленных в высокотемпературной зоне реактора, с образованием преимущественно устойчивого поллуцита (CsAlSi2O6). Общую схему процесса хемосорбции можно представить в следующем виде:
(7)
$\begin{gathered} 4{\text{CsI}} + 2({\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{3}} \cdot 4{\text{Si}}{{{\text{O}}}_{2}}) + {{{\text{O}}}_{2}} \to \\ \to 4{\text{CsAlS}}{{{\text{i}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{6\;}}}}} + 2{{{\text{I}}}_{2}}. \\ \end{gathered} $По данным табл. 1 степень диссоциации иодида цезия в разных экспериментах составляет 85–100% и повышается с увеличением температуры процесса улавливания. Суммарная эффективность улавливания иодида цезия с различной концентрацией при разных расходах газа-носителя полной сборкой КЭ с алюмосиликатным активным слоем и активным слоем AgNO3, определяемая соотношением прироста массы всех КЭ по Cs2O (в пересчете на Cs), I и CsI к массе испарившегося иодида цезия, в выбранном интервале температур составила 97.8–99.6%. Эффективность раздельного улавливания цезия находится в таких же пределах.
Сорбционная емкость испытуемых контактных элементов (первых в сборке) по оксиду цезия без учета цезия, содержащегося в CsI, составила 0.12–0.31 г Cs2O /г КЭ. Повышение ее значений происходит под влиянием нескольких факторов: с ростом температуры эксперимента увеличивается скорость испарения CsI и скорость процесса хемосорбции; также количество испарившегося иодида цезия увеличивается за счет обновления поверхности его навески в тигле при повышении объемного расхода газа-носителя.
Неразложившаяся часть иодида цезия удерживается в структуре ВПЯМ за счет физической адсорбции. Сорбционная емкость по CsI на любом КЭ не превышает 0.03 г/г. Расчет распределения уловленной массы цезия в форме его алюмосиликатов и в составе иодида цезия проводился по данным рентгенофазового анализа (РФА).
Степень использования активного слоя по отношению к теоретической, рассчитанной по материальному балансу уравнения (7), для основной массы экспериментов составляет 60–90%, что свидетельствует о возможности дополнительного улавливания Cs2O.
Для сравнения отметим, что обозначенная в работе [19] при улавливании CsI в окислительной среде (N2 + 21%O2, 4%H2/Ar + 10%O2) максимальная сорбционная емкость по цезию составляет 0.18 г Cs/г фильтра.
Типичная дифрактограмма образца КЭ после испытаний при температуре 900°С представлена на рис. 3. Кроме материалов керамической основы – корунда (α-Al2O3 – 57.2 мас. %) и муллита (3Al2O3⋅2SiO2 – 4.8 мас. %), в фазовом составе присутствуют основной продукт хемосорбции – поллуцит (CsAlSi2O6 – 36.3 мас. %) и 1.7 мас. % неразложившегося CsI.
Рис. 3.
Фазовый состав образца КЭ после улавливания Cs2O при texp = 900°С, газ-носитель – (Ar + O2).
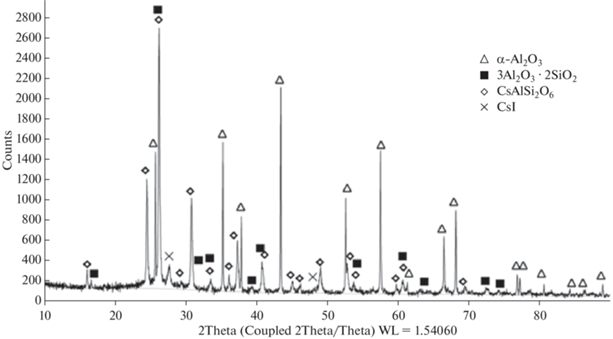
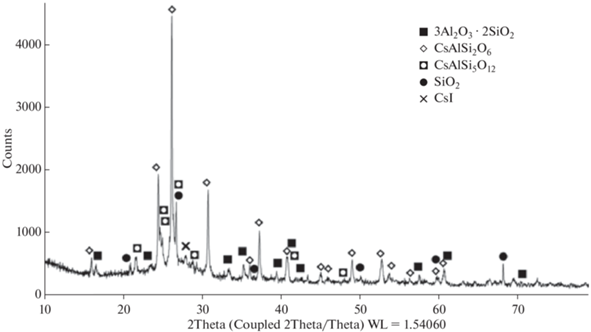
При более низкой температуре сорбционная емкость по Cs2O снижается, что соответствует данным по улавливанию оксида цезия, генерированного кальцинацией CsNO3 [5–7]; а в фазовом составе идентифицируется промежуточный продукт хемосорбции – цезиевый нефелин (CsAlSiO4) – в различных пропорциях с поллуцитом (от 1 : 1 до 1 : 10). На рис. 4 представлен фазовый состав образца КЭ данной серии после испытаний при температуре 800°С, мас. %: корунд (48.1), муллит (8.0), CsAlSi2-O6 (39.2), CsAlSiO4 (4.7).
Рис. 4.
Фазовый состав образца КЭ после улавливания Cs2O при texp = 800°С, газ-носитель – (Ar + O2).
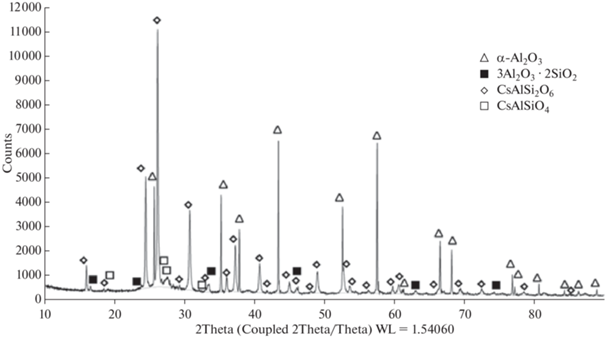
Максимальная сорбционная емкость (0.31 г Cs2O/г КЭ) получена при повышенной до 960°С температуре в воздушной атмосфере и увеличении продолжительности эксперимента до 20 ч (2 периода испытаний по 10 ч). Таким образом подтверждена возможность повторного использования частично отработавших и не набравших максимальную сорбционную емкость КЭ. При этом, по данным РФА образуется еще один известный устойчивый алюмосиликат цезия с высококремнеземной цеолитной структурой – CsAlSi5O12 [2]. Поллуцит в данном случае является промежуточным соединением и его превращение в форму Cs2O⋅Al2O3⋅10SiO2, наблюдаемое в разных экспериментах со степенью до 50%, объясняется избытком оксида кремния в составе основного связующего ВПЯМ, который, очевидно, вовлечен в процесс хемосорбции, а остаток его присутствует в образце в виде кварца. При этом , расчетная степень использования активного слоя составляет более 100%, что означает участие в процессе хемосорбции керамической основы КЭ. Представленные на дифрактограмме образца из данной серии фазы (рис. 5) имеют следующее содержание, мас. %: муллит (28.1), CsAlSi2O6 (39.9), CsAlSi5O12 (20.9), кварц (SiO2 – 10.2) и CsI (0.9).
Результаты электронно-зондового микроанализа (ЭЗМА) участка поверхности образца КЭ из этой серии после испытаний приведены на рис. 6 и в табл. 2. Элементный состав на диаграмме (Cs, Al, Si, O) близок к рассчитанному на основании фазового состава с учетом соотношения CsAlSi2O6 к CsAlSi5O12. Также в нем присутствуют примеси Na и K из материала ВПЯМ. Полученные данные позволяют утверждать, что отработавший полностью активный слой КЭ и частично внешний слой керамической основы, имеющей изначально близкое к продуктам хемосорбции содержание оксидов алюминия и кремния, состоят только из алюмосиликатов цезия.
Рис. 6.
Диаграмма элементного состава участка поверхности образца КЭ после улавливания оксида цезия.
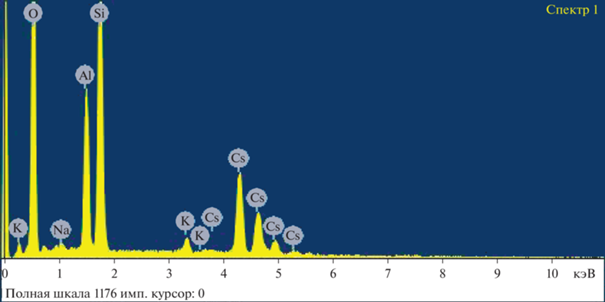
Таблица 2.
Весовое содержание элементов в активном слое образца КЭ после хемосорбции оксида цезия
| Элемент | Содержание, мас. % | |||
|---|---|---|---|---|
| теоретическое | диаграмма | расчетное по данным РФА | ||
| CsAlSi2O6 | CsAlSi5O12 | |||
| Cs | 42.6 | 27.0 | 34.4 | 36.0 |
| Al | 8.7 | 5.5 | 7.9 | 7.6 |
| Si | 17.9 | 28.5 | 18.4 | 21.8 |
| O | 30.8 | 39.0 | 37.9 | 34.6 |
| K | 0.0 | 0.0 | 1.2 | 0.0 |
| Na | 0.0 | 0.0 | 0.4 | 0.0 |
Образовавшийся по реакции (4) молекулярный йод поступает в холодную зону реактора, где реагирует с активным слоем AgNO3 установленных в ней КЭ с образованием основного продукта хемосорбции – иодида серебра:
(8)
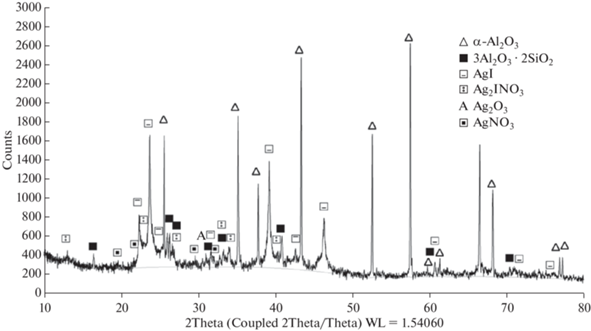
$2{\text{AgN}}{{{\text{O}}}_{{\text{3}}}} + {{{\text{I}}}_{2}} \to 2{\text{AgI}} + 2{\text{N}}{{{\text{O}}}_{2}} + {{{\text{O}}}_{2}}.$Дифрактограмма образца КЭ с практически полностью прореагировавшим активным слоем нитрата серебра представлена на рис. 7.
Кроме материалов керамической основы (корунд – 65.9 мас. %, муллит – 14.4 мас. %) и иодида серебра (11.5 мас. %) в продуктах хемосорбции идентифицируется комплексное соединение – нитрат дисереброиода (Ag2INO3 – 5.9 мас. %), остаток непрореагировавшего AgNO3 (1.8 мас. %) и следовые количества оксида серебра(III) – Ag2O3 (0.5 мас. %).
В ряде образцов, как и в случае с КЭ алюмосиликатного состава, РФА обнаруживает незначительное количество CsI, прошедшего в результате проскока в холодную зону реактора и уловленного КЭ с активным нитратом серебра. Фиксация иодида цезия обоими типами КЭ при температурах 900 и 200°С свидетельствует о возможности улавливания керамическими ВПЯМ соединений различных ЛПД как в парогазовой фазе, так и в форме образовавшихся после их кристаллизации радиоаэрозолей, по механизму физической адсорбции.
Иодат серебра (AgIO3), который может образовываться по реакции (4) наряду с иодидом в качестве промежуточного продукта, очевидно, разлагается при температурах выше температуры его кипения (200°С) до AgI:
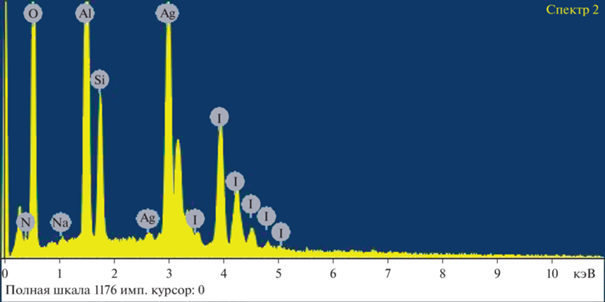
и на дифрактограммах образцов КЭ после испытаний не обнаружен.На рис. 8 и в табл. 3 приведены диаграмма элементного состава и весовое содержание элементов для участка поверхности АС образца КЭ после улавливания I2. Содержание серебра и иода подтверждает образование иодида серебра и нитрата дисереброиода в соотношении, определенном РФА, при высокой сорбционной емкости со степенью использования АС данного контактного элемента, близкой к 100%. В отличие от данных ЭЗМА для КЭ алюмосиликатного состава, кроме пиков элементов, составляющих продукты хемосорбции, на диаграмме появляются пики характеристического рентгеновского излучения элементов из внешнего слоя керамической основы (Al, Si, O) и примесного Na, понижающие экспериментальное содержание Ag и I в активном слое по сравнению с расчетным.
Таблица 3.
Весовое содержание элементов в активном слое образца КЭ после хемосорбции иода
| Элемент | Содержание, мас. % | |||
|---|---|---|---|---|
| теоретическое | диаграмма | расчетное по данным РФА | ||
| AgI | Ag2INO3 | |||
| Ag | 46.0 | 53.3 | 29.2 | 48.5 |
| I | 54.0 | 31.4 | 25.8 | 46.3 |
| Al | 0.0 | 0.0 | 10.0 | 0.0 |
| Si | 0.0 | 0.0 | 4.7 | 0.0 |
| O | 0.0 | 11.9 | 28.3 | 4.0 |
| N | 0.0 | 3,4 | 1.7 | 1.2 |
| Na | 0.0 | 0.0 | 0.3 | 0.0 |
Эффективность улавливания I2 в форме AgI КЭ с активным слоем AgNO3 соответствует значениям суммарной эффективности улавливания CsI; сорбционная емкость испытуемых образцов находится в пределах 0.07–0.11 г/г, практически достигая своего максимума с учетом больших размеров КЭ; а рассчитанная по реакции (8) степень использования активного слоя составляет 70–98%. При расчете к приросту массы образца КЭ добавляется масса выделяющихся газообразных продуктов разложения нитрата серебра.
Газодинамическое сопротивление всей сборки реактора с 4 контактными элементами (рис. 2), равное перепаду давления на входе и выходе из него, при расходе газа-носителя 240 л/ч (линейная скорость потока 8 см/с) составляет 15 Па до начала эксперимента и 22 Па после улавливания CsI, а сопротивление незагруженного реактора – 7 Па. Полученные данные подтверждают одно из основных преимуществ КЭ на основе керамических ВПЯМ – минимальное сопротивление газовому потоку и высокую газопроницаемость, а также неизменность структуры и прочности блочно-ячеистого каркаса в процессе эксплуатации.
Раздельное улавливание радионуклидов цезия и иода контактными элементами с соответствующими сорбционно-активными слоями (Al2O3⋅4SiO2 и AgNO3), в отличие от улавливания аэрозолей CsI, позволяет дифференцировать образовавшиеся вторичные ТРО, содержащие радионуклиды цезия и иода, по классам опасности и определить технологии их дальнейшей иммобилизации. КЭ, насыщенные цезием, являются тепловыделяющими высокоактивными отходами (РАО I класса) [20] и предпочтительным методом организации их длительного хранения является упаковка в евробидоны с иммобилизацией расплавом стекломассы. Для насыщенных иодом КЭ, являющихся среднеактивными отходами (РАО II класса), рекомендуемая форма хранения – упаковка в стандартные контейнеры с иммобилизацией цементным компаундом.
ЗАКЛЮЧЕНИЕ
Синтезированные контактные элементы на основе керамических ВПЯМ с нанесенным алюмосиликатным активным слоем и активным слоем нитрата серебра показали высокую эффективность улавливания (97.8–99.6%) в процессах локализации оксида цезия и молекулярного иода, образовавшихся при разложении иодида цезия (степень диссоциации 85–100%) в окислительной среде. Динамическая сорбционная емкость разработанных КЭ достигает 0.31 г Cs2O/г КЭ и 0.11 г I2/г КЭ, что превышает емкость всех известных цезиевых и иодных твердых сорбентов. Показано, что набор сорбционной емкости по цезию до максимального значения возможен при повторном использовании частично отработавших КЭ.
Основными продуктами хемосорбции при оптимальных температурах 900 и 200°С, соответственно, являются поллуцит (CsAlSi2O6) и иодид серебра (AgI). При более низких температурах сорбционная емкость снижается, а в продуктах хемосорбции повышается содержание цезиевого нефелина – CsAlSiO4. При температуре 960°С и увеличении времени эксперимента наблюдается образование еще одного устойчивого алюмосиликата цезия высококремнеземной цеолитной структуры – CsAlSi5O12, а в образцах КЭ после улавливания иода в значимом количестве присутствует комплексное соединение – нитрат дисереброиода (Ag2INO3).
По результатам настоящего исследования поставлена задача дальнейшего повышения сорбционной емкости контактных элементов по изотопам Cs за счет повышения степени использования активного слоя и материала керамической основы до предела, ограниченного нормированной активностью и тепловыделением упаковок с кондиционированными отработавшими КЭ.
После оптимизации эксплуатационных характеристик и масштабирования к заданной производительности блочно-ячеистые КЭ нового поколения могут быть рекомендованы для применения в составе опытно-промышленных ЛСГО высокотемпературных операций в условиях эксплуатации модулей переработки ОЯТ. Их высокая сорбционная емкость с учетом рекомендаций по иммобилизации отработавших КЭ позволит значительно снизить количество вторичных ТРО.
Работа выполнена при поддержке Проектного направления “Прорыв”.
ОБОЗНАЧЕНИЯ
| A | динамическая сорбционная емкость, г/г КЭ (г/г АС) |
| C | концентрация CsI в газовом потоке, г/л |
| E | суммарная эффективность улавливания CsI всеми образцами сборки, % |
| W | объемный расход газа-носителя, л/ч |
| d | диаметр образца КЭ |
| h | высота образца КЭ |
| m | масса испарившегося CsI, г |
| ppi | количество пор на линейный дюйм |
| t | температура эксперимента, °C |
| τ | время проведения эксперимента, ч |
| η | степень использования активного слоя, % |
ИНДЕКСЫ
Список литературы
Очкин А.В., Бабаев Н.С., Магомедбеков Э.П. Введение в радиоэкологию. М.: ИздАТ, 2003.
Shin J.M., Park J.J., Song K.-Ch. Cesium Trapping Characteristics on Fly Ash Filter According to Different Carrier Gas // Proceedings of Intern. Conf. “Global’07”. Boise. Idaho, USA. 2007. P. 610.
Jae Hwan Yang, Joo Young Yoon, Ju Ho Lee, Yung-Zun Cho. A kaolinite-based filter to capture gaseous cesium compounds in off-gas released during the pyroprocessing head-end process // Annals of Nuclear Energy. 2017. V. 103. P. 29.
Баранов С.В., Баторшин Г.Ш., Максименко А.Д., Сизов П.В., Алой А.С., Стрельников А.В., Гаспарян М.Д., Грунский В.Н., Беспалов А.В. Алюмосиликатные фильтры для высокотемпературной хемосорбции паров цезия // Вопросы радиационной безопасности. 2013. № 1. С. 3.
Гаспарян М.Д., Грунский В.Н., Беспалов А.В., Магомедбеков Э.П., Попова Н.А. Керамические высокопористые блочно-ячеистые фильтры-сорбенты для улавливания паров цезия // Огнеупоры и техническая керамика. 2013. № 7–8. С. 3.
Гаспарян М.Д., Грунский В.Н., Беспалов А.В., Магомедбеков Э.П., Попова Н.А., Баранов С.В., Баторшин Г.Ш., Бугров К.В., Занора Ю.А., Истомин И.А., Степанов С.В., Макаров О.Н. Перспективы применения керамических высокопористых блочно-ячеистых фильтров-сорбентов газообразного радиоактивного цезия в решении вопросов обеспечения экологической безопасности производств атомной отрасли // Экология промышленного производства. 2014. № 1. С. 26.
Гаспарян М.Д. Локализация летучих радионуклидов на керамических высокопористых блочно-ячеистых материалах в процессах обращения с РАО и ОЯТ. Дис. … докт. техн. наук. М.: 2016.
Lewis B.J., Iglesias F.C., Cox D.S., Gheorghiu E.A. Model for Fission Gas Release and Fuel Oxidation Behavior for Defected UO2 Elements // Nuclear Technology. 1990. V. 92. P. 353.
Крюков Ф.Н., Кислый В.А., Кормилицын М.В., Кузьмин С.В., Маершин А.А., Никитин О.Н., Строжук С.В., Шишалов О.В. Распределение продуктов деления в облученном виброуплотненном оксидном топливе // Атомная энергия. 2005. Т. 99. № 5. С. 380.
Мазанников М.В., Потапов А.М., Вылков А.И., Суздальцев А.В., Зайков Ю.П. Способ окислительной обработки отработавшего нитридного ядерного топлива. Пат. 2775563 РФ. 2022.
Кулюхин С.А., Каменская А.Н., Михеев Н.Б., Мелихов И.В., Коновалова Н.А., Румер И.А. Химия радиоактивного йода в газовой среде: фундаментальные и прикладные аспекты // Радиохимия. 2008. Т. 50. № 1. С. 3.
Устинов О.А., Двоеглазов К.Н., Тучкова А.И., Шадрин А.Ю. Локальная система газоочистки при окислении отработавшего нитридного топлива // Атомная энергия. 2017. Т. 123. № 4. С. 203.
Грунский В.Н., Беспалов А.В., Гаспарян М.Д., Давидханова М.Г., Кабанов А.Н., Лукин Е.С., Попова Н.А., Харитонов Н.И. Синтез полифункциональных высокопористых блочно-ячеистых материалов на основе оксидной керамики // Огнеупоры и техническая керамика. 2016. № 6. С. 3.
Jin Myeong Shin, Jang Jin Park, Jae Won Lee, Sang Ho Na, Young Ja Kim, Geun IL Park. Design of Engineering Scale Off-Gas Trapping system at KAERI // Proceeding of GLOBAL 2011, Makuhari. Japan. Paper № 395956. P. 1.
Гаспарян М.Д., Грунский В.Н., Магомедбеков Э.П., Беспалов А.В., Игнатов А.В., Лебедев С.М. Локализация радиоактивного йодистого метила на керамических сорбентах // Огнеупоры и техническая керамика. 2011. № 11–12. С. 24.
Плющев В.Е., Степина С.Б., Федоров П.И. Химия и технология редких и рассеянных элементов. Часть I / Под ред. К.А. Большакова. М.: Высшая школа, 1976.
Scheer M.D., Fine G.J. Entropies, Heats of Sublimation, and Dissociation Energies of the Cesium Halides // J. Chem. Phys. 1962. V. 36. № 6. P. 1647.
Ровный С.И., Пятин Н.П., Истомин И.А. Улавливание 129I при переработке отработавшего ядерного топлива энергетических установок // Атомная энергия. 2002. Т. 92. № 6. С. 496.
Jae Hwan Yang, Joo Young Yoon, Seok-Min Hong, Ju Ho Lee,Yung-Zun Cho. An efficient capture of cesium from cesium iodide (CsI) off-gas by aluminosilicate sorbents in the presence of oxygen // J. Industrial and Engineering Chemistry. 2019. V. 77. P. 146.
Постановление Правительства РФ от 19 октября 2012 г. № 1069. О критериях отнесения твердых, жидких и газообразных отходов к радиоактивным отходам, критериях отнесения радиоактивных отходов к особым радиоактивным отходам и к удаляемым радиоактивным отходам и критериях классификации удаляемых радиоактивных отходов.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии