Теоретические основы химической технологии, 2023, T. 57, № 6, стр. 638-645
Разделение промышленной смеси продуктов фторирования декалина или нафталина. Физико-химические основы кристаллизации бинарных смесей цис- и транс-перфтордекалина и перфторбутилциклогексана
А. В. Полковниченко a, *, Н. Н. Кулов a, А. В. Кисель a, Н. Н. Курицын a, С. Я. Квашнин a, Е. В. Лупачев a, **
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
* E-mail: polkovnichenkoav@gmail.com
** E-mail: egorlu91@gmail.com
Поступила в редакцию 25.09.2023
После доработки 27.09.2023
Принята к публикации 29.09.2023
- EDN: IGHVCO
- DOI: 10.31857/S0040357123060179
Аннотация
Получены физико-химические данных о фазовых переходах жидкость–твердое в бинарных системах транс-перфтордекалин (транс-ПФД)–цис-перфтордекалин (циc-ПФД), транс-ПФД–перфторбутилциклогексан (БЦГ) и цис-ПФД–БЦГ. Все три системы характеризуются наличием температурного экстремума на диаграмме плавкости. Для системы транс-ПФД–БЦГ линия ликвидуса может быть описана уравнением для простых эвтектических систем при значениях коэффициента активности принятых $\gamma _{i}^{l}$ = 1, что говорит о поведении системы, близком к идеальному. На примере смеси цис-ПФД–БЦГ рассмотрен процесс объемной кристаллизации. Показано, что из смесей цис-ПФД–БЦГ с исходным содержанием ${{x}_{{цис{\text{ - ПФД}}}}}$ = 0.7348 и 0.6447 мол. д. за 3 цикла кристаллизации можно выделить цис-ПФД чистотой более 0.99 мол. д.
ВВЕДЕНИЕ
Перфтордекалин (ПФД) – перфторированный циклоалкан, нашедший широкое применение в медицине благодаря своим газорастворяющим свойствам. ПФД используется как компонент искусственной крови [1–3], в офтальмологии [4, 5], трансплантологии [6], при удалении татуировок [7, 8] и т.д. ПФД также применяют в водородной энергетике [9, 10], агрономии [11, 12], при производстве полимеров [13, 14]. ПФД имеет два пространственных изомера цис-ПФД и транс-ПФД; основным товарным продуктом является смесь цис- и транс-ПФД состава, близкого к эквимолярному.
В промышленности ПФД получают фторированием декалина или нафталина. Процесс характеризуется образованием большого количества примесей ввиду частичной деструкции углеродной цепи [2, 15]. Первичная очистка дистилляцией и промывка щелочными растворами позволяет получить ПФД-сырец с содержанием целевого товарного продукта (смеси цис- и транс-изомеров эквимолярного состава) около 93 маcс. % [15], что соответствует ТУ 95-1233-92.
Одним из эффективных методов получения ПФД высокой чистоты является кристаллизация [15, 16]. В [15] предложен метод получения ПФД чистотой более 99 маcс. % из ПФД-сырца. Было показано, что за одну ступень кристаллизации можно повысить чистоту ПФД с 93 до 97.2–98.2 маcс. %. Чистота более 99 маcс. % достигается за две ступени кристаллизации. В [16] предложен метод получения ПФД чистотой более 99.9 маcс. %. Авторы отмечают, что одним из факторов, снижающих эффективность кристаллизационной очистки перфторуглеродов, “является их низкая специфичность и энергия межмолекулярного взаимодействия, что облегчает встраивание молекул перфторированных примесей в решетку растущего кристалла”. С целью нивелировать этот эффект авторы [16] предлагают добавлять к разделяемой смеси растворители. В зависимости от используемого растворителя для получения ПФД чистотой 99.9 маcс. % из ПФД-сырца требовалось от 5 до 2 ступеней кристаллизации. Отмечается, что на каждой ступени кристаллизации происходит изменение соотношения цис-ПФД и транс-ПФД. Данный эффект также наблюдался в работе [17], где изучалась эффективность кристаллизационного разделения промышленных смесей цис-ПФД и транс-ПФД различного состава. Следует отметить, что в работах посвященных очистке ПФД, как кристаллизационными, так и другими методами, как правило ставится задача получения смеси цис-ПФД и транс-ПФД эквимолярного состава. Вопросы разделения цис- и транс-изомеров и выделения побочных продуктов реакции электрохимического фторирования декалина (например, перфторбутилциклогексана (БЦГ)) практически не изучались. Также стоит отметить, что решение задачи создания научно обоснованной технологии кристаллизационного разделения смесей невозможна при отсутствии физико-химических данных по равновесию жидкость–твердое. Для систем ПФД и его примесей такие данные в литературе отсутствуют.
Целью настоящей работы является получение физико-химических данных по фазовым переходам жидкость–твердое в бинарных системах транс-ПФД–цис-ПФД, транс-ПФД–БЦГ и цис-ПФД–БЦГ.
МАТЕРИАЛЫ И МЕТОДЫ
В качестве объекта исследования в настоящей работе рассмотрены три бинарных системы транс-ПФД–цис-ПФД, транс-ПФД–БЦГ и цис-ПФД–БЦГ. Используемые реактивы (транс-ПФД, цис-ПФД и БЦГ) были очищены методами гетероазеотропной ректификации и кристаллизации в лаборатории из фракций, полученных с производства. Чистоту цис-ПФД, транс-ПФД и БЦГ определяли с помощью газовой хроматографии (GC2010 Plus Shimadzu с пламенно-ионизационным детектором; капиллярная колонка Rtx-1701 12054; газ-носитель – азот). Содержание перфторированных и водородсодержащих примесей дополнительно контролировалось методом ЯМР-спектроскопии (BrukerAVANCE-300 radiospectrometer) по 19F, 1Н спектрам. Чистота реактивов, используемых в настоящей работе, приведена в табл. 1.
Таблица 1.
Сведения об используемых веществах
| Вещество | CAS | Источник | Чистота ГХа, ЯМРb, маcс. д. |
Содержание воды КФc, маcс. д. |
|---|---|---|---|---|
| цис-перфтордекалин | 60433-11-6 | Очищено в лаборатории | >0.996a, b | |
| транс-перфтордекалин | 60433-12-7 | >0.998a, b | <0.000015 | |
| Перфторбутилциклогексан | 374-60-7 | >0.997a, b | ||
| Четыреххлористый углерод | 56-23-5 | Sigma-Aldrich | >0.995a | <0.00002 |
| Диметилсульфоксид | 67-68-5 | AlfaAesar | >0.999a | <0.001 |
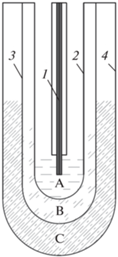
Для определения температуры плавления (Тп) исследуемых образцов использовали метод визуально-политермического анализа [18–20]. Эксперименты проводили на установке, представленной на Рис. 1. Образец А заливают во внутреннюю пробирку 2 с термометром 1, которую помещают в пробирку 3 большего диаметра, наполненную хладоносителем B. В качестве хладоносителя использовался медицинский спирт. Обе пробирки вместе опускают в сосуд Дьюара 4 с хладагентом С (сухой лед или жидкий азот) и охлаждают. После полной кристаллизации раствор постепенно нагревают при перемешивании. Контроль скорости нагревания образца А осуществляется путем изменения глубины погружения пробирки 2 в пробирку 3. Температура исчезновения последних кристаллов принимается за температуру плавления образца. Фиксация момента исчезновения последнего кристалла осуществляется визуально.
Рис. 1.
Установка для определения температуры плавления жидкостей методом визуально-политермического анализа. 1 – термометр, 2 – внутренняя пробирка, 3 – внешняя пробирка, 4 – сосуд Дьюара, А – исследуемый образец, B – хладоноситель, C– хладагент.
Для системы цис-ПФД–БЦГ проведена серия опытов по объемной кристаллизации. Исходный образец (f) в круглодонной колбе помещался в морозильный ларь Vestfrost HF 396 и выдерживался в течение 16 ч при постоянной температуре (Ткр). Далее для разделения жидкой (l) и кристаллической (s) фракций сосуд с образцом переворачивали, и оставляли стекать жидкую фазу в приемник при той же температуре (Ткр) в течение 8 ч. Полученные жидкая и кристаллическая фракции взвешивались и анализировались методом ЯМР по спектру 19F. Полученная твердая фракция отправлялась на следующую ступень кристаллизации при более высокой температуре.
Для приготовления образцов и определения массы фракций использовали компаратор массы AND МС-1000 с величиной стандартного отклонения u(m) = ±0.0005 г. Для определения температуры использовали спиртовой термометр Labortherm-N (–89…+35°C; цена деления 1°С) с величиной стандартного отклонения u(T) = ±1°С. Все эксперименты проводились при атмосферном давлении.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Апробация метода визуально-политермического анализа осуществлялась сравнением результатов измерения Тп чистых веществ (транс-ПФД, цис-ПФД, БЦГ, диметилсуьфоксида (ДМСО) и четыреххлористого углерода (CCl4)) с литературными данными. Результаты апробации приведены в табл. 2.
Результаты измерения температуры плавления бинарных смесей транс-ПФД–цис-ПФД, транс-ПФД–БЦГ, цис-ПФД–БЦГ методом визуально-политермического анализа представлены в табл. 3.
Таблица 3.
Данные о температуре плавления бинарных смесей перфторированных циклоалканов a
| транс-ПФД (1)–цис-ПФД (2) | транс-ПФД (1)–БЦГ (2) | цис-ПФД (1)– БЦГ (2) | |||
|---|---|---|---|---|---|
| Tп, °С | x1, мол. д. | Tп, °С | x1, мол. д. | Tп, °С | x1, мол. д. |
| –5.7 | 0 | –39.5 | 0 | –39.5 | 0 |
| –6.5 | 0.0965 | –42.2 | 0.0500 | –49.3b | 0.0998 |
| –8.5 | 0.1989 | –47.8 | 0.1000 | –52.0b | 0.1472 |
| –9.0 | 0.2543 | –48.0 | 0.0973 | –56.5b | 0.1999 |
| –8.0 | 0.3438 | –40.7 | 0.1494 | –64.0b | 0.2986 |
| –7.0 | 0.3928 | –31.8 | 0.2000 | –75.0b | 0.3496 |
| –7.0 | 0.3998 | –20.2 | 0.3008 | –61.0b | 0.3933 |
| –5.5 | 0.4759 | –10.0 | 0.4001 | –54.0b | 0.3998 |
| –2.4 | 0.5313 | –3.1 | 0.5001 | –46.5 | 0.4499 |
| –1.5 | 0.5313 | 3.5 | 0.5990 | –42.5 | 0.4835 |
| 1.5 | 0.5867 | 8.7 | 0.7001 | –41.0 | 0.4908 |
| 3.5 | 0.6000 | 14.5 | 0.8001 | –31.3 | 0.6103 |
| 7.0 | 0.6421 | 18.0 | 0.9001 | –23.0 | 0.7037 |
| 14.1 | 0.7806 | 20.0 | 0.9008 | –17.0 | 0.8022 |
| 18.5 | 0.8914 | 20.5 | 0.9501 | –12.0 | 0.9009 |
| 23.3 | 1 | 23.3 | 1 | –5.7 | 1 |
Для бинарных смесей, характеризующихся наличием точки эвтектики, линия ликвидуса может быть описана уравнением, предложенным в [25, 26]:
(1)
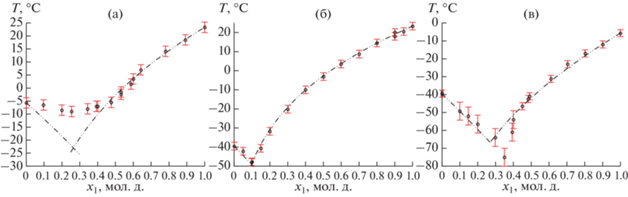
$\ln x_{i}^{l}\gamma _{i}^{l} = - \frac{{\Delta {{h}_{{п,i}}}}}{{R({{T}_{п}} + 273.15)}}\left( {1 - \frac{{({{T}_{п}} + 273.15)}}{{({{T}_{{п,i}}} + 273.15)}}} \right),$Сравнение экспериментальных (табл. 3) и рассчитанных по уравнению (1) данных о температуре плавления систем транс-ПФД–цис-ПФД, транс-ПФД–БЦГ, цис-ПФД–БЦГ приведены на рис. 2. При расчете линии ликвидуса по уравнению (1) использовали значения ${{T}_{{п,i}}}$ и $\Delta {{h}_{{п,i}}}$ представленные в табл. 4; значения коэффициента активности приняты $\gamma _{i}^{l}$ = 1.
Рис. 2.
Данные о температуре плавления бинарных смесей перфторированных циклоалканов. (а) транс-ПФД (1)–цис-ПФД (2); (б) транс-ПФД (1)–БЦГ (2); (в) цис-ПФД (1)–БЦГ (2). Точки – экспериментальные данные (табл. 3); линия – данные, рассчитанные по уравнению (1) при значениях $\gamma _{i}^{L}$ = 1.
Результаты опытов по объемной кристаллизации системы цис-ПФД–БЦГ представлены в табл. 5 и на рис. 3. Коэффициент разделения $D_{i}^{{s/l}}$ был рассчитан по уравнению (2):
(2)
$\begin{array}{*{20}{c}} {D_{{ij}}^{{s/l}} = \frac{{{{x_{i}^{s}} \mathord{\left/ {\vphantom {{x_{i}^{s}} {x_{i}^{l}}}} \right. \kern-0em} {x_{i}^{l}}}}}{{{{x_{j}^{s}} \mathord{\left/ {\vphantom {{x_{j}^{s}} {x_{j}^{l}}}} \right. \kern-0em} {x_{j}^{l}}}}},} \end{array}$Таблица 5.
Данные по объемной кристаллизации смеси цис-ПФД (1)–БЦГ (2)a
| Ступень | № образца | m, г | x1, мол. д. | T, °C | $D_{{{\text{12}}}}^{{s/l}}$ | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| f | s | l | Δb | f | s | l | ||||
| I | 1 | 937.6807 | 419.5862 | 515.6422 | 2.4523 | 0.7252 | 0.8999 | 0.5107 | –41 | 8.61 ± 0.09 |
| 2 | 902.2457 | 264.6432 | 636.1401 | 1.4624 | 0.6452 | 0.9124 | 0.5368 | 8.99 ± 0.11 | ||
| II | 1 | 415.6284 | 182.3990 | 230.6872 | 2.5422 | 0.8999 | 0.9770 | 0.8551 | –18 | 7.20 ± 0.32 |
| 2 | 257.2539 | 130.2236 | 127.5417 | –0.5114 | 0.9124 | 0.9643 | 0.8370 | 5.26 ± 0.15 | ||
| III | 1 | 178.8020 | 94.1850 | 84.1200 | 0.4970 | 0.9770 | 0.9932 | 0.9560 | –14 | 6.72 ± 1.00 |
| 2 | 127.1754 | 46.6252 | 79.6021 | 0.9481 | 0.9643 | 0.9939 | 0.9483 | 8.88 ± 1.47 | ||
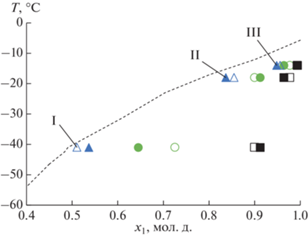
Рис. 3.
Результаты эксперимента по объемной кристаллизации смеси цис-ПФД (1) – БЦГ (2). Линия – линия ликвидуса (табл. 3). Точки – данные по объемной кристаллизации (табл. 5).  – состав жидкой фазы; $\square $ – состав кристаллической фазы;
– состав жидкой фазы; $\square $ – состав кристаллической фазы;  – состав исходной смеси. Не закрашено – образец 1; закрашено – образец 2. Римские
цифры – номер ступени кристаллизации.
– состав исходной смеси. Не закрашено – образец 1; закрашено – образец 2. Римские
цифры – номер ступени кристаллизации.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В [22] Тп БЦГ определялась методом дифференциальной сканирующей калориметрии (ДСК). За Тп в [22] принята точка начала теплового эффекта при нагревании образца –45.31°С; пик теплового эффекта при плавлении приходится на ‒40.40°С, конец – на –37.95°С. Согласно данным табл. 2 для БЦГ Тп = –39.5°С, что согласуется со значением температуры для пика теплового эффекта плавления, полученного в работе [22]. По аналогии с БЦГ, данные, полученные в настоящей работе для транс-ПФД (Тп = 23.3°С) и цис-ПФД (Тп = –5.7°С) методом визуально-политермического анализа, также соответствуют пику теплового эффекта плавления ДСК ($T_{{{\text{пик}}}}^{{{\text{ДСК}}}}$ = 23.55°С для транс-ПФД; $T_{{{\text{пик}}}}^{{{\text{ДСК}}}}$ = –5.44°С для цис-ПФД – собственные неопубликованные данные). Для CCl4 и ДМСО экспериментальные и литературные данные по температуре плавления хорошо согласуются. Таким образом, разница в измеренных методами визуально-политермического анализа и ДСК значениях может быть обусловлена различиями этих методов. Стоит отметить и отличие в чистоте БЦГ, используемого в настоящей работе и в работе [22].
Согласно данным табл. 3 и рис. 2 линия ликвидуса во всех трех исследуемых системах (транс-ПФД–цис-ПФД, транс-ПФД–БЦГ и цис-ПФД–БЦГ) имеет минимум температуры плавления.
Для системы транс-ПФД–цис-ПФД минимум соответствует температуре –9.0°С при ${{x}_{{транс{\text{ - ПФД}}}}}$ = = 0.2543 мол. д.; в области низких концентраций транс-ПФД экспериментальные данные лежат выше значений, рассчитанных по уравнению (1) для случая идеальной эвтектической системы (рис. 2а). Вид линии ликвидус в системе транс-ПФД–цис-ПФД объясняет наблюдаемое в [17] концентрирование цис-ПФД, вещества с более низкой температурой плавления, в кристаллической фазе при низких концентрациях транс-ПФД. Минимум температур плавления, наблюдаемый в системе транс-ПФД–цис-ПФД, разбивает концентрационный диапазон на две области. В области концентраций 0 < хтранс-ПФД < < 0.25–0.3 мол. д. тугоплавким является цис-изомер, а в области концентраций 0.25–0.3 < хтранс-ПФД < < 1 мол. д. тугоплавким является транс-изомер.
Для системы транс-ПФД–БЦГ линия ликвидуса, рассчитанная по уравнению (1), хорошо согласуется с экспериментальными данными табл. 3 для всего концентрационного диапазона (рис. 2б); минимум соответствует температуре –48.0°С при ${{x}_{{транс{\text{ - ПФД}}}}}$ = 0.0973 мол. д.
Для системы цис-ПФД–БЦГ в диапазоне концентраций 0 < ${{x}_{{цис{\text{ - ПФД}}}}}$ < 0.5 мол. д. наблюдается повышение вязкости с образованием гелеобразной структуры при охлаждении смеси ниже ‒50°С. При этом, кристаллизация происходит только после существенного переохлаждения образца ($\left| {\left. {T - {{T}_{{{\text{кр}}}}}} \right|} \right.$ > 25°C). При нагревании этих образцов также образуется гелеобразная структура с вкраплениями кристаллов и пузырьков воздуха, что существенно затрудняет визуальную фиксацию момента плавления последнего кристалла (рис. 4). Как следствие, это приводит к снижению точности определения температуры плавления образца. Образование гелеобразной структуры может быть вызвано наличием фазового перехода твердое–твердое у цис-ПФД [21].
Рис. 4.
Процесс плавления смеси цис-ПФД (1)–БЦГ (2) состава ${{x}_{1}}$ = 0.1999 мол. д. (табл. 3): (а) –65; (б) –59; (в) –56°С.

Для системы цис-ПФД–БЦГ минимум температуры соответствует –75.0°С при ${{x}_{{цис{\text{ - ПФД}}}}}$ = = 0.3496 мол. д.; вид линии ликвидуса по данным табл. 3 существенно отклоняется от рассчитанного по уравнению (1) в области температурного экстремума (рис. 2в).
Согласно данным табл. 5 составы жидкой фазы, полученные в процессе объемной кристаллизации, согласуются с экспериментальным данными о фазовом переходе жидкость–твердое (табл. 3) в системе цис-ПФД–БЦГ (рис. 4). При этом, во всех экспериментах жидкая фаза, полученная в процессе объемной кристаллизации, содержит меньше легкоплавкого компонента, чем составы, определенные методом визуально-политермического анализа при тех же температурах. Это характерно для процесса объемной кристаллизации и может быть обусловлено захватом маточного раствора при кристаллизации и попаданием мелких кристаллов в жидкость при разделении фаз.
Стоит отметить, что наличие экстремума является термодинамическим ограничением на процесс кристаллизационного разделения. В то же время, кристаллизация может быть эффективной при разделении смесей с составом, отличающимся от эвтектического. Так из смесей цис-ПФД– БЦГ с исходным содержанием ${{x}_{{цис{\text{ - ПФД}}}}}$ = 0.7348 и 0.6447 мол. д. за 3 цикла удалось выделить цис-ПФД чистотой более 0.99 мол. д. (табл. 5, рис. 3).
ЗАКЛЮЧЕНИЕ
В настоящей работе получены физико-химические данныe о фазовых переходах жидкость-твердое в бинарных системах транс-ПФД–цис-ПФД, транс-ПФД–БЦГ и цис-ПФД–БЦГ. Все три системы характеризуются наличием температурного экстремума на диаграмме плавкости. Для системы транс-ПФД–БЦГ линия ликвидуса может быть описана уравнением для простых эвтектических систем при значениях коэффициента активности принятых $\gamma _{i}^{l}$ = 1, что говорит о поведении системы, близком к идеальному.
Наличие температурного экстремума на линии ликвидуса в системах транс-ПФД–цис-ПФД, транс-ПФД–БЦГ и цис-ПФД–БЦГ является термодинамическим ограничением на процесс кристаллизационного разделения. Эффекты, которыми сопровождается кристаллизация смеси цис-ПФД – БЦГ при температурах ниже ‒50°С (гелеобразные структуры), являются техническими ограничениями при организации процесса. В то же время, на примере процесса объемной кристаллизации смеси цис-ПФД–БЦГ показано, что данный метод может быть эффективным при разделении смесей, с составом отличающимся от эвтектического. Так из смесей цис-ПФД–БЦГ с исходным содержанием ${{x}_{{цис{\text{ - ПФД}}}}}$ = = 0.7348 и 0.6447 мол. д. за 3 цикла кристаллизации удалось выделить цис-ПФД чистотой более 0.99 мол. д. Если рассматривать в качестве исходной смеси 93 маcс. %. ПФД-сырец, кристаллизация позволяет очистить ПФД от БЦГ и других близкокипящих примесей [15, 16]. В [17] также показана эффективность данного метода для исходных смесей других составов.
Исследование выполнено за счет гранта Российского научного фонда № 22-29-00791, https://rscf.ru/project/22-29-00791/.
ЯМР исследования проводились с использованием оборудования ЦКП ФМИ ИОНХ РАН (The NMR analytic was performed using the equipment of the JRC PMR IGIC RAS). Титрование по Карлу-Фишеру проводилось с использованием оборудования ЦКП “Исследовательский химико-аналитический центр НИЦ “Курчатовский институт”.
ОБОЗНАЧЕНИЯ
| БЦГ | перфторбутилциклогексан |
| ДМСО | диметилсульфоксид |
| ДСК | дифференциальная сканирующая калориметрия |
| цис-ПФД | цис-перфтордекалин |
| транс-ПФД | транс-перфтордекалин |
| CCl4 | четыреххлористый углерод |
| D | коэффициент разделения |
| m | масса, г |
| T | температура, °С |
| u | стандартное отклонение |
| x | состав, мол. д. |
| ∆ | погрешность материального баланса, г |
| $\Delta {{h}_{{п,i}}}$ | энтальпия плавления, Дж/моль |
| γ | коэффициент активности |
ИНДЕКСЫ
Список литературы
Maevsky E., Ivanitsky G., Bogdanova L., Aksenova O., Karmen N., Zhiburt E., Senina R., Pushkin S., Maslennikov I., Orlov A., Marinicheva I. Clinical Results of Perftoran Application: Present and Future. Artif. Cells Nanomed. Biotechnol. 2005. V. 33. P. 37–46.https://doi.org/10.1081/BIO-200046654
Gervits L.L. Perfluorocarbon-based blood substitutes Russian experience. In Fluorine in Medicine in the 21st Century; UMIST: Manchester, UK, 1994. P. 1–9.
Julia Laudien, Christoph Groß-Heitfeld, Christian Mayer, Herbert de Groot, Michael Kirsch, Katja B Ferenz Perfluorodecalin-Filled Poly(n-butyl-cyanoacrylate) Nanocapsules as Potential Artificial Oxygen Carriers: Preclinical Safety and Biocompatibility // J. Nanosci. Nanotechnol. 2015. V. 15. № 8. P. 5637–5648. https://doi.org/10.1166/jnn.2015.10044
Caporossi T., De Angelis L., Pacini B., Rizzo S. Amniotic membrane for retinal detachment due to paravascular retinal breaks over patchy chorioretinal atrophy in pathologic myopia. European J. Ophthalmology. 2020. V. 30(2). P. 392–395. https://doi.org/10.1177/1120672119891415
Papastavrou V.T., Chatziralli I., McHugh,D. Gas Tamponade for Retinectomy in PVR-Related Retinal Detachments: A Retrospective Study. OphthalmolTher 6, 161–166 (2017). https://doi.org/10.1007/s40123-017-0078-6
Schaschkow A., Mura C., Bietiger W., Peronet C., Langlois A., Bodin F., Dissaux C., Bruant-Rodier C., Pinget M., Jeandidier N., Juszczak M.T., Sigrist S., Maillard E. Impact of an autologous oxygenating matrix culture system on rat islet transplantation outcome // Biomaterials. 2015. V. 52. P. 180–188. https://doi.org/10.1016/j.biomaterials.2015.02.031
Vangipuram R., Hamill S.S., Friedman P.M. Perfluorodecalin-infused patch in picosecond and Q-switched laser-assisted tattoo removal: Safety in Fitzpatrick IV–VI skin types. Lasers Surg. Med., (2019), 51: 23–26. https://doi.org/10.1002/lsm.23022
Torbeck R.L., Saedi N. Optimization of Laser Tattoo Removal: Optical Clearing Agents and Multiple Same-Day Treatments via the R0 and R20 Methods. CurrDerm Rep 5, 136–141 (2016). https://doi.org/10.1007/s13671-016-0139-4
Bin Tian, Baojun Yang, Jian Li, Zhen Li, Wenlong Zhen, Yuqi Wu, Gongxuan Lu. Water splitting by CdS/Pt/WO3-CeOx photocatalysts with assisting of artificial blood perfluorodecalin // J. Catalysis. V. 350. 2017. P. 189–196. https://doi.org/10.1016/j.jcat.2017.03.012
Wei Gao, Wenyan Zhang, Gongxuan Lu. A two-pronged strategy to enhance visible-light-driven overall water splitting via visible-to-ultraviolet upconversion coupling with hydrogen-oxygen recombination inhibition // Applied Catalysis B: Environmental. V. 212. 2017. P. 23–31. https://doi.org/10.1016/j.apcatb.2017.04.063
Kirchhelle C., Moore I. A Simple Chamber for Long-term Confocal Imaging of Root and Hypocotyl Development. J. Vis. Exp. (123), e55331, (2017). https://doi.org/10.3791/55331
Sykłowska-Baranek K., Rymaszewski W., Gaweł M., Rokicki P., Pilarek M., Grech-Baran M., Hennig J., Pietrosiuk A. Comparison of elicitor-based effects on metabolic responses of Taxus × media hairy roots in perfluorodecalin-supported two-phase culture system. Plant Cell Rep 38, 85–99 (2019). https://doi.org/10.1007/s00299-018-2351-0
Romain Lhermerout, Kristina Davitt. Contact angle dynamics on pseudo-brushes: Effects of polymer chain length and wetting liquid // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2019. V. 566. P. 148–155. https://doi.org/10.1016/j.colsurfa.2019.01.006
Bo Song, Kun Hu, Anjun Qin, Ben Zhong Tang. Oxygen as a Crucial Comonomer in Alkyne-Based Polymerization toward Functional Poly(tetrasubstituted furan)s // Macromolecules. 2018. V. 51 (18). P. 7013–7018. https://doi.org/10.1021/acs.macromol.8b01293
Bispen T.A., Kochnev A.D., Moldavskij D.D., Sergeeva A.A. Method of purifying perfluorodecalin, 2015. RU 2544849 C1. Published online. 2015.
Gorelenko S., Zachesova U.V., Osipov G.N., Kazakov P.V., Mirzabekova N.S., Eleev A.F. Preparation of the high purity perfluorodecalin // Fluorine Notes. 2016. V. 5. P. 3.
Kisel A.V., Polkovnichenko A.V., Lupachev E.V., Kuritsyn N.N., Kvashnin S.Y., Kulov N.N. The Process of Isolation, Using Crystallization of Cis- and Trans-Isomers, of Perfluorodecalines from an Industrial Mixture of Electrochemical Fluorination of Napthaline. Eng. Proc. 2023. V. 37. P. 85. https://doi.org/10.3390/ECP2023-14640
Бергман А.Г., Лужная Н.П. Физико-химические основы изучения и использования соляных месторождений хлорид-сульфатного типа / Акад. наук СССР. Ин-т общей неорган. химии им. Н.С. Курнакова. Москва : Изд-во Акад. наук СССР, 1951.
Данилов В.П., Фролова Е.А., Кондаков Д.Ф., Авдюшина Л.И., ОрловаВ.Т. Поиск низкотемпературных противогололедных композиций в водно-солевой системе Ca(NО3)2–Mg(NО3)2–Н2О и исследование их свойств // Химическая технология. 2010. Т. 11. № 4. С. 193–198.
Seregin V.O., Pestov S.M., Zubairov R.M. Phase equilibria in 4-pentyloxybenzoic acid - long-chain n-alkane systems // Fine Chemical Technologies. 2019. V. 14(6). P. 66–75. https://doi.org/10.32362/2410-6593-2019-14-6-66-75
Domalski E.S., Hearing E.D. Heat Capacities and Entropies of Organic Compounds in the Condensed Phase. Volume III. J Phys. Chem. Ref. Data. 1996. V. 25. P. 1–525. https://doi.org/10.1063/1.555985
Polkovnichenko A.V., Lupachev E.V., Kisel’ A.V., Kvashnin S.Ya., Kulov N.N. Perfluoro(7-Methylbicyclo[4.3.0]Nonane) and Perfluoro(Butylcyclohexane): Physicochemical, Thermophysical, and Spectral Data // J. Chem. Eng. Data. 2023. V. 68. № 3. P. 499–517. https://doi.org/10.1021/acs.jced.2c00588
Morrison J.A. Richards E.J. Thermodynamic study of phase transitions in carbon tetrachloride // J. Chem. Thermodynam., 1976. V. 8. P.1033-1038. https://doi.org/10.1016/0021-9614(76)90134-8
Williams M. The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals, 15th Edition / Ed. O’Neil M.J. Cambridge, UK: Royal Society of Chemistry. 2013. p. 2708. ISBN 9781849736701
Yalkowsky S.H., Wu M. Estimation of the ideal solubility (crystal–liquid fugacity ratio) of organic compounds // J. Pharmaceutical Sciences. 2010. V. 99. № 3. P. 1100–1106. https://doi.org/10.1002/jps.21897
Alhadid A., Mokrushina L., Minceva M. Formation of glassy phases and polymorphism in deep eutectic solvents // J. Molecular Liquids. 2020. V. 314. P. 113667. https://doi.org/10.1016/j.molliq.2020.113667
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии


