Высокомолекулярные соединения (серия А), 2020, T. 62, № 2, стр. 128-137
НАНЕСЕНИЕ ХИТОЗАНОВОГО ПОКРЫТИЯ НА ПОРИСТЫЕ МАТРИЦЫ CELGARD В ПРИСУТСТВИИ ДИОКСИДА УГЛЕРОДА ПОД ДАВЛЕНИЕМ
В. В. Зефиров a, c, М. А. Пигалёва a, c, В. Г. Сергеев b, М. О. Галлямов a, c, *
a Московский государственный университет имени М.В. Ломоносова. Физический факультет
119991 Москва, Ленинские горы, 1, Россия
b Московский государственный университет имени М.В. Ломоносова. Химический факультет
119991 Москва, Ленинские горы, 1, Россия
c Институт элементоорганических соединений им. А.Н. Несмеянова Российской академии наук
119991 Москва, ул. Вавилова, 28, Россия
* E-mail: glm@spm.phys.msu.ru
Поступила в редакцию 03.07.2019
После доработки 01.09.2019
Принята к публикации 15.10.2019
Аннотация
Показано, что из растворов хитозана в воде, насыщенной диоксидом углерода под высоким давлением, т.е. при формировании угольной кислоты, можно наносить хитозановое покрытие на поверхность пор полиолефиновых матриц Celgard. Для обеспечения стабильности покрытия исходно гидрофобные матрицы следует предварительно обрабатывать в присутствии пероксиугольной кислоты, образующейся при насыщении водного раствора пероксида водорода диоксидом углерода при высоком давлении. Морфология нанесенного покрытия изучена методами микроскопии высокого разрешения. Привнесенные гидрофильные свойства оценены по изменению характера смачивания поверхности матриц водой. Установлено, что модифицированная хитозаном гидрофилизованная матрица, несмотря на более низкий характерный размер пор, имеет в ~1.5 раза более высокую проницаемость по отношению к воде, чем исходная матрица.
ВВЕДЕНИЕ
Задача модификации свойств поверхности исходно гидрофобных полиолефинов вообще и полипропилена актуальна в самых различных отраслях современной химической технологии, особенно для пористых материалов. Последние оказываются широко востребованными в качестве разделительных мембран. Методы модификации поверхностей пористых матриц, в частности, с целью их гидрофилизации [1], известны и систематизированы в ряде обзоров [1–3]. Подчеркивается, что выпускаемые сегодня промышленностью материалы мембран являются по большей части поверхностно-модифицированными [3].
Хитозан используют для модификации поверхности весьма широко (материалы для фильтрационных, каталитических и газоразделительных мембран, пористых матриц для электролита в электрохимических источниках тока, и т.д. [4]). Хитозановое покрытие влияет на природу взаимодействия того или иного компонента смешанной флюидной (жидкой или газообразной) системы со стенками пор матрицы. За счет этого оно определяет баланс транспортных свойств (селективность фильтрации [5, 6]), а также долговременную устойчивость материала к загрязнениям, в том числе биологического происхождения, чему часто подвержены гидрофобные поверхности ПП [7]. Пленка хитозана может служить адгезивом для других функциональных агентов, например, при создании на основе пористого ПП каталитических [8] и фотокаталитических [9] мембран.
В некоторых электрохимических источниках тока в настоящее время традиционными материалами являются пористые мембраны Celgard и их аналоги, обладающие комплексом оптимальных характеристик при использовании в качестве матриц для электролита (разделителей для электродов) [10]. Так, в металл-ионных аккумуляторах, широко производящихся промышленностью, наиболее востребованы матрицы Celgard трехслойной структуры ПП–ПЭ–ПП [11]. В такой геометрии роль центральной полиэтиленовой прослойки сэндвича состоит в обеспечении безопасности в случае неконтролируемого повышения температуры устройства при его выходе из строя. Слой ПЭ при нагревании в определенный момент плавится и плотно блокирует поры еще не расплавленной ПП-части композита, тем самым останавливая электрохимическую реакцию [11]. Однако хорошо зарекомендовавшие себя в литий-ионных аккумуляторах с неводными электролитами гидрофобные пористые матрицы, смачивающиеся такими электролитами, но не смачивающиеся полярными средами, не в полной мере удовлетворяют критериям работоспособности в электрохимических источниках тока некоторых других типов (топливные элементы, проточные батареи), но могут быть адаптированы и для этих задач [12]. При использовании редокс-активных макромолекул они применимы для проточных батарей без какой-либо модификации [13]. В литературе описаны примеры контролируемого уменьшения размера пор в матрицах Celgard для обеспечения селективности ионного транспорта в проточных батареях [14, 15]. Также доступные матрицы типа Celgard успешно модифицируются для использования в новых перспективных источниках тока, например, Li–S-батареях [16]. Применительно к топливным элементам удерживание фосфорнокислотного электролита в пористых полиолефиновых матрицах может быть обеспечено кремнеземными включениями, модифицированными по поверхности амфифильными реакционноспособными добавками, имеющими сродство к электролиту [17]. Помимо химически связываемых низкомолекулярных добавок перспективно нанесение полиэлектролитов, создающих требуемую стабильность за счет электростатического взаимодействия и их высокомолекулярной природы [18].
В связи с этим большое внимание привлекает модификация пористых исходно гидрофобных матриц хитозаном. Хитозан, несмотря на то, что является природным, а не синтетическим полимером, проявляет требуемую высокую стабильность в электрохимических источниках тока [19]. В частности, хитозан рассматривается как возможный материал для модификации мембран проточных ванадиевых батарей [20, 21]. Известны работы, где обсуждается перспективность полного отказа от синтетических полимерных материалов в коммерциализованных батарейках в пользу природных, включая хитозан, в силу все возрастающих потребностей промышленности в плане масштабов их производства и связанных с этим рисков для экологии [22]. Утверждается, что большие объемы расходования пористого ПП уже делают целесообразным переход к природному сырью с точки зрения экологически рационального развития возобновляемых источников энергии [22]. Действительно, сама концепция альтернативной энергетики подразумевает необходимость учета экологических факторов и при производстве материалов для химических источников тока, служащих звеньями в цепи передачи энергии конечному потребителю: топливных элементов, проточных батарей, новых типов аккумуляторов и т.п.
В медицине ПП также является широко востребованным материалом, однако гидрофобность его поверхности способствует адсорбции белков и последующему заселению бактериями [23]. Нежелательную гидрофобность поверхности ПП можно устранять нанесением ряда биоактивных соединений [24], включая хитозановые покрытия, привносящие биоцидный эффект [25, 26].
В задачах разделения необходима селективность пористой мембраны. Селективность массопереноса в пористой структуре можно контролировать и модифицировать, в том числе варьированием размера (диаметра) пор за счет нанесения покрытий [2]. Удобным инструментом здесь является послойное нанесение поликатион-полианионных слоев, позволяющее достигать высокой степени контролируемости [27]. Мембраны Celgard могут служить основой для создания подобных композитов [28].
При нанесении хитозановых пленок на ПП последний подвергают предварительной обработке, например, плазмой [29, 30] или химическими окислительно-активными реагентами, такими как персульфаты [31, 32]. В противном случае адгезия хитозанового покрытия к немодифицированной гидрофобной поверхности ПП оказывается недостаточной. Оба подхода к предобработке оптимальны при работе с гладкими поверхностями, но не позволяют однородно модифицировать стенки пор пористых материалов.
Недавно была предложена процедура предобработки пористых ПП матриц Celgard в пероксиугольной кислоте, формируемой при насыщении водного раствора пероксида водорода диоксидом углерода под высоким давлением [33–35 ]. Эта среда характеризуется выраженной окислительной способностью, превосходящей, согласно литературным данным, таковую для исходного пероксида вследствие формирования более окислительно-активной пероксиугольной кислоты: H2O2 + CO2 → HOCOOOH [36]. Такая модификация позволила создать якорные группы на поверхности пор, для последующей более прочной фиксации органического (полидопамин) [33] и неорганического (кремнезем) [34, 35] материалов. Полученные композиты перспективны при использовании в проточных батареях. Важно отметить, что используемый модифицирующий агент (пероксиугольная кислота) самонейтрализуется при декомпрессии [36]. Данное обстоятельство может быть важным и для медицины, и для электрохимии, поскольку здесь требуются высокая степень чистоты материалов и отсутствие остаточных следов посторонних агентов (модификаторов или их нейтрализаторов).
Кроме того, был предложен метод модификации протезов клапанов сердца с помощью нанесения хитозана из раствора в угольной кислоте, также формируемой при насыщении воды диоксидом углерода под давлением [37, 38]. Такой подход позволил повысить биосовместимость, антимикробные свойства и устойчивость к деградационным процессам кальцификации данных материалов в организме.
В развитие этого подхода в настоящей работе исследуется возможность модификации хитозановым покрытием пористых ПП-матриц Celgard. По аналогии с разработанным ранее методом, матрицы также должны подлежать предобработке в пероксиугольной кислоте для лучшей адгезии хитозанового покрытия. Нанесение слоя хитозана, поликатиона, на предварительно окисленную в пероксиугольной кислоте полианионную поверхность ПП моделирует первый этап возможного последующего формирования поликатион-полианионных покрытий методом послойного нанесения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы
Для образования растворов угольной и пероксиугольной кислот использовали диоксид углерода (99.995%, Московский газоперерабатывающий завод), водный раствор перекиси водорода (≥35%, “Sigma-Aldrich”), а также очищенную воду, свежеприготовленную на установке “Milli-Q Synthesis” (“Millipore”). Такая же вода служила для промывки мембран и измерений краевого угла.
В качестве мембраны применяли пористый материал Celgard® H2512 толщиной 25 мкм, который, по информации производителя (“Celgard”, LLC, США), представляет собой трехслойную структуру ПП–ПЭ–ПП и имеет пористость 50%. Перед экспериментом образцы очищали ацетоном.
Для нанесения покрытий использовали хитозан сорта medium molecular weight, № 448877 (“Aldrich”).
Методы
Процедура предварительной обработки в пероксиугольной кислоте. Перед модификацией исходные образцы Celgard размером 3 × 3 см2 или 5 × 5 см2 помещали в изопропиловый спирт для начального заполнения пор. Затем образцы промывали в воде и без высушивания помещали в нижнюю часть реактора высокого давления, содержащего 35%-ный водный раствор перекиси водорода. Объем реактора составлял 20 мл (для образцов размером 3 × 3 см2) или 30 мл (для образцов размером 5 × 5 см2), материалом реактора являлась нержавеющая сталь.
Герметизованный реактор заполняли жидким диоксидом углерода при температуре 23°С до давления 400 атм с помощью генератора давления #81-5.75-10 (“High Pressure Equipment Company”, США), что соответствовало плотности жидкого диоксида углерода около 1 г/см3, согласно программе NIST Chemistry WebBook, Thermophysical Properties of Fluid Systems (США) [39]. Соотношение водного раствора перекиси водорода и жидкого диоксида углерода составляло 1:1 по объему. Давление контролировали манометром. В этих условиях, при насыщении водного раствора перекиси водорода диоксидом углерода, формируется раствор пероксиугольной кислоты [36]. Систему выдерживали в течение 1 суток. Далее осуществляли декомпрессию автоклава в течение 10–15 мин. Извлеченный из реактора образец промывали в воде для удаления следов перекиси водорода и использовали для последующего нанесения хитозанового покрытия.
Процедура нанесения хитозанового покрытия. Для нанесения хитозанового покрытия сначала в другом аналогичном реакторе высокого давления готовили раствор хитозана в угольной кислоте. Хитозан в количестве 100 мг (для 20 мл реактора) или 150 мг (для 30 мл реактора) помещали в реактор, содержащий магнитную мешалку с тефлоновой оболочкой. После герметизации реактор заполняли жидким диоксидом углерода до давления 400 атм при температуре 23°С, что также соответствовало плотности около 1 г/см3. Соотношение воды и жидкого диоксида углерода составляло 1 : 1 по объему. В таких условиях в водной фазе, насыщенной диоксидом углерода, формировалась угольная кислота, в растворе которой хитозан растворяется [37, 38]. Растворение проводили при интенсивном перемешивании (700 об/мин) с помощью магнитной мешалки в течение недели. По завершении растворения реактор декомпрессировали в течение 15–20 мин. В реактор помещали предобработанный в пероксиугольной кислоте образец мембраны. Реактор герметизировали и заполняли жидким диоксидом углерода при температуре 23°С до давления 400 атм, что соответствовало той же плотности около 1 г/см3. Систему выдерживали при этих условиях в течение нескольких дней без перемешивания. По завершении экспозиции и декомпрессии (15–20 мин) образец промывали в воде, высушивали на воздухе и исследовали.
Измерения краевого угла смачивания. Динамику квазистатически отступающего краевого угла измеряли на установке “Femtoscan Radian” (Центр перспективных технологий, Россия). На образец мембраны наносили каплю с исходным объемом 10 мкл с помощью микродозатора с капиллярным наконечником. Динамика испарения капли определялась нормальными лабораторными условиями, и измерения занимали, как правило, около 1 ч. Изображения капли фиксировали на цифровую камеру установки с интервалом в 1 мин.
Измерение угла на записанных изображениях выполняли с помощью открытой программы ImageJ (National Institutes of Health, США) и открытого дополнительного модуля LBADSA для нее. Данный модуль позволяет аппроксимировать формы капли уравнением Юнга–Лапласа [40].
Для контроля воспроизводимости результатов динамику краевого угла изучали на трех различных участках поверхности образца, полностью высушенного от каких-либо следов предыдущей капли. Получаемые зависимости краевого угла от времени нормировали на полное время испарения капли, что позволяло перейти к нормированному времени. Ранее было показано [33–35], что зависимость краевого угла от нормированного времени является инвариантом, не зависящим для конкретного образца от реальной скорости испарения капли. Это оправдывает применение использованной процедуры усреднения по итогам трех измерений, что позволяет оценить статистический разброс значений угла и связать его с возможной неоднородностью поверхностных свойств образца. Такие усредненные значения угла с погрешностями, характеризуемыми стандартными отклонениями средних арифметических, в зависимости от нормированного времени использовали при анализе и сопоставлении гидрофильных/гидрофобных свойств различных образцов.
Анализ поверхности. Поверхность образцов была исследована методом сканирующей электронной микроскопии на приборе “Supra 40” (“Carl Zeiss”, Германия) в режиме регистрации вторичных электронов при ускоряющем напряжении 2 кВ и рабочем расстоянии 5 мм без напыления металла на образец.
Морфологию поверхности образцов визуализировали методом атомно-силовой микроскопии на приборе “MultiMode SPM” со сканирующей частью MMAFM-2 и электронным контроллером Nanoscope-IIIa (Digital Instruments, США). Использовали кремниевые кантилеверы NCH (длина 125 мкм, радиус кривизны кончика иглы менее 8 нм) производства “NanoWorld” (Швейцария). Изображения записывали в режиме топографии по измерению сигнала обратной связи с плотностью информации 512 × 512 точек, при частоте строчной развертки 1 Гц. Анализ и построение полученных изображений проводили с помощью программ Nanoscope (“Digital Instruments”, США) и Femtoscan Online (Центр перспективных технологий, Россия).
Анализ проницаемости мембран по отношению к воде. Эксперименты по проницаемости мембран по отношению к воде под давлением выполняли с использованием мембранной ячейки с держателем фильтра высокого давления из нержавеющей стали “High Pressure Filter Holder” (”Millipore Corporation”, США). Экспериментальная установка схематически показана на рис. 1. Мембрана 1 была помещена на перфорированный суппорт в ячейку высокого давления с фланцевым соединением 2. Эффективная площадь мембраны, определяемая уплотняющими кольцами из ПТФЭ, составляла 9.6 см2. Вода к мембране поступала из проточного автоклава 3 под давлением азота (99.996%, Московский газоперерабатывающий завод), который из баллона 5 поступал в редуктор 4, понижающий давление до 1 атм избыточного давления.
Рис. 1.
Схематическое изображение установки для измерения проницаемости воды через мембрану: 1 – мембрана, 2 – ячейка высокого давления, 3 – автоклав с водой, 4 – редуктор с манометром, 5 – баллон с азотом, 6 – мерный цилиндр.
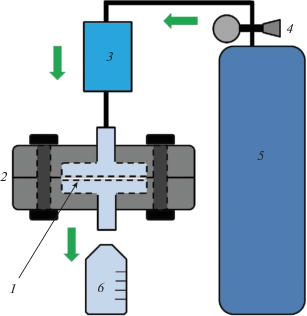
Перед началом экспериментов, мембраны пропитывали изопропиловым спиртом для лучшей смачиваемости водой. В противном случае мембраны, особенно исходные немодифицированные, оставались излишне гидрофобными и не пропускали воду под приложенным давлением, что согласуется с результатами работы [31]. После начала эксперимента выжидали пока через мембрану не пройдет около 20 мл воды, что гарантировало полное удаление остаточного спирта из пор. Затем в течение 5 мин мерный сосуд 6 заполняли водой при неизменном приложенном давлении, полученные данные регистрировали. Указанную процедуру повторяли трижды. Если результаты всех измерений были близки, то полученное усреднением число фиксировали и заносили в таблицу (статистический разброс описывали стандартным отклонением среднего арифметического). В противном случае измерения повторяли, пока не устанавливался стационарный режим. Проницаемость мембраны рассчитывали по формуле P = V/(St), где V – объем воды, прошедший через мембрану, S – эффективная площадь мембраны в держателе, t – время протекания воды.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты сравнительного анализа гидрофобных/гидрофильных свойств поверхности исходных и модифицированных образцов с помощью динамики краевого угла высыхающей капли представлены на рис. 2. Для наглядности сопоставления результатов на рис. 3 приведены соответствующие рис. 2 изображения капель на различных этапах высыхания. Для исходного образца наблюдается динамика, фактически совпадающая с ранее опубликованными данными [33–35] для материала Celgard 2325. Выбранный в настоящей работе в качестве исходного материал Celgard H2512 имеет сходную трехслойную пористую структуру и пористость.
Рис. 2.
Краевой угол высыхающих капель воды на поверхностях мембран Celgard в зависимости от нормированного времени: 1 – исходный образец, 2 – образец после предобработки (H2O2 + CO2), 3 – образец с нанесенным слоем хитозана. Показан статистический разброс значений углов.
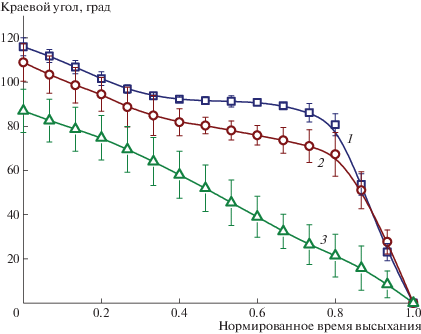
Рис. 3.
Фотографии капель воды, соответствующие рис. 2, на различных этапах высыхания (слева направо – начальный, 1/4, 1/2, 3/4 от полного времени высыхания) на поверхностях мембран Celgard: a – исходный, б – после предобработки, в – с нанесенным слоем хитозана. Начальный объем капли 10 мкл, размер кадра 3.7 × 2.9 мм.

Характерной особенностью зависимости краевого угла от нормированного времени для исходного образца Celgard H2512 (рис. 2) является наличие трех выраженных участков примерно одинаковой длительности. На начальном участке, составляющем первую треть от полного времени высыхания, наблюдается прилипание капли: краевой угол уменьшается при фактически постоянной площади области контакта капли и подложки. На втором участке, составляющем вторую треть от полного времени высыхания, краевой угол по мере испарения капли остается практически постоянным, площадь контакта подложки и высыхающей капли монотонно уменьшается. На завершающем третьем этапе вновь проявляется прилипание. Однако здесь объем капли уже существенно меньше по сравнению с исходным, а значит, поверхностная концентрация возможных примесей (следовых дисперсных частиц или амфифильных молекул) может оказаться довольно высокой и влияющей на процесс смачивания. В связи с этим динамику изменения краевого угла на завершающем этапе испарения капли необходимо интерпретировать с учетом указанных возможных осложняющих факторов.
Результаты для мембраны после обработки в присутствии пероксиугольной кислоты (водный раствор H2O2 + CO2 под давлением) также достаточно типичны. Качественно они совпадают с данными [33–35], где использовалась сходная процедура предварительной обработки для сходного материала мембраны. Отличие состоит в том, что в настоящей работе мембрану обрабатывали при комнатной, а не при повышенной температуре, чтобы сделать процесс более технологичным. Тем не менее, наблюдаемый эффект в целом аналогичен описанному ранее. Так, ход кривой для предварительно обработанной мембраны показывает, что гидрофильность мембраны несколько возрастает после модификации: краевой угол на всех этапах высыхания капли меньше по сравнению с таковым для исходного образца.
Наилучшую смачиваемость водой имеет мембрана, подвергнутая предобработке в пероксиугольной кислоте и последующему нанесению хитозанового покрытия (рис. 2). Ход кривой также оказывается достаточно типичным. Качественно он весьма близок аналогичным зависимостям для предобработанных в перокисугольной кислоте мембран Celgard с нанесенным затем покрытием полидопамина [33] или внедренными дисперсными частицами кремнезема [34, 35].
На изображениях капель воды в разные моменты высыхания (рис. 3) можно наглядно наблюдать возрастающую по мере предварительной обработки и нанесения покрытия смачиваемость поверхности подложки водой, что проявляется в заметном растекании по поверхности модифицированной матрицы Celgard.
Сравнительный анализ поверхностей образцов с помощью сканирующей электронной микроскопии (рис. 4) выявил следующее. Поверхности исходного образца (рис. 4a) и образца, предварительно обработанного в пероксиугольной кислоте (рис. 4б), выглядят фактически одинаковыми. Таким образом, предварительная обработка в пероксиугольной кислоте заметно не влияет на морфологию внешней поверхности пленки и стенок наружных пор. Следовательно, наблюдаемая возросшая гидрофильность предобработанного образца должна быть связана только с изменением химической природы поверхности: вероятно, с увеличением числа кислородсодержащих поверхностных групп.
Рис. 4.
Электронно-микроскопические изображения поверхности мембран Celgard, исходной (a), предобработанной (б) и с нанесенным слоем хитозана (в). Увеличение 50 000, размер масштабной линии 1.5 мкм.

У мембраны с нанесенным хитозановым покрытием морфология поверхности несколько отличается. Так, поры имеют меньший характерный размер. Были проведены измерения видимого в электронный микроскоп латерального размера пор в направлении ориентации тяжей. Для исходного и предварительно обработанного материалов он равен 90 ± 30 нм и 80 ± 30 нм соответственно. Для покрытого хитозаном материала указанный размер составляет 57 ± 19 нм, что в 1.5 раза меньше исходного. Это может служить индикатором присутствия хитозанового покрытия.
Те же образцы в сходных условиях, т.е. без напыления металла, были исследованы с помощью АСМ (рис. 5). Сопоставление исходного (рис. 5a, 5г) и предварительно обработанного в пероксиугольной кислоте (рис. 5б, 5д) образцов также показывает отсутствие видимых различий морфологии. Тем самым подтверждается, что разное поведение высыхающей капли на таких поверхностях (большая смачиваемость, выраженное прилипание для предварительно обработанного в пероксиугольной кислоте образца по сравнению с исходным) должно объясняться только наличием якорных групп на окисленной поверхности.
Рис. 5.
АСМ-изображения поверхности мембран Celgard, исходной (а, г), предобработанной (б, д) и с нанесенным слоем хитозана (в, е). Размер кадра 12 × 12 (а–в) и 6×6 мкм (г–е), шкала высот 100 нм. Квадратами на изображениях верхнего ряда показаны участки, отсканированные повторно с большим разрешением (показаны в нижнем ряду). Размер масштабной линии 1.5 мкм.

Интересно отметить различия в результатах визуализации двух методов анализа поверхности – сканирующей электронной микроскопии и АСМ. На обоих типах изображений прослеживаются тяжи, сформированные в результате применяемой производителем процедуры растяжения материала. Эти тяжи визуализированы примерно одинаковым образом обоими методами. Однако характер пор, локализованных между тяжами, различается. На электронно-микроскопических изображениях они имеют кратероподобный характер, причем структура дна “кратеров” не прослеживается. На АСМ-изображениях видно, что между тяжами расположены узкие щелевидные поры, сформированные фибриллами, идущими в направлении, перпендикулярном ориентации тяжей. По-видимому, на результат визуализации в электронном микроскопе значительное влияние оказывает воздействие электронного пучка, приводящее, в том числе, к заряжению диэлектрика (процедура напыления металла не была применена намеренно, чтобы не маскировать структуру поверхности). Эффекты заряжения проявляются на изображениях рис. 4. Фибриллы, очевидно, заряжаются одноименно, что способствует их взаимному отталкиванию. Как следствие, имеет место трансформация узких щелевидных пор, четко различимых на АСМ-изображениях, в более округлые кратероподобные поры, визуализированные с помощью электронного микроскопа.
Также нужно учитывать возможное силовое воздействие зонда АСМ на поверхность мембраны, которое может вызывать ее деформации в направлении по нормали к поверхности [41]. Вследствие деформации дно пор будет прописано более четко и на меньшей глубине. Важно также подчеркнуть, что латеральный размер пор в АСМ при количественных измерениях будет систематически занижен. Это обусловлено конечностью остроты иглы и ограниченностью ее проникновения в узкие поры [42]. Указанную специфику процессов визуализации обоих методов, не свободных от возможных артефактов, следует учитывать при анализе и сопоставлении получаемых изображений. Тем не менее, два использованных метода анализа морфологии поверхности представляются удачно дополняющими друг друга.
Для образца с нанесенной хитозановой пленкой на АСМ-изображениях (рис. 5в, 5е) также прослеживаются некоторые особенности, не наблюдаемые в случае исходного (рис. 5a, 5г) и предварительно обработанного в пероксиугольной кислоте (рис. 5б, 5д) образцов. В частности, оказываются различимы тонкие фибриллы, ориентированные так же, как и крупные тяжи (на рис. 5в, 5е – вертикально). Эти фибриллы локализованы между крупными тяжами и не наблюдаются для образцов двух других типов. Следовательно, их возникновение можно связать с влиянием нанесенного хитозанового покрытия. Указанные хитозановые фибриллы могут дополнительно скреплять противоположные стенки щелевидных пор, препятствуя увеличению расстояния между ними из-за отталкивания, обусловленного одноименной заряженностью при наблюдениях в электронном микроскопе. Такой механизм может объяснить меньший размер пор для мембраны с хитозановым покрытием, регистрируемый в электронной микроскопии (рис. 4). Кроме того, у образца с нанесенной хитозановой пленкой щелевидные поры оказываются менее четко выраженными, а поверхность ПП-фибрилл, ориентированных перпендикулярно тяжам, выглядит менее гладкой, чем в исходном или предварительно обработанном образцах. Эти различия в морфологии могут указывать на присутствие нанесенного хитозанового покрытия малой толщины. Принимая во внимание шкалу высот изображений (рис. 5) и измеряемую в АСМ высоту фибрилл над уровнем подложки, составляющую 4.6 ± 1.9 нм, толщину покрытия можно оценить в несколько единиц нанометров.
Методы микроскопии высокого разрешения показывают, что присутствие хитозана оказывает незначительное влияние на морфологию матрицы. В то же время измерения краевого угла свидетельствуют о весьма заметном повышении гидрофильности материала в результате нанесения хитозана. Это позволяет сформулировать вывод о том, что хитозановое покрытие нанометровой толщины на ПП-матрице способно существенно изменить физико-химические свойства ее поверхности.
Объемные свойства мембраны характеризуются ее проницаемостью [31, 43, 44]. В мембранной установке были измерены значения потока воды через мембрану, устанавливающиеся под давлением в одну атмосферу. Результаты измерения проницаемости представлены в табл. 1. Оказалось, что предварительная обработка мембраны в пероксиугольной кислоте повышает ее проницаемость на 29%. Покрытие же предварительно обработанной мембраны хитозаном увеличивает ее проницаемость еще на 15%.
Таблица 1.
Проницаемость исследованных матриц Celgard по отношению к воде
| Матрица | Проницаемость, л/(м2 ч) | |
|---|---|---|
| I | II | |
| Исходная | 125 ± 7 | 142 ± 8 |
| Предварительно обработанная | 156 ± 9 | 183 ± 11 |
| Модифицированная хитозаном | 175 ± 4 | 210 ± 4 |
Таким образом, при нанесении хитозановой пленки на предварительно обработанный образец удается достичь увеличения проницаемости в ~1.5 раза по сравнению с исходным образцом, несмотря на наблюдаемое методами микроскопии снижение характерного латерального размера пор. Разработанные композиты могут иметь улучшенную селективность за счет механизма отсеивания по размеру и найти применение в задачах фильтрации. Нанесение поликатионного хитозанового покрытия на полианионную (после обработки в пероксиугольной кислоте) поверхность матриц Celgard является первым шагом модификации. Последующую обработку можно проводить с использованием традиционного метода послойного нанесения в растворах поликатионных и полианионных полимеров, в том числе в растворах под давлением. Это даст инструмент дальнейшей оптимизации селективности композитов.
Немаловажно и то, что хитозановое покрытие придает мембранам бактерицидные свойства. Действительно, для полученных сходным образом покрытий на коллагеновых матрицах ранее нами был обнаружен ярко выраженный антибактериальный эффект для целого ряда клинических штаммов [37].
ЗАКЛЮЧЕНИЕ
Применение растворителей на основе диоксида углерода под давлением позволяет решить важную для ряда приложений задачу нанесения хитозанового покрытия на пористые ПП-мембраны Celgard. Процедура модификации включает предобработку матриц в насыщаемом под давлением диоксидом углерода водном растворе перекиси водорода, т.е. в присутствии пероксиугольной кислоты, а затем – собственно осаждение покрытия из раствора хитозана в воде, также насыщаемой под давлением диоксидом углерода, т.е. в присутствии угольной кислоты. Обе среды имеют выигрышное свойство самонейтрализации при декомпрессии. Полученные композиты по сравнению с исходной матрицей характеризуются увеличенной гидрофильностью и большей проницаемостью по отношению к воде, несмотря на уменьшенный размер пор, измеренной методами микроскопии. Это может способствовать улучшенной селективности композитных мембран в задачах фильтрации. Присутствие антимикробного хитозанового покрытия должно обеспечить долговременную стабильность работы мембраны за счет бактерицидных свойств. Дальнейшее развитие данного подхода возможно при переходе к последовательному нанесению многих полианионных и поликатионных слоев, в том числе с использованием растворителей под давлением.
Работа выполнена при финансовой поддержке Российского научного фонда (проект 16-13-10338-П).
Список литературы
Kang G.-d., Cao Y.-m. // J. Membr. Sci. 2014. V. 463. P. 145.
Lalia B.S., Kochodan V., Hashaikeh R., Hital N. // Desalination. 2013. V. 326. P. 77.
Khulbe K.C., Feng C., Matsuura T. // J. Appl. Polym. Sci. 2010. V. 115. P. 855.
Paul M., Jons S.D. // Polymer. 2016. V. 103. P. 417.
Zhao Zh., Zheng J. Wang M., Zhang H., Han Ch.C. // J. Membr. Sci. 2012. V. 394–395. P. 209.
Chanachai A., Meksup K., Jiraratananon R. // Sep. Purif. Technol. 2010. V. 72. P. 217.
Kang M.S., Chun B., Kim S.S. // J. Appl. Polym. Sci. 2001. V. 81. P. 1555.
Luo Q., He B., Liang M., Kong A., Li J. // Fuel 2017. V. 197. P. 51.
Zhao Y., Tao Ch., Xiao G., Su H. // RSC Adv. 2017. V. 7. P. 11211.
Arora P., Zhang Zh.(J.) // Chem. Rev. 2004. V. 104. P. 4419.
Orendorff Ch.J. // Electrochem. Soc. Interface 2012. V. 21. № 2. P. 61.
Shi Y., Eze Ch., Xiong B., He W., Zhang H., Lim T.M., Ukil A., Zhao J. // Appl. Energ. 2019. V. 238. P. 202.
Nagarjuna G., Hui J., Cheng K.J., Shen M., Moore J.S., Rodríguez-López J. // J. Am. Chem. Soc. 2014. V. 136. P. 16309.
Ma J., Yang Z., Wang X., Qu X., Liu J., Lu Y., Hu Z., Yang Z. // Polymer. 2007. V. 48. P. 4305.
Suriyakumar S., Stephan A.M., Angulakshmi N., Hassan M.H., Alkordi M.H. // J. Mater. Chem. A. 2018. V. 6. P. 14623.
Li C., Ward A.L., Doris S.E., Pascal T.A., Prendergast D., Helms B.A. // Nano Lett. 2015. V. 15. P. 5724.
Gruzd A.S., Trofimchuk E.S., Nikonorova N.I., Nesterova E.A., Meshkov I.B., Gallyamov M.O., Khokhlov A.R. // Int. J. Hydrogen Energy. 2013. V. 38. № 10. P. 4132.
Meier-Haack J., Müller M., Lunkwitz K. // Polymer Membranes for Sustainable Technologies, in Polymers – Opportunities and Risks II. The Handbook of Environmental Chemistry / Ed. by P. Eyerer, M. Weller, C. Hübner. Berlin: Heidelberg: Springer, 2010.
Spirk S. // Polysaccharides in Batteries, in Polysaccharides as Battery Components, Springer Briefs in Molecular Science. Cham: Springer, 2018.
Yue M., Zhang Y., Wang L. // J. Appl. Polym. Sci. 2013. V. 127. P. 4150.
Lu Sh., Wu Ch., Liang D., Tan Q., Xiang Y. // RSC Adv. 2014. V. 4. P. 24831.
Zhang T.-W., Shen B., Yao H.-B., Ma T., Lu L.-L., Zhou F., Yu Sh.-H. // Nano Lett. 2017. V. 17. P. 4894.
Ren Y., Zhao J., Wang X. // Text. Res. J. 2018. V. 88. № 2. P. 182.
Goddard J.M., Hotchkiss J.H. // Prog. Polym. Sci. 2007. V. 32. P. 698.
Elsabee M.Z., Abdou E.S., Nagy Kh.S.A., Eweis M. // Carbohydr. Polym. 2008. V. 71. P. 187.
Abudonia K.S., Saad G.R., Naguib H.F., Eweis M., Zahran D., Elsabee M.Z. // J. Polym. Res. 2018. V. 25. P. 125.
Joseph N., Ahmadiannamini P., Hoogenboom R., Vankelecom I.F.J. // Polym. Chem. 2014. V. 5. P. 1817.
Stroeve P., Vasquez V., Coelho M.A.N., Rabolt J.F. // Thin Solid Films. 1996. V. 284–285. P. 708.
Rochery M., Lam T.M., Crighton J.S. // Macromol. Symp. 1997. V. 119. P. 277.
Nikitin D., Choukourov A., Titova V., Kuzmicheva L., Lipatova I., Mezina E., Aleksandriiskii V., Shelemin A., Khalakhan I., Slavinska D., Biederman H. // Carbohydr. Polym. 2016. V. 154. P. 30.
Garg D.H., Lenk W., Berwald S., Lunkwitz K., Simon F., Eichhorn K.-J. // J. Appl. Polym. Sci. 1996. V. 60. P. 2087.
Stawski D., Sahariah P., Hjálmarsdóttir M., Wojciechowska D., Puchalski M., Másson M. // J. Text. I. 2017. V. 108. № 6. P. 1041.
Gvozdik N.A., Zefirov V.V., El’manovich I.V., Karpushkin E.A., Stevenson K.J., Sergeyev V.G., Gallya-mov M.O. // Colloid J. 2018. V. 80. № 6. P. 761.
Elmanovich I.V., Zefirov V.V., Sizov V.E., Kondratenko M.S., Gallyamov M.O. // Dokl. Phys. Chem. 2019. V. 485. P. 53.
Zefirov V.V., Sizov V.E., Kondratenko M.S., Elmanovich I.V., Abramchuk S.S., Sergeyev V.G., Gallyamov M.O. // J. Supercritical Fluids. 2019. V. 150. P. 56.
Pigaleva M.A., Elmanovich I.V., Kononevich Y.N., Gallyamov M.O., Muzafarov A.M. // RSC Adv. 2015. V. 5. P. 103573.
Gallyamov M.O., Chaschin I.S., Khokhlova M.A., Grigorev T.E., Bakuleva N.P., Lyutova I.G., Kondratenko J.E., Badun G.A., Chernysheva M.G., Khokhlov A.R. // Mater. Sci. Eng. C 2014. V. 37. P. 127.
Gallyamov M.O., Chaschin I.S., Bulat M.V., Bakuleva N.P., Badun G.A., Chernysheva M.G., Kiselyova O.I., Khokhlov A.R. // J. Biomed. Mater. Res. B. 2018. V. 106. P. 270.
NIST Chemistry WebBook, Thermophysical Properties of Fluid Systems. http://dx.doi.org/10.18434/T4D303
Stalder A.F., Melchior T., Müller M., Sage D., Blu T., Unser M. // Colloids Surf. A. 2010. V. 364 P. 72.
Gallyamov M.O., Yaminsky I.V. // Surf. Investig. 2001. V. 16. № 7. P. 1127.
Gallyamov M.O., Yaminskii I.V. // Surf. Investig. 2001. V. 16. № 7. P. 1135.
Yang Y.F., Li Y., Li Q.L., Wan L.Sh., Xu Zh.K. // J. Membr. Sci. 2010. V. 362. P. 255.
Minhas F.T., Memon S., Bhanger M.I., Iqbal N., Mujahid M. // Appl. Surf. Sci. 2013. V. 282. P. 887.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)


