Высокомолекулярные соединения (серия А), 2021, T. 63, № 2, стр. 83-91
ВЛИЯНИЕ БОРНОЙ КИСЛОТЫ НА СТРУКТУРУ И СВОЙСТВА БОРОСИЛОКСАНОВ
В. И. Мащенко a, *, Н. Н. Ситников b, c, И. А. Хабибуллина b, Д. Н. Чаусов a, А. В. Шеляков c, В. В. Спиридонов d
a Московский государственный областной университет
141014 Мытищи, Московская обл., ул. Веры Волошиной, 24, Россия
b Исследовательский центр имени М.В. Келдыша
125438 Москва, Онежская ул., 8, Россия
c Национальный исследовательский ядерный университет “МИФИ”
115409 Москва, Каширское ш., 31, Россия
d Московский государственный университет им. М.В. Ломоносова. Химический факультет
119991 Ленинские горы, Москва, Россия
* E-mail: mashchenko@genebee.msu.su
Поступила в редакцию 03.06.2020
После доработки 06.10.2020
Принята к публикации 20.10.2020
Аннотация
Изучены боросилоксановые материалы, полученные путем смешения и термостатирования полидиметилсилоксана с концевыми гидроксильными группами и борной кислоты. Образцы, синтезированные при комнатной температуре и при температуре свыше 220°С, представляют собой непрозрачные каучукоподобные массы. Отмывка от борной кислоты приводит к получению однофазных прозрачных боросилоксанов, также обладающих каучукоподобными свойствами. Исследования проведены методами элементного анализа, динамического рассеяния света, синхронного термического анализа и поляризационной оптической микроскопии. Вязкоупругие свойства образцов охарактеризованы реологическими методами, а также способностью изготовленных из полимеров шарообразных образцов к растеканию и отскоку. Показано, что в исходном состоянии в них присутствуют микрокристаллические включения борной кислоты, которые рассеивают видимый свет. Повышенная температура синтеза и наличие непрореагировавшей борной кислоты увеличивают упругость материалов и снижают их термостабильность. Боросилоксан, полученный при повышенной температуре, содержит на порядок больше бора, чем боросилоксан, синтезированный при комнатной температуре, в то время как радиус эффективной гидродинамической сферы в 5 раз меньше в высокотемпературном боросилоксане. Реологические свойства представленных образцов различны. Эти материалы могут найти применение в многослойных самозалечивающихся и амортизирующих композитах, а также в материалах с контролируемой липкостью.
Устойчивый интерес, проявляемый к материалам и системам, обладающим различными “умными” свойствами, среди которых регулируемая липкость, способность к самозаживлению и диссипации энергии удара [1–3], обусловлен перспективами их практического применения в современных технологиях. С момента первого синтеза в 1943 году [4] материалы на основе соединений боросилоксана (БС) привлекают все бόльшее внимание разработчиков и исследователей ввиду целого комплекса таких свойств.
С точки зрения молекулярной структуры боросилоксаны относятся к классу кремнийорганических соединений, содержащих группировку R–Si–O–B=, где R – углеводородный радикал. Они являются продуктами реакции между органосилоксанами (преимущественно полидиметилсилоксаном) и борокислородными соединениями, чаще всего борной кислотой. В зависимости от структуры молекулы и ММ исходного органосилоксана, условий синтеза, а также от количества и свойств введенных функциональных добавок (наполнителей, пластификаторов, загустителей и т.д.) материалы на основе БС могут обладать различными механическими свойствами. Они могут находиться как в твердом, так и в жидком агрегатном состоянии, а также иметь вязкую, высокоэластичную или стеклообразную консистенцию [5].
Материалы на основе боросилоксана применяют в различных областях. Например, их активно используют в средствах спортивной защиты в качестве поглотителей ударной энергии, эффективно защищающих человека в таких экстремальных видах спорта, как мото- и велогонки, горные лыжи и других, и могут выпускать под торговой маркой D3O [6]. Целый ряд разработок посвящен БС, служащим для пропитки других материалов. Так, кевларовую ткань пропитывают БС, чтобы повысить ударную прочность бронежилетов и других средств защиты от пуль и осколков. Эти образцы обладают лучшими свойствами в сравнении с непропитанными кевларом и носят название “жидкая броня” [3].
Еще одним важным свойством боросилоксанов является способность быстро (подобно обычной жидкости) восстанавливать целостность при соединении разделенных частей без каких-либо следов в месте разрыва, причем разрыв может происходить как по хрупкому, так и по вязкому механизму. Такая способность БС делает его весьма перспективным материалом для различных систем с самозалечивающимися свойствами. Авторами работы [7] на основе БС и углеродных нанотрубок были созданы гибкие электропроводящие нанокомпозиты, обладающие самозалечивающимися свойствами. В работе [8] получены и исследованы боросилоксановые покрытия для защиты металла от коррозии, а в работах [9–12] БС был использован в качестве самозалечивающегося слоя в составе многослойных композитов. Также рассматривается возможность применения боросилоксана в электронике и оптической технике [13–15] в качестве антимикробного средства для механической дезинфекции кожи рук [16, 17].
Несмотря на то что уникальные свойства боросилоксанов подробно исследованы и описаны в научно-технической литературе, особенности структуры, обусловливающие комплекс вязкоупругих характеристик, до настоящего времени выступают предметом научных дискуссий [5, 18–36]. Выдвигаются предположения о сложном многофазном строении БС [2]. В пользу этого мнения свидетельствует схожесть поведения БС с дилатантными дисперсиями, называемыми в англоязычной литературе STF-материалами (Shear Thickening Fluid). Большинство исследователей STF-материалов полагают, что они загущаются из-за образования так называемых гидрокластеров [37–45], которые связываются посредством водородных связей. Ряд других ученых связывают его дилатантные свойства с водородными связями [19, 20], а в работах [21, 26, 28] показано, что донорно-акцепторные взаимодействия между бором и кислородом соседних молекул являются ключевой причиной неньютоновских свойств. В одной из последних работ [19] предполагается, что вклад в неньютоновское поведение вносят как водородные связи, так и донорно-акцепторные взаимодействия.
Хорошо известно [4, 18, 20, 22, 26], что при длительном нагревании полидиметилсилоксана с борной кислотой при температуре свыше 200°С образуется БС. Молекулярная масса такого материала обычно значительно меньше ММ исходного ПДМС, она составляет порядка от сотен до тысяч Дальтон [20, 22]. Несомненно и то, что БС образуется при взаимодействии с борной кислотой при более низких значениях температуры при наличии у ПДМС концевых гидроксильных групп [4, 34–36]. В работе [19] продемонстрировано, что на концах силоксановых молекул вместо гидроксильных групп появляются группировки Si–O–B(OH)2. В структуре БС, полученного при нагревании, методом ИК-спектроскопии обнаружены группы Si–O–B, B–O–B и В–OH [18, 20, 22, 24]. Методами ГПХ и ИК-спектроскопии показано [20], что БС имеют надмолекулярную структуру, узлами которой выступают водородные связи, образованные на концах БС группировками Si–O–B(OH)2. Таким образом [18–36], наличие неньютоновских свойств у БС обусловлено нековалентными взаимодействиями между соседними молекулами. Комплекс вязкоупругих свойств ярко выражен уже при небольшом содержании бора в молекулах БС (от долей до нескольких процентов). С увеличением содержания бора растет и температура стеклования боросилоксанов [26, 27].
В работах [22, 26] показано, что неньютоновские свойства БС теряются при взаимодействии с растворителями, но проявляются вновь после высушивания образцов. Указывается также [22, 46], что гидролиз БС, полученных при повышенных значениях температуры, протекает в несколько стадий, первая из которых – гидролиз групп B–O–B с образованием свободной борной кислоты.
На практике для упрощения технологического процесса получения материалов на основе БС избыточную борную кислоту не удаляют из реакционной смеси после синтеза. При этом в молекулярной структуре БС присутствует как бор, так и гидроксильные группы, которые могут оказывать влияние на неньютоновские и прочие свойства материалов на основе БС.
Цель данной работы – исследовать влияние температуры синтеза и остаточной борной кислоты на структуру и свойства боросилоксанов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Образцы соединений боросилоксана получали методом смешения компонентов ПДМС и ортоборной кислоты с выдержкой в различных условиях. В качестве исходных веществ использовали ПДМС с концевыми гидроксильными группами марки “СКТН А” (вязкость 2 Па с, М ~ 20 × 103) и тонкодисперсную борную кислоту марки “Б” по ГОСТ 18704-78 (содержание основного вещества 99.9%, массовая доля борного ангидрида 57.1%, средний размер частиц 75 мкм). Массовое соотношение ПДМС и борной кислоты составляло 10 : 1.
Образцы “низкотемпературного” боросилоксана (БС-НТ) получали смешением компонентов и выдерживанием в течение 24 ч при нормальных условиях. Во избежание седиментации введенных частиц борной кислоты в процессе реакции смесь периодически перемешивали. По истечении 24 ч седиментации частиц борной кислоты в БС-НТ не происходило. Образцы “высокотемпературного” боросилоксана (БС-ВТ) получали нагреванием компонентов при температуре выше 220°С в реакционном сосуде по технике, описанной в работе [47]. Для этого на дно химического стакана емкостью 100 мл помещали отмеренное количество борной кислоты и сверху наливали ПДМС. Химический стакан располагали на лабораторной плитке и нагревали в течение 24 ч. Температуру синтеза контролировали при помощи погруженного в смесь электронного термометра. В процессе синтеза наблюдали интенсивное выделение парообразных веществ. Смесь самопроизвольно перемешивалась и гомогенизировалась.
Очистку образцов БС от непрореагировавшей (“свободной”) борной кислоты проводили растворением БС в избытке этанола с последующим добавлением избытка воды, кипячением и трехкратным промыванием водно-спиртовым раствором 40%.
Анализ содержания бора в образцах, отмытых от свободной борной кислоты, осуществляли с применением спектрографа “PGS-2” (Германия), оснащенного многоканальным анализатором эмиссионных спектров производства ООО “ВМК-Оптоэлектроника” (Россия). Применяли метод добавок в трех повторных экспериментах. Источник возбуждения – непрерывная дуга переменного тока генератора “Шаровая молния ШМ-250”. Пробу массой 60 мг помещали в кратер графитового электрода квалификации о.с.ч. Измерения проводили в дуге переменного тока при силе тока в 3 А (50 Гц) в течение 15 с, затем при силе тока 20 А в течение 85 с до полного выгорания пробы. Для анализа использовали линии бора 249.6772 и 249.7723 нм. В качестве сравнения применяли линию кремния (элемент минеральной основы проб). Регистрацию и расшифровку спектров осуществляли при помощи программы “Атом 3.3”. Расчет вели по методу линейной аппроксимации.
Размер частиц определяли методом динамического светорассеяния на фотометре “ALV-5” (“ALV”, Германия), снабженном лазером He–Nе мощностью 25 мВт (l = 632.8 нм) при угле рассеяния 90°. Автокорреляционные функции флуктуаций интенсивности рассеянного света измеряли с помощью 280-канального логического коррелометра “ФотоКорр-М”. Перед измерениями образцы обеспыливали двух-трехкратным пропусканием через мембранные фильтры “Millipore” со средним размером пор 1.2 мкм. Результаты измерений обрабатывали регуляризацией по методу Тихонова. Радиус эквивалентных гидродинамических сфер рассчитывали по уравнению Стокса. В качестве растворителя использовали толуол квалификации ч.д.а.
Реологические испытания проводили на реометре “Anton Paar MCR 302” (Швейцария). Использовали ячейку типа “плоскость–плоскость” диаметром 25 мм. Образцы термостатировали при помощи элемента Пельтье при 23°С. Амплитуда относительной деформации, при которой измеряли частотные зависимости динамического модуля, составляла 0.1%.
Вязкость определяли измерением времени растекания шарика из БС массой 2 гр по поверхности стеклянной подложки. Относительное увеличение диаметра b находили по формуле:
где D0, Di – диаметр начальный и в момент времени t соответственно.Упругие свойства образцов характеризовали с помощью измерения величины относительного упругого отскока а (%) по следующей методике. Образец БС шарообразной формы массой 2 гр сбрасывали с высоты H на плоскую стеклянную поверхность. Визуально фиксировали высоту отскока шарика h. Рассчитывали отношение высоты отскока к начальной высоте, с которой был сброшен шарик:
Синхронный термический анализ (СТА) осуществляли на термоанализаторе “STA 449 F1 Jupiter” (“NETZSCH”). Микроструктуру образцов характеризовали с помощью поляризационного оптического микроскопа “ПОЛАР 3” (“Альтами”, Россия) в скрещенных поляризаторах.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
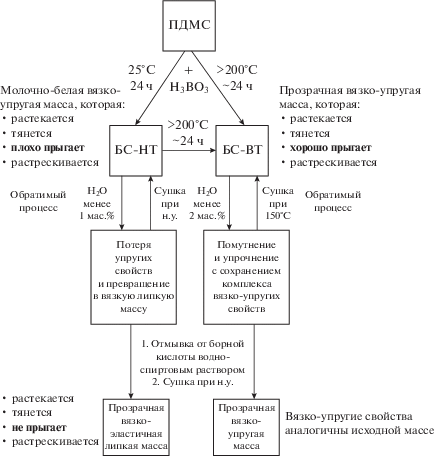
После смешения ПДМС и борной кислоты были получены образцы низкотемпературного и высокотемпературного боросилоксана, которые дополнительно подвергались очистке от свободной борной кислоты (рис. 1).
Реакция БС-НТ, протекающая при комнатной температуре, заметна сразу после смешения компонентов. Видно, что вязкость мутно-белой суспензии постепенно меняется от исходного значения 2 Па с до более чем 1000 Па с, это было установлено с помощью ротационного вискозиметра в одной из предыдущих работ [14]. По истечении 24 ч имелась вязкоупругая масса молочно-белого цвета, из которой можно было скатать шарик или придать любую другую форму. Такая масса вытягивается в нити и растрескивается при быстром приложении нагрузки, а под воздействием силы тяжести БС-НТ растекается по поверхности подложки (рис. 2).
Рис. 2.
Образцы БС-НТ, БС-ВТ до отмывки от борной кислоты (БК) и без нее сразу после придания шарообразной формы (а) и после растекания (б).
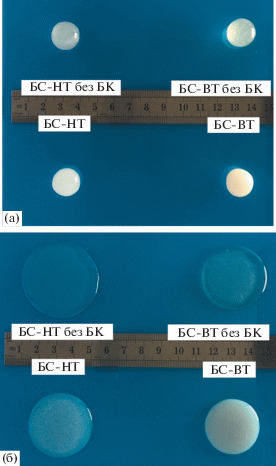
Следует отметить, что сделанный для сравнения образец ПДМС с метильными концевыми группами (ПМС-100) и таким же количеством борной кислоты – молочно-белая текучая суспензия со склонностью к седиментации частиц борной кислоты, не проявляющий никаких упругих свойств. Таким образом, для образцов БС, синтезируемых при комнатной температуре, необходимы гидроксильные группы в структуре исходного ПДМС.
При получении БС-ВТ вязкость реакционной смеси быстро увеличивается с повышением температуры и по достижении температуры синтеза реакция протекает бурно с выделением белых паров. Высокотемпературный боросилоксан может быть также синтезирован нагреванием БС-НТ, так как он является промежуточным соединением БС-ВТ. Критериями полноты прохождения реакции служили: получение однородной прозрачной текучей массы без видимых вкраплений; способность к отскоку скатанного из БС-ВТ шарика; также то, что образцы не прилипали к рукам.
Образец БС-ВТ представляет собой прозрачную массу, которая быстро мутнеет на воздухе (рис. 2а). Помутневшие образцы становятся более твердыми, упругими и хрупкими, но сохраняют способность к растеканию по подложке, как и все исследованные образцы (рис. 2б).
Отмытые от борной кислоты и высушенные образцы БС – прозрачные массы с вязкоупругими свойствами, которые рвутся, растекаются и вытягиваются в нити, однако упругие свойства в БС-ВТ без борной кислоты сохраняются, а у БС-НТ без нее практически утрачиваются.
Содержание бора в образцах БС-НТ и БС-ВТ после отмывки в пересчете на концевые группы –B(OH)2 составило ~0.30 ± 0.15 и 5.0 ± 2.5 мас. % соответственно. Теоретический расчет количества концевых групп –B(OH)2, присоединенных к исходному ПДМС с массой 20000 г/моль дает величину ~0.6 мас. %, что хорошо согласуется по порядку величины с результатами элементного анализа. Заниженное содержание бора в отмытых от борной кислоты образцах БС-НТ может быть связано как с погрешностью проведенных анализов и допущениями при расчетах, так и с частичным гидролизом БС-НТ в процессе отмывки от свободной борной кислоты.
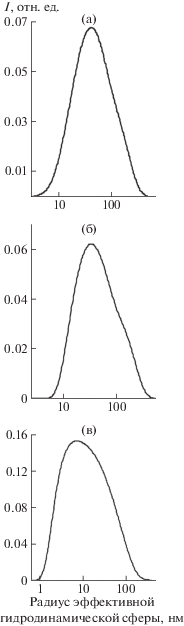
Методом динамического рассеяния света (рис. 3) показано, что разница между ПДМС и отмытыми БС-НТ и БС-ВТ заключается в молекулярной массе молекул. Гидродинамический размер ПДМС равен 82 нм, а БС-НТ и БС-ВТ – 64 и 14 нм соответственно. Уменьшение гидродинамического размера при образовании БС-НТ, по-видимому, связано с изменением полярности исходной молекулы ПДМС за счет увеличения количества гидроксильных групп на ее концах. Гидродинамический размер БС-ВТ значительно меньше БС-НТ, что, скорее всего, вызвано разрывом связей Si–O–Si в ПДМС при нагревании в присутствии борной кислоты и, как предполагается, сопровождается встраиванием в местах разрыва концевых групп Si–O–B(OH)2.
Рис. 3.
Функции распределения ПДМС (а), БС-НТ (б) и БС-ВТ (в) по гидродинамическому размеру частиц: а – 41 нм, б – 32 нм, в –7 нм.
При исследовании образцов с помощью поляризационного оптического микроскопа в скрещенных поляризаторах было обнаружено, что исходный ПДМС, а также БС без свободной борной кислоты не демонстрируют двойное лучепреломление. В структуре БС-НТ видны частички исходной борной кислоты (рис. 4а), в то время как в исходном образце БС-ВТ, не успевшем прореагировать с атмосферой, практически отсутствуют участки ДЛП (рис. 4б).
Рис. 4.
Микрофотографии вытянутых образцов БС-НТ (а) и БС-ВТ (б) в скрещенных поляризаторах. Направление вытяжки совпадает с длинной осью образцов.

На рис. 4 по характерному чередованию темных и светлых полос хорошо просматривается направление вытяжки данных образцов, что свидетельствует об их анизотропии, обусловленной деформированием. Это служит хорошей иллюстрацией проявления высокоэластических свойств образцами БС при механическом воздействии. Со временем ориентированные образцы БС релаксируют и становятся изотропными.
Исследование исходных компонентов реакции методом СТА показало, что ПДМС полностью термостабилен до температуры 250°С (рис. 5а, кривые 1), а образец борной кислоты имеет несколько пиков на ДСК и потерю массы в диапазоне 100–190°С (кривые 2).
Рис. 5.
Синхронный термический анализ ТГА (1–3) и ДСК (1'–3') образцов: а – ПДМС (1) и борная кислота (2); б – БС-НТ исходный (1) и БС-НТ без борной кислоты (2); в – БС-ВТ исходный (1), БС-ВТ насыщенный водой до постоянной массы при н.у. (2) и БС-ВТ без борной кислоты (3).
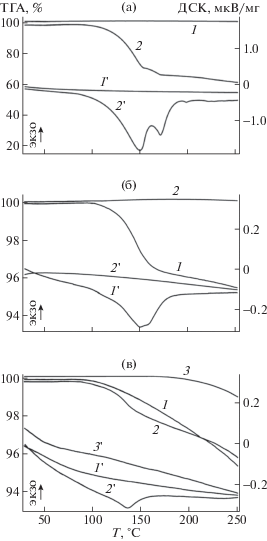
Наблюдаемые пики поглощения тепла на кривой ДСК и потеря массы связаны с процессами плавления борной кислоты, а также последовательным разложением ортоборной кислоты до метаборной и тетраборной. В интервале температуры от 160 до 180°С происходят процессы плавления компонентов образовавшейся смеси. Совместное протекание процессов плавления и разложения при нагревании борной кислоты подтверждается литературными данными [48, 49].
Пик на кривой ДСК для образца БС-НТ (рис. 5б), имеющий максимум при температуре ~150°С, очевидно, обусловлен описанными выше процессами, связанными с борной кислотой, а также реакцией между ней и ПДМС. Этот пик отсутствует в образце БС-НТ без борной кислоты. Видна высокая термостабильность в рассматриваемом диапазоне температуры образца БС-НТ без борной кислоты, которая подобна исходному ПДМС (рис. 5б, кривые 2).
На кривой дифференциальной сканирующей калориметрии БС-ВТ, не контактировавшего с влажной атмосферой (рис. 5в, кривые 1), отсутствуют пики, характерные для процессов с борной кислотой, хотя термостойкость образца значительно ниже, чем у БС-НТ. Это, по-видимому, обусловлено протеканием реакций, связанных с продолжающимся процессом синтеза БС и, соответственно, уменьшением молекулярной массы БС, ускоряемых остаточной борной кислотой.
На кривых 2, рис. 5в представлен образец БС-ВТ, выдержанный в атмосфере при нормальных условиях до постоянной массы. На кривой ДСК присутствует пик, а на кривой ТГА наблюдается соответствующая ему потеря массы. Ряд проверочных экспериментов методами СТА показал, что этот процесс сопровождается выделением воды, которую БС-ВТ захватывает из воздушной атмосферы. Этот процесс обратим: выдерживание образца на воздухе после прогревания опять приводит к его помутнению и набору массы (~2 мас. %). Удаление несвязанной борной кислоты из БС-ВТ приводит к тому, что образец БС-ВТ без нее становится устойчиво прозрачным на воздухе, присутствующих ранее характерных сигналов от выделения воды на СТА не наблюдается (рис. 5в, кривые 3). БС-ВТ без борной кислоты также имеет лучшую термостабильность, чем исходный БС-ВТ.
На рис. 6 представлены оптическое изображение и микрофотографии, снятые с помощью поляризационного оптического микроскопа, участка образца до и после взаимодействия с окружающей атмосферой. На микрофотографиях, сделанных в скрещенных поляризаторах, отчетливо видно ДЛП в области помутнения образца (рис. 6б, 6в).
Рис. 6.
а. – Оптическое изображение БС-ВТ, где часть образца находится под покровным стеклом; б, в – микрофотографии в скрещенных поляризаторах участка образца, выделенного рамкой на рис. 6а и 6б соответственно.

Предполагается, что склонность к частичному гидролизу БС-ВТ влагой воздуха с характерным помутнением образцов обусловлена гидролизом метаборосилоксановых группировок с образованием свободной борной кислоты и групп Si–O–B(OH)2 в БС-ВТ. Наличие метаборосилоксановых группировок в БС-ВТ, полученных данным способом, отмечено в литературе [19, 20, 22, 25–27, 44]. На рис. 6в четко прослеживаются микросферолитные образования, свидетельствующие, видимо, об образовании и высаживании свободной ортоборной кислоты, гидролизованной влагой воздуха.
Данные реологических испытаний показали, что у БС-НТ в исходном состоянии частотная зависимость модуля потерь представляется нелинейной кривой (рис. 7). Зависимость модуля потерь пересекается с зависимостью модуля накопления в точке ее экстремума (точка кроссовера) при частоте 9 рад/с. Такое поведение характерно для полимерных материалов в вязко-текучем состоянии. В низкотемпературном БС в отмытом состоянии модули потерь и накопления растут с увеличением частоты, и точка кроссовера располагается в области 50 рад/с. Отмытый БС-НТ проявляет свойства, характерные для адгезивов [50–53]. БС-НТ, наполненный борной кислотой, демонстрирует свойства, присущие традиционным полимерным материалам в вязко-текучем состоянии [54, 55].
Рис. 7.
Частотные зависимости модулей накопления G ′ и потерь G ′′ для образцов БС-НТ (а) и БС-ВТ (б) в исходном и отмытом состоянии.
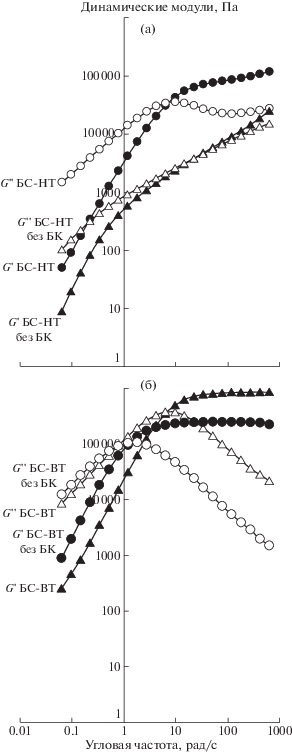
В высокотемпературном БС в обоих случаях частотные зависимости модулей потерь и накопления имеют одинаковый характер, свойственный максвелловским жидкостям. Точка кроссовера в образце БС-ВТ в исходном состоянии, как и в исходном БС-НТ, располагается в области 9 рад/с, а в БС-ВТ в отмытом состоянии в области 2 рад/с.
В рассматриваемых диапазонах частот модуль потерь в БС-НТ растет на высоких частотах, а в БС-ВТ падает, с чем связаны худшие упругие характеристики БС-НТ. Борная кислота в БС-ВТ, скорее всего, выполняет роль усиливающего мелкодисперсного наполнителя.
Измерения растекания образцов из шарообразной формы для образцов исходных БС и БС без борной кислоты показали, что образцы без борной кислоты растекаются быстрее, чем исходные, что подтверждают представленные выше реологические исследования.
Скорость растекания БС-ВТ ниже, чем БС-НТ. Это можно объяснить тем, что несвязанная борная кислота также выступает в качестве активного загущающего наполнителя.
Исследования упругих характеристик образцов методом отскока шарика от подложки продемонстрировали, что образцы, наполненные борной кислотой, более упругие и лучше отскакивают от подложки. Образцы БС-ВТ без борной кислоты также подтверждают хороший отскок, в то время как образцы БС-НТ без нее практически не отделяются от подложки после удара.
Изучение упругих свойств показало, что БС-НТ и БС-ВТ в исходном состоянии, до отмывки от “несвязанной” борной кислоты, более упруги по сравнению с образцами, очищенными от нее. Величина отскока шарика БС-НТ в исходном состоянии составляет 29%, а после отмывки 0–4%. В случае образца БС-ВТ в исходном состоянии отскок составляет 88%, а после отмывки 70%.
Молекулярная масса образцов БС-ВТ меньше, а содержание бора выше, а соответственно больше и группировок Si–O–B(OH)2 на одну молекулу, отвечающих за водородные и донорно-акцепторные связи между молекулами. Различие вязкоупругих характеристик БС-НТ и БС-ВТ, по-видимому, обусловлено тем, что плотность динамической сетки зацеплений, образованной нековалентными взаимодействиями, выше в случае БС-ВТ.
Работа поддержана грантом Российского фонда фундаментальных исследований (грант № 18-29-18095 (мк)).
Список литературы
Boval’dinova K.A., Sherstneva N.E., Fel’dshtein M.M., Moskalets A.P., Khokhlov A.R. // Polymer Science B. 2019. V. 61. № 4. P. 458.
Алешина А.Л., Шибаев А.В., Филиппова О.Е., Хохлов А.Р. // Докл. РАН. Сер. Химия, науки о материалах. 2020. Т. 491. С. 64.
Xu C., Wang Y., Wu J., Song S., Cao S., Xuan S., Jiang W., Gong X. // Comp. Sci. Technol. 2017. V. 153. P. 168.
McGregor R.R., Warrick E.L. Pat. 2431878A USA. 1943.
Borisov S.N., Voronkov M.G., Lukewitz E.Ya. Organoelement Compounds. Derivatives of Inorganogens. Leningrad: Publishing House “Chemistry”, 1966.
Palmer R.M., Green P.C. Pat. 7,381460 USA. 2008.
Wu T., Chen B. // ACS Appl. Mater. Int. 2016. V. 8. № 36. P. 24071.
Puneet P., Vedarajan R., Matsumi N. // Electrochem. Commun. 2018. № 93. P. 1.
Ситников Н.Н., Хабибуллина И.А., Мащенко В.И., Ризаханов Р.Н. // Перспективные материалы. 2018. № 2. С. 5.
Sitnikov N.N., Khabibullina I.A., Mashchenko V.I., Rizakhanov R.N. // Inorg. Mater. Appl. Res. 2018. V. 9. № 5. P. 785.
Sitnikov N.N., Mostovaya K.S., Khabibullina I.A., Mashchenko V.I. // Videoscience: Network J. 2019. V. 2. № 14. P. 1.
Ситников Н.Н., Хабибуллина И.А., Мащенко В.И., Шеляков А.В., Мостовая К.С., Высотина Е.А. // Перспективные материалы. 2020. № 4. С. 11.
Ермакова М.В., Мащенко В.И., Чаусова О.В., Соломатин А.С., Волосникова Н.И., Чаусов Д.Н. // Жидк. кристаллы и их практич. использование. 2019. V. 19. № 4. С. 61.
Mashchenko V.I., Sitnikov N.N., Khabibullina I.A., Ermakova M.V., Chausov D.N., Chausova O.V. // J. Phys.: Conf. Ser. 2019. № 1309. P. 012026.
Mashchenko V.I., Solomatin A.S., Shashkova Yu.O., Belyaev V.V. // Bull. of the Moscow Region State University. 2017. № 2. P. 34.
Мащенко В.И., Медведева И.В., Молоканова Ю.П. // Вестн. Московского гос. обл. ун-та. Сер. Естественные науки. 2015. № 2. С. 18.
Мащенко В.И., Алексеев А.Н., Картавенко Т.В., Оленин А.В. Пат. 2473216 Россия. 2013.
Моцарев Г.В., Соболевский М.В., Розенберг В.Р. Карбофункциональные органосиланы и органосилоксаны. М.: Химия, 1990.
Tang M., Wang W., Xu D., Wang Z. // Ind. Eng. Chem. Res. 2016. V. 55. № 49. P. 12582.
Liu Z., Picken S.J., Besseling N.A.M. // Macromolecules. 2014. V. 47. № 14. P. 4531.
Li X., Zhang D., Xiang K., Huang G. // Synth. RSC Adv. 2014. V. 4. № 62. P. 32894.
Зинченко Г.A., Милешкевич В.П., Козлова Н.В. // Высокомолек. соед. А. 1981. Т. 23. № 6. С. 1282.
Гридина В.Ф., Клебанский A.Л., Дорофеенко Л.П., Крупнова Л.Е. // Высокомолек. соед. А. 1967. Т. 9. № 9. С. 1946.
Грубер В.Н., Клебанский A.Л., Козлова Н.В., Кузьмина Е.В., Круглова Г.A. // Высокомолек. соед. А. 1972. Т. 14. № 7. С. 1638.
Лобков В.Д., Клебанский A.Л., Коган Э.В. // Высокомолек. соед. 1967. Т. 9. № 5. С. 1099.
Митрофанов Л.А., Сидорович Е.A., Карлин A.В., Марей A.И. // Высокомолек. соед. А. 1969. Т. 11. № 4. С. 782.
Грубер В.Н., Клебанский A.Л., Круглова Г.A., Кузьмина Е.В., Сидорович Е.A., Мокроусова Л.Я., Павлов Г.Н., Марей A.И. // Высокомолек. соед. А. 1972. Т. 14. № 7. С. 1476.
Грубер В.Н., Клебанский A.Л., Дегтева T.Г., Кузьминский A.С., Михайлова T.A., Кузьмина Е.В. // Высокомолек. соед. 1965. Т. 7. № 3. С. 462.
Ахмед-заде К.А., Закревский В.А., Митрофанов Л.А. // Высокомолек. соед. Б. 1975. Т. 17. № 9. С. 661.
Соколова M.A., Зинченко Г.A., Карташова Г.Г., Поддубный И.Я., Милешкевич В.П. // Высокомолек. соед. А. 1983. Т. 25. № 1. С. 3.
Рейхсфельд В.O., Ханходжаева Д.A. // Высокомолек. соед. А. 1967. Т. 9. № 3. С. 638.
Гридина В.Ф., Клебанский A.Л., Дорофеенко Л.П., Крупнова Л.Е., Козлова Н.В. // Высокомолек. соед. А. 1969. Т. 11. № 2. С. 426.
Зацепина T.И., Бродский M.Л., Фролова Е.A., Трапезников A.A., Грубер В.Н., Круглова Г.A. // Высокомолек. соед. 1970. Т. 12. № 11. С. 2559.
Khelevina O.G., Malyasova A.S. // Russ. J. Appl. Chem. 2014. V. 87. № 4. P. 480.
Khelevina O.G. // Russ. J. Appl. Chem. 2012. V. 85. № 2. P. 277.
Modell J., Thuresson S. Pat 7,862894 USA. 2006.
Farr R.S., Melrose J.R., Ball R.C. // Phys. Rev. E. 1997. V. 55. № 6. P. 7206.
Talreja K., Chauhan I., Ghosh A., Majumdar A., Butola B.S. // RSC Adv. 2017. № 7. P. 49787.
Li D., Wang R., Liu X., Fang S., Sun Y. // Polymers. 2018. № 10. P. 1356.
Ye F., Zhu W., Jiang W., Wang Z., Chen Q., Gong X., Xuan S. // J. Nanopart Res. 2013. № 15. P. 2122.
Barnes H.A. // J. Rheol. 1989. № 33. P. 329.
Bergenholtz J., Brady J.F., Vicic M. // J. Fluid Mech. 2002. V. 456. P. 239.
Chatterjee V.A., Dey P., Verma S.K., Bhattacharjee D., Biswas I., Neogi S. // Mater. Res. Express. 2019. № 6. P. 075702.
Li M., Lyu B., Yuan J., Dong C., Dai W. // Int. J. Machine Tools Manufact. 2015. V. 94. P. 88.
Bosco A., Calado V., Maia J. // Mater. Res. 2019. V. 22. № 5. P. 1.
Wang G., Liu X., Mi C., Fan H., Xu B., Bai X. // Pigment Resin Technol. 2018. V. 47. № 4. P. 308.
Мащенко В.И., Ситников Н.Н., Хабибуллина И.А. Пат. 2714203 Россия. 2019.
Lidin R.A., Molochko V.A., Andreeva L.L., Lidin R.A. Chemical Properties of Inorganic Substances. Moscow: Publishing House “Chemistry”, 2000.
Tkachev K.V., Plyshevsky Yu.S. Technology of Inorganic Compounds of Boron. Leningrad: Publishing House “Chemistry”, 1983.
Семчиков Ю.Д. Высокомолекулярные соединения. М.: Академия, 2010.
Borodulina T., Bermesheva E., Smirnova N., Ilyin S., Brantseva T., Antonov S. // J. Adhesion Sci. Technol. 2014. V. 28. № 16. P. 1629.
Brantseva T., Antonov S., Kostyuk A., Ignatenko V., Smirnova N., Korolev Y., Ilyin S. // Eur. Polym. J. V. 76. P. 228.
Pocius A.V. Adhesion and Adhesives Technology: An Introduction. Munchen: Hanser Publishers, 2002.
Малкин А.Я. Основы реологии. СПб.: ЦОП “Профессия”, 2018.
Malkin A.Y., Ilyin S.O., Arinina M.P., Kulichikhin V.G. // Coll. Polym. Sci. 2017. V. 295. № 4. P. 555.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия А)