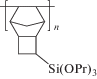Высокомолекулярные соединения (серия Б), 2019, T. 61, № 6, стр. 468-474
АДДИТИВНАЯ ПОЛИМЕРИЗАЦИЯ ТРИЦИКЛОНОНЕНА, СОДЕРЖАЩЕГО СИЛАТРАНОВЫЕ ГРУППЫ
Д. А. Алентьев a, Д. М. Джапаридзе a, М. В. Бермешев a, *
a Институт нефтехимического синтеза им. А.В. Топчиева Российской академии наук
119991 Москва, Ленинский пр., 29, Россия
* E-mail: bmv@ips.ac.ru
Поступила в редакцию 19.06.2019
После доработки 11.07.2019
Принята к публикации 25.07.2019
Аннотация
Впервые исследована аддитивная полимеризация производного норборнена, содержащего силатрановую группу. Продемонстрирована возможность синтеза насыщенного полимера на основе данного мономера в присутствии Pd- и Ni-катализаторов. Найдены условия полимеризации, при которых полимеры образуются с высоким выходом. Они являются нерастворимыми, термостойкими и аморфными. Исследованы физико-химические свойства синтезированного полимера.
ВВЕДЕНИЕ
Гомо- и сополимеры на основе циклоалкенов представляют интерес для создания полимерных материалов с высокими температурами стеклования, термической и химической стабильностью [1–5]. Такие полимеры в зависимости от природы боковых заместителей могут обладать высокой прозрачностью, низким влагопоглощением, а также служить потенциальными материалами для мембранного газоразделения [6–8], первапорации [9, 10], изготовления фоторезистов [11], адгезивов [12], подложек для катализаторов [13] и т.д. Привлекательной группой среди циклоалкенов являются норборнен и его производные. Такие мономеры, как правило, синтезируют с использованием реакций [4 + 2]- и [2 + 2 + 2]-циклоприсоединения или модификацией норборнадиена-2,5 [7, 14–16]. Это позволяет получать широкий набор мономеров данного типа с закономерно изменяемым строением и далее отслеживать влияние строения мономерного звена на свойства синтезируемых из данных мономеров полимеров. Кроме того, норборнены могут полимеризоваться по нескольким направлениям с образованием разных полимеров [1, 17–19]. Таким образом, благодаря перечисленным выше преимуществам открываются широкие возможности для макромолекулярного дизайна и направленного синтеза полимеров с заданными свойствами на основе норборненов. Недавно было показано, что введение в боковые заместители полинорборненов подвижных фрагментов Si–O–C приводит к появлению интересных газотранспортных свойств, например, высокой селективности разделения газообразных углеводородов [6, 8, 20]. К настоящему моменту успешно синтезированы полимеры с различным числом фрагментов Si–O–C в боковых заместителях (такие как группы SiMe3 – n(OEt)n), а также с разной длиной алкильных групп в –(AlkO)3Si-заместителях. Во всех случаях наблюдался рост селективности газоразделения с увеличением числа фрагментов Si–O–C или размера триалкоксисилильного заместителя. В рамках дальнейшего развития данного направления перспективным представляется синтез новых полимеров с другим типом Si–O–C-содержащих групп. Так, недавно был получен метатезисный полинорборнен с силатрановой группой в боковой цепи [21]. В настоящей работе мы впервые исследовали аддитивную полимеризацию этого мономера. Необходимо отметить, что аддитивная полимеризация замещенных норборненов сильно чувствительна к введению заместителя и особенно заметно снижается активность мономеров при введении объемных или полярных групп [1]. Силатрановый фрагмент сочетает в себе оба названных фактора (является объемным и содержит реакционноспособные центры), следовательно, поиск эффективных каталитических систем для вовлечения производного норборнена с таким заместителем в аддитивную полимеризацию представлял особый интерес.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы и методы
Все прекатализаторы, сокатализаторы и трициклогексилфосфин (“Aldrich”) использовали без дополнительной очистки. Pd-N-гетероциклический карбеновый комплекс (SIPrPd(cinn)Cl) синтезировали по методике [22]; однокомпонентный катализатор на основе никеля ((η6-PhMe)Ni(C6F5)2) – по методике [23]. 1,2-Дихлорэтан абсолютизировали над P2O5, хлороформ – над CaH2 и хранили в атмосфере аргона. 3-Силатранилтрицикло[4.2.1.02.5]нон-7-ен (TCNSA) получали по методике, описанной ранее в работе [24].
Спектры ЯМР 13C твердого тела (CP/MAS) регистрировали на спектрометре “Varian Unity Inova AS500” (США) при частоте 125 МГц. Калориметрические исследования выполняли на дифференциальном сканирующем калориметре фирмы “Mettler” (США) марки ТА-4000 с нагревательной ячейкой DSC-30 при скорости повышения температуры 20 град/мин в атмосфере аргона и на воздухе. Рентгенофазовый анализ выполняли с использованием детектора ASX (“Bruker”, США) и излучения CuKα (длина волны λ = = 1.54 Å).
Аддитивная полимеризация TCNSА
Полимеризация TCNSА на Pd-катализаторе. Методика описана на примере аддитивной полимеризации TCNSА при соотношении TCNSА : : Pd(OAc)2 : NaBARF : PCy3 = 500 : 1 : 5 : 2. Другие эксперименты проводили аналогично. Каталитическую смесь готовили непосредственно перед полимеризацией. Для этого в атмосфере аргона смешивали 2.0 мг (8.9 × 10–6 моля) Pd(OAc)2, 39 мг (4.5 × 10–5 моля) тетракис-[3,5-бис-(трифторметил)фенил]бората натрия (NaBARF) и 5.0 мг (1.8 × 10–5 моля) трициклогексилфосфина (PCy3). Затем полученную смесь растворяли в 3.9 мл абсолютного 1,2-дихлорэтана и перемешивали 5 мин. В атмосфере аргона в виалу вносили 200 мг (6.8 × 10–4 моля) TCNSА, затем вводили 4.0 мл абсолютного 1,2-дихлорэтана и перемешивали до полного растворения. К раствору добавляли 0.6 мл каталитической смеси и перемешивали 5 мин, после чего оставляли на 1 ч 20 мин. Образовавшийся белый осадок центрифугировали, отделяли и промывали на экстракторе Сокслета абсолютным 1,2-дихлорэтаном в течение 3 ч. Полученный белый порошкообразный полимер сушили в вакууме до постоянной массы. Выход 153 мг (76%).
ЯМР 13C CP/MAS (δ, м.д.): 66.2–35.7, 35.7–18.5.
ИК (ATR, см–1): 3000–2800 (С–H), 1500–1220, 1160–1030 (Si–O), 1012, 950–835, 810–640.
Полимеризация TCNSА на Ni-катализаторе. Методика представлена на примере полимеризации TCNSА при соотношении мономер : катализатор = 100 : 1. Другие эксперименты проводили аналогично. Раствор катализатора готовили непосредственно перед полимеризацией. Для этого в атмосфере аргона в виалу помещали 10 мг (1.1 × × 10–5 моля, чистота 54 мол.%) (η6-PhMe)Ni(C6F5)2, вводили 2.2 мл абсолютного 1,2-дихлорэтана. Смесь перемешивали 5 мин и фильтровали от твердого остатка. В атмосфере аргона в виалу вносили 100 мг (3.4 × 10–4 моля) TCNSА, затем добавляли 0.67 мл раствора катализатора и перемешивали в течение 2 мин, после чего реакционную смесь разбавляли 1 мл абсолютного 1,2-дихлорэтана и оставляли на 1 ч. Полученную неподвижную бледно-розовую массу промывали на экстракторе Сокслета абсолютным 1,2-дихлорэтаном в течение 3 ч. Введенный белый порошкообразный полимер сушили в вакууме до постоянной массы. Выход: 100 мг (100%).
Спектры ЯМР 13C CP/MAS и ИК аналогичны спектрам РTCNSА полученного на Pd-катализаторе.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В качестве мономера норборненового ряда, содержащего силатрановую группу, использовали TCNSA. Ранее нами уже была изучена его метатезисная полимеризация. Было показано, что он вступает в эту реакцию довольно активно, образуя аморфный стеклообразный полимер, растворимый в 1,2-дихлорэтане и апротонных диполярных растворителях [21].
В настоящей работе детально изучена аддитивная полимеризация TCNSA в присутствии различных каталитических систем.
Ранее было показано, что наиболее активными катализаторами для аддитивной полимеризации кремнийсодержащих норборненов являются комплексы палладия и никеля, активируемые бор- и алюминийорганическими сокатализаторами [1, 6, 25, 26]. Исходя из этого, для изучения аддитивной полимеризации TCNSА были опробованы различные каталитические системы на основе Pd и Ni (табл. 1). Оказалось, что практически все Pd-содержащие системы позволяют вовлекать TCNSA в аддитивную полимеризацию. Однако активность каталитической системы существенно зависела от природы используемого сокатализатора. Наиболее оптимальным сокатализатором для систем на основе Pd оказался NaBARF в присутствии трициклогексилфосфина (PCy3). Так, например, в случае сокатализатора TrFABA соответствующие полимеры не удавалось получить, либо наблюдалось образование лишь следов полимеров. Это может быть связано с взаимодействием карбокатиона Tr+ (Ph3C+) с аминогруппой, содержащейся в мономере, приводящим к дезактивации этого сокатализатора. Наиболее оптимальной с точки зрения активности и доступности Pd-системой для полимеризации TCNSA среди опробованных является Pd(OAc)2/NaBARF/PCy3. В качестве Ni-катализаторов были взяты как классические двух- и трехкомпонентные системы, так и комплекс (η6-PhMe)Ni(C6F5)2, не требующий введения сокатализатора в систему. Каталитические системы на основе Ni оказались менее активными, чем Pd-катализаторы. В присутствии систем на основе солей никеля(II), активированных бор- и/или алюминийорганическими сокатализаторами, которые проявили ранее высокую активность при полимеризации Me3Si-замещенных норборненов [7, 27], полимеризацию TCNSА осуществить не удалось. Однако довольно высокую активность проявил однокомпонентный катализатор на основе никеля – (η6-PhMe)Ni(C6F5)2. Он позволил получить желаемый полимер с выходом, близким к количественному при невысоком мольном соотношении мономер : катализатор (табл. 1). Интересно, что вне зависимости от природы прекатализатора, сокатализатора, а также условий полимеризации (растворителя, концентрации мономера, температуры, времени реакции) полимеризация протекает с образованием продукта, не растворимого в органических растворителях, таких как: н-гексан, толуол, хлороформ, 1,2-дихлорэтан, ТГФ, ацетон, ДМФА, ДМСО, тетраметилмочевина. В отдельных случаях (при использовании каталитических систем на основе Pd) на начальной стадии полимеризации (при низких конверсиях мономера) реакционная смесь становилась вязкой, что, по-видимому, связано с образованием олигомерных фракций. Однако выделить растворимый олигомер/полимер не удалось: попытки осаждения различными растворителями приводили к формированию небольшого количества порошкообразного вещества, далее являющегося нерастворимым.
Таблица 1.
Условия аддитивной полимеризации TCNSА
| Каталитическая система | Мольное соотношение мономер : катализатор : : другие компоненты каталитической системы | Концентрация мономера в реакционной смеси с × 10, моль/л | Время реакции, ч | Выход, % |
|---|---|---|---|---|
| Pd(OAc)2/MAO | 3000 : 1 : 1000 | 3.2 | 300 | 21 |
| Pd(OAc)2/TrFABA | 3000 : 1 : 3 | 4.3 | 300 | – |
| Pd(OAc)2/TrFABA/PCy3 | 3000 : 1 : 3 : 3 | 3.1 | 300 | 3 |
| Pd(OAc)2/NaBARF/PCy3 | 500 : 1 : 5 : 2 | 1.5 | 1.3 | 76 |
| 1000 : 1 : 5 : 2 | 1.5 | 1.3 | 58 | |
| 3000 : 1 : 5 : 2 | 2.6 | 3.5 | 13 | |
| SIPrPd(cinn)Cl/AgOTf | 1000 : 1 : 2 | 3.1 | 300 | 48 |
| SIPrPd(cinn)Cl/AgSbF6 | 1000 : 1 : 2 | 3.1 | 300 | 35 |
| SIPrPd(cinn)Cl/NaBARF/PCy3 | 1000 : 1 : 5 : 2 | 3.1 | 100 | 53 |
| Ni(EtHex)2/MAO | 1000 : 1 : 3 | 3.1 | 300 | – |
| Ni(EtHex)2/NaBARF/MAO | 1000 : 1 : 3 : 200 | 3.0 | 300 | – |
| (η6-PhMe)Ni(C6F5)2 | 100 : 1 | 5.1 | 1 | 100 |
| 500 : 1 | 5.1 | 1 | 29 |
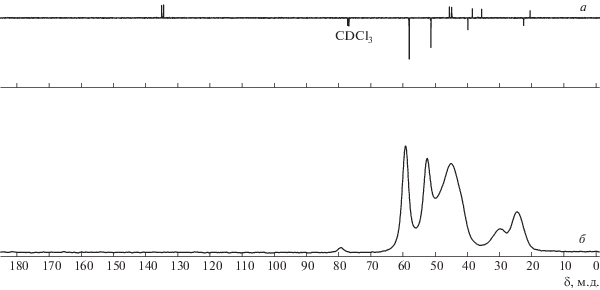
По данным ЯМР-спектроскопии твердого тела, в процессе аддитивной полимеризации TCNSA действительно получается насыщенный полимер: сигналы при 130–140 м.д. на спектре ЯМР 13C полимера отсутствуют (рис. 1). Спектр представлен широкими сигналами в области 18–70 м.д., характерными для аддитивных полинорборненов [28] и силатрановой группы [24]. Более узкие сигналы (с максимумами при 59 и 53 м.д.), по-видимому, относятся к атомам углерода в силатрановой группе: на спектре мономера этим атомам углерода соответствуют сигналы при 51 и 58 м.д. [24].
По данным рентгенофазового анализа, аддитивный PTCNSA является аморфным (рис. 2). Его дифрактограмма аналогична дифрактограмме метатезисного PTCNSA и представлена одним широким пиком при 2θ = 15° (табл. 2). Дифрактограммы других аддитивных полинорборненов (незамещенного полинорборнена и родственного политрициклононена, содержащего три(н-алкокси)силильные группы) схожи между собой и принципиально отличаются от дифрактограммы аддитивного РTCNSА. На них присутствует два пика: при 2θ ≈ 10° и 20° (табл. 2). Исходя из этого, а также учитывая схожесть дифрактограмм метатезисного и аддитивного PTCNSA, можно предположить, что в случае РTCNSА силатрановая группа вносит больший вклад во вторичную структуру полимера, чем основные цепи.
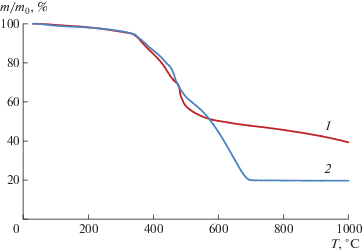
Аддитивный PTCNSA проявил высокую термическую стабильность. По данным ТГА (рис. 3), температура его разложения (95% потери массы) составляет 330°C в аргоне и на воздухе. Термическое разложение полимера на воздухе в отличие от разложения в аргоне приводит к образованию твердого остатка, составляющего ~20% изначальной массы, не изменяющегося при повышении температуры. Это свидетельствует об окислении полимера кислородом воздуха. Следует отметить, что остаток SiO2, который может образоваться из полимера, равен 20% от изначальной массы. Исходя из этого, именно SiO2, по-видимому, и является твердым остатком. Аддитивный PTCNSA является стеклообразным: его температура стеклования не проявляется на кривых ДСК и скорее всего превышает температуру разложения.
Комбинация жестких основных цепей и объемных жестких заместителей может обеспечить формирование интересной пористой структуры в аддитивном PTCNSA, а полимер – представлять потенциальный интерес в качестве материала для хранения газов или наполнителя при создании композиционных мембранных материалов для газоразделения.
ЗАКЛЮЧЕНИЕ
Впервые изучена аддитивная полимеризация силатранил-замещенного производного норборнена. Показано, что данный мономер, несмотря на наличие в его структуре реакционноспособных фрагментов Si–O–C и аминогрупп, может быть успешно вовлечен в аддитивную полимеризацию с образованием насыщенного гомополимера. Найдены эффективные катализаторы аддитивной полимеризации на основе соединений как Pd, так и Ni, позволяющие получать полимеры с высоким выходом. Вне зависимости от природы используемого катализатора и условий полимеризация приводит к не растворимому в органических растворителях полимеру. Синтезированный новый полимер является стеклообразным, аморфным, а также обладает высокой термической стабильностью.
Авторы выражают благодарность М.А. Топчию, А.Ф. Асаченко, П.С. Грибанову, М.С. Нечаеву за предоставление образцов Pd-N-гетероциклического карбенового комплекса (SIPrPd(cinn)Cl).
Работа выполнена в рамках государственного задания ИНХС РАН.
Список литературы
Bermeshev M.V., Chapala P.P. // Prog. Polym. Sci. 2018. V. 84. P. 1.
Khanarian G., Celanese H. // Opt. Eng. 2001. V. 40. № 6. P. 1024.
Bykov V.I., Makovetskii K.L., Popov D.S., Bermeshev M.V., Butenko T.A., Filatova M.P., Finkel’shtein E.Sh. // Polymer Science B. 2012. V. 54. № 1–2. P. 99.
Yin H., Chapala P., Bermeshev M., Pauw B.R., Schönhals A., Böhning M. // ACS Appl. Polym. Mater. 2019. V. 1. № 4. P. 844.
Porz M., Paulus F., Höfle S., Lutz T., Lemmer U., Colsmann A., Bunz U.H.F. // Macromol. Rapid Commun. 2013. V. 34. № 20. P. 1611.
Alentiev D.A., Egorova E.S., Bermeshev M.V., Starannikova L.E., Topchiy M.A., Asachenko A.F., Gribanov P.S., Nechaev M.S., Yampolskii Yu.P., Finkelshtein E.Sh. // J. Mater. Chem. A. 2018. V. 6. № 40. P. 19393.
Alentiev D.A., Bermeshev M.V., Starannikova L.E., Bermesheva E.V., Shantarovich V.P., Bekeshev V.G., Yampolskii Y.P., Finkelshtein E.S. // J. Polym. Sci., Polym. Chem. 2018. V. 56. № 12. P. 1234.
Maroon C.R., Townsend J., Gmernicki K.R., Harrigan D.J., Sundell B.J., Lawrence J.A., Mahurin S.M., Vogiatzis K.D., Long B.K. // Macromolecules. 2019. V. 52. № 4. P. 1589.
Kang B.-G., Kim D.-G., Register R.A. // Macromolecules. 2018. V. 51. № 10. P. 3702.
Kim D.-G., Takigawa T., Kashino T., Burtovyy O., Bell A., Register R.A. // Chem. Mater. 2015. V. 27. № 19. P. 6791.
Feiring A.E., Crawford M.K., Farnham W.B., Feldman J., French R.H., Junk C.P., Leffew K.W., Petrov V.A., Qiu W., Schadt F.L., Tran H.V., Zumsteg F.C. // Macromolecules. 2006. V. 39. № 9. P. 3252.
Bermesheva E.V., Alentiev D.A., Moscalets A.P., Bermeshev M.V. // Polymer Science B. 2019. V. 61. № 3.
García-Loma R., Albéniz A.C. // Asian J. Org. Chem. 2019. V. 8. № 3. P. 304.
Uozumi Y., Sang-Yong L., Hayashi T. // Tetrahedron Lett. 1992. V. 33. № 47. P. 7185.
Bulgakov B.A., Bermeshev M.V., Demchuk D.V., Lakhtin V.G., Kazmin A.G., Finkelshtein E.S. // Tetrahedron. 2012. V. 68. № 9. P. 2166.
Finkelshtein E., Gringolts M., Bermeshev M., Chapala P., Rogan Yu. // Membrane Materials for Gas and Vapor Separation / Ed. by Yu. Yampolskii, E. Finkelshtein. Chichester: Wiley, 2017. P.143.
Bielawski C.W., Grubbs R.H. // Prog. Polym. Sci. 2007. V. 32. № 1. P. 1.
Bermeshev M.V., Bulgakov B.A., Genaev A.M., Kostina J.V., Bondarenko G.N., Finkelshtein E.Sh. // Macromolecules. 2014. V. 47. № 16. P. 5470.
Gaylord N.G., Deshpande A.B., Mandal B.M., Martan M. // J. Macromol. Sci. A. 1977. V. 11. № 5. P. 1053.
Sundell B.J., Lawrence Iii J.A., Harrigan D.J., Vaughn J.T., Pilyugina T.S., Smith D.R. // RSC Adv. 2016. V. 6. № 57. P. 51619.
Alent'iev D.A., Dzhaparidze D.M., Chapala P.P., Bermeshev M.V., Belov N.A., Nikiforov R.Yu., Starannikova L.E., Yampol’skii Yu.P., Finkel’shtein E.Sh. // Polymer Sciemce B. 2018. V. 60. № 5. P. 612.
Viciu M.S., Germaneau R.F., Nolan S.P. // Org. Lett. 2002. V. 4. № 23. P. 4053.
Brezinski M.M., Klabunde K.J. // Organometallics. 1983. V. 2. № 9. P. 1116.
Alentiev D.A., Chapala P.P., Filatova M.P., Finkelshtein E.Sh., Bermeshev M.V. // Mendeleev Commun. 2016. V. 26. № 6. P. 530.
Tsai S.D., Register R.A. // Macromol. Chem. Phys. 2018. V. 219. № 11. P. 1800059.
Lipian J., Mimna R.A., Fondran J.C., Yandulov D., Shick R.A., Goodall B.L., Rhodes L.F., Huffman J.C. // Macromolecules. 2002. V. 35. № 24. P. 8969.
Gringol’ts M.L., Bermeshev M.V., Syromolotov A.V., Starannikova L.E., Filatova M.P., Makovetskii K.L., Finkel’shtein E.Sh. // Pet. Chem. 2010. V. 50. № 5. P. 352.
Alentiev D., Dzhaparidze D., Gavrilova N., Shantarovich V., Kiseleva E., Topchiy M., Asachenko A., Gribanov P., Nechaev M., Legkov S., Bondarenko G., Bermeshev M. // Polymers. 2018. V. 10. № 12. P. 1382.
Zhao C.-T., do Rosário Ribeiro M., de Pinho M.N., Subrahmanyam V.S., Gil C.L., de Lima A.P. // Polymer. 2001. V. 42. № 6. P. 2455.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)