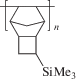Высокомолекулярные соединения (серия Б), 2019, T. 61, № 6, стр. 475-480
АДДИТИВНАЯ СОПОЛИМЕРИЗАЦИЯ КРЕМНИЙСОДЕРЖАЩЕГО ТРИЦИКЛОНОНЕНА С ДИМЕРОМ НОРБОРНАДИЕНА-2,5
Д. А. Алентьев a, Д. М. Джапаридзе a, М. В. Бермешев a, *, Л. Э. Старанникова a, М. П. Филатова a, Ю. П. Ямпольский a, Е. Ш. Финкельштейн a
a Институт нефтехимического синтеза им. А.В. Топчиева Российской академии наук
119991 Москва, Ленинский пр., 29, Россия
* E-mail: bmv@ips.ac.ru
Поступила в редакцию 11.06.2019
После доработки 17.07.2019
Принята к публикации 26.07.2019
Аннотация
Синтезирована серия аддитивных сополимеров 3-триметилсилилтрицикло[4.2.1.02,5]нон-7-ена с бифункциональным сомономером – димером норборнадиена-2,5. Продемонстрировано, что при введении небольшого количества димера норборнадиена-2,5 (до 0.3 мол. %) наблюдается увеличение молекулярной массы полимера. При использовании большого количества димера норборнадиена-2,5 образуются сшитые нерастворимые полимеры. На примере сополимера, содержащего 0.3 мол. % звеньев димера норборнадиена-2,5, показано, что введение бифункционального сомономера не приводит к существенному снижению газопроницаемости, а разработанный метод может применяться для увеличения молекулярных масс аддитивных полимеров, улучшения их механических свойств и придания полимерам устойчивости к пластификации.
ВВЕДЕНИЕ
В последние несколько десятилетий активно проводится поиск новых полимерных материалов для мембранного газоразделения. Одним из результатов такого поиска стал успешный синтез новых классов высокопроницаемых стеклообразных полимеров: полиацетиленов [1–4], полимеров с внутренней микропористостью [5–7], термически перегруппированных полимеров [8, 9] и т.д. Эти полимеры обладают рекордными коэффициентами газопроницаемости. Однако их практическое использование ограничено вследствие ряда причин [10–13]: старение во времени из-за большого свободного объема (по релаксационным, сорбционным и другим механизмам), низкая селективность разделения газов, недостаточно хорошие механические свойства и т.д. Привлекательным классом высокопроницаемых стеклообразных полимеров являются аддитивные полинорборнены, содержащие группы Me3Si. Они обладают большим свободным объемом и являются микропористыми материалами. Эти полимеры представляют интерес для разделения газообразных углеводородов и выделения фракции С3+ из природного и попутного нефтяного газов [14–16]. Однако у них есть недостатки, характерные для стеклообразных полимеров (такие как старение, в отдельных случаях – не очень хорошие пленкообразующие свойства из-за сложности получения высокомолекулярных продуктов при полимеризации), и, кроме того, они подвержены пластификации углеводородами C3+. Введение бифункциональных сомономеров на стадии полимеризации может способствовать устранению указанных недостатков. При их применении, в зависимости от их количества, могут образовываться разветвленные или сшитые полимерные структуры, которые могут иметь лучшие пленкообразующие свойства, большую устойчивость к углеводородам C3+, а также, возможно, большую стабильность свойств во времени [17]. В настоящей работе в качестве бифункционального сомономера предложен димер норборнадиена-2,5. Данный мономер содержит две химически эквивалентные двойные связи, способные к полимеризации и находящиеся на значительном расстоянии относительно друг друга (по сравнению, например, с норборнадиеном-2,5). Ранее было показано, что указанный димер обладает высокой активностью в аддитивной гомополимеризации, которая приводила к образованию нерастворимых сшитых микропористых полимеров с высокой удельной поверхностью [18]. Это свидетельствует о том, что димер норборнадиена-2,5 подходит в качестве сомономера для создания разветвленных и сшитых полимеров при аддитивной полимеризации Me3Si-замещенных норборненов, а также ввиду высокой пористости гомополимеров на его основе. Нам представлялось, что при использовании его в качестве модификатора не должно наблюдаться значительного снижения уровня газопроницаемости Me3Si-замещенных аддитивных полинорборненов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы и методы
Спектры ЯМР 1H регистрировали на спектрометре “AvanceTM DRX-500” (“Bruker”, США) на рабочей частоте 500.13 МГц. В качестве растворителя использовали CDCl3. Сигналы относили по остаточным протонам в CDCl3 (7.24 м.д.). Молекулярную массу полимеров оценивали методом гельпроникающей хроматографии на хроматографе высокого давления “Waters” (США) (колонка Microgel mix 1–5 мкм 500 мм × 7.7 мм Chrompack, растворитель – ТГФ, объем пробы 100 мкл, концентрация образцов 1–2 мг/мл), оснащенном рефрактометрическим детектором. Калибровку проводили по полистирольным стандартам с М = (1 × 103)–(1 × 106). Расчет молекулярно-массовых характеристик осуществляли по калибровочной зависимости, которая является линейной в диапазоне (1 × 103)–(1 × 106).
Газохроматографический анализ выполняли на газовом хроматографе “Кристалл 5000” (“Хроматэк”, Россия) с капиллярной колонкой “SGE Analytical Science” (Австралия) (капиллярная колонка PDMS DB-5 (полидиметилсилоксан, содержащий 5% фенильных групп), 25 м × 0.32 мм, газ-носитель азот) и пламенно-ионизационным детектором (температура на детекторе 200°С, расход водорода 25 мл/мин, воздуха – 250 мл/мин, азота – 25 мл/мин). Параметры колонки: температура термостатирования колонки 40°С, давление газа-носителя 71.519 кПа, поток газа-носителя 2.5 мл/мин, скорость газа-носителя 39.7 см/с, сбросный расход 30 мл/мин. Температура на испарителе 250°C.
Механические свойства полимерных пленок определяли с использованием разрывной машины (скорость деформации 0.33 мм/с, длина пленки 1.00 см).
Толуол абсолютизировали кипячением над Na (4 ч) с последующей перегонкой в аргоне. Хлороформ абсолютизировали кипячением над CaH2 (5 ч) с последующей перегонкой в аргоне. Абсолютные растворители хранили в аргоне. Ацетат палладия, тетракис-[3,5-бис-(трифторметил)фенил]борат натрия (NaBARF), трициклогексилфосфин (PCy3) (“Aldrich”), метанол, этанол использовали без дополнительной очистки.
3-Триметилсилилтрицикло[4.2.1.02,5]нон-7-ен (TCNSi) получали по стандартной методике путем исчерпывающего метилирования 3-трихлорсилилтрицикло[4.2.1.02,5]нон-7-ена метилиодидом [19].
Димер норборнадиена (DNBD) синтезировали в виде смеси с тримером норборнадиена-2,5 (4 : 1) олигомеризацией норборнадиена-2,5 в присутствии Ni(COD)2 [20] и выделяли в чистом виде (>98%) многократной перекристаллизацией из этанола.
Аддитивная сополимеризация TCNSi с DNBD
Процедура описана на примере сополимеризации TCNSi с DNBD при соотношении TCNSi : : DNBD : Pd(OAc)2 : NaBARF : PCy3 = 3000 : 10 : 1 : : 5 : 2. Другие эксперименты проводились аналогично. Каталитическую смесь готовили непосредственно перед полимеризацией. Для этого в реактор Шленка помещали 1.69 мг (7.53 × 10–3 ммоля) Pd(OAc)2, 33.36 мг (3.76 × 10–2 ммоля) NaBARF и 4.22 мг (1.51 × 10–2 ммоля) PCy3. Реактор Шленка три раза вакуумировали и заполняли аргоном, затем в инертной атмосфере вводили 7.31 мл абсолютного хлороформа. Смесь перемешивали 5 мин. В предварительно трижды отвакуумированную и заполненную аргоном круглодонную стеклянную ампулу вводили 1.50 г (7.80 ммоля) TCNSi, 0.552 мл (2.60 × 10–2 ммоля) раствора DNBD в абсолютном хлороформе (4.70 × 10–2 моль/л) и 5 мл абсолютного толуола. Полимеризацию инициировали добавлением 2.52 мл (2.60 × 10–3 ммоль Pd) каталитической смеси. Смесь перемешивали, ампулу запаивали и оставляли при 30°C на 160 ч. Затем реакционную смесь растворяли в толуоле (2 мл) и осаждали в метанол. Полимер отделяли, промывали 3 раза метанолом и сушили в вакууме. Полимер дважды переосаждали из толуола в метанол и сушили в вакууме при 80–90°C до постоянной массы. Выход 1.02 г (68%). Mw = 1.1 × 106, Ð = 5.4.
ЯМР-спектры сополимера оказались идентичными спектрам TCNSi [19]. Механические свойства: E = 640 МПа, ε = 11%, σ = 33 МПа.
Приготовление пленок и измерение коэффициентов газопроницаемости
Пленки получали поливом на целлофановую подложку из 5%-ного раствора полимера в толуоле. После испарения растворителя пленку выдерживали в вакууме до постоянной массы (остаточное давление при вакуумировании составляло не более 1 мм рт. ст.). Толщина пленок 80–90 мкм.
Коэффициенты проницаемость газов измеряли на газохроматографической установке при температуре 20–22°С и перепаде парциального давления пенетранта 1 атм. Поток пенетранта пропускали при атмосферном давлении сверху пленки, а снизу пленки подавали при атмосферном давлении газ-носитель Не (при определении P(He) и P(H2) – азот). Погрешность измерения коэффициентов газопроницаемости 5–10%.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В настоящей работе была изучена аддитивная сополимеризация 3-триметилсилилтрицикло[4.2.1.02,5]нон-7-ена с димером норборнадиена-2,5.
Сополимеризацию осуществляли в присутствии каталитической системы Pd(OAc)2/NaBARF/PCy3, при мольном соотношении TCNSi : катализатор = = 3000 : 1 и различных соотношениях TCNSi : : DNBD (табл. 1). Растворителем служила система толуол–хлороформ (70 об. % толуола).
Таблица 1.
Аддитивная сополимеризация TCNSi с DNBD
| Содержание DNBD в смеси мономеров, мол. % | Выход, % | Mw × 10–3 | Ð | Содержание звеньев DNBD в сополимере*, мол. % |
|---|---|---|---|---|
| 0 | 56 | 637 | 2.9 | 0 |
| 0.01 | 65 | 647 | 3.1 | 0.015 |
| 0.05 | 68 | 689 | 3.2 | 0.08 |
| 0.1 | 61 | 747 | 4.0 | 0.15 |
| 0.3 | 68 | 1098 | 5.4 | 0.45 |
| 1 | 67 | Не растворяется | 1.5 | |
| 3 | 69 | 4.5 | ||
Показано, что введение DNBD в качестве сомономера даже в небольшом количестве (менее 0.1 мол. %) способствует повышению молекулярной массы полимера. Введение DNBD в количестве 1 мол. % и более приводит к образованию геля, содержащего сшитый нерастворимый полимер, причем степень сшивки возрастает с увеличением количества сомономера: при 1 мол. % DNBD сополимер набухает сильнее, чем при 3 мол. %. Для дальнейшего изучения свойств был выбран сополимер, содержащий 0.3 мол. % звеньев DNBD : он остается растворимым, при этом его молекулярная масса достигает 1.1 × 106. Необходимо отметить, что ранее не удавалось достичь таких высоких молекулярных масс при аддитивной гомополимеризации TCNSi. Согласно данным ЯМР-спектроскопии, в результате сополимеризации образуется разветвленный полимер: в спектрах полимеров отсутствуют сигналы двойных связей. Это указывает на то, что обе двойные связи DNBD вступают в полимеризацию.
Данные по газопроницаемости аддитивного сополимера TCNSi с 0.3 мол. % DNBD, а также гомополимеров TCNSi, полученных в присутствии различных каталитических систем, представлены в табл. 2. Приведенные данные свидетельствуют о том, что введение DNBD практически не сказывается на проницаемости постоянных газов по сравнению с РTCNSi [21] и вызывает снижение на 25% проницаемости углеводородов C3+. Это, по-видимому, связано с тем, что в присутствии углеводородов сополимер пластифицируется в меньшей степени, чем гомополимер на основе TCNSi, поскольку сополимер является разветвленным.
Таблица 2.
Коэффициенты проницаемости газов РTCNSi и сополимера TCNSi с DNBD
| Полимер, № | Структура полимера | Значения P (Баррер) для газов | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| He | H2 | O2 | N2 | CO2 | CH4 | C2H6 | C3H8 | н-C4H10 | ||
| 1* [14] | 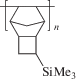 |
930 | 2060 | 990 | 390 | 5300 | 1010 | 1360 | 1470 | 13 030 |
| 2** [21] |  |
1270 | 2820 | 1080 | 430 | 5980 | 1130 | 1720 | 1880 | 14 700 |
| 3 |  |
1300 | 2780 | 1040 | 430 | 5400 | 1030 | 1640 | 1450 | 10 800 |
| 4*** |  |
1460 | 3250 | 1470 | 670 | 7060 | 1650 | 2270 | 2300 | 16 800 |
Значения идеальных селективностей газоразделения сополимера в большинстве случаев близки к значениям для РTCNSi. Исключение составляют селективности разделения углеводородов (С3/С1 и C4/C1), значения которых для сополимера ниже, чем для РTCNSi.
Обработка сополимера TCNSi с 0.3 мол. % DNBD этанолом приводила к эффекту, характерному для высокопроницаемых стеклообразных полимеров [15, 22], – увеличению коэффициентов газопроницаемости (на 10–60%) и небольшому снижению селективности разделения газов (табл. 2 и 3).
Таблица 3.
Селективности разделения газов для поли(TCNSi) и сополимера TCNSi с DNBD
По механическим свойствам аддитивный сополимер TCNSi с 0.3 мол. % DNBD (модуль Юнга E = 640 МПа, относительное удлинение при разрыве ε = 11%, прочность на разрыв σ = 33 МПа) оказался близок к аддитивному гомополимеру TCNSi (E = 650 МПа, ε = 8%, σ = 35 МПа). Эти данные указывают на то, что введение 0.3 мол. % бифункциональных звеньев в аддитивный РTCNSi способствует небольшому увеличению относительного удлинения при разрыве и незначительному снижению прочности на разрыв.
ЗАКЛЮЧЕНИЕ
Разработан новый способ модификации аддитивных полинорборненов на примере поли(3-триметилсилилтрициклононена), позволяющий повышать их молекулярную массу за счет формирования разветвленных структур. Проведенные исследования в дальнейшем помогут решить проблемы, связанные с образованием в аддитивной полимеризации низкомолекулярных продуктов, придавать хорошие пленкообразующие свойства перспективным для мембранного газоразделения кремнийсодержащим полинорборненам, не способным формировать пленки, а также придавать полимерам устойчивость к пластификации углеводородами.
Работа выполнена в рамках государственного задания ИНХС РАН.
Список литературы
Takada K., Matsuya H., Masuda T., Higashimura T. // J. Appl. Polym. Sci. 1985. V. 30. № 4. P. 1605.
Platé N.A., Bokarev A.K., Kaliuzhnyi N.E., Litvinova E.G., Khotimskii V.S., Volkov V.V., Yampol’skii Y.P. // J. Membr. Sci. 1991. V. 60. № 1. P. 13.
Yave W., Peinemann K.-V., Shishatskiy S., Khotimskiy V., Chirkova M., Matson S., Litvinova E., Lecerf N. // Macromolecules. 2007. V. 40. № 25. P. 8991.
Bakhtin D.S., Kulikov L.A., Legkov S.A., Khotimskiy V.S., Levin I.S., Borisov I.L., Maksimov A.L., Volkov V.V., Karakhanov E.A., Volkov A.V. // J. Membr. Sci. 2018. V. 554. P. 211.
McKeown N.B., Budd P.M. // Chem. Soc. Rev. 2006. V. 35. № 8. P. 675.
Borisov I., Bakhtin D., Luque-Alled Jose M., Rybakova A., Makarova V., Foster A.B., Harrison W.J., Volkov V., Polevaya V., Gorgojo P., Prestat E., Budd P.M., Volkov A. // J. Mater. Chem. A. 2019. V. 7. № 11. P. 6417.
Carta M., Malpass-Evans R., Croad M., Rogan Y., Jansen J.C., Bernardo P., Bazzarelli F., McKeown N.B. // Science. 2013. V. 339. № 6117. P. 303.
Park H.B., Jung C.H., Lee Y.M., Hill A.J., Pas S.J., Mudie S.T., Wagner E.V., Freeman B.D., Cookson D.J. // Science. 2007. V. 318. № P. 254.
Kim S., Lee Y.M. // Prog. Polym. Sci. 2015. V. 43. P. 1.
Low Z.-X., Budd P.M., McKeown N.B., Patterson D.A. // Chem. Rev. 2018. V. 118. № 12. P. 5871.
Hill A.J., Pas S.J., Bastow T.J., Burgar M.I., Nagai K., Toy L.G., Freeman B.D. // J. Membr. Sci. 2004. V. 243. № 1–2. P. 37.
Yin H., Chapala P., Bermeshev M., Schönhals A., Böhning M. // ACS Macro Lett. 2017. V. 6. № 8. P. 813.
Nagai K., Masuda T., Nakagawa T., Freeman B.D., Pinnau I. // Prog. Polym. Sci. 2001. V. 26. № 5. P. 721.
Gringolts M., Bermeshev M., Yampolskii Yu., Starannikova L., Shantarovich V., Finkelshtein E. // Macromolecules. 2010. V. 43. № 17. P. 7165.
Chapala P.P., Bermeshev M.V., Starannikova L.E., Belov N.A., Ryzhikh V.E., Shantarovich V.P., Lakhtin V.G., Gavrilova N.N., Yampolskii Yu.P., Finkelshtein E.Sh. // Macromolecules. 2015. V. 48. № 22. P. 8055.
Gmernicki K.R., Hong E., Maroon C.R., Mahurin S.M., Sokolov A.P., Saito T., Long B.K. // ACS Macro Lett. 2016. V. 5. № 7. P. 879.
Commarieu B., Potier J., Compaore M., Dessureault S., Goodall B.L., Li X., Claverie J.P. // Macromolecules. 2016. V. 49. № 3. P. 920.
Alentiev D., Dzhaparidze D., Gavrilova N., Shantarovich V., Kiseleva E., Topchiy M., Asachenko A., Gribanov P., Nechaev M., Legkov S., Bondarenko G., Bermeshev M. // Polymers. 2018. V. 10. № 12. P. 1382.
Bermeshev M.V., Syromolotov A.V., Gringolts M.L., Lakhtin V.G., Finkelshtein E.Sh. // Tetrahedron Lett. 2011. V. 52. № 46. P. 6091.
Джемилев У.М., Поподько Н.Р., Козлова Е.В. // Металлокомплексный катализ в органическом синтезе. Алициклические соединения. М.: Химия, 1999.
Alentiev D.A., Egorova E.S., Bermeshev M.V., Starannikova L.E., Topchiy M.A., Asachenko A.F., Gribanov P.S., Nechaev M.S., Yampolskii Yu.P., Finkelshtein E.Sh. // J. Mater. Chem. A. 2018. V. 6. № 40. P. 19393.
Alentiev D.A., Bermeshev M.V., Starannikova L.E., Bermesheva E.V., Shantarovich V.P., Bekeshev V.G., Yampolskii Yu.P., Finkelshtein E.Sh. // J. Polym. Sci., Polym. Chem. 2018. V. 56. № 12. P. 1234.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)