Высокомолекулярные соединения (серия Б), 2020, T. 62, № 5, стр. 395-400
МОДИФИКАЦИЯ ПОЛИМЕТАЛЛОФОСФАТОВ ПЕНТАЭРИТРИТОМ
А. Ю. Шаулов a, *, Р. А. Сакович a, Е. М. Нечволодова a, А. В. Грачев a, Е. В. Стегно a, В. М. Лалаян a, Л. А. Ткаченко a
a Федеральный исследовательский центр химической физики им. Н.Н. Семенова Российской академии наук
119991 Москва, ул. Косыгина, 4, Россия
* E-mail: ajushaulov@yandex.ru
Поступила в редакцию 25.04.2020
После доработки 06.05.2020
Принята к публикации 20.05.2020
Аннотация
Рассмотрены композиции алюмоборо- и алюмохромофосфата с четырехатомным спиртом пента-эритритом – компонентом, образующим с фосфатными группами водородные и химические связи. Обнаружена экстремальная зависимость температуры размягчения от концентрации пентаэритрита, сопровождающаяся симбатным изменением влагоустойчивости. Измерены тепло-, термостойкость, кислородный индекс отвержденных композиций и прочность на изгиб композитов, армированных базальтовой тканью. Рассчитана энергия межмолекулярных связей мономерных звеньев фосфатов с пентаэритритом и проведено компьютерное моделирование конформации комплексов. Установлена бόльшая химическая активность алюмохромофосфата по сравнению с алюмоборофосфатом.
Полиметаллофосфаты в качестве продуктов поликонденсации олигомерных металлофосфатов относятся к разряду неорганических полиоксидов – полимеров, нашедших применение в различных отраслях промышленности, в частности при создании широко используемых высокотемпературных материалов [1–5].
Вместе с тем, олигомеры металлофосфатов, являясь водорастворимыми химически активными соединениями, могут служить для получения в “мягких” условиях “низкоплавких” термопластов с температурой размягчения и текучести, близкой к органическим полимерам.
Низкие значения температуры позволяют осуществлять модификацию полиоксидов органическими соединениями и формировать новый тип композитов через расплавы смесей неорганических и органических полимеров с применением традиционных технологий переработки пластмасс.
Отличительной особенностью неорганических полиоксидов можно назвать негорючесть и отсутствие вредных продуктов термической деструкции, а модификация органическими соединениями позволяет регулировать их релаксационные свойства и гидролитическую устойчивость [6–9].
Негорючие и гидролитически устойчивые высокомолекулярные соединения на основе олигомерных металлофосфатов традиционно получают при температуре выше 250°С поликонденсацией с использованием гетерогенных водных дисперсий, содержащих химически активные оксиды металлов.
Настоящая работа связана с исследованием возможности регулирования свойств полимеров применением соединений, образующих прочные водородные связи с фосфатами, содержащими активные гидроксильные группы в более “мягких” условиях. В качестве модифицирующих реагентов олигомерных полиоксидов наряду с аминами [10, 11] рассмотрена возможность использования таких водорастворимых органических соединений как спирты. Определены условия, при которых реализуется каждый из этих механизмов, изучены свойства полученных продуктов. Представленные композиции могут также выступать в качестве связующих армированных композитов, гомогенных составов, обеспечивающих эффективную пропитку волокнистых наполнителей.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали 55%-ный водный раствор алюмоборофосфата (АБФС) в соотношении компонентов P : Al : B = 1.5 : 0.5 : 0.03 (ООО “Торговый Дом ВЗХР” – Воскресенский завод химических реагентов; Россия), 75%-ный водный раствор алюмохромофосфата (АХФС) в соотношении компонентов P : Al : Cr = 1.0 : 0.17 : 0.1. Модификатором металлофосфатов различной химической структуры служил четырехатомный спирт – пентаэритрит технический (ПЭР), способный к образованию химических и донорно-акцепторных связей с ОН-группами фосфата (ГОСТ 9286-8012). В качестве армирующего наполнителя применяли базальтовую ткань БТ-100 (ГОСТ-СТО 59987361-009-2008).
Точность проведенных измерений составляла ±8–10%.
Термическую обработку образцов осуществляли при подъеме температуры со скоростью 10 град/мин с последующей выдержкой при заданном значении 160 и 180°С. Термомеханический анализ выполняли на приборе “Netzsch–TMA 402/2/G” (“Netzsch”, Германия), для термогравиметрического анализа использовали прибор “Netzsch-DSK Jupiter STA 449 F3” (“Netzsch”, Германия). Скорость изменения температуры составляла в обоих случаях 10 град/мин. Влагопоглощение образцов определяли при 20°С в течение 48 ч при 98%-ной влажности атмосферы.
Механические испытания на изгиб армированных композитов вели по утку по трехточечной схеме на разрывной машине “LRX Plus” (“Lloyd Instruments”, Великобритания). Кислородный индекс измеряли по ГОСТ 12.1.044-89. Спектры регистрировали на ИК-фурье-спектрометре “Vertex-70” (“Bruker”, Германия) с разрешением 4 см–1 с горизонтальной приставкой “GladiATR” (“Pike Technologies”, США): элемент внутреннего отражения – алмаз, n = 2.4 при однократном отражении и угле падения излучения 45°. Регистрацию и обработку спектров проводили с помощью пакета программ Opus 7.0 (“Bruker”, Германия). Квантово-химические расчеты выполняли с использованием ресурсов суперкомпьютерного комплекса МГУ им. М.В. Ломоносова методом теории функционала плотности DFT [12] с функционалом bh-lyp [13] при помощи квантово-химического пакета Turbomole [14]. Оптимизацию геометрии осуществляли в двойном дзета-базисе SVP [15], а для расчета значений энергии взаимодействия использовали абсолютную электронную энергию комплексов, рассчитанную в тройном дзета-базисе TZVP [16], при использовании которого ошибка вычисления энергии комплексообразования BSSE резко уменьшается, и ею можно пренебречь [17]. Эффект растворителя в вычислениях не учитывали.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В качестве металлофосфатов были выбраны олигомеры алюмоборофосфата и алюмохромофосфата, модификация которых проведена тетрафункциональным спиртом пентаэритритом.
Параметрами, отражающими релаксационные свойства полученных продуктов, являлись температура размягчения – температура потери механической устойчивости “низкоплавкой” фракции Тразм и температура текучести Ттек расплавов смесей. Рассмотрены термостойкость и влагопоглощение полимеров, а также горючесть и механические свойства армированных композитов.
Учитывая возможность двух различных механизмов изменения релаксационных свойств в результате физического и химического взаимодействия фосфатных групп с гидроксильными группами спиртов, были определены условия их реализации.
Логично предположить, что донорно-акцепторные взаимодействия между компонентами происходят при более низких значениях температуры, а при повышении температуры возможно их химическое взаимодействие.
Свойства полученных комплексов и сравнительная химическая активность фосфатов установлена по термомеханическим характеристикам продуктов взаимодействия алюмоборо- и алюмохромофосфата с заданной концентрацией пентаэритрита (180°С, 0.5 ч) фосфат : ПЭР = 1.0 : 0.1. Показано, что Тразм отвержденных образцов АБФС и АХФС составляет 113 и 152°С, а продуктов их взаимодействия с ПЭР 136 и более 300°С соответственно. Отсюда можно заключить, что АХФС более химически активен (рис. 1).
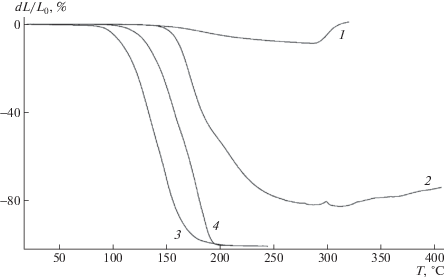
Рис. 1.
ТМА полифосфатов и их комплексов с пентаэритритом: 1 – АХФС, 2 – АХФС–10% ПЭР, 3 – АБФС, 4 – АБФС–10% ПЭР; Т = 180°С, 0.5 ч.
Сделанный вывод подтверждается анализом продуктов термической обработки металлофосфатов АБФС и АХФС (180°С, 30 мин) методом ИК-фурье-спектроскопии. В спектрах прослеживается характерная для фосфатной группы широкая интенсивная полоса в области 1350–800 см–1 со слабо выраженными максимумами при 1180, 1050 и 860 см–1 и полушириной полосы ∼350 см–1 [18, 19].
После термической обработки смесей фосфатов с ПЭР (10–40 мас. %) на фоне широкой огибающей появляется ряд дополнительных максимумов, относящихся к продуктам взаимодействия компонентов: 1185, 1135, 1035 и 965 см–1. Положение этих максимумов в спектрах смесевых композиций отличается на 5–10 см–1, а интенсивность новых полос в спектрах АХФС–ПЭР на 10–15% выше, чем в спектрах АБФС–ПЭР и закономерно возрастает с увеличением концентрации ПЭР.
Вывод о более высокой активности АХФС подтверждается также эндотермическим тепловым эффектом в процессе поликонденсации, более чем вдвое превышающим тепловой эффект поликонденсации АБФС (табл. 1).
Таблица 1.
Термогравиметрические и калориметрические данные исходных компонентов АБФС, АХФС и их смесей с 20 мас. % ПЭР (Т = 180°С, 30 мин)
| Компоненты | Тнач, °С | –Δm, % (при Т = 315°C) | –Q, дж/г | Интервал Т, °С | +Q, дж/г | Интервал Т, °С |
|---|---|---|---|---|---|---|
| АБФС | 115.6 | 11.4 | 28.2 | 160–250 | – | – |
| АХФС | 160.8 | 10.4 | 65.8 | 150–270 | – | – |
| ПЭР | 207.9 | 95.0 | 206.0 | 210–325 | – | – |
| АБФС–20% ПЭР | 185.1 | 13.8 | 40.5 | 185–265 | 40.5 | 280–415 |
| АХФС–20% ПЭР | 215.8 | 7.0 | 71.0 | 125–250 | 102.9 | 280–415 |
Изучение концентрационной зависимости термомеханических свойств композиций АБФС–ПЭР (180°С) и АХФС–ПЭР (160°С) в широком диапазоне соотношений обнаружило нелинейную зависимость с максимумами (более высокая температура обработки АБФС–ПЭР выбрана на основании вывода о меньшей активности АБФС) (рис. 2).
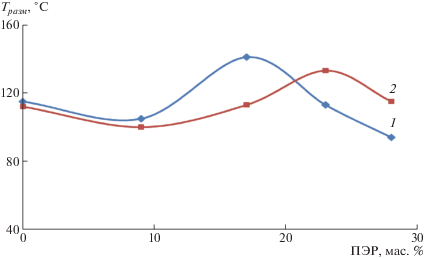
Рис. 2.
Зависимость температуры размягчения поликомплексов АБФС–ПЭР (1) и АХФС–ПЭР (2) от концентрации ПЭР.
Обнаруженная экстремальная зависимость подобна наблюдавшейся ранее для поликомплексов АБФС–гексаметилендиамин [20].
Следует обратить внимание, что дальнейшее увеличение содержания ПЭР сопровождается уменьшением Тразм поликомплексов, что может быть связано с пластификацией поликомплексов избыточным содержанием пентаэритрита. Показано, что изменение Ттек обеих композиций симбатно изменению Тразм.
Исходя из полученных значений Тразм и Ттек можно предположить, что в АХФС–ПЭР при 160°С прослеживается образование поликомплексов с участием водородных связей, а при более высокой температуре происходит химическая реакция, приводящая к образованию пространственно сшитого полимера, сопровождающаяся существенным возрастанием Тразм (рис. 3).
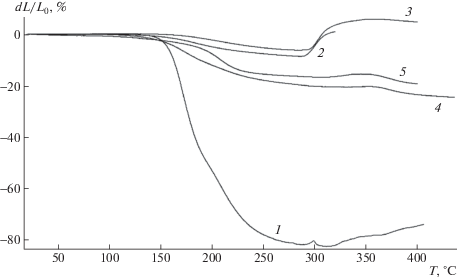
Рис. 3.
ТМА поликомплексов АХФС–ПЭР, полученных при концентрации ПЭР 0 (1), 10 (2), 20 (3), 30 (4) и 40 мас. % (5).
Другим важным параметром, отражающим влияние пентаэритрита на свойства полиметаллофосфатов, является влагопоглощение поликомплексов.
На рис. 4 приведены зависимости влагопоглощения от концентрации ПЭР для обеих смесей, полученных при 180°С. Виден различный характер зависимостей и практически полное отсутствие влагопоглощения для композиции АХФС при концентрации пентаэритрита 15–17 мас. %, что дополнительно свидетельствует о более высокой химической активности хромофосфата.
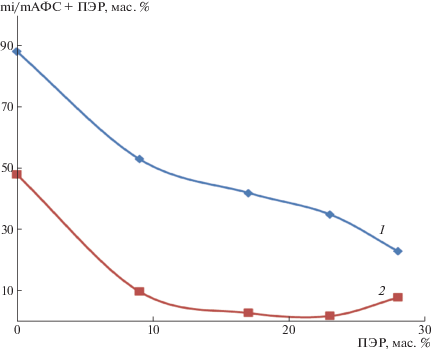
Рис. 4.
Зависимость влагопоглощения поликомплексов АБФС–ПЭР (1) и АХФС–ПЭР (2) от концентрации ПЭР при выдержке в атмосфере с 98%-ной влажностью; Т = 20°С, 48 ч.
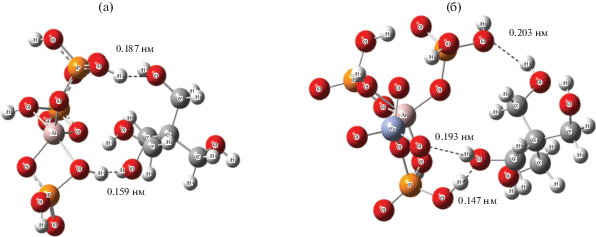
С помощью квантово-химических расчетов определена структура мономера алюмохромфосфата. Показано, что атом хрома вступает во взаимодействие с атомом кислорода цепи, связывающим атомы фосфора и алюминия –Р–О–Аl.
Рассчитаны значения энергии межмолекулярных взаимодействий мономерных звеньев АБФС и АХФС с пентаэритритом (наличие в цепи бора не учитывается ввиду его низкого содержания).
Показано, что между мономерным звеном АБФС и ПЭР образуется две водородные связи с суммарной энергией 30 ккал/моль: –Р–ОН…О(Н)–С– длиной 0.187 и 0.159 нм с энергией 10 и 20 ккал/моль соответственно (более высокое значение энергии второй связи обусловлено координацией атома кислорода фосфата с атомами фосфора и алюминия). Для сравнения, средняя энергия связи АФС–Н2О составляет 15.2 ккал/моль.
Наряду с этим, АХФС образует с пентаэритритом три водородные связи с общей энергией ΔE = = 41.9 ккал/моль.
В связи с возможностью использования полученных полифосфатов в качестве связующих армированных композитов выполнены измерения их термостойкости – температуры начала потери массы образца, а также тепловых эффектов процессов, протекающих при термическом воздействии.
Полученные данные термогравиметрических и калориметрических измерений исходных компонентов и продуктов их взаимодействия после обработки при 180°С в течение 30 мин (см. табл. 1) позволили сделать следующие выводы:
– эндотермические эффекты при термической обработке до 270°С для АХФС (65.8 ккал/моль) и АБФС (28.2 ккал/моль) различаются в 2.3 раза;
– теплостойкость сшитой структуры АХФС–ПЭР (160.8°С) превышает теплостойкость поликомплекса АБФС–ПЭР (115.6°С) на 45.2°С;
– термостойкость, определенная как потеря массы при обработке до 315°С сшитой структуры АХФС–ПЭР (7.0%), больше термостойкости поликомплекса АБФС–ПЭР (13.8%) в ∼2 раза;
– экзотермический эффект, связанный с окислением непрореагировавшего пентаэритрита в смеси АХФС–ПЭР (102.9 ккал/моль), в 2.5 раза больше, чем в поликомплексе АБФС–ПЭР (40.5 ккал/моль).
На основе модифицированных полифосфатов и базальтовой ткани получены армированные композиты и измерена их прочность на изгиб при следующих условиях: четыре слоя ткани, температура прессования образцов 180°С, время прессования 30 мин (табл. 2).
Таблица 2.
Механические свойства композитов, армированных базальтовой тканью
| Состав связующего | Прочность на изгиб, МПа | Модуль Юнга, ГПа | Деформация, % | Плотность, г/см3 | Содержание наполнителя, мас. % |
|---|---|---|---|---|---|
| АБФС–20% ПЭР | 139 ± 20 | 25.2 | 0.8 | 1.9 | 68.0 |
| АХФС–20% ПЭР | 138 ± 30 | 18.9 | 0.9 | 1.9 | 63.5 |
Таким образом, определены кислородные индексы композитов АФС–20% ПЭР и АХФС–20% ПЭР, показано отсутствие воспламенения в чистом кислороде.
Работа выполнена по Госзаданию Министерства науки и образования России (тема 45.11.ГЗ № 0082-2019-0008. АААА-А-20-120030590042-8. Дата регистрации 05/03/2020).
Список литературы
Ван Везер // Фосфор и его соединения. М.: Изд-во иностр. лит-ры, 1962.
Продан Е.А., Продан Л.И., Еременко Н.Ф. // Триполифосфаты и их применение. Минск: Наука и техника, 1969.
Голынко-Вольфсон С.Л., Сычев М.М., Судакас Л.Г., Скобло Л.И. Химические основы технологии и применения фосфатных связок и покрытий. Л.: Химия, 1968.
Копейкин В.А., Петрова А.П., Рашкован И.Л. Материалы на основе металлофосфатов. М.: Химия, 1976.
Копейкин В.А., Клементьева B.C., Красный Б.Л. Огнеупорные растворы на фосфатных связующих. М.: Металлургия, 1986.
Shaulov A.Yu., Berlin A.A. // Additives in Polymers. Analysis and Applications / Ed. by A.A. Berlin, S.Z. Rogovina, G.E. Zaikov. Boca Raton: CRC, 2015. P. 364. Hard ISBN 978177188128.
Ray N., Sherliker F. Pat. 3,732,181 USA. 1973.
Urman K., Otaigbe J.U. // Prog. Polym. Sci. 2007. V. 32. P. 1462.
Шаулов А.Ю., Владимиров Л.В., Грачев А.В., Лалаян В.М., Нечволодова Е.М., Сакович Р.А., Скачкова В.К., Стегно Е.В., Ткаченко Л.А., Патлажан С.А., Берлин А.А. // Хим. физика. 2020. Т. 39. № 1. С. 75.
Nechvolodova E.M., Sakovich R.A., Grachev A.V., Vla-dimirov L.V., Shashkin D.P., Tkachenko L.A., Shau-lov A.Yu., Berlin A.A. // Russ. J. Phys. Chem. B. 2017. V. 11. № 5. P. 839.
Nechvolodova E.M., Sakovich R.A., Grachev A.V., Glagolev N.N., Motyakin M.V., Shaulov A.Yu., Berlin A.A. // Russ. J. Phys. Chem. B. 2017. V. 11. № 3. P. 499.
Gross E.K.U., Kohn W. // Adv. Quantum Chem. 1990. V. 21. P. 255.
Becke A.D. // J. Chem. Phys. 1993. V. 98. P. 1372.
Furche F., Ahlrichs R., Hattig C., Klopper W., Sierka M., Weigend F. // Comput. Mol. Sci. 2014. V. 4. P. 91.
Schafer A., Horn H., Ahlrichs R. // J. Chem. Phys. 1992. V. 97. P. 2571.
Weigend F., Ahlrichs R. // Phys. Chem. Chem. Phys. 2005. V. 7. P. 3297.
Mentel L.M., Baerends E.J. // J. Chem. Theory Comput. 2014. V. 10. № 1. P. 252.
Bellamy L.J. Infrared Spectra of Complex Molecules. New York: Wiley, 1958.
Justrzebski W., Sitar Z.M., Rokita M., Bulat K. // Spectrochim. Acta. A. 2011. V. 79. P. 722.
Nechvolodova E.M., Sakovich R.A., Grachev A.V., Tkachenko L.A., Shaulov A.Yu. // Russ. J. Phys. Chem. B. 2020. V. 14. № 2. P. 318.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)