Высокомолекулярные соединения (серия Б), 2021, T. 63, № 1, стр. 71-80
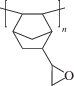
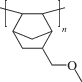
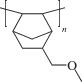
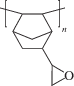
АДДИТИВНЫЙ ПОЛИМЕР НА ОСНОВЕ 5-(МЕТОКСИМЕТИЛ)НОРБОРНЕНА: СИНТЕЗ И ГАЗОТРАНСПОРТНЫЕ СВОЙСТВА
Д. А. Алентьев a, b, *, Д. П. Зарезин b, М. А. Рудакова b, Р. Ю. Никифоров b, Н. А. Белов b, М. В. Бермешев b
a Российский химико-технологический университет им. Д.И. Менделеева
125047 Москва, Миусская пл., 9, Россия
b Институт нефтехимического синтеза им. А.В. Топчиева Российской академии наук
119991 Москва, Ленинский пр., 29, Россия
* E-mail: d.alentiev@ips.ac.ru
Поступила в редакцию 10.08.2020
После доработки 21.09.2020
Принята к публикации 08.10.2020
Аннотация
На основе коммерчески доступного (5-норборнен-2-ил)метанола по реакции Вильямсона синтезирован 5-(метоксиметил)норборнен. Изучена его аддитивная полимеризация, найдены условия, при которых с хорошим выходом образуется высокомолекулярный продукт. Исследованы газотранспортные свойства синтезированного аддитивного полинорборнена для широкого набора газов (He, H2, O2, N2, CO2, CH4). На основании полученных данных сделаны выводы о влиянии наличия простой эфирной группы в боковой цепи полинорборненов на их газотранспортные свойства. Показано, что простая эфирная группа способствует снижению уровня газопроницаемости и увеличению селективности разделения газов CO2/N2 и CO2/CH4.
ВВЕДЕНИЕ
Разработка новых подходов к дизайну материалов для полимерных газоразделительных мембран является важной задачей химии высокомолекулярных соединений. Полимеры на основе производных норборнена – удобные объекты для решения этой задачи, поскольку норборнены обладают богатой химией и способны активно вступать в полимеризацию по трем различным направлениям, позволяя получать большое разнообразие полимерных структур [1]. Одной из наиболее актуальных задач мембранной технологии является разработка высокоэффективных мембран для выделения углекислого газа из промышленных газовых потоков. В последние годы активно развивается подход к созданию полимеров с повышенной селективностью газоразделения CO2/N2, основанный на введении в боковую цепь полинорборненов заместителей, содержащих алкоксисилильные и простые эфирные фрагменты [2–7]. Так, аддитивный политрициклононен, содержащий триметоксисилильные группы в боковой цепи, имел селективность газоразделения CO2/N2, равную 36, причем данные для этого полимера находились выше верхней границы 2008 года на диаграмме Робсона для пары газов CO2/N2 [2]. В работе [5] было показано, что введение в триалкоксисилильную группу дополнительных простых эфирных фрагментов способствует увеличению растворимости CO2 и соответственно, повышению селективности газоразделения CO2/N2. Позднее на примере аддитивного полинорборнена, содержащего 2-метоксиэтокси-группы в боковой цепи, было показано, что фрагменты C–O сами по себе, без наличия кремнийорганических групп, способствуют увеличению проницаемости углекислого газа [7]. Соединения, применяемые в указанных работах как мономеры, сложны в синтезе и требуют наличия дорогостоящих исходных реагентов. В связи с этим разработка более простых подходов к синтезу мономеров, содержащих фрагменты C–O, является актуальной задачей. В настоящей работе с помощью реакции Вильямсона из (5-норборнен-2-ил)метанола был синтезирован 5-(метоксиметил)норборнен [8, 9]. Коммерческая доступность исходного соединения и простота протекания реакции – важные преимущества данного подхода как с точки зрения возможности получения широкого круга мономеров для фундаментальных исследований взаимосвязей структура–свойства, так и с точки зрения потенциальной возможности применения синтезируемых полимеров. В работе впервые изучена аддитивная полимеризация 5-(метоксиметил)норборнена, исследованы газотранспортные свойства синтезированного полимера.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы и методы
Тетрагидрофуран кипятили над NaOH в течение 4 ч и перегоняли в аргоне, затем дважды по 4 ч кипятили над натрием и перегоняли в аргоне. Хлороформ кипятили 5 ч над CaH2 и перегоняли в аргоне. (5-Норборнен-2-ил)метанол (85% эндо-изомера, 15% экзо-изомера, “Aldrich”) сушили над CaH2 и перегоняли в аргоне. Метанол, толуол, изопропанол, гидрид натрия, иодистый метил, тетракис-[3,5-бис-(трифторметил)фенил]борат натрия (NaBARF), ацетат палладия, трициклогексилфосфин (“Aldrich”) использовали без дополнительной очистки.
Аддитивную полимеризацию проводили в атмосфере аргона в главбоксе “MBraun”.
Спектры ЯМР регистрировали на спектрометре “Avance 600” (“Bruker”, США) на рабочих частотах 600 и 150 МГц соответственно для спектров ЯМР 1H и ЯМР 13C. Растворитель CDCl3. Сигналы в спектрах ЯМР 1H относили по остаточным протонам в CDCl3 (7.24 м.д.), в спектрах ЯМР 13С – по центральному пику CDCl3 (77.00 м.д.).
Молекулярную массу оценивали методом ГПХ на хроматографе высокого давления “Waters”, оснащенном рефрактометрическим детектором. Колонка – Microgel mix 1–5 мкм 500 мм × 7.7 мм Chrompack. Растворитель хлороформ, объем пробы 100 мкл, концентрация полимера в пробе 1 мг/мл. Калибровку осуществляли по ПС-стандартам, M = (1 × 103)–(1 × 106). Молекулярно-массовые характеристики рассчитывали по калибровочной зависимости, которая была линейной в диапазоне (1 × 103)–(1 × 106).
Калориметрические измерения выполняли на дифференциальном сканирующем калориметре “TA-4000” (“Mettler Toledo”, США) с ячейкой DSC-30 при скорости нагревания 20 град/мин в атмосфере аргона. Термогравиметрический анализ проводили на синхронном термоанализаторе “TGA/DSC 1” (“Mettler Toledo”) в атмосфере аргона и на воздухе при скорости нагревания 10 град/мин в диапазоне температур от 30 до 1000°C.
Рентгенофазовый анализ выполняли с использованием детектора ASX (“Bruker”, США) и излучения CuKα (длина волны λ = 1.54 Å).
Плотность полимера определяли методом гидростатического взвешивания в изопропаноле по методике, описанной в работе [10], а также на пикнометре “Ultrapyc 1200e” (рабочий газ гелий, объем измерительной ячейки 4.5 см3).
Синтез мономера 5-(метоксиметил)норборнена
Трехгорлую круглодонную колбу на 150 мл, снабженную обратным холодильником, заполняли аргоном, используя стандартную методику Шленка. В колбу помещали 1.9 г (48 ммоль, 1.2 экв.) 60%-ной суспензии гидрида натрия в минеральном масле, промывали ее абсолютным тетрагидрофураном (3 раза по 15 мл), приливали 50 мл абсолютного тетрагидрофурана и 5 г (40 ммоль) (5-норборнен-2-ил)метанола. Смесь перемешивали в течение 1 ч при кипячении. Затем к реакционной смеси добавляли 6.9 г (48 ммоль, 1.2 экв.) иодистого метила и кипятили в течение 5–6 ч. После завершения реакции реакционную смесь фильтровали и упаривали в вакууме. Продукт очищали с помощью флэш-хроматографии (элюент хлороформ–гексан в соотношении 5 : 1), затем сушили над натрием и перегоняли в вакууме. Выход 4.5 г (81%).
Аддитивная полимеризация 5-(метоксиметил)норборнена
Пример приведен для аддитивной полимеризации 5-(метоксиметил)норборнена при соотношении мономер/катализатор 1000/1. Другие эксперименты выполняли аналогично.
Все процедуры проводили в главбоксе. Каталитическую смесь готовили непосредственно перед полимеризацией. Для этого в виале смешивали 1.20 мл (1.20 × 10–2 ммоль) раствора Pd(OAc)2 в абсолютном хлороформе (1.0 × 10–2 M), 1.32 мл (3.96 × 10–2 ммоль) раствора NaBARF в абсолютном хлороформе (3.0 × 10–2 M) и 0.43 мл (1.82 × × 10–2 ммоль) раствора трициклогексилфосфина в абсолютном хлороформе (6.0 × 10–3 M). Смесь перемешивали 5 мин. В виалу объемом 8 мл вводили 0.10 г (7.2 × 10–1 ммоль) 5-(метоксиметил)норборнена. Полимеризацию инициировали добавлением 0.43 мл (7.2 × 10–4 ммоль Pd) каталитической смеси. Смесь перемешивали, затем нагревали при 45°C в течение 20 ч, после чего разбавляли 1.5 мл абсолютного хлороформа, снова нагревали при 45°C в течение 20 ч. Образовавшийся вязкий раствор осаждали в метанол. Затем полимер отделяли, промывали 3 раза метанолом и сушили в вакууме. Полученный полимер дважды переосаждали из толуола в метанол и сушили в вакууме при 80–90°C до постоянной массы. Выход 0.084 г (84%). ρ = 1.06 г/см3 (определенная методом гидростатического взвешивания) 1.15 г/см3 (определенная на пикнометре). Mw = 9.0 × 105, Ð = 5.2.
ЯМР 1H (δ, м.д., CDCl3): 3.90–2.86 (м., 5H, CH3–O; CH2–O); 2.79–0.35 (м., 9H, C(1–7)–H).
ЯМР 13С (δ, м.д., CDCl3): 59.20–58.10 (CH3–O; CH2–O); 46.00–29.00 (С(1–7)).
Подготовка полимерных пленок и измерение коэффициентов газопроницаемости
Пленки приготавливали поливом 5%-ного раствора полимера в толуоле в стальной цилиндр с целлофановой пленкой, натянутой на дно. После испарения растворителя пленку выдерживали в вакууме до постоянной массы (остаточное давление при вакуумировании не превышало 1 мм рт. ст.). Толщина пленки 70 мкм.
Коэффициенты проницаемости P и диффузии D газов He, H2, O2, N2, CO2, CH4 определяли на установке “Баротрон” при температуре 22°С по методике, описанной ранее [11].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Синтез мономера
Мономер 5-(метоксиметил)норборнен был синтезирован с помощью реакции Вильямсона между (5-норборнен-2-ил)метилатом натрия, полученным из коммерчески доступного (5-норборнен-2-ил)метанола, и иодистым метилом:
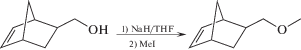
Реакция протекала при нагревании в абсолютном тетрагидрофуране в течение 5–6 ч. Полноту протекания реакции контролировали методом газовой хроматографии. В результате целевой мономер был получен с высоким выходом (81%). Синтезированный мономер представляет собой смесь 85% эндо-изомера и 15% экзо-изомера.
Аддитивная полимеризация
Аддитивную полимеризацию синтезированного мономера осуществляли в присутствии разработанной ранее [12] каталитической системы: Pd(OAc)2 в качестве прекатализатора, борорганический сокатализатор NaBARF, трициклогексилфосфин в молярном соотношении 1 : 5 : 2. Мономер оказался менее активен в аддитивной полимеризации, чем изученные ранее кремнийзамещенные норборнены [12, 13]: при комнатной температуре достигались только невысокие конверсии мономера. При небольшом нагревании (45°C) полимеризация протекала с образованием вязкого раствора в течение 20 ч. Полное завершение реакции происходило через 40 ч после инициирования:
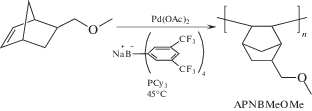
Далее путем варьирования соотношения мономер : катализатор (табл. 1) были найдены оптимальные условия полимеризации – соотношение мономер : катализатор = 1500 : 1, концентрация мономера 0.67 моль/л, температура 45°C. При более высоких соотношениях мономер : катализатор выход полимера существенно снизился, при более низких получался полимер с невысокой молекулярной массой. Сравнительно большие значения Ð обусловлены бимодальными молекулярно-массовыми распределениями, что, вероятно, связано с образованием двух типов активных центров при активации Pd(OAc)2. Это требует более глубоких исследований.
Таблица 1.
Условия аддитивной полимеризации 5-(метоксиметил)норборнена
| Соотношение мономер : Pd | Выход, % | Mw × 10–3 | Ð |
|---|---|---|---|
| 500 : 1 | 94 | 460 | 4.4 |
| 1000 : 1 | 84 | 900 | 5.2 |
| 1500 : 1 | 62 | 1300 | 4.7 |
| 3000 : 1 | 49 | 1500 | 4.0 |
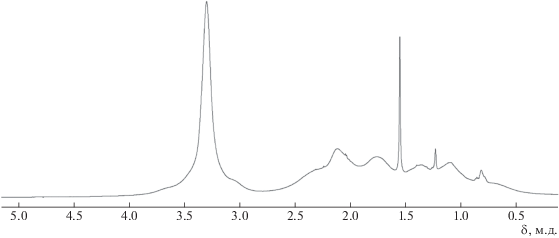
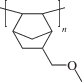
Структура синтезированного полимера – аддитивного поли(5-(метоксиметил)норборнена) (APNBMeOMe) была подтверждена методом ЯМР-спектроскопии (рис. 1). Химические сдвиги и форма сигналов свидетельствуют о том, что при полимеризации образовался насыщенный полимер, содержащий боковые метокси-группы. Также были исследованы термические свойства синтезированного аддитивного полимера. По данным ТГА (рис. 2), синтезированный аддитивный полимер является термически стабильным. Его температура разложения (определяемая как температура 5% потери массы) составляет 390°C в атмосфере аргона и 300°C на воздухе. Термическая стабильность APNBMeOMe превышает термическую стабильность аддитивных полинорборненов с триметилсилильными боковыми группами и соизмерима с термической стабильностью аддитивных поли(5-алкилнорборненов) [14]. APNBMeOMe оказался стеклообразным полимером, а его температура стеклования более 300°C и не наблюдается на ДСК.
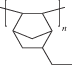
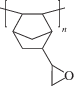
По данным рентгенофазового анализа синтезированный полимер оказался некристаллическим. Его дифрактограмма представлена двумя широкими пиками, характерными для аддитивных полинорборненов (рис. 3): пик при 5°–12°, соответствующий расстояниям между цепями либо сегментами, и пик при 17°–22°, соответствующий расстояниям между структурными фрагментами в пределах одной цепи. Положения максимумов пиков и отвечающие им расстояния для полимера близки к таковым для аддитивных полинорборненов, содержащих в боковой цепи этильные или эпокси-группы (табл. 2) [15].
Газотранспортные свойства
Для APNBMeOMe были определены коэффициенты проницаемости, диффузии и растворимости He, H2, O2, N2, CO2, CH4 (табл. 3–5). В изученном APNBMeOMe коэффициенты проницаемости легких газов оказались в 4 раза ниже, чем у аддитивного полинорборнена с этильными группами (APNBEt, табл. 3). В то же время они выше соответствующих характеристик для полинорборненов, содержащих родственные по строению и полярности эпокси-группы: в 1–3 раза по сравнению с аддитивным полинорборненом с эпокси-группами в боковой цепи (APNBEO) и в 10–300 раз по сравнению с ранее изученным эпоксидированным метатезисным полинорборненом (EO-MPNB) [10]. Доля свободного объема в APNBMeOMe, рассчитанная по методу Бонди, составляет 9–16% (в зависимости от метода определения плотности полимера). Необходимо отметить, что в ряду трех аддитивных полимеров (APNBMeOMe, APNBEt, APNBEO) уровень газопроницаемости коррелирует с долей свободного объема. Для синтезированного полимера наблюдается необычное по сравнению с другими полимерами поведение проницаемости по CO2. При переходе от этильной группы в боковой цепи аддитивного полинорборнена к метоксиметильной P(CO2) уменьшается менее значительно (в ∼2 раза, в то время как для других газов – в 3–4 раза). Это свидетельствует о том, что наличие в боковой цепи полинорборненов простой эфирной группы благоприятно для транспорта CO2. Однако из приведенных данных неясно, на какой фактор влияет наличие простой эфирной группы: на коэффициент диффузии или коэффициент растворимости.
Таблица 3.
Коэффициенты газопроницаемости APNBMeOMe по сравнению с другими аддитивными полимерами
| Полимер | FFV*, % | P, Баррер | ||||||
|---|---|---|---|---|---|---|---|---|
| He | H2 | O2 | N2 | CO2 | CH4 | |||
 |
[15] | 19.0 | 188 | 310 | 72 | 21 | 390 | 37 |
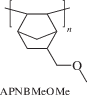 |
9.0**, 16.0*** | 48 | 80 | 20 | 6 | 180 | 12 | |
 |
[15] | 9.0 | 45 | 67 | 7.6 | 3.8 | 119 | 7.1 |
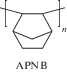 |
[17] | 15.0 | 29 | 42 | 6.9 | 1.5 | 34 | 2.6 |
 |
[10] | 15.5 | 4.5 | 4.1 | 0.21 | 0.031 | 1.1 | 0.042 |
Сравнение полученных результатов с ранее опубликованными для незамещенного аддитивного полинорборнена свидетельствуют о том, что введение фрагмента CH2–O–CH3 в качестве бокового заместителя приводит к увеличению газопроницаемости. Эффект от введения рассматриваемого фрагмента в полимерную цепь при этом оказался несколько ниже, чем эффект от введения этильной группы (APNBEt).
Снижение уровня газопроницаемости при переходе от полинорборнена с алкильными заместителями к полинорборнену с алкокси-группой можно объяснить тем, что алкокси-группы являются полярными, что способствует более плотной упаковке макромолекул за счет диполь-дипольных взаимодействий, так же как ранее было обнаружено и для полинорборнена с боковыми эпокси-группами [15]. Из рассмотрения табл. 4 можно сделать вывод, что введение алкокси-группы в боковую цепь APNB приводит к уменьшению коэффициентов диффузии газов (O2, N2, CO2, CH4) в 1.8–2.5 раза, однако по абсолютному значению они остаются выше коэффициента диффузии D газов для APNBEO и для EO-MPNB. Это указывает на то, что алкокси-группы, обладающие большими вращательными степенями свободы, благоприятствуют диффузии газов в большей степени, чем жесткие эпокси-группы.
Коэффициенты растворимости газов (O2, N2, CH4) подчиняются тем же тенденциям, что и коэффициенты диффузии, и возрастают в ряду APNBEO–APNBMeOMe–APNBEt. Напротив, коэффициент растворимости углекислого газа в этом же ряду убывает. Следовательно, наличие кислородсодержащих групп (простых эфирных либо эпоксидных) действительно способствует повышенной растворимости CO2 в полимере, и именно этим фактором, а не диффузией, обусловлено особое поведение проницаемости CO2. Еще одним доказательством данного факта являются высокие значения селективности растворимости (S(CO2)/S(N2)) для полинорборненов с кислородсодержащими группами, которые изменяются в ряду APNBEt < APNBMeOMe < < EO-MPNB < APNBEO (табл. 6). Возможной причиной такого эффекта могут быть специфические взаимодействия молекулы CO2 и заместителей, содержащих фрагменты C–O.
Для синтезированного полимера идеальные селективности газоразделения по парам газов, содержащим CO2 (CO2/N2, CO2/CH4), оказались выше, чем для аддитивного полимера с этильными заместителями (APNBEt) и соизмеримы с указанными параметрами для полимера с эпоксидными группами (APNBEO, табл. 7). Это обусловлено особым поведением проницаемости по CO2. По другим парам газов идеальные селективности для APNBMeOMe оказались близки к селективностям для APNBEt.
На зависимости идеальной селективности проницаемости α(CO2/N2) от коэффициента проницаемости углекислого газа (диаграммы Робсона, рис. 4) данные для исследуемого APNBMeOMe находятся в выгодном положении по сравнению с ранее изученными эпоксидированным метатезисным полинорборненом, аддитивным полинорборненом с эпокси-группами и сравнимы по сочетанию селективности и проницаемости с полинорборненами с триалкоксисилильными группами [6].
Рис. 4.
Зависимость идеальной селективности проницаемости от коэффициента проницаемости газа в логарифмических координатах (диаграмма Робсона) для пары газов СО2/N2 для полинорборненов разного строения: 1 – APNBMeOMe, 2 – APNBEt [15], 3 – APNBEO [15], 4 – аддитивные поли(триалкилоксисилилнорборнены) (APNBSi(OAlk)3 [6]), 5, 6 – метатезисный и аддитивный поли(триалкоксисилилтрициклононены) (MPTCNSi(OAlk)3 и APTCNSi(OAlk)3 соответственно [2]), 7 – модифицированный поли(норборнендикарбоксиимид) [20], 8 – эпоксидированный метатезисный полинорборнен EO-MPNB [10],

ЗАКЛЮЧЕНИЕ
Таким образом, на примере аддитивного поли(5-(метоксиметил)норборнена) предложен простой подход к дизайну и синтезу замещенных полинорборненов для газоразделительных мембран, основанный на реакции Вильямсона коммерчески доступного (5-норборнен-2-ил)метанола с алкилгалогенидами и последующей аддитивной полимеризации полученного мономера в присутствии каталитической системы на основе Pd. Найдены условия аддитивной полимеризации, при которых с высоким выходом образуются высокомолекулярные продукты. Синтезированный полимер является некристаллическим, стеклообразным и обладает высокой термической стабильностью. Исследованы газотранспортные свойства аддитивного поли(5-(метоксиметил)норборнена). Показано, что введение в боковую цепь полинорборненов простой эфирной группы способствует снижению уровня газопроницаемости, но при этом значения селективности газоразделения CO2/N2 и CO2/CH4 значительно возрастают. Эта закономерность в дальнейшем может быть применена для создания высокоселективных мембран для выделения CO2 из промышленных газовых потоков.
Обобщение и сравнение полученных данных с результатами для эпоксидированных полимеров было проведено Р.Ю. Никифоровым и Н.А. Беловым в рамках Госзадания ИНХС РАН.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (номер проекта 19-33-60035).
Список литературы
Finkelshtein E., Gringolts M., Bermeshev M., Chapala P. // Membrane Materials for Gas and Vapor Separation/ Ed. by Yu. Yampolskii, E. Finkelshtein. Chichester: Wiley, 2017. P. 143.
Alentiev D.A., Egorova E.S., Bermeshev M.V., Starannikova L.E., Topchiy M.A., Asachenko A.F., Gribanov P.S., Nechaev M.S., Yampolskii Yu.P., Finkelshtein E.Sh. // J. Mater. Chem. A. 2018. V. 6. P. 19393.
Belov N., Nikiforov R., Starannikova L., Gmernicki K.R., Maroon C.R., Long B.K., Shantarovich V., Yampolskii Yu. // Eur. Polym. J. 2017. V. 93. P. 602.
Gmernicki K.R., Hong E., Maroon C.R., Mahurin S.M., Sokolov A.P., Saito T., Long B.K. // ACS Macro Lett. 2016. V. 5. P. 879.
Maroon C.R., Townsend J., Gmernicki K.R., Harrigan D.J., Sundell B.J., Lawrence J.A., Mahurin S.M., Vogiatzis K.D., Long B.K. // Macromolecules. 2019. V. 52. P. 1589.
Maroon C.R., Townsend J., Higgins M.A., Harrigan D.J., Sundell B.J., Lawrence J.A., O’Brien J.T., O’Neal D., Vogiatzis K.D., Long B.K. // J. Membr. Sci. 2020. V. 595. P. 117532.
Higgins M.A., Maroon C.R., Townsend J., Wang X., Vogiatzis K.D., Long B.K. // J. Polym. Sci. 2020.
Haigh D.M., Kenwright A.M., Khosravi E. // Tetrahedron. 2004. V. 60. P. 7217.
Ho Kim S., Worsley M.A., Valdez C.A., Shin S.J., Dawedeit C., Braun T., Baumann T.F., Letts S.A., Kucheyev S.O., Wu K.J.J., Biener J., Satcher, Jr. J.H., Hamza A.V. // RSC Adv. 2012. V. 2. P. 8672.
Belov N.A., Gringolts M.L., Morontsev A.A., Starannikova L.E., Yampol’skii Yu.P., Finkel’stein E.Sh. // Polymer Science B. 2017. V. 59. № 5. P. 560.
Alent’iev D.A., Dzhaparidze D.M., Chapala P.P., Bermeshev M.V., Belov N.A., Nikiforov, R.Yu., Starannikova L.E., Yampol’skii Yu.P., Finkel’shtein E.Sh. // Polymer Science B. 2018. V. 60. № 5. P. 612.
Alent’iev D.A., Dzhaparidze D.M., Bermeshev M.V., Starannikova L.E., Filatova M.P., Yampol’skii Yu.P., Finkel’shtein E.Sh. // Polymer Science B. 2019. V. 61. № 6. P. 812.
Alentiev D.A., Bermeshev M.V., Starannikova L.E., Bermesheva E.V., Shantarovich V.P., Bekeshev V.G., Yampolskii Yu.P., Finkelshtein E.Sh. // J. Polym. Sci., Polym. Chem. 2018. V. 56. P. 1234.
Wozniak A.I., Bermesheva E.V., Gavrilova N.N., Ilyasov I.R., Nechaev M.S., Asachenko A.F., Topchiy M.A., Gribanov P.S., Bermeshev M.V. // Macromol. Chem. Phys. 2018. V. 219. P. 1800323.
Wozniak A.I., Bermesheva E.V., Andreyanov F.A., Borisov I.L., Zarezin D.P., Bakhtin D.S., Gavrilova N.N., Ilyasov I.R., Nechaev M.S., Asachenko A.F., Topchiy M.A., Volkov A.V., Finkelshtein E.Sh., Ren X.-K., Bermeshev M.V. // React. Funct. Polym. 2020. V. 149. P. 104513.
Wozniak A.I., Borisov I.L., Bermesheva E.V., Zarezin D.P., Volkov A.V., Finkel’shtein E.Sh., Bermeshev M.V. // Polymer Science B. 2020. V. 62. № 3. P. 218.
Finkelshtein E.Sh., Makovetskii K.L., Gringolts M.L., Rogan Yu.V., Golenko T.G., Starannikova L.E., Yampolskii Yu.P., Shantarovich V.P., Suzuki T. // Macromolecules. 2006. V. 39. P. 7022.
Matteucci S., Yampolskii Yu., Freeman B.D., Pinnau I. // Materials Science of Membranes for Gas and Vapor Separation / Ed. by Yu. Yampolskii, I. Pinnau, B. Freeman. Chichester: Wiley, 2006. P. 1.
Askadskii A.A. // Computational Materials Science of Polymers. Cambridge: Cambridge Int. Sci. Publ. Ltd., 2003. P. 16.
Kim D., Hossain I., Kim Y., Choi O., Kim T.-H. // Polymers. 2020. V. 12. P. 1674.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)