Высокомолекулярные соединения (серия Б), 2021, T. 63, № 6, стр. 469-478
КИНЕТИКА РАСТВОРЕНИЯ ПОЛИАКРИЛОНИТРИЛА В N-МЕТИЛМОРФОЛИН-N-ОКСИДЕ В ОТСУТСТВИЕ И ПРИСУТСТВИИ ЦЕЛЛЮЛОЗЫ
Е. Э. Пальчикова a, *, И. С. Макаров a, М. И. Виноградов a, Л. К. Голова a, Г. К. Шамбилова b, В. Г. Куличихин a
a Институт нефтехимического синтеза им. А.В. Топчиева Российской академии наук
119991 Москва, Ленинский пр., 29, Россия
b НАО “Атырауский университет имени Х. Досмухамедова”
060011 Атырау, Студенческий пр., 212, Казахстан, Россия
* E-mail: shatokhina@ips.ac.ru
Поступила в редакцию 15.06.2021
После доработки 05.08.2021
Принята к публикации 19.08.2021
Аннотация
С помощью метода оптической микроскопии в широком диапазоне температуры изучена кинетика растворения сополимера акрилонитрила в различных кристаллогидратах N-метилморфолин-N-оксида и в 12%-ном растворе целлюлозы в N-метилморфолин-N-оксиде. Скорость и особенности процесса растворения определены гидратной формой растворителя. В приложении кинетики реакции первого порядка рассчитана энергия активации растворения исследуемых систем. Кинетические характеристики растворения полиакрилонитрила и целлюлозы в N-метилморфолин-N-оксиде могут быть положены в основу нахождения оптимальных температурно-временных параметров процесса получения совместных растворов полиакрилонитрила и целлюлозы, а также новых композитных прекурсоров углеродных волокон.
В настоящее время основными промышленными полимерами, используемыми для формования прекурсоров углеродных волокон, являются полиакрилонитрил и целлюлоза. Углеродные волокна на основе этих полимеров обладают уникальными характеристиками: высокой прочностью и модулем упругости при относительно низкой плотности, высокой стойкостью к химическим реагентам, прекрасными теплозащитными характеристиками, высокой климатической стабильностью [1, 2]. Основными сферами применения углеродных волокон традиционно остаются автомобилестроение, аэрокосмическое и специальные производства, строительство, спортивный инвентарь [3], но также выделяются относительно новые, например, − получение высокопрочных композиционных материалов методом 3D-печати [4].
К сожалению, сополимеры стандартного состава (90−95% акрилонитрила, 5−7% метилакрилата и 1.5−2.0% акриловой или итаконовой кислот) считаются неплавкими, и их переработка в волокна возможна только через растворы. Высокая полярность макромолекул ПАН ограничивает круг пригодных органических растворителей, наиболее популярными из которых являются апротонные [5, 6] − диметилформамид, диметилацетамид, диметилсульфоксид и N-метилпирролидон (МП) [7–10]. Применяя эти растворители, обычно получают растворы с концентрацией порядка 18% (табл. 1). Дальнейшее увеличение содержания ПАН в системе приводит к высоким значениям вязкости, а следовательно, к трудностям при переработке высококонцентрированных растворов [6].
Необходимо отметить, что перечисленные выше растворители обладают некоторыми недостатками, среди которых высокая упругость паров, токсичность, нестабильность растворов вследствие гигроскопичности, трудность регенерации и другими [12, 13]. Высокая гигроскопичность ДМСО требует специальных герметичных условий приготовления растворов, так как при содержании воды более 5% раствор становится гелеобразным. Растворы ПАН в водном роданите натрия ведут себя стабильнее, но их использование вызывает коррозию металлов, что требует специального оборудования для их переработки [14].
Проведенные ранее исследования [15, 16] показали, что полярный, донорный растворитель N-метилморфолин-N-оксид (MMO) − наиболее эффективный прямой растворитель целлюлозы − обладает высокой растворяющей способностью и по отношению к сополимерам ПАН различной природы. MMO является экологически чистым растворителем и позволяет получать высококонцентрированные растворы ПАН, содержащие до 50% полимера.
Изучение механизма растворения ПАН в ММО [17, 18] позволило установить, что в процессе твердофазной активации системы ПАН–ММО и при последующем переводе ее при нагревании в вязкотекучее состояние протекают реакции комплексообразования, причем доминирует взаимодействие между электроноакцепторными карбоксильными группами ПАН и электронодонорной высокополярной N → O-связью молекул ММО [19]. При значениях температуры выше 120°С в растворах ПАН в ММО происходят необратимые изменения в химическом строении макромолекул ПАН, свидетельствующие об образовании циклических структур группами CN и формировании в макромолекулах ПАН областей полисопряжения [20, 21]. Регулирование глубины этого процесса позволяет, по крайней мере, частично провести термоокислительную стабилизацию ПАН еще в растворе, а не в волокне−прекурсоре.
Процесс растворения полимера фактически является первой и одной из важнейших стадий формования волокон. Дело в том, что от качества раствора зависят и его реологические свойства, и способность к струеобразованию (так называемая прядомость), и стабильность процесса формования, и свойства получаемого волокна. С практической точки зрения, это связано с аппаратурным оформлением процесса, энергозатратами на его проведение, т.е. с экономикой в целом. Законы термодинамики позволяют определить направление процесса, его начальный и конечный пределы, также оценить фазовые состояния как исходной бинарной системы, так и образующегося свежесформованного волокна. Однако термодинамика не дает ответы на вопросы о скорости и стадийности процесса. Определение механизма и скорости процесса растворения − основные задачи кинетики, а их успешное выполнение позволит решить проблемы в целом.
Анализ литературы показал, что к настоящему моменту, в отличие от работ по исследованию кинетики процесса растворения целлюлозы в ММО [22–25], полностью отсутствуют данные о кинетике растворения сополимеров ПАН в ММО. Изучение кинетических особенностей растворения ПАН дает возможность определить не только особенности процесса для бинарной системы, но и развить идеологию получения совместных растворов ПАН и целлюлозы в общем растворителе – ММО, что исключительно важно для представления и использования новых гибридных прекурсоров углеродных волокон.
В этой связи, целью данной работы является изучение кинетических особенностей растворения тройного сополимера ПАН не только в различных кристаллогидратах ММО, но и в растворе целлюлозы в ММО.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для изучения процессов растворения применяли тройной сополимер ПАН (Общество с ограниченной ответственностью “Саратоворгсинтез”) следующего состава: 93.0% акрилонитрила, 5.7% метилакрилата и 1.3% итаконовой кислоты в виде штапельного волокна “Нитрон”. Растворителем ПАН выступал N-метилморфолин-N-оксид (“Demochem”, Китай) с различным содержанием воды: в случае моногидратной формы при содержании воды 13.3 мас. % (температура плавления Тпл ~ 76°C), для высокоплавкой формы MMO концентрация воды составляла 10.1 мас. % (Тпл = 110−120°С). Для подавления деструкционных процессов при приготовлении растворов использовали пропилгаллат ~0.5% (“Sigma-Aldrich”, США). Целлюлоза Байкальского целлюлозно-бумажного комбината (Россия) со степенью полимеризации 600, влагосодержанием ~8 мас. % и содержанием основной фракции (α-целлюлозы) ~94% служила для приготовления 12%-ного раствора в ММО путем твердофазного растворения [22].
Содержание воды в ММО устанавливали методом титрования по Фишеру (“ЭКСПЕРТ-007М”, Россия), а также по точке плавления растворителя, определенного с помощью метода ДСК на калориметре DSC-2920 (“TA Instruments”, США).
Для нахождения кинетических параметров растворения ПАН в MMO применяли метод оптической микроскопии [23, 26]. Диаметр волокон предварительно измеряли на микроскопе “БИОМЕД–6ПО” (“Биомед”, Россия). Волокна, окруженные порошком растворителя, помещали между предметным и покровным стеклами, далее стекла вставляли в герметичную кювету для минимизации контакта с окружающей средой. При нагревании образца до температуры плавления MMO волокно начинало растворяться, и изменение его геометрии регистрировали с помощью фотокамеры. Полученные фотографии анализировали в программном комплексе Imagej. По изменению количества (площади) полимера в рабочей области определяли его концентрацию в изначально дисперсионной среде. Полученные значения площади, выраженные в пикселях, пересчитывали в микроны. Площадь волокон S коррелирует непосредственно с их концентрацией С, позволяя задействовать метод начальных значений скорости [27], из которого следует, что скорость изменения площади образца (r = –dS/dt) определяет повышение концентрации полимера в растворе. Волокна разного диаметра позволяют варьировать концентрацию в процессе растворения, что дает возможность применять аппарат химической кинетики.
Как известно, процесс растворения ПАН в ММО, являясь результатом электронного донорно-акцепторного взаимодействия высокого энергетического порядка между полимером и высокополярным растворителем, имеет не только физическую, но и физико-химическую природу [19]. В этой связи, использование кинетического аппарата химических реакций для описания таких процессов, на первый взгляд, кажется недостаточно корректным. Однако основываясь на работах [28–30], посвященных выявлению и установлению определенной взаимосвязи химического типа взаимодействий с физическим, такой подход представяется достаточно обоснованным, тем более что процесс растворения, как и химические реакции, имеет необратимый характер.
Скорость химической реакции можно выразить следующим уравнением:
где Сi – концентрация реагирующего вещества.Скорость химической реакции – величина всегда положительная, поэтому, если она определяется по исходному веществу, концентрация которого убывает в процессе реакции, то правая часть должна быть отрицательной. Для установления порядка реакции обычно используют зависимости lnC от времени, позволяющие анализировать кинетику процесса растворения на основе уравнения химической реакции первого порядка:
Здесь k – константа скорости растворения, которая для реакции первого порядка имеет размерность обратного времени [31]; a – порядок реакции; r – скорость растворения; С – концентрация (площадь S) растворяющегося ПАН.
Важно отметить, что k значительно меняется в зависимости от температуры и не зависит от концентрации реагирующих веществ и времени [32]. Согласно уравнению Аррениуса, зависимость константы скорости реакции k от температуры может быть описана следующим активационным выражением:
где E – энергия активации [Дж/моль], A – предэкспоненциальный множитель.РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Содержание воды в ММО влияет на его температуру плавления и растворяющую способность [33, 34]. В качестве экспресс-метода для определения температуры плавления MMO задействован метод ДСК. На рис. 1 представлена термограмма для моногидрата ММО с эндопиком плавления в области 76°С.
Определив с помощью метода Фишера содержание воды в MMO, была построена калибровочная зависимость, позволяющая быстро оценивать концентрацию воды в растворителе по его точке плавления. Так, используемый в работе моногидрат ММО содержит 13.3% воды, а высокоплавкий ММО – 10%.
Эволюция процесса растворения, а именно изменение площади образцов волокон ПАН во времени при 80, 85, 90 и 95°С для моногидрата ММО и при 110, 115, 120 и 125°С для высокоплавкого ММО, была зафиксирована с помощью фотосъемки.
При использовании моногидрата MMO со временем диаметр волокна ПАН сначала равномерно уменьшается (рис. 2), а далее происходит фрагментация волокна, уменьшение толщины и длины фрагментированных остатков волокна вплоть до полного растворения. Продолжительность полного растворения до 10 мин.
Рис. 2.
Стадии растворения ПАН-волокна в моногидрате ММО при 85°С через 0.5 (а), 2 (б), 4 (в), 6 (г), 8.5 (д) и 9 мин (е).

В случае применения более реакционноспособного высокоплавкого MMO, процесс растворения ПАН волокна протекает с гораздо более высокой скоростью. Детали процесса растворения ПАН в высокоплавком MMO рассмотрены ниже, а здесь имеет смысл остановиться на специфической особенности процесса.
Так, при контакте молекул растворителя с полимером, как и в системе целлюлоза–ММО, отсутствует стадия набухания, предшествующая растворению полимеров. Другими словами, образец при контакте с растворителем становится оптически прозрачным, но в размерах не увеличивается. По-видимому, большой размер молекул растворителя позволяет им проникать только в аморфные области структуры полимеров и скорость их диффузии в волокно сопоставима со скоростью взаимодействия группы N−O с функциональными группами полимеров (прежде всего, с карбоксильными и нитрильными), вызывающей растворение.
Кинетические параметры растворения ПАН в моногидрате MMO
Основным измеряемым параметром является площадь проекции волокна, которая была установлена с помощью программного обеспечения. Это привносит некоторую неточность в определение абсолютных размеров волокон и, особенно, их фрагментов, однако для целей данной работы она несущественна. На основании полученных данных построены зависимости изменения площади волокон различного начального размера в моногидрате MMO при разных значениях температуры (рис. 3а, 3в, 3д, 3ж). Далее, оценивая скорость уменьшения площади по начальному линейному участку зависимости S = f(t) и принимая, что достигаемая в конце процесса растворения концентрация пропорциональна исходной площади волокон, были построены зависимости скорости растворения от концентрации (рис. 3б, 3г, 3е, 3з).
Рис. 3.
Зависимости изменения площади волокна ПАН от времени и скорости растворения от начальной площади волокна ПАН при 80°С, где y = 0.8599x – 1.6954 и R2 = 0.6179 (а, б); при 85°С, где y = 0.9341x – 1.5744 и R2 = 0.6738 (в, г); при 90°С, где y = 1.0439x − 1.4998 и R2 = 0.6596 (д, е); при 95°С, где y = 1.052x − 1.3977 и R2 = 0.672 (ж, з).
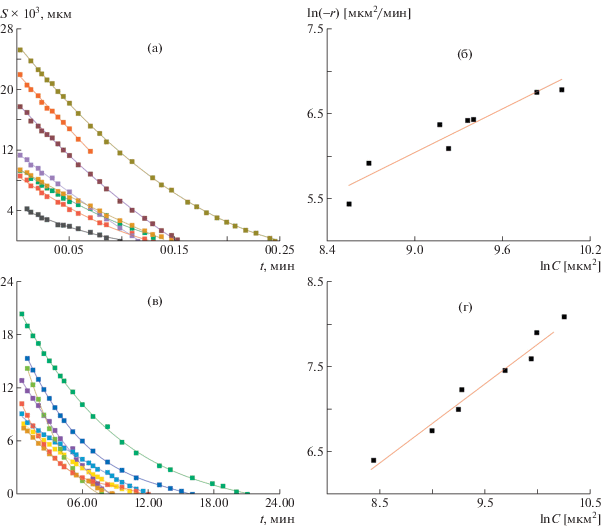
Рис. 3.
Окончание

Полученные при температуре от 80 до 95°С первичные данные по изменению площади волокон (левый ряд графиков) использовались для расчета начальных значений скорости следующим образом. Для реакций первого порядка константа скорости численно равна скорости реакции при концентрации всех реагирующих веществ, равных 1 моль/л, и концентрация экспоненциально зависит от времени [27]. Поэтому зависимости скорости от начальной концентрации в логарифмических координатах (правый ряд графиков) позволяют выявить такие параметры, как порядок реакции a и константу скорости k, которые входят в кинетическое уравнение (2).
Полученные значения были проанализированы в зависимости от температуры в координатах уравнения (3) (рис. 4).
Рис. 4.
Зависимость скорости растворения ПАН в моногидрате ММО от температуры в координатах уравнения Аррениуса (y = −2587.5x + 5.6386, R2 = 0.993).

Обобщенные результаты кинетического исследования растворения ПАН волокон в моногидрате ММО приведены в табл. 2.
Таблица 2.
Кинетические характеристики процесса растворения волокон ПАН в моногидрате ММО
| Т, °С | a | k, мин−1 | A | E, кДж/моль |
|---|---|---|---|---|
| 80 | 0.86 | 0.17 | 281.0 | 21.5 |
| 85 | 0.93 | 0.21 | ||
| 90 | 1.04 | 0.22 | ||
| 95 | 1.05 | 0.24 |
Как и следовало ожидать, представленные выше кинетические параметры, с небольшим разбросом значений, указывают на первый порядок “реакции” процесса растворения. Значения констант скорости согласуются с порядком реакции.
Кинетические параметры растворения ПАН в высокоплавком MMO
По аналогии с использованным подходом к анализу кинетики растворения волокон ПАН в моногидрате MMO исследован процесс растворения тех же волокон в высокоплавком ММО. Как уже упоминалось выше, растворение в высокоплавком растворителе проходит гораздо быстрее, чем в моногидрате MMO, и характер изменения формы растворяемого волокна не столь плавный, нежели в первом случае. В данном случае можно свидетельствовать о “варикозности”, появляющейся с первых мгновений взаимодействия волокна с растворителем (рис. 5).
Рис. 5.
Стадии растворения ПАН волокна в высокоплавком ММО при 115°С во времени через 4 (а), 7 (б), 11 (в), 14 (г), 18 (д) и 22 с (е).

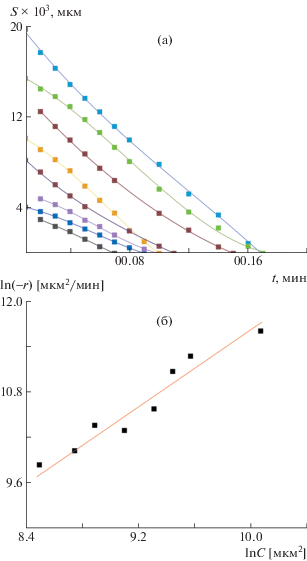
Причина формирования столь неровной поверхности обусловлена активностью растворителя и аморфно-кристаллической природой ПАН в волокне. Прежде всего, растворитель проникает в аморфную фазу, содержание которой примерно одинаково по длине волокна. Чтобы не повторять кинетические кривые для всех исследованных значений температуры (110, 115, 120 и 125°С), так как они однотипны, приведем в качестве рассмотрения только одну – 120°С и, следуя разработанному ранее аппарату, зависимость скорости процесса от концентрации сформированного раствора (рис. 6).
Рис. 6.
Зависимости изменения площади волокна ПАН от времени (а) и скорости растворения в высокоплавком MMO от начальной площади волокна, где y = 1.2813x − 1.1832 и R2 = 0.5842 (б).
Среднее время растворения моноволокна ПАН в высокоплавком MMO составляет 25−30 с, что практически в 20 раз быстрее, чем в случае моногидрата MMO. Таким образом, переход от моногидратной к высокоплавкой форме растворителя приводит к повышению скорости растворения и изменению характера протекания процесса, т.е. кинетика процесса растворения ПАН лимитируется донорной активностью ММО по отношению к полимеру.
Оценка энергии активации процесса растворения была проведена так же, как и в предыдущем случае (рис. 7).
Рис. 7.
Зависимость скорости растворения ПАН в высокоплавком ММО от температуры в координатах уравнения Аррениуса (y = −1036.5x + 1.4591, R2 = 0.9375).
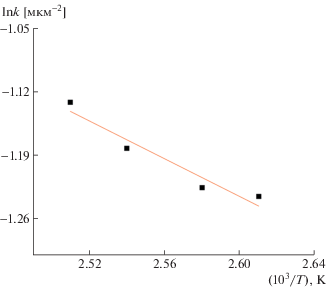
Обобщенные результаты кинетического исследования растворения ПАН волокон в высокоплавком ММО представлены в табл. 3.
Таблица 3.
Кинетические характеристики растворения ПАН в высокоплавком ММО
| Т, °С | a | k, мин−1 | A | E, кДж/моль |
|---|---|---|---|---|
| 110 | 1.24 | 0.28 | 4.3 | 8.6 |
| 115 | 1.27 | 0.29 | ||
| 120 | 1.28 | 0.30 | ||
| 125 | 1.31 | 0.32 |
Сравнивая данные табл. 2 и 3 видно, что энергия активации растворения ПАН в высокоплавком MMO в 2 раза меньше, чем при растворении ПАН в моногидрате ММО. Это согласуется с порядком и константой скорости реакции, значения которых почти на 40% больше, чем для процесса растворения ПАН в моногидрате ММО. Таким образом, скорость растворения и характер его протекания определяется растворяющей способностью кристаллогидратной формы ММО.
Данные для ПАН и найденные ранее значения энергии активации для растворения целлюлозы [35] представлены ниже.
| Образец | Целлюлоза в моногидрате MMO | ПАН в моногидрате MMO | ПАН в высокоплавком ММО |
| E, кДж/моль | 42.8 | 21.5 | 8.6 |
Так, для системы целлюлоза–моногидрат MMO значения энергии активации растворения в 2 раза больше, чем для пары ПАН–моногидрат MMO и в 5 раз выше, чем для системы ПАН–MMO. Полученные значения энергии активации процесса растворения ПАН и целлюлозы в высокополярном растворителе – MMO находятся в логическом соответствии с термодинамическими параметрами процесса растворения различных полимеров в MMO с разной донорной активностью. По абсолютным величинам они, как минимум, на порядок ниже типичных значений энергии активации химических реакций, что позволяет сделать вывод о корректности использованного алгоритма определения кинетических параметров химических реакций для системы с энергетически сильным ЭДА-взаимодействием.
Кинетические параметры растворения ПАН в 12%-ном растворе целлюлозы в высокоплавком ММО
Возможность сочетания в одном гибридном волокне гидрофильной, “хлопкоподобной” целлюлозы и гидрофобного, “шерстеподобного” ПАН − чрезвычайно интересная и важная задача как для текстильной промышленности, так и для получения новых прекурсоров углеродного волокна. Поэтому в данной работе был исследован и процесс растворения ПАН в 12%-ном растворе целлюлозы в высокоплавком MMO. Визуализация этого процесса продемонстрирована на рис. 8.
Рис. 8.
Микрофотографии растворения ПАН волокна в 12%-ном растворе целлюлозы в высокоплавком ММО при 120°С через 0 (а), 4 (б), 8 (в), 14 (г), 23 (д) и 36 с (е).

Хронология растворения, представленная на рис. 9а (для экономии места кинетические кривые приведены только для одной температуры – 120°С), подобна растворению ПАН волокна в высокоплавком MMO. Присутствие целлюлозы в системе приводит к увеличению временного интервала полного растворения волокна на 30% и составляет ~36 с. Далее, следуя разработанному ранее подходу, была построена зависимость скорости процесса от концентрации сформированного раствора (рис. 9б). Аналогичным образом рассчитаны кинетические параметры для данного случая специфического растворения ПАН-волокон в полимерном растворе. Видно, что ПАН прекрасно растворяется в растворе целлюлозы, что может быть эффективно использовано при приготовлении совместных прядильных растворов. Более того, порядок “реакции” и в этом случае незначительно превышает единицу. Судя по рис. 10 и данным, сгруппированным в табл. 4, величина энергии активации также находится в разумных пределах, хотя присутствие в растворителе целлюлозы несколько повышает энергетический барьер растворения.
Рис. 9.
Зависимости изменения площади волокна ПАН от времени (а) и скорости растворения от начальной площади волокна (б) в 12%-ном растворе целлюлозы в ММО при 120°С, где y = 1.2323x − 1.2535 и R2 = 0.56.

Рис. 10.
Зависимость скорости растворения ПАН в 12%-ном растворе целлюлозы в ММО от температуры в координатах уравнения Аррениуса (y = −1471.4x + 2.4607, R2 = 0.9411).

Таблица 4.
Кинетические характеристики растворения ПАН в 12%-ном растворе целлюлозы в ММО
| Т, °С | a | k, мин−1 | A | E, кДж/моль |
|---|---|---|---|---|
| 110 | 1.1410 | 0.2508 | 11.7 | 12.2 |
| 115 | 1.1484 | 0.2618 | ||
| 120 | 1.2323 | 0.2855 | ||
| 125 | 1.2813 | 0.2873 |
Таким образом, в настоящей работе с помощью метода оптической микроскопии визуализирован и изучен процесс растворения ПАН в ММО различной донорной активности при разных значениях температуры и в растворе целлюлозы в том же растворителе. Используя аналогию в описании кинетики химической реакции и процесса растворения с формированием донорно-акцепторных связей, рассчитан порядок и константы скорости “реакции” растворения ПАН в моногидрате ММО, высокоплавком ММО и в растворе целлюлозы в MMO. По значениям констант скорости при различных значениях температуры оценена энергия активации процесса растворения ПАН в разных гидратных формах ММО и в растворе целлюлозы. Показано, что ПАН быстрее растворяется в безводном ММО, чем в моногидрате. Обнаруженный факт более быстрого растворения ПАН, чем целлюлозы, и достаточно эффективное растворение ПАН в растворе целлюлозы может служить основой лабораторной технологии получения совместных прядильных растворов и формования из них композитных волокон.
Работа выполнена в рамках гранта Российского научного фонда (проект № 17-79-30108).
Список литературы
Kulichikhin V.G., Skvortsov I.Yu., Mironova M.I., Ozerin A.N., Kurkin T.S., Berkovich A.K., Frenkin E.I., Malkin A.Ya. // Adv. Polym. Technol. 2018. V. 37. № 4. P. 1099.
Kolobkov A.S., Malakhovskii S.S. // Fibre Chem. 2020. V. 52. P. 1.
Eslami Farsani R., Shokuhfar A., Sedghi A. // Fibre Chem. 2006. V. 38. P. 383.
Azarov A.V., Kolesnikov V.A., Khaziev A.R. // IOP Conf. Ser. Mater. Sci. Eng. 2020. V. 934. P. 012049.
Hattori M., Yamazaki H., Saito M., Hisatani K., Okajima K. // Polym. J. 1996. V. 28. № 7. P. 594.
Iovleva M., Smirnova V., Budnitskii G. // Fibre Chem. 2001. V. 33. № 4. P. 262.
Wu Q.Y., Chen X.N., Wan L.S., Xu Z.K. // J. Phys. Chem. B. 2012. V. 116. № 28. P. 8321.
Ziabicki A. // Fundamentals of Fibre Formation: the Science of Fibre Spinning and Drawing. London: Wiley, 1976.
Конкин А.А. Углеродные и другие жаростойкие волокнистые материалы. M.: Химия, 1974.
Skvortsov I.Y., Toms R.V., Prokopov N.I., Chernikova E.V., Kulichikhin V.G. // Polymer Science A. 2018. V. 60. № 6. P. 894.
Макаров И.С., Голова Л.К., Кузнецова Л.К., Шляхтин А.В., Нифантьев И.Э., Куличихин В.Г. Пат. 2541473 Россия. 2013.
Byrne N., Leblais A., Fox B. // J. Mater. Chem. A. 2014. V. 2. P. 3424.
Хан На, Чжан Синсян, Ван Нин, Сюн Цзюньчэн, Пэн Вэйвэй. Пат. CN102806022B Китай. 2012.
Xu L., Qiu F. // Mater. Sci. Polym. 2015. V. 64. P. 130.
Frank N.E., Varga J.K. Pat. 4145532 US. 1979.
Голова Л.К. // Химические волокна. 1996. № 1. С. 13.
Макаров И.С., Голова Л.К., Кузнецова Л.К., Виноградов М.И., Куличихин В.Г. Пат. 2707600 Россия. 2019.
Kulichikhin V., Golova L., Makarov I., Bondarenko G., Makarova V., Ilyin S., Skvortsov I., Berkovich A. // Eur. Polym. J. 2017. V. 92. P. 326.
Kulichikhin V.G., Golova L.K., Makarov I.S., Bondarenko G.N., Ilyin S.O., Berkovich A.K. // Polymer Science C. 2016. V. 58. № 1. P. 74.
Тимошков П.Н., Севастьянов Д.В., Усачева М.Н., Хрульков А.В. // Тр. ВИАМ. 2019. № 11. С. 83.
Беркович А.К., Cергеев В.Г., Медведев В.А., Малахо А.П. Синтез полимеров на основе акрилонитрила. Технология получения ПАН и углеродных волокон. М.: МГУ, 2010.
Голова Л.К. // Рос. хим. журн. 2002. № 1. С. 49.
Tierney J.W. // Kinetics of Cellulose Dissolution in N-Methyl Morpholine-N-Oxide and Evaporative Processes of Similar Solutions. Master’s Thesis. Tennessee: Univ. of Tennessee Press, 2005.
Куличихин В.Г., Голова Л.К. // Научные основы химической технологии углеводов. М.: Издательство ЛКИ, 2008. С. 223.
Chen F., Sawada D., Hummel M., Sixta H., Budtova T. // Cellulose. 2020. V. 27. № 13. P. 7399.
Chernikova E.V., Toms R.V., Prokopov N.I., Duflot V.R., Plutalova A.V., Legkov S.A., Gomzyak V.I. // Polymer Science B. 2017. V. 59. № 1. P. 28.
Fogler H.S. Elements of Chemical Reaction Engineering. New York: Prentice Hall, 1999.
Бацанов С.С. Структурная химия. Факты и зависимости. М.: Диалог-МГУ, 2000. С. 292.
Сироткин О.С., Сироткин Р.О., Шибаев П.Б. // Регион. науч.-практ. конф. “Методология и практика химического образования в свете развития знаний о природе и обществе”. Казань: Казанский гос. педагогический ун-т, 2005. С. 332.
Сироткин О.С., Сироткин Р.О., Шибаев П.Б. // Вестн. Казанского технол. ун-та. 2011. № 1. С. 22.
Кубасов А.А. Теоретические основы химической кинетики. Химическая кинетика и катализ. М.: Химия, 2005. С. 158.
Яблонский Г.С., Быков В.И., Горбань А.Н. Кинетические модели каталитических реакций. Новосибирск: Наука, 1983. С. 255.
Johnson D.L. Pat. 3447939 USA. 1969.
Голова Л.К., Куличихин В.Г., Папков С.П. // Высокомолек. соед. А. 1986. Т. 28. № 9. С. 1995.
Блейшмидт Н.В., Древаль В.Е., Бородина О.Е., Голова Л.К., Куличихин В.Г. // Высокомолек. соед. А. 1997. Т. 39. № 9. С. 1511.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)



