Высокомолекулярные соединения (серия Б), 2022, T. 64, № 1, стр. 3-19
ТИОЛ-ЕН “КЛИК-РЕАКЦИИ” КАК ПЕРСПЕКТИВНЫЙ ПУТЬ ПОЛУЧЕНИЯ ПОЛИМЕРНЫХ МАТЕРИАЛОВ
Д. С. Казыбаева a, Г. С. Ирмухаметова a, В. В. Хуторянский a, b, *
a Казахский национальный университет им. аль-Фараби
050040 Алматы, пр. Аль-Фараби, 71, Казахстан
b Reading School of Pharmacy, University of Reading
RG66AX Whiteknights, PO Box 224, United Kingdom
* E-mail: v.khutoryanskiy@reading.ac.uk
Поступила в редакцию 14.07.2021
После доработки 31.08.2021
Принята к публикации 28.10.2021
- EDN: PFVYIM
- DOI: 10.31857/S2308113922010053
Аннотация
Обзор посвящен относительно новому и перспективному способу синтеза новых органических соединений и полимерных материалов, основанному на концепции “клик-химии”. Описаны типы “клик-реакций” (циклоприсоединения, нуклеофильное раскрытие колец, карбонильная химия неальдольного типа, присоединения к углерод-углеродным кратным связям) и приведены соответствующие примеры. Наиболее подробно рассмотрены тиол-ен “клик-реакции”, основанные на присоединении тиола к непредельным функциональным группам органических молекул, условия и механизмы их протекания. Показана разнообразная и обширная область применения тиол-ен “клик-химии” для получения биосовместимых материалов, материалов для культивирования и инкапсулирования клеток, синтеза блок-сополимеров, создания деградируемых материалов, новых гомогенных и гибридных сетчатых структур, в хроматографии, гликополимерном синтезе, иммобилизации белков, стабилизация/функционализация капсул и многослойных систем, функционализированных микро- и наногелей, в том числе для использования в наномедицине и при создании противоопухолевых препаратов.
ВВЕДЕНИЕ
За последние два столетия были сформированы основные принципы построения органических молекул. Одна из главных задач, стоящая перед учеными, – оптимизировать синтезы сложных веществ таким образом, чтобы они были легкими в исполнении и в то же время эффективными. В этом преуспела группа ученых, возглавляемая К.В. Sharpless [1], обозначившая новую концепцию синтеза органических молекул с помощью реакций, которые не дают побочных продуктов и позволяют получать гетероатомные молекулярные системы с высоким выходом в мягких условиях. Данный подход обозначается одним емким термином – “клик-химия”, термин происходит от английского “click” и обозначает соединение молекулярных блоков так же легко, как соединение двух частей пряжки ремня безопасности. Свое название он получил неслучайно, поскольку суть этого понятия заключается в подражании природе. Как природа создает новые вещества скреплением маленьких блоков, так и ученые могут проводить синтезы сложных структур из небольших модулей.
Химическая реакция должна удовлетворять ряду критериев, чтобы подходить под концепцию “клик-химии”: реакция должна быть модульной, с широкой областью применения, давать высокие выходы, генерировать только безопасные побочные продукты, которые могут быть удалены без использования хроматографии, и быть стереоспецифической (но не обязательно энантиоселективной). Требуемые характеристики процесса включают в себя простые условия реакции (в идеале процесс должен быть не чувствительным к кислороду и воде), легкодоступные исходные материалы и реагенты, отсутствие растворителя или использование мягкого растворителя (такого, как вода) или легко удаляемого растворителя и отсутствие сложностей при выделении продукта. Очистка, если требуется, должна осуществляться нехроматографическими методами, такими как кристаллизация или дистилляция, и продукт должен быть стабильным в физиологических условиях [1].
К “клик-реакциям” относятся следующие:
– циклоприсоединения, в основном 1,3-диполярные циклоприсоединения [2] и циклоприсоединения Дильса [3];
– нуклеофильное раскрытие колец напряженных гетероциклических электрофилов, таких как азиридины, эпоксиды, циклические сульфаты, ионы азиридиния, ионы эписульфония и т.д. [1];
– карбонильная химия неальдольного типа, включающая образование мочевин, тиомочевин [4], гидразонов, простых эфиров оксимов [5], амидов, ароматических гетероциклов и т.д. [6]. Карбонильные реакции альдольного типа обычно не очень выгодны в термодинамическом отношении, протекают слишком медленно и дают побочные продукты, поэтому и не могут рассматриваться как “клик-реакции”;
– присоединения к углерод-углеродным кратным связям, такие как эпоксидирование [7], азиридинирование, дигидроксилирование [8], присоединение сульфенилгалогенидов, присоединения нитрозилгалогенидов и некоторые реакции Михаэля [9].
Впервые представленная научной группой Sharpless в 1999 г. на 217-м ежегодном собрании Американского химического общества, “клик-химия” на данный момент является достаточно широко развивающимся направлением, о чем свидетельствует почти экспоненциальный рост количества публикаций. Поиск литературы с помощью Web of ScienceTM, проведенный в середине июля 2021 г., выявил в общей сложности свыше 27 тысяч публикаций, содержащих ключевые слова “клик-химия” или “клик-реакция”, которые включали журнальные статьи, обзоры, препринты, рефераты, патенты и диссертации.
ОСНОВНЫЕ ПРИНЦИПЫ ТИОЛ-ЕН “КЛИК-РЕАКЦИЙ”
Остановимся подробнее на так называемых тиол-ен “клик-реакциях”. Термин “тиол-ен” будет использоваться для обозначения присоединения тиола к двойной связи независимо от механизма реакции (молекулярного или ионного). Следует отметить, что термин “тиол-ен” уже начал использоваться в русскоязычной литературе [10].
Тиол-еновая реакция, известная более 100 лет [11], представляет собой простое гидротиолирование связи C=C:
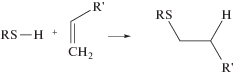
Следует указать на несколько причин, почему тиол-ен-реакции считаются перспективным и достаточно привлекательным инструментом в органическом синтезе. Во-первых, такие реакции могут протекать в различных условиях, включая радикальный путь [12], через каталитические процессы, с участием кислот и оснований [13, 14], при отсутствии катализатора в высокополярных растворителях, таких как вода или диметилформамид [15], или с помощью супрамолекулярного катализа с использованием, например, β-циклодекстрина [16]. Во-вторых, роль субстрата может выполнять широкий спектр соединений с непредельными связями, включая активированные и неактивированные частицы, а также многократно замещенные олефиновые связи. Ниже приведены примеры непредельных функциональных групп, способных к “клик-реакциям” с тиолами.
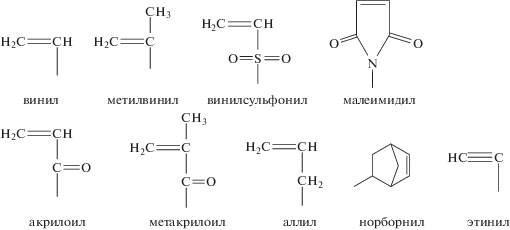
Отметим, что реакционная способность соединений может значительно меняться в зависимости от механизма реакции и характера замещения по связи C=C. В-третьих, в реакции может участвовать практически любой тиол, в том числе многофункциональные соединения, хотя реакционная способность может зависеть от прочности связи S–H и механизма расщепления, т.е. имеет место или гомолитический или гетеролитический разрыв связи. Наконец, такие реакции, как правило, очень быстры и могут длиться всего секунды, устойчивы к присутствию воздуха/кислорода и влаги (при условии, что концентрация кислорода не приближается к концентрации тиола), и приводят к почти количественному образованию соответствующего тиоэфира региоселективным образом.
Взаимодействие тиолов с ненасыщенными соединениями широко изучается с начала ХХ века, и работы до 1940 г. были рассмотрены в обзоре F.R. Mayo и C. Walling [17]. Тиолы могут присоединяться к изолированным двойным связям двумя путями: присоединение в соответствии с правилом Марковникова происходит в присутствии серы и серной кислоты, тогда как в отсутствие добавленного катализатора присоединение осуществляется вопреки данному правилу по свободнорадикальному механизму. Последней реакции способствуют кислород, органические пероксиды и свет, и она ингибируется гидрохиноном и пиперидином [18].
Как правило, тиол-ен реакции проводятся в радикальных условиях. При этом они протекают как типичный цепной процесс со стадиями инициирования, роста и обрыва цепи [19]:
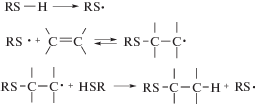
Инициирование осуществляется под действием пероксидов, азосоединений и т.д. или при УФ-облучении, что приводит к образованию тиильного радикала RS·, а также других побочных продуктов [19]. Термическое расщепление связи S–H также можно использовать для образования тиильных радикалов [20]. Рост цепи – это двустадийный процесс: сначала прямое присоединение тиильного радикала через связь C=C с образованием промежуточного углеродно-центрированного радикала, за которым следует передача цепи на вторую молекулу тиола с получением продукта присоединения тиолена с антимарковниковской ориентацией с сопутствующим образованием нового тиильного радикала. Возможные реакции обрыва включают типичные процессы радикал-радикального присоединения [21].
Помимо тиол-ен реакций, опосредованных радикалами, гидротиолирование может быть легко осуществлено при слабом щелочном или нуклеофильном катализе. Оно несколько менее универсальное, чем тиол-ен реакция по радикальному механизму, поскольку для эффективности необходима активация связи C=C, т.е. наличие электронакцепторных групп, обуславливающих дефицит электронов. Однако, учитывая большое количество коммерчески доступных активированных соединений с двойными связями, в том числе многофункциональных соединений, очевидна дальнейшая перспектива синтеза новых многообещающих материалов [22]. Ниже приведена схема механизмов, катализируемых основанием, нуклеофилом. Здесь В – основание, EWG – электроноакцепторная группа (перепечатано из работы [23] с разрешением American Chemical Society).
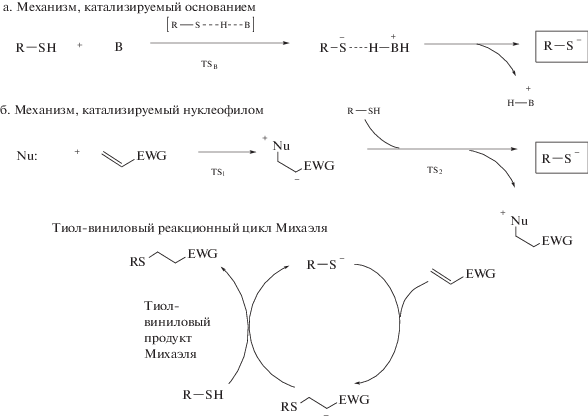
Как показано выше, реакция присоединения Михаэля включает использование каталитических количеств основания (например, амина) для облегчения реакции между тиолом и электроно-дефицитной винильной группой с образованием продукта присоединения тиоэфира. Обычно путь реакции выглядит следующим образом: в присутствии общего основания, такого как триэтиламин, протон отделяется от тиола с образованием тиолат-аниона вместе с сопряженной кислотой. Тиолат-анион является сильным нуклеофилом, инициирующим присоединение аниона через электронодефицитный бета-углеродный атом соединения с двойной связью с образованием промежуточного углерод-центрированного аниона, который, будучи сильным основанием, отрывает водород от сопряженной кислоты и дает в качестве продукта тиоэфир [24].
Исследования [13, 25] установили, что, хотя и основание, и нуклеофил способны успешно катализировать реакцию присоединения тиол-Михаэля, фосфины ускоряют присоединение тиол-Михаэля к метакрилатам с минимальными побочными реакциями, и по сравнению с основанием нуклеофильные фосфины катализируют реакцию намного быстрее и эффективнее. Сам нуклеофил не катализирует реакцию; вместо этого он реагирует с электроно-дефицитной связью C=C с образованием сильного основания.
В зависимости от того, какие комбинации мономеров используются в той или иной тиол-ен “клик-реакции” возможно формирование различных структур. Так, взаимодействие монофункциональных мономеров приводит к образованию только одиночных аддуктов, тогда как бифункциональные мономеры могут образовывать линейные полимеры. Использование мономеров с функциональностью больше двух ведет к формированию полимерных сеток [26]. Соответственно образование тиол-ен полимеров достижимо двумя способами: радикальной тиол-ен “клик” полимеризацией мономеров и постмодификацией уже существующей полимерной цепи, так называемого макромономера, тиол-ен “клик- реакцией” [27].
Первые наблюдения полимеризации за счет тиол-ен присоединения были опубликованы von Braun и Murjahn [28], которые получили нелетучий продукт при попытке синтеза пропен-2-тиола-1. Радикальная тиол-ен полимеризация – это ступенчатый процесс, для которого желательно эквимольное соотношение тиольных и непредельных функциональных групп 1 : 1 во избежание протекания побочных реакций [29]. Радикальная полимеризация состоит из нескольких стадий: инициирования, роста цепи и обрыва, а также стадии передачи цепи:
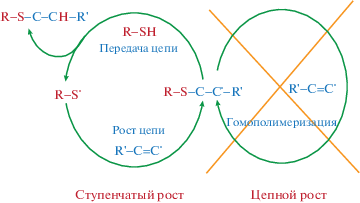
(Перепечатано из работы [22] с разрешения John Wiley and Sons.)
Сначала образуются тиильные радикалы за счет разложения тиола, которое может быть фото- или термоинициировано, с участием инициаторов или без них. Далее тиильный радикал атакует двойную связь и присоединяется к олефину. Наконец, происходит передача цепи, и неспаренный электрон от углеродно-центрированного радикала переносится на другую тиольную группу, тем самым генерируя новый тиильный радикал, что повторно запускает цикл. Обрыв цепи осуществляется путем рекомбинации радикалов [30–32].
Кинетика полимеризации относительно проста на протяжении большей части процесса, так как ММ в данной системе растет медленно. Лимитирующая стадия тиол-ен полимеризации определяется отношением константы скорости роста цепи kр к константе передачи цепи kпц, т.е. kр/kпц. Можно выделить три случая влияния данного соотношения: константы скорости двух стадий приблизительно равны kпц ≈ kр, медленная передача цепи с kпц ≪ kр и медленный рост цепи с kпц ≫ kр. Так, N.B. Cramer с сотрудниками [26] обнаружили, что передача цепи является лимитирующей стадией при идеальной ступенчатой тиол-ен реакции, где отсутствует гомополимеризация. В таком случае углеродно-центрированный радикал всегда переносится на тиольный фрагмент. Использование нескольких типов непредельных функциональных групп и/или непредельных групп, склонных к гомополимеризации (таких как акрилаты и метакрилаты), приводит к дополнительной стадии гомополимеризационного роста цепи [33]. При этом углерод-центрированный радикал гомополимеризуется с другой непредельной функциональной группой, образуя продукт гомополимеризационного роста цепи и другой углерод-центрированный радикал.
Один из важнейших факторов, влияющих на кинетику полимеризации, – химическое строение используемых мономеров. Существует большое количество различных типов непредельных функциональных групп, которые можно использовать в тиол-ен полимеризации. В работе [12] была предложена приблизительная последовательность изменения реакционной способности непредельных соединений: норборнен > виниловый эфир > пропенил > алкен ≈ этенилат > N-виниламиды > аллиловый эфир ~ аллилтриазин ~ ~ аллилизоцианурат > акрилат > ненасыщенный сложный эфир > N-замещенный малеимид > акрилонитрил ~ метакрилат > стирол > сопряженные диены.
Реакционная способность непредельных соединений за некоторым исключением снижается с уменьшением электронной плотности углерод-углеродной двойной связи. Норборнен, метакрилат, стирол и сопряженные диены не подчиняются общей закономерности. Скорость свободнорадикального присоединения тиолов к норборнену исключительно высока, поскольку добавление тиильного радикала через двойную связь значительно снимает напряженность кольца, и последующее отщепление водорода происходит быстрее. Углеродно-центрированные радикалы, которые образуются при взаимодействии тиильного радикала с углерод-углеродной связью метакрилата, стирола или сопряженного диена, очень стабильны и образуют радикалы (метакриловые, бензильные или аллильные), которые имеют низкие константы скорости отщепления водорода. Также стоит отметить, что несопряженные диены в отличие от сопряженных участвуют в тиол-ен реакциях достаточно быстро в соответствии с точным положением непредельной связи.
Наиболее распространенными тиолами для полимеризации являются алкилтиолы, тиолпропионаты, тиолгликолаты и тиолфенолы [33]. В работе [34] было изучено влияние степени замещения тиолов на кинетику тиол-ен полимеризации. В целом увеличение замещения тиола не влияет на скорость тиол-ен реакции при типичных условиях полимеризации, и для наблюдения значительного различия в скорости реакции требуются ухудшенные условия инициирования. Так, первичный тиол реагирует наиболее быстро, за ним следуют вторичные, а затем третичные тиолы, что объясняется стерическими эффектами от увеличения замещения.
Влияние растворителя на кинетику тиол-ен полимеризации рассмотрено в работе [35]. Проведенные исследования показали, что полярность растворителя несущественно влияет на константу скорости роста цепи, тогда как значения константы скорости передачи цепи больше зависят от свойств среды и могут быть увеличены при использовании неполярных растворителей.
В отличие от традиционной радикальной полимеризации кислород не является ингибитором в случае тиол-ен полимеризации. В присутствии кислорода происходят дополнительные реакции передачи цепи, кислород включается в растущие полимерные цепи в виде пероксил-радикала, который участвует в стадии передачи цепи на тиол, образуя тиильный радикал [36].
Далее следует остановиться на использовании макромономеров в тиол-ен реакциях. С помощью тиол-ен “клик-реакций” можно получать макромолекулярные системы сложной архитектуры, например гребнеобразные, звездообразные, дендритные полимеры [37].
В работе [38] функционализированные гребнеобразные полимеры получают введением тиольных функциональных групп в реакционноспособную основную цепь, а именно тиоглюкозы в цепь с непредельными группами. Звездообразные полимеры можно синтезировать, начиная с ядра или с лучей. Последний подход позволяет намного легче достигать этой цели. Сначала получают тиол-функциональный полимер, который затем можно легко “прикрепить” к многолучевому ядру, несущему реакционноспособные непредельные группы [39]. Тиол-ен реакцию можно использовать и для синтеза циклических полимеров [40]. Двумя основными типами синтетических методологий циклизации являются следующие: реакции с замыканием цикла и полимеризация с расширением цикла. В работе [41] α, ω-малеимидо-функциональные стереорегулярные поли (лактиды) были успешно циклизованы с использованием бифункциональных тиолов, что служит примером реакции с замыканием цикла. Подобные реакции следует эффективно проводить при более низких концентрациях, поскольку при увеличении ММ побочные реакции ступенчатого роста будут преобладать над реакциями циклизации. В то же время полимеризация с расширением кольца позволяет получать определенные типы полимеров без осложнений в виде узлов или связанных колец. Для полимеризации с расширением цикла мономер встраивается в циклический инициатор с образованием более крупного кольца. Тиол-ен реакции также можно применять для синтеза дендритных полимеров (см. ниже).
S.P.S. Koo c соавторами [42] исследовали условия и ограничения полимер-полимерной конъюгации с помощью радикальных тиол-ен реакций. Несмотря на высокие скорость реакции и эффективность радикальных тиол-ен реакций при высоких концентрациях, сложности возникают при проведении этой реакции в условиях разбавления, которые часто необходимы для полимер-полимерной конъюгации (межцепного комплексообразования), так как полимеры характеризуются ограниченной растворимостью [43]. Были выявлены следующие закономерности: конъюгация полимера с аналогом небольшой молекулы происходит успешно, даже если для достижения высокой эффективности конъюгации необходимо использовать избыток низкомолекулярного соединения, при этом конъюгация полимера с молекулой более высокой ММ молекулярной массы менее эффективна; полимер-полимерная конъюгация зачастую не протекает, если исходные материалы используются в эквимольных соотношениях (или близких к ним). Эффективность тиол-ен взаимодействия между двумя макромолекулами снижается из-за конкурирующих реакций бимолекулярного обрыва. Если скорость обрыва близка или превышает скорости инициирования, роста и передачи цепи, конверсия будет строго ограничена, и образование побочных продуктов может быть значительным. Соответственно эффективность конъюгации и степень образования побочного продукта зависит от инициатора, непредельной группы и тиолсодержащего компонента [44].
ПРИМЕНЕНИЕ ТИОЛ-ЕН “КЛИК- ХИМИИ”
Тиол-ен “клик-химия” имеет обширную область применения, включая (но не ограничиваясь) получение биосовместимых сетчатых материалов [45], синтез блок сополимеров [44], создание деградируемых материалов [46], синтез дендримеров [47], создание новых гомогенных [48] и гибридных сетчатых структур [49], функционализированных микросфер [50] и наночастиц [51], хроматографию [52], нанопечать и литографию [53], жидкие кристаллы [54], оптические [55] и голографические материалы [56], гликополимерный синтез [38], иммобилизацию белков [57], стабилизацию/функционализацию капсул и многослойных систем [58].
Биомедицина
Группа C.N. Bowman осуществила первичные исследования в направлении деградации тиол-еновых полимеров. В работе [59] изучали, в частности, разлагаемые тиол-акрилатные фотополимеры. Они представляют собой новый класс биоматериалов, особенностью которых является быстрая полимеризация в физиологических условиях при воздействии ультрафиолетового света, в присутствии фотоинициаторов или без них, и на глубине более 10 см. Эти материалы формируются in situ, и однородность их химического состава обеспечивает высокую степень контроля конечных свойств материала. В работе [46] был получен биодеградируемый гель на основе циклического ацетального мономера с реагирующей диаллильной группой и многофункциональных тиолов также методом тиол-ен фотополимеризации. J. Vandenbergh с соавторами [60, 61] занимались синтезом биодеградируемых линейных поли(β-тиоэфиров) ступенчатой тиол-ен полимеризацией из простых дитиолов и диакрилатов. Авторы [62] получали бифункциональные деградируемые 2-оксазолины тиол-ен реакцией димеркаптоацетата гликоля или 2,2'-(этилендиокси)диэтантиола и 2-бут-3'-енил-2-оксазолина или 2-дец-9'-енил-2-оксазолина. Наиболее вероятно, что деградация полимеров в упомянутых выше работах происходит за счет гидролиза сложноэфирных связей, как это было показано ранее [63, 64].
Наша группа получила деградируемые гели на основе пентаэритритолтетракис(3-меркаптопропионата) (ПЭМП) с пентаэритритолтетраакрилатом (ПЭТА) и триметилолпропантриакрилатом посредством тиол-ен “клик-реакции” [65]. Ниже показано предлагаемое строение этих гелей и схема, описывающая реакцию между ПЭТА и ПЭМП, приводящую к образованию сшитой сетки (перепечатано из работы [65] с разрешения “John Wiley and Sons”).
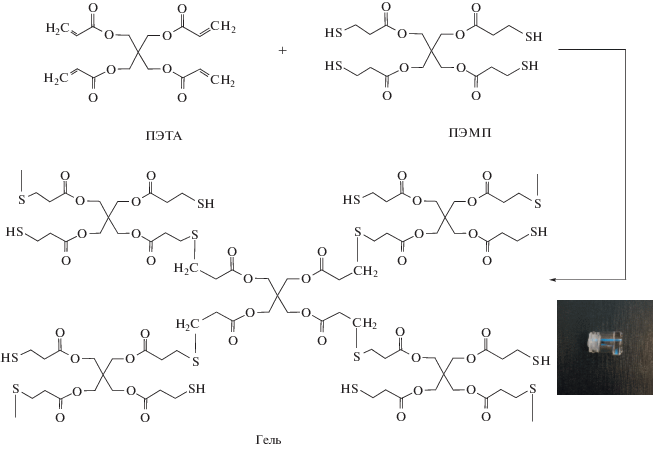
Биодеградацию материалов изучали в различных условиях in vitro. Было установлено, что гели подвергаются очень медленной гидролитической деградации, и этот процесс не ускоряется в присутствии эстеразы. Окислительная деградация данных материалов протекает более интенсивно и в некоторых случаях приводит к полному распаду полимерной сетки на мелкие частицы.
Деструкция полимеров может быть использована при разработке материалов биомедицинского назначения для доставки малых лекарственных молекул [66], а также белковых молекул [67, 68]. Гидрогели ПЭГ, полученные в результате тиол-ен “клик-реакций”, создают подходящие условия для устойчивой и локализованной доставки биоактивных малых молекул, например глюкокортикоидов [69]. Для подтверждения концепции синтетический глюкокортикоид дексаметазон был присоединен к N-концу пептида, разлагаемого матричной металлопротеиназой, который затем легко сополимеризовался в каркасы геля ПЭГ с помощью механизма тиол-ен полимеризации. Конъюгированный дексаметазон был локально изолирован до высвобождения путем расщепления пептидного линкера, инициированного секретируемыми клетками матричной металлопротеиназы, и был доступен только для поглощения локальными совместно инкапсулированными клетками. В работе [70] гидрогели на основе ПЭГ, сшитые с бычьим сывороточным альбумином, чувствительным к нейтрофильной эластазе человека, были получены путем тиол-ен фотополимеризации. Данные гидрогели показали способность к разложению при распознавании клеточного ответа на участках воспаления. Авторы продемонстрировали, что синтезированный гидрогель можно использовать в качестве платформы для доставки белковых лекарств, и, возможно он также подходит для контролируемого высвобождения многих других гидрофильных лекарств, чтобы избежать их денатурации из-за гидрофобного взаимодействия в организме. Бычий сывороточный альбумин поместили в полимерную матрицу данного материала, и он выборочно высвобождался при воздействии нейтрофильной эластазы человека.
Следует уделить внимание еще одному биомедицинскому применению тиол-ен “клик” химии, такому как создание материалов для культивирования клеток [71]. Разработка имитаторов внеклеточного матрикса приобрела популярность как способ создания легко настраиваемых материалов, которые напоминают естественную среду вокруг клеток [72]. В работе [73] сополимерные прекурсоры гидрогеля на основе акрилата метоксиполиэтиленгликоля, Цис-Арг-Гли-Асп-Сер, 5-норборнен-2-метиламина были синтезированы с использованием комбинации RAFT-полимеризации, пост-полимеризационного аминолиза и тиол-ен “клик-реакций”. Прекурсор был сшит в видимом свете тиол-ен “клик-реакцией” с использованием эозина-Y в качестве катализатора, как более щадящей методикой фотосшивки по отношению к клеткам, чем УФ-облучение. Наконец, применение этих гидрогелей в 3D-культурах клеток было продемонстрировано с использованием клеток аденокарциномы протоков поджелудочной железы.
Такие платформы очень удобны для изучения роста, морфогенеза, лекарственной устойчивости и экспрессии маркеров раковых стволовых клеток в клетках аденокарциномы протоков поджелудочной железы в 3D-культурах клеток, как в работе [74]. Авторы синтезировали десмоплазий-имитирующие гидрогели, т.е. гидрофильные полимерные материалы, способные имитировать опухолевые ниши, путем сшивания полиэтиленгликоля-тетра-норборнена с пептидным субстратом с бис-цистеиновыми концевыми группами посредством тиол-ен полимеризации. Пептидный сшивающий агент обладает высокой специфичностью в отношении матричной металлопротеиназы мембранного типа. В работах [75–77] стратегия тиол-ен “клик-реакций” применяется для получения гидрогелей, используемых при инкапсулировании клеток. Авторы [77] получили гидрогели на основе метакрилированной гиалуроновой кислоты и мульти-тиол-функционализированного цвиттер-ионного сополимера на основе поли(карбоксибетаинметакрилата) и N,N'-бис-(акрилоил)цистамина в физиологических условиях без присутствия какого-либо катализатора и УФ-излучения. Благодаря превосходным противообрастающим свойствам цвиттер-ионного компонента гидрогели продемонстрировали устойчивость к адсорбции белков и антиклеточную адгезию. Результаты также свидетельствуют о регулируемой деградации полученных гидрогелей. В работе [78] были получены гидрогелевые каркасы для тканевой инженерии на основе функционализированного полиэтиленгликоля, бис-(ангидрида аллилпропионовой кислоты) (БАПА), 3-меркаптопропионовой кислоты и п-толуолсульфоновой кислоты. Ниже показано формирование сетки MoДПЭГ (модульный, разлагаемый ПЭГ) посредством сшивания ПЭГ-БАПА и ПЭГ-SH (перепечатано из работы [78] с разрешением “John Wiley and Sons”).
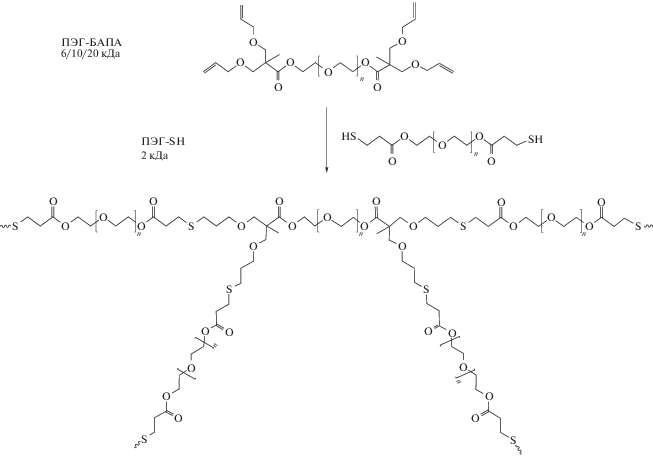
Наряду с обычными гидрогелями методом тиол-ен “клик-химии” можно получать различные микро- и наногели [79, 80]. Даже если макромасштабные гидрогели можно вводить и отверждать in situ [81, 82], их применение все еще в значительной степени ограничено из-за пониженной проницаемости биологически значимых макромолекул. Эти недостатки можно преодолеть используя микро- или наночастицы гидрогеля или микро- и наногели [83]. Авторы [84] синтезировали фотодеградируемые микрочастицы со средним диаметром 22 мкм методом обратной суспензионной полимеризации. В работе [85] тиол-ен фото-клик-реакцией были получены микрогели на основе ПЭГ через три различные системы двухфазной суспензионной полимеризации жидкость–жидкость. В одной из систем были использованы гексан в качестве органической фазы и 1% Спан-80/Твин-80 (1 : 3) в качестве ПАВ. Водный преполимерный раствор состоял из 10 мас. % макромера ПЭГ-тетра-нонборнен (ПЭГ-4-НБ), сшивающего агента дитиотреитол в стехиометрическом соотношении к нонборненовым группам и фотоинициатора Эозин-Y. Обратную суспензию вода-в-масле готовили путем встряхивания двухфазной системы, а сшивание геля происходило под воздействием видимого света в течение 30 с:
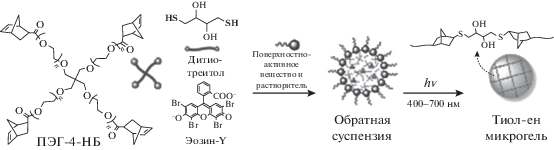
(Перепечатано из работы [85] с разрешением “John Wiley and Sons”.)
Были сформированы полидисперсные тиол-ен микрогели (10–130 мкм) со средним диаметром 70 ± 3 мкм. Также в данной работе были успешно получены двуслойные микрогели, которые являются достаточно перспективными материалами в области биомедицины.
В последние годы множество полимерных наноносителей, таких как наногели, наночастицы, нанокапсулы, дендримеры и полимерные мицеллы, широко исследуются в качестве потенциальных систем доставки лекарств [86]. В работе [87] были получены pH-чувствительные наногели с орто-сложноэфирными связями на основе диакриламида сложного ортоэфира, пентаэритритол тетра(3-меркаптопропионата) и метоксилполиэтиленгликоль акрилата. В работе [88] тиол-ен сополимеризацией пентаэритритолтетра(3-меркаптопропионата), диакрилата полиэтиленгликоля, акрилата метоксилполиэтиленгликоля и N-акрилоил-3-аминофенилбороновой кислоты был получен новый чувствительный к глюкозе наногель. О глюкозочувствительности материалов на основе фенилбороновой кислоты упоминается также в других источниках [89–91].
А. Storha с соавторами [51] описали синтез тиолированных и акрилированных функциональных наночастиц из пентаэритритолтетракис(3-меркаптопропионата) и пентаэритритолтетраакрилата методом тиол-ен “клик-химии как попытку получить тиолированные наноносители со способностью к набуханию в органических растворителях для их последующей загрузки физиологически-активными веществами. Этот синтез был предпринят как альтернатива ранее полученным тиолированным кремнийсодержащим наночастицам на основе 3-меркаптопропилтриметоксисилана [92–94]. Тиолированные наночастицы были мукоадгезивными аналогично тиолсодержащим полимерам, которые широко применяются при разработке новых лекарственных форм для трансмукозальной доставки лекарств [95].
В работе [96] тиол-ен “клик-реакция” была использована в ходе синтеза наночастиц, чувствительных к окислению. Ниже приведена схема метода получения сшитых наночастиц полипропиленсульфида. Сшивки основаны на сульфонах (частицы A), 50 : 50 сульфонах/дисульфидах (частицы B) или дисульфидах (частицы C) (перепечатано из работы [96] с разрешением “International Union of Pure and Applied Chemistry”).
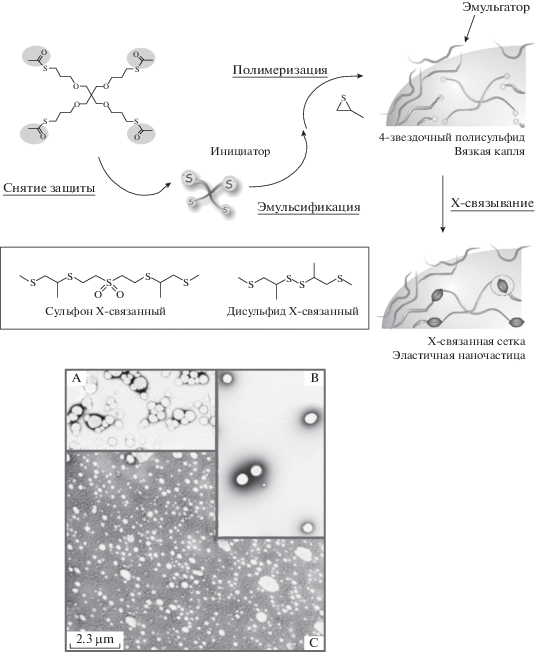
Такие наночастицы были получены эмульсионной полимеризацией пропиленсульфида с раскрытием цикла при использовании тетрафункционального инициатора. Результатом полимеризации является полипропилен сульфид с активными тиолат-ионами на концах растущих цепей. Полимеризация обрывалась путем введения дивинилсульфона, что приводило к сшиванию образующихся крестообразных макромолекул и формированию эластичных наночастиц. Данные наночастицы проявляли гидрофобную природу в водных дисперсиях, но при их контакте с окислителями (например, пероксидом водорода), превращались в гидрофильные частицы. Авторами обсуждаются возможности применения таких наночастиц для доставки лекарств при лечении воспалительных процессов.
В работах [97, 98] тиол-ен реакции использовали для получения флуоресцентно-меченых наночастиц, а также для их функционализации короткоцепными поли(2-оксазолинами). Тиолированные наночастицы на основе 3-меркаптопропилтриметоксисилана метили флуоресцеин-O-метакрилатом и Alexa 546 с концевым малеимидом или BODIPY TMR C5 малеимидом. Флуоресцентный краситель прикреплялся к наночастицам посредством тиол-ен “клик-реакции”. Модификацию поверхности наночастиц поли(2-оксазолинами) осуществляли посредством взаимодействия тиолов с поли(2-оксазолинами), содержащими непредельную (алкин) концевую группу.
Авторы [99] сообщают о “клик-синтезе” биоразлагаемых наночастиц и нанокапсул посредством УФ-индуцированного тиол-ен сшивания полимеров-прекурсоров на основе полилактида в прозрачных миниэмульсиях. В работе [100] показано, что резорцинарентиол-кавитанд может образовывать полые полимерные нанокапсулы разной толщины и жесткости с различными алкенами реакцией тиол-ен “клик-химии”. Также стоит отметить потенциал данного синтеза нанокапсул для применения их в качестве нанореакторов и в наномедицине. Авторы [101] синтезировали нанокапсулы сшитого полимера с цвиттер-ионными внешними оболочками УФ-индуцированной тиол-ен “клик-реакцией” между дитиольным сшивающим агентом и гидрофобным аллил-функционализированным блоком сополимера в периферийной области масляных нанокапель в миниэмульсии. Полученные нанокапсулы имели средний гидродинамический диаметр 136 нм. Нанокапсулы обладают такими важными биомедицинскими характеристиками, как биоразлагаемость, биосовместимость и высокая коллоидная стабильность, что делает их достаточно привлекательными материалами для диагностики рака.
В работе [102] полиаллильные карбоксилановые дендримеры третьего поколения были модифицированы объемными тиолами фотоинициируемым тиол-ен присоединением. В работе [47] стратегия дивергентного роста в комбинации с тиол-ен “клик-химией” и традиционных реакций этерификации были использованы для получения дендримеров четвертого поколения. Ниже показана схема синтеза дендримера с использованием тиол-ен “клик-химии”. (Перепечатано из работы [47] с разрешения American Chemical Society.)
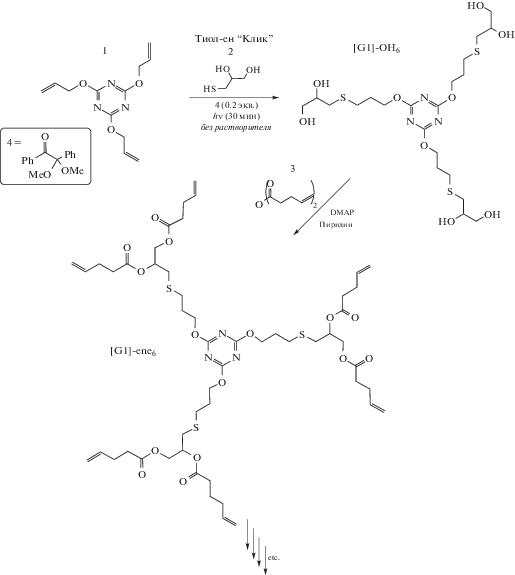
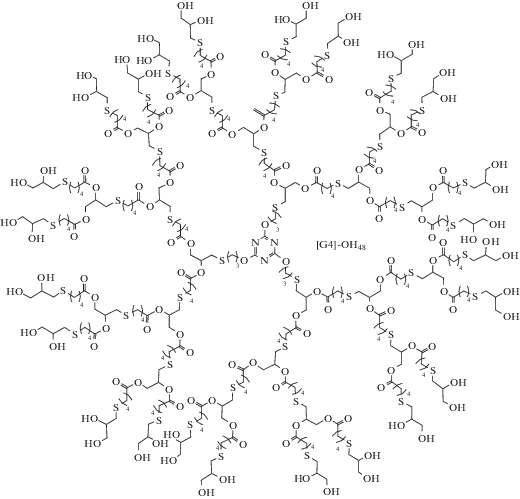
Отсутствие растворителя, комнатная температура, облучение УФ-светом были основными условиями тиол-ен “клик-реакции”. Дендримеры были впоследствии функционализированы фрагментами тиогликолевой кислоты, 4-(пирен-1-ил)-бутил-2-меркаптоацетата и 9-флуоренилметоксикарбонил цистеина. Авторы [103] предложили ускоренный синтез серии дендримеров пятого поколения на основе 2,2-бис-(гидроксиметил)пропионовой кислоты комбинацией тиол-ен “клик-реакций” и реакций этерификации с использованием библиотеки сменных модульных мономеров AB2/CD2 всего за пять стадий, исключив необходимость в выполнении стадий защиты/снятия защиты. В работе [104] также была разработана эффективная стратегия ортогонального связывания для получения многофункциональных дендримеров с использованием углеводных строительных блоков, основанная на сочетании тиол-ен и SN2 реакций. В исследованиях поверхностного плазмонного резонанса дендример, покрытый β-D-галактопиранозидом, проявлял нМ связывающую аффинность с бактериальным лектином, экстрагированным из Pseudomonas aeruginosa.
В работе [105] статистические и блок-сополимеры на основе поли(2-гидроксиэтилметакрилата) и поли[олиго-(этиленгликоль) метилэфирметакрилата] были модифицированы пент-4-еновым ангидридом для получения полимеров с боковой винильной группой. Последующая конъюгация с цис-диамминдихлороплатиной приводит к образованию полимеров с подвешенными платиносодержащими физиологически-активными веществами. Гидрофобность препарата придала блок-сополимерам амфифильный характер, что привело к образованию мицелл. Авторы [106] синтезировали ряд биоразлагаемых полиэфиров с несколькими боковыми меркапто-группами поликонденсацией в расплаве диол полиэтиленгликоля, 1,4-бутандиола и меркаптоянтарной кислоты в присутствии трифторметансульфоната скандия [Sc(OTf)3] в качестве катализатора. Стоит отметить, что недеградируемые тиол-ен “клик-полимеры” перспективны в биомедицине в качестве стоматологических реставрационных композитов благодаря некоторым характеристикам, таким как быстрая скорость полимеризации, высокая конверсия функциональных групп и снижение усадочного напряжения при полимеризации [107, 108]. В работе [109] олигомеры, функционализированные тиолами, были образованы посредством реакций присоединения Михаэля с использованием синтезированных мономеров тетра-(2-меркаптоэтил) силана и дивинилсульфона. Затем полученные олигомеры фотополимеризовали с эквимольным количеством двойных связей триметилпропандиаллилового эфира.
Протеомика и функционализация белков
Принципы тиол-ен “клик-химии” широко применяются при изучении белков [110]. Одним из перспективных направлений в этой области является создание ферментных реакторов [111–113], которые имеют большой потенциал для наблюдения за перевариванием белков в реальном времени и экспресс-анализе. Так, авторы [113] получили реактор с иммобилизованным ферментом на основе органического монолита триметилолпропантриметакрилата тиол-ен “клик-реакцией”. В работе [114] монолитные колонки на основе тетраметоксисилана и винилтриметоксисилана, функционализированные октадецилом, были адаптированы для протеомного анализа с использованием капиллярной жидкостной хроматографии и масс-спектрометрии. Функционализация монолитных колонок была проведена тиол-ен “клик-реакцией” винильных групп с 1-октадекантиолом, 3-меркапто-1-пропансульфонатом натрия и 2,2-α-(этилендиокси)диэтантиол/винилфосфоновой кислотой соответственно. Было обнаружено, что полученная монолитная колонка 37 см в длину и 75 мм в диаметре может идентифицировать 3918 уникальных пептидов и 1067 уникальных белков. Функционализация самих белков также может быть осуществлена с помощью тиол-ен “клик-реакций” [115], а именно, модификация ПЭГ некоторых белков за счет взаимодействия их тиольных групп с малеимидами [116], гликозилирование белков с образованием гликопротеинов [117, 118], полимер-протеин конъюгация [119, 120] и т.д. Все эти реакции являются частными примерами образования сополимеров, например в работе [121] один из полимеров был винил-терминирован, а второй имел свободные SH-группы, тогда как в работе [122] бисмалеимид, 1,8-бис-малеимидодиэтиленгликоль, был использован для соединения RAFT-полимеризованного термочувствительного поли (N-изопропилакриламида) и овальбумина двумя последовательными тиол-ен реакциями.
Распознавание и разделение веществ
Хроматография – наиболее широко используемый метод разделения в химических лабораториях, он используется для анализа, выделения и очистки соединений. В создании хроматографических и экстракционных материалов [52] часто применяются методы тиол-ен “клик-химии”, а именно для приготовления монолитных колонок [123, 124], стационарных фаз [125–128], сорбентов [129, 130]. Например, в работе [126] тиол-ен “клик-реакции” были применены для иммобилизации полиакриламида на алкенил-модифицированном диоксиде кремния при получения новой стационарной фазы для гидрофильной жидкостной хроматографии. Ряд типичных полярных соединений использовали для оценки ее хроматографических характеристик, а нуклеозиды и олигосахариды были выбраны для изучения потенциального применения при разделении полярных соединений.
Материалы для обнаружения других веществ, в том числе и ионов металлов [131, 132], также можно получать с использованием тиол-ен “клик-химии”. Загрязнение природных вод тяжелыми металлами остается нерешенной экологической проблемой, требующей развития технологий очистки. В статье [133] предложена разработка новой биогубки для адсорбции тяжелых металлов. Биогубка представлена альгинатной биополимерной сеткой, инкапсулированной восстановленным оксидом графена, модифицированным наночастицами оксида железа, и ковалентно присоединенными молекулами мультитиола (пентаэритритолтетракисмеркаптопропионата) с использованием фотоинициированной тиол-ен “клик-реакции”. Графеновая биогубка с SH-функционализацией превзошла опубликованные в литературе адсорбенты ионов тяжелых металлов (Cu, Co, Pb и Cd) в морской воде.
Работа [134] сообщает о тиол-ен “клик-синтезе” нового магнитного мезопористого композита диоксид кремния–хитозан для селективного улавливания Hg (II) и высокой каталитической активности отработанного Hg (II) адсорбента.
Очистка выбросов
Быстрая и эффективная ликвидация утечки или выбросов органических соединений, таких как нефть и другие масла, является одной из приоритетных экологических проблем. В последнее время использование трехмерных (3D) пористых материалов, обладающих супергидрофобностью и высокой пористостью, рассматривается как потенциально эффективный метод удаления нефти. Благодаря сродству к маслу и водоотталкивающим свойствам эти специальные трехмерные материалы могут избирательно поглощать масла из воды. В работе [135] для удаления масел были разработаны супергидрофобные меламиновые губки с использованием методов тиол-ен “клик химии”. Материал получали в две стадии: формирование слоя тиольных групп реакцией меркаптосиланов со вторичными аминогруппами на поверхности меламиновой губки и последующее взаимодействие этих групп с длинноцепочечными метакрилатами для придания супергидрофобности. Подобные губки также были получены на основе целлюлозы и полиуретана в работах [136, 137].
В последнее время мембранная технология привлекает к себе особенный интерес при очистке нефтесодержащих сточных вод. Причиной стали высокая эффективность разделения, низкое энергопотребление и экономичные производственные процессы. В частности, мембранные технологии открывают путь к эффективному отделению эмульсий от воды. Несмотря на эти преимущества мембранной технологии, используемые полимерные мембраны имеют некоторые недостатки. Например, они легко загрязняются или даже забиваются масляными веществами в процессе фильтрации, что приводит к значительному сокращению срока службы мембран. Один из эффективных путей улучшения противообрастающих свойств мембраны – гидрофильная модификация. В работах [138, 139] описана высокогидрофильная полиакрилонитрильная мембрана и ее модификация, разработанная с помощью тиол-ен “клик-химии”. Эффективность разделения нескольких видов эмульсий “масло в воде” достигает 99.9%.
Получение супергидрофобных покрытий
Супергидрофобные материалы могут быть представлены не только в виде губок и мембран, также супергидрофобные покрытия можно наносить на различные поверхности. В последние годы очень популярным стало нанесение супергидрофобных покрытий на стекло, бумагу, дерево, металл и ткани. В работах [130, 141] были получены супергидрофобные хлопчатобумажные ткани с использованием тиол-ен “клик-химии”. X. Chen с сотрудниками провели реакцию между винил-триметоксисиланом и меркаптаном в ультрафиолетовом свете с образованием гидрофобного реагента, который затем гидролизовали в соответствующих условиях [141]. Супергидрофобность достигается обезвоживанием гидролизованного продукта и конденсацией с помощью хлопчатобумажной ткани при высоких температурах. Контактный угол смачивания данных поверхностей водой составлял 159°, а угол скольжения 7.2°.
Создание адгезивных материалов
Помимо использования тиол-ен “клик-химии” для создания и модификации материалов, такие реакции могут обеспечивать усиленную способность полимеров к адгезии по отношению к биологическим поверхностям. Так, в ряде работ последних лет была показана усиленная адгезивность полимеров функционализированных акрилоильными [142–144], метакрилоильными [145, 146] и малеимидными [149, 150] группами по отношению к слизистым поверхностям человека и животных. Данная способность обусловлена возможностью образования ковалентных связей между материалами, содержащими непредельные группы и муцинами, содержащими тиольные группы и присутствующими на поверхности слизистых мембран. Важно отметить, что такие “клик-реакции” происходят довольно быстро при физиологических условиях. Это дает возможность использования полимеров и коллоидных частиц с поверхностными непредельными группами в качестве био- и мукоадгезивных носителей лекарственных веществ.
ЗАКЛЮЧЕНИЕ
Мы надеемся, что настоящий обзор дал некоторое представление о принципах и применении тиол-ен “клик-химии”, поскольку данный метод в последние годы получил широкое распространение в разнообразных областях науки и техники. Значительный вклад был внесен в создание материалов биомедицинского назначения, чему мы посвятили большую часть обзора. Кроме того, тиол-ен “клик-химия” является отличным инструментом для создания материалов самого различного назначения. Так, с его помощью получают хроматографические и экстракционные материалы, супергидрофобные материалы для ликвидации выбросов органических соединений. Исследования с использованием тиол-ен “клик-химии” продолжают набирать обороты, а значит, впереди будет еще множество разработок прикладного характера.
Авторы благодарят Министерство образования и науки Республики Казахстан за финансовую поддержку при работе над обзором (грант номер АРО8052780).
Список литературы
Kolb H.C., Finn M.G., Sharpless K.B. // Angew. Chem. Int. Ed. 2001. V. 40. № 11. P. 2004.
Li P.-Z., Wang X.-J., Zhao Y. // Coord. Chem. Rev. 2019. V. 380. P. 484.
Gregoritza M., Brandl F.P. // Eur. J. Pharm. Biopharm. 2015. V. 97. P. 438.
Štrukil V. // Beilstein J. Org. Chem. 2017. V. 13. P. 1828.
Ulrich S., Boturyn D., Marra A., Renaudet O., Dumy P. // Eur. J. A. 2014. V. 20. № 1. P. 34.
Mirjafari A. // Chem. Commun. 2018. V. 54. № 24. P. 2944.
Guzmán D., Ramis X., Fernández-Francos X., De la Flor S., Serra A. // Prog. Org. Coatings. 2018. V. 114. P. 259.
Kolb H.C., Van Nieuwenhze M.S., Sharpless K.B. // Chem. Rev. 1994. V. 94. № 8. P. 2483.
Kolb H.C., Sharpless K.B. // Drug Discov. Today. 2003. V. 8. № 24. P. 1128.
Svidchenko E.A., Tarasenkov A.N., Surin N.M., Aisin R.R., Demchenko N.V., Cherkaev G.V., Muza-farov A.M. // Polymer Science B. 2019. V. 61. № 3. P. 275.
Posner T. // Berichte der Dtsch. Chem. Gesellschaft. 1905. V. 38. № 1. P. 646.
Hoyle C.E., Lee T.Y., Roper T. // J. Polym. Sci., Polym. Chem. 2004. V. 42. № 21. P. 5301.
Chan J.W., Hoyle C.E., Lowe A.B. // J. Am. Chem. Soc. 2009. V. 131. № 16. P. 5751.
Chan J.W., Yu B., Hoyle C.E., Lowe A.B. // Chem. Commun. 2008. № 40. P. 4959.
Kakwere H., Perrier S. // J. Am. Chem. Soc. 2009. V. 131. № 5. P. 1889.
Krishnaveni N.S., Surendra K., Rao K.R. // Chem. Commun. 2005. № 5. P. 669.
Mayo F.R., Walling C. // J. Org. Chem. 1940. V. 27. № 2. P. 351.
Knuth C., Bavley A., Lazier W.A. // J. Org. Chem. 1954. V. 19. № 5. P. 845.
Griesbaum K. // Angew. Chem. Int. Ed. Eng. 1970. V. 9. № 4. P. 273.
Voronkov M.G., Deryagina E.N. // Russ. Chem. Rev. 1990. V. 59. № 8. P. 778.
Sinha A.K., Equbal D. // Asian J. Org. Chem. 2019. V. 8. № 1. P. 32.
Hoyle C.E., Bowman C.N. // Angew. Chem. Int. Ed. 2010. V. 49. № 9. P. 1540.
Xi W., Wang C., Kloxin C.J., Bowman C.N. // ACS Macro Lett. 2012. V. 1. № 7. P. 811.
Nair D.P., Podgórski M., Chatani S., Gong T., Xi W., Fenoli C.R., Bowman C.N. // Chem. Mater. 2014. V. 26. № 1. P. 724.
Liu M., Tan B.H., Burford R.P., Lowe A.B. // Polym. Chem. 2013. V. 4. № 11. P. 3300.
Cramer N.B., Davies T., O’Brien A.K., Bowman C.N. // Macromolecules. 2003. V. 36. № 12. P. 4631.
Smith A.D., Tennyson A.G., Smith R.C. // Sustain. Chem. 2020. V. 1. № 3. P. 209.
von Braun J., Murjahn R. // Berichte der Dtsch. Chem. Gesellschaft. A, B. 1926. V. 59. № 6. P. 1202.
Morgan C.R., Magnotta F., Ketley A.D. // J. Polym. Sci., Polym. Chem. Ed. 1977. V. 15. № 3. P. 627.
Cramer N.B., Scott J.P., Bowman C.N. // Macromolecules. 2002. V. 35. № 14. P. 5361.
Cramer N.B., Reddy S.K., O’Brien A.K., Bowman C.N. // Macromolecules. 2003. V. 36. № 21. P. 7964.
Cook W.D., Chen F., Pattison D.W., Hopson P., Beaujon M. // Polym. Int. 2007. V. 56. № 12. P. 1572.
Cramer N.B., Bowman C.N. // Thiol-X Chemistries in Polymer and Materials Science. The Royal Society of Chemistry. 2013. № 6. P. 1.
Long K.F., Bongiardina N.J., Mayordomo P., Olin M.J., Ortega A.D., Bowman C.N. // Macromolecules. 2020. V. 53. № 14. P. 5805.
Munar I., Flndlk V., Degirmenci I., Aviyente V. // J. Phys. Chem. A. 2020. V. 124. № 13. P. 2580.
O’Brien A.K., Cramer N.B., Bowman C.N. // J. Polym. Sci., Polym. Chem. 2006. V. 44. № 6. P. 2007.
Geng Z., Shin J.J., Xi Y., Hawker C.J. // J. Polym. Sci., Polym. Chem. 2021. V. 59. № 11. P. 963.
Chen G., Amajjahe S., Stenzel M.H. // Chem. Commun. 2009. № 10. P. 1198.
Chan J.W., Yu B., Hoyle C.E., Lowe A.B. // Polymer (Guildf). 2009. V. 50. № 14. P. 3158.
Jia Z., Monteiro M.J. // J. Polym. Sci., Polym. Chem. 2012. V. 50. № 11. P. 2085.
Stanford M.J., Pflughaupt R.L., Dove A.P. // Macromolecules. 2010. V. 43. № 16. P. 6538.
Koo S.P.S., Stamenović M.M., Prasath R.A., Inglis A.J., Du Prez F.E., Barner-Kowollik C., Van Camp W., Junker T. // J. Polym. Sci., Polym. Chem. 2010. V. 48. № 8. P. 1699.
Derboven P., D’Hooge D.R., Stamenovic M.M., Espeel P., Marin G.B., Du Prez F.E., Reyniers M.F. // Macromolecules. 2013. V. 46. № 5. P. 1732.
Fairbanks B.D., Love D.M., Bowman C.N. // Macromol. Chem. Phys. 2017. V. 218. № 18. P. 1.
Machado T.O., Sayer C., Araujo P.H.H. // Eur. Polym. J. 2017. V. 86. P. 200.
Wang K., Lu J., Yin R., Chen L., Du S., Jiang Y., Yu Q. // Mater. Sci. Eng. C. 2013. V. 33. № 3. P. 1261.
Killops K.L., Campos L.M., Hawker C.J. // J. Am. Chem. Soc. 2008. V. 130. № 15. P. 5062.
Li Q., Zhou H., Hoyle C.E. // Polymer (Guildf). 2009. V. 50. № 10. P. 2237.
Sangermano M., Colucci G., Fragale M., Rizza G. // React. Funct. Polym. 2009. V. 69. № 9. P. 719.
Yang X., Zhu L.-W., Wan L.-S., Zhang J., Xu Z.-K. // J. Mater. Res. 2013. V. 28. № 4. P. 642.
Štorha A., Mun E.A., Khutoryanskiy V.V. // RSC Adv. 2013. V. 3. № 30. P. 12275.
Ghamat S.N., Talebpour Z., Mehdi A. // Trends Anal. Chem. 2019. V. 118. P. 556.
Campos L.M., Meinel I., Guino R.G., Schierhorn M., Gupta N., Stucky G.D., Hawker C.J. // Adv. Mater. 2008. V. 20. № 19. P. 3728.
Li Y., Zhang Y., Goswami M., Vincent D., Wang L., Liu T., Li K., Keum J.K., Gao Z., Ozcan S., Gluesenkamp K.R., Rios O., Kessler M.R. // Soft Matter. 2020. V. 16. № 7. P. 1760.
Zuo J., Liu Z., Luo C., Lin F. // Prog. Org. Coatings. 2021. V. 151. P. 106048.
Hu Y., Kowalski B.A., Mavila S., Podgórski M., Sinha J., Sullivan A.C., McLeod R.R., Bowman C.N. // ACS Appl. Mater. Interfaces. 2020. V. 12. № 39. P. 44103.
Jonkheijm P., Weinrich D., Köhn M., Engelkamp H., Christianen P.C.M., Kuhlmann J., Maan J.C., Nüsse D., Schroeder H., Wacker R., Breinbauer R., Niemeyer C.M., Waldmann H. // Angew. Chemie Int. Ed. 2008. V. 47. № 23. P. 4421.
Connal L.A., Kinnane C.R., Zelikin A.N., Caruso F. // Chem. Mater. 2009. V. 21. № 4. P. 576.
Rydholm A.E., Bowman C.N., Anseth K.S. // Biomaterials. 2005. V. 26. № 22. P. 4495.
Vandenbergh J., Ranieri K., Junkers T. // Macromol. Chem. Phys. 2012. V. 213. № 24. P. 2611.
Vandenbergh J., Peeters M., Kretschmer T., Wagner P., Junkers T. // Polymer (Guildf). 2014. P. 1.
Luef K.P., Petit C., Ottersböck B., Oreski G., Ehrenfeld F., Grassl B., Reynaud S., Wiesbrock F. // Eur. Polym. J. The Authors, 2017. V. 88. P. 701.
Nair L.S., Laurencin C.T. // Prog. Polym. Sci. 2007. V. 32. № 8–9. P. 762.
Leja K., Lewandowicz G. // Polish J. Environ. Stud. 2010. V. 19. № 2. P. 255.
Kazybayeva D.S., Irmukhametova G.S., Khutoryanskiy V.V. // Polym. Adv. Technol. 2021. V. 32. P. 2682.
Shih H., Lin C.C. // Biomacromolecules. 2012. V. 13. № 7. P. 2003.
Rehmann M.S., Garibian A.C., Kloxin A.M. // Macromol Symp. 2014. V. 329. № 1. P. 58.
McCall J.D., Anseth K.S. // Biomacromolecules. 2012. V. 13. № 8. P. 2410.
Yang C., Mariner P.D., Nahreini J.N., Anseth K.S. // J Control Release. 2012. V. 162. № 3. P. 612.
Aimetti A.A., Machen A.J., Anseth K.S. // Biomaterials. 2009. V. 30. № 30. P. 6048.
Sawicki L.A., Kloxin A.M. // Biomater. Sci. 2014. V. 2. № 11. P. 1612.
Nicolas J., Magli S., Rabbachin L., Sampaolesi S., Nicotra F., Russo L. // Biomacromolecules. 2020. V. 21. № 6. P. 1968.
Tan V.T.G., Nguyen D.H.T., Utama R.H., Kahram M., Ercole F., Quinn J.F., Whittaker M.R., Davis T.P., Justin Gooding J. // Polym. Chem. 2017. V. 8. № 39. P. 6123.
Ki C.S., Lin T.Y., Korc M., Lin C.C. // Biomaterials. 2014. V. 35. № 36. P. 9668.
Lin C.C., Raza A., Shih H. // Biomaterials. 2011. V. 32. № 36. P. 9685.
Kuang L., Damayanti N.P., Jiang C., Fei X., Liu W., Narayanan N., Irudayaraj J., Campanella O., Deng M. // J. Appl. Polym. Sci. 2019. V. 136. № 5. P. 47212.
Zhang Y., Liu S., Li T., Zhang L., Azhar U., Ma J., Zhai C., Zong C., Zhang S. // Carbohydr. Polym. 2020. V. 236. P. 116021.
Lüchow M., Fortuin L., Malkoch M. // J. Polym. Sci. 2020. V. 58. № 22. P. 3153.
Zhang X., Malhotra S., Molina M., Haag R. // Chem. Soc. Rev. 2015. V. 44. № 7. P. 1948.
Jiang Y., Chen J., Deng C., Suuronen E.J., Zhong Z. // Biomaterials. 2014. V. 35. № 18. P. 4969.
Christopher D. Pritchard // Biomaterials. 2011. V. 32. № 2. P. 587.
Liu Y., Liu M., Zhang Y., Cao Y., Pei R. // New J. Chem. 2020. V. 44. № 27. P. 11420.
Oh J.K., Drumright R., Siegwart D.J., Matyjaszewski K. // Prog. Polym. Sci. 2008. V. 33. № 4. P. 448.
Tibbitt M.W., Han B.W., Kloxin A.M., Anseth K.S. // J. Biomed. Mater. Res. A. 2012. V. 100. № 7. P. 1647.
Fraser A.K., Ki C.S., Lin C.C. // Macromol. Chem. Phys. 2014. V. 215. № 6. P. 507.
Venditti I. // J. King Saud Univ. Sci. 2019. V. 31. № 3. P. 398.
Wang J., Wang X., Yan G., Fu S., Tang R. // J. Colloid Interface Sci. 2017. V. 508. P. 282.
Zhao L., Xiao C., Ding J., He P., Tang Z., Pang X., Zhuang X., Chen X. // Acta Biomater. 2013. V. 9. № 5. P. 6535.
Lacina K., Skládal P., James T.D. // Chem. Cent. J. 2014. V. 8. № 1. P. 60.
Nurpeissova Z.A., Alimkhanova S.G., Mangazbayeva R.A., Shaikhutdinov Y.M., Mun G.A., Khutoryanskiy V.V. // Eur. Polym. J. 2015. V. 69. P. 132.
Elsherif M., Hassan M.U., Yetisen A.K., Butt H. // ACS Nano. 2018. V. 12. № 3. P. 2283.
Irmukhametova G.S., Mun G.A., Khutoryanskiy V.V. // Langmuir. 2011. V. 27. P. 9551.
Irmukhametova G.S., Fraser B.J., Keddie J.L., Mun G.A., Khutoryanskiy V.V. // Langmuir. 2012. V. 28. P. 299.
Al Mahrooqi J.H., Mun E.A., Williams A.C., Khutoryanskiy V.V. // Langmuir. 2018. V. 34. № 28. P. 8347.
Bernkop-Schnürch A. // Adv. Drug Deliv. Rev. 2005. V. 57. № 11. P. 1569.
Khutoryanskiy V.V., Tirelli N. // Pure Appl. Chem. 2008. V. 80. P. 1703.
Mansfield E.D.H., Sillence K., Hole P., Williams A.C., Khutoryanskiy V.V. // Nanoscale. 2015. V. 7. № 32. P. 13671.
Mansfield E.D.H., de la Rosa V.R., Kowalczyk R.M., Grillo I., Hoogenboom R., Sillence K., Hole P., Williams A.C., Khutoryanskiy V.V. // Biomater. Sci. 2016. V. 4. № 9. P. 1318.
Zou J., Hew C.C., Themistou E., Li Y., Chen C.K., Ale-xandridis P., Cheng C. // Adv. Mater. 2011. V. 23. № 37. P. 4274.
Balasubramanian R., Han S., Chamberlayne C. // RSC Adv. 2013. V. 3. № 29. P. 11525.
Sun H., Yan L., Carter K.A., Zhang J., Caserto J.S., Lovell J.F., Wu Y., Cheng C. // Langmuir. 2019. V. 35. № 5. P. 1440.
Tarasenkov A.N., Getmanova E.V., Tatarinova E.A., Buzin I., Demchenko N.V., Cherkaev G.V., Muzafa-rov A.M. // Russ. Chem. Bull. 2017. V. 66. № 9. P. 1675.
Montañez M.I., Campos L.M., Antoni P., Hed Y., Walter M.V., Krull B.T., Khan A., Hult A., Hawker C.J., Malkoch M. // Macromolecules. 2010. V. 43. P. 6004.
Kottari N., Chabre Y.M., Shiao T.C., Rej R., Roy R. // Chem. Commun. 2014. V. 50. № 16. P. 1983.
Huynh V.T., Chen G., Souza P. De, Stenzel M.H. // Biomacromolecules. 2011. V. 12. № 5. P. 1738.
Huang Y., Sun R., Luo Q., Wang Y., Zhang K., Deng X., Zhu W., Li X., Shen Z. // J. Polym. Sci., Polym. Chem. 2016. V. 54. № 1. P. 99.
Lu H., Carioscia J.A., Stansbury J.W., Bowman C.N. // Dent. Mater. 2005. V. 21. № 12. P. 1129.
Carioscia J.A., Lu H., Stanbury J.W., Bowman C.N. // Dent. Mater. 2005. V. 21. № 12. P. 1137.
Podgorski M., Becka E., Claudino M., Flores A., Shah P.K., Stansbury J.W., Bowman C.N. // Dent. Mater. 2015. V. 31. № 11. P. 1255.
Nolan M.D., Scanlan E.M. // Front. Chem. 2020. V. 8. P. 1060.
Chen Y., Wu M., Wang K., Chen B., Yao S., Zou H., Nie L. // J. Chromatogr. A. 2011. V. 1218. № 44. P. 7982.
Zhao X., Fan P.R., Mo C.E., Huang Y.P., Liu Z.S. // J. Chromatogr. A. 2020. V. 1611. P. 460618.
Fan P.R., Zhao X., Wei Z.H., Huang Y.P., Liu Z.S. // Eur. Polym. J. 2020. V. 124. P. 109456.
Liu Z., Liu J., Liu Z., Wang H., Ou J., Ye M., Zou H. // J. Chromatogr. A. 2017. V. 1498. P. 29.
Tang W., Becker M. // Chem. Soc. Rev. 2014. V. 43. P. 7013.
Porfiryeva N.N., Moustafine R.I., Khutoryanskiy V. V. // Polymer Science C. 2020. V. 62. № 1. P. 62.
Dondoni A., Massi A., Nanni P., Roda A. // Eur. J. A. 2009. V. 15. № 43. P. 11444.
Dondoni A., Marra A. // Chem. Soc. Rev. 2012. V. 41. № 2. P. 573.
Jones M.W., Mantovani G., Ryan S.M., Wang X., Brayden D.J., Haddleton D.M. // Chem. Commun. 2009. № 35. P. 5272.
Slavin S., Khoshdel E., Haddleton D.M. // Polym. Chem. 2012. V. 3. № 6. P. 1461.
Grover G.N., Alconcel S.N.S., Matsumoto N.M., Maynard H.D. // Macromolecules. 2009. V. 42. № 20. P. 7657.
Li M., De P., Li H., Sumerlin B.S. // Polym. Chem. 2010. V. 1. № 6. P. 854.
Liu Z., Ou J., Zou H. // Trends Anal. Chem. 2016. V. 82. P. 89.
Ribeiro L.F., Masini J.C., Svec F. // Trends Anal. Chem. 2019. V. 118. P. 606.
Yao X., Tan T.T.Y., Wang Y. // J. Chromatogr. A. 2014. V. 1326. P. 80.
Yang D., Yu D.P., Dong X.F., Shen A.J., Jin G.W., Guo Z.M., Yan J.Y., Liu M.Y., Liang X.M. // Chinese J. Anal. Chem. 2015. V. 43. № 10. P. 1439.
Tang X., Li X., Sun Y., Xiao Y., Wang Y. // J. Sep. Sci. 2018. V. 41. № 13. P. 2710.
Yin C., Chen W., Zhang J., Zhang M., Zhang J. // Sep. Purif. Technol. 2019. V. 210. P. 175.
Chu Q., Liu Y., Jiang S., Zhu Y., Lyu H., Xie Z. // Anal. Chim. Acta. 2021. V. 1146. P. 109.
Mompó-Roselló Ó., Vergara-Barberán M., Lerma-García M.J., Simó-Alfonso E.F., Herrero-Martínez J.M. // Microchem. J. 2021. V. 164. P. 106018.
Zuo Y., Zhang Y., Gou Z., Lin W. // Sensors Actuators B. 2019. V. 291. P. 235.
Cao J., Zuo Y., Lu H., Yang Y., Feng S. // J. Photochem. Photobiol. A 2018. V. 350. P. 152.
Yap P.L., Auyoong Y.L., Hassan K., Farivar F., Tran D.N.H., Ma J., Losic D. // Chem. Eng. J. 2020. V. 395. P. 124965.
He H., Meng X., Yue Q., Yin W., Gao Y., Fang P., Shen L. // Chem. Eng. J. 2021. V. 405. P. 126743.
Hou K., Jin Y., Chen J., Wen X., Xu S., Cheng J., Pi P. // Mater. Lett. 2017. V. 202. P. 99.
Wu Z., Li Y., Zhang L., Zhong Y., Xu H., Mao Z., Wang B., Sui X. // RSC Adv. 2017. V. 7. № 33. P. 20147.
Liang L., Dong Y., Liu Y., Meng X. // Polymers (Basel). 2019. V. 11. № 12. P. 2072.
Shen X., Liu P., He C., Xia S., Liu J., Cheng F., Suo H., Zhao Y., Chen L. // Sep. Purif. Technol. 2021. V. 255. P. 117418.
Shen X., Liu T., Xia S., Liu J., Liu P., Cheng F., He C. // Ind. Eng. Chem. Res. 2020. V. 59. № 46. P. 20382.
Meng G., Yan J., Wu J., Zhang W., Wang Y., Wang Q., Liu Z., Guo X. // Fibers Polym. 2020. V. 21. № 2. P. 245.
Chen X., Chu R., Xing T., Chen G. // Colloids Surfaces A Physicochem. Eng. Asp. 2021. V. 611. P. 125803.
Davidovich-Pinhas M., Bianco-Peled H. // J. Mater. Sci. Mater. Med. 2010. V. 21. № 7. P. 2027.
Brannigan R.P., Khutoryanskiy V.V. // Colloids Surf. B. 2017. V. 155. P. 538.
Porfiryeva N.N., Nasibullin S.F., Abdullina S.G., Tukhbatullina I.K., Moustafine R.I., Khutoryanskiy V.V. // Int. J. Pharm. 2019. V. 562. P. 241.
Kolawole O.M., Lau W.M., Khutoryanskiy V.V. // Int. J. Pharm. 2018. V. 550. № 1. P. 123.
Agibayeva L.E., Kaldybekov D.B., Porfiryeva N.N., Garipova V.R., Mangazbayeva R.A., Moustafine R.I., Semina I.I., Mun G.A., Kudaibergenov S.E., Khutoryanskiy V.V. // Int. J. Pharm. 2020. V. 577. P. 119093.
Tonglairoum P., Brannigan R.P., Opanasopit P., Khutoryanskiy V.V. // J. Mater. Chem. B. 2016. V. 4. № 40. P. 6581.
Shtenberg Y., Goldfeder M., Schroeder A., Bianco-Peled H. // Carbohydr. Polym. 2017. V. 175. P. 337.
Sahatsapan N., Rojanarata T., Ngawhirunpat T., Opanasopit P., Tonglairoum P. // Carbohydr. Polym. 2018. V. 202. P. 258.
Kaldybekov D.B., Filippov S.K., Radulescu A., Khutoryanskiy V.V. // Eur. J. Pharm. Biopharm. 2019. V. 143. P. 24.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия Б)


