Водные ресурсы, 2020, T. 47, № 3, стр. 291-301
О химическом составе воды в малых притоках и прибрежной зоне озера Байкал в период экологического кризиса
В. В. Тахтеев a, c, *, Е. Р. Хадеева b, И. О. Еропова a, c, О. Г. Лопатовская a
a Иркутский государственный университет
664003 Иркутск, Россия
b Институт географии им. В.Б. Сочавы СО РАН
664033 Иркутск, Россия
c Байкальский музей Иркутского НЦ СО РАН
664520 пос. Листвянка, Иркутской обл., Россия
* E-mail: Amphipoda@yandex.ru
Поступила в редакцию 02.10.2019
После доработки 28.11.2019
Принята к публикации 24.12.2019
Аннотация
В связи с наблюдаемым в последние годы экологическим кризисом на ряде участков прибрежной зоны оз. Байкал в июне 2018 г. исследован химический состав вод в семи точках этой зоны на различном расстоянии от населенных пунктов и в шести малых притоках озера. Для сопоставления данных по разным биологическим сезонам в озере отбор проб воды был повторен в августе–сентябре 2019 г. на четырех предыдущих точках и пяти дополнительных. Наименее минерализованными оказались притоки южной части Байкала. Общая минерализация байкальских вод остается невысокой и не выходит за пределы фоновых значений предыдущих десятилетий, содержание экологически опасных элементов также низкое, за исключением повышенной концентрации стронция в термальных водах руч. Горячинского. В то же время в большинстве точек в водах Байкала отмечено повышенное содержание азота, а в средней части озера (Баргузинский залив у пос. Максимиха, у п-ова Святой Нос и у о. Большой Ушканий) зарегистрировано аномально высокое содержание фосфатов – 0.413–0.941 мг/л. Значительное обогащение вод Байкала биогенными элементами, способное вызывать экстремально высокие величины биомассы водорослей в конце лета – начале осени, наблюдалось не только вблизи населенных пунктов, но и в удаленных от них районах и не обусловлено вносом этих элементов с водами притоков. Это требует выявления источников их поступления. В конце августа – начале сентября 2019 г., в период активного поглощения фосфора летним фитопланктоном и донными водорослями, содержание фосфатов в Среднем Байкале снизилось, оставаясь повышенным (0.09 мг/л) в районе Максимихи, но резко повысилось (1.33 мг/л) в термальном руч. Горячинском. Воды в районе г. Слюдянки (южная часть озера) в этот период содержали большое количество нитратов (1.67–1.94 мг/л); наибольшее их значение отмечено в районе Максимихи (2.39 мг/л). Очень высокое содержание биогенных элементов в водах Байкала, очевидно, требует серьезных комплексных мер по снижению антропогенной нагрузки на экосистему озера.
ВВЕДЕНИЕ
Озеро Байкал считается крупнейшим на планете хранилищем пресной воды высокого качества. Однако в последние несколько лет на некоторых участках прибрежной зоны озера наблюдаются кризисные явления, связанные с антропогенным эвтрофированием и массовым развитием водорослей [8, 20, 25–27], прежде всего представителей рода Spirogyra, а также c бактериальным загрязнением прибрежных вод в местах расположения крупных поселков [18]. Проблема вызвана, в числе прочего, значительным увеличением потока туристов на берега Байкала, развитием инфраструктуры туризма и, как следствие, увеличением поступления биогенных соединений фосфора и азота в воды озера. В результате аномально обильного развития водорослей прибрежные мелководья оказываются непригодными для нереста августовского стада бычка-желтокрылки Cottocomephorus grewingkii (Dyb.) [22], молодь которого служит одним из основных пищевых компонентов байкальского омуля, а береговые пляжи становятся эстетически непривлекательными и грязными из-за скоплений огромного количества водорослей, здесь же подвергающихся гниению [27]. Климатические особенности последнего десятилетия – повышение температуры воздуха и воды, маловодность, ослабление ветровых течений – усугубили эти негативные процессы [15].
Биогенные элементы поступают в Байкал как непосредственно с побережий, так и с водами крупных и малых притоков. При этом вклад малых притоков изучен значительно меньше, чем крупных, но он тоже важен для формирования качества прибрежных вод озера. Так, в 2012 г. в небольшой р. Максимихе (приток средней части Байкала) было зафиксировано повышенное содержание нитратов (0.26 мг/л) и фосфатов (0.22 мг/л), была повышена общая минерализация воды в приустьевом участке до 135 мг/л [25]. В гидрокарбонатно-кальциевых водах Байкала в докризисный период общее содержание основных ионов составляло 90–100 мг/л, в водах его притоков в среднем несколько выше – 108–120 мг/л [1, 2]. Фоновое содержание фосфатного фосфора в поверхностных байкальских водах колебалось от 0.003 до 0.057 мг/л в зависимости от сезона года и содержания фитопланктона (в среднем за 1948–1955 гг. – 0.019 мг/л); содержание нитратного азота – от 0 до 0.078 мг/л (среднегодовая величина – 0.035 мг/л) [1]. Содержание кремния в водах Байкала было невелико, редко превышaло 1200–1400 мг/м3 в поверхностных водах и значительно снижалось в период подледного развития диатомовых водорослей (600–800 мг/м3, редко менее) [1].
Цель данной работы – определить современный химический состав воды в малых притоках Байкала и на прилегающих к ним участках озера в период, непосредственно предшествующий массовой вегетации водорослей при различной антропогенной нагрузке.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Выбраны шесть малых притоков и прилегающих к ним участков побережья в южной и средней частях Байкала (рисунок). Часть районов исследования удалена от населенных пунктов, поэтому они могли бы считаться чистыми и условно чистыми (у м. Киркирей в Южном Байкале, в бух. Таланка и у м. Маркова в Среднем Байкале). Другая их часть расположена у достаточно крупных поселков, в которых летом много отдыхающих (Клюевка, Горячинск, Максимиха). В качестве “чистого” района обследовано также побережье ненаселенного Большого Ушканьего острова, лишенного водотоков (рисунок, точка 7). Из водотоков не подвержены антропогенному влиянию (за исключением влиянию через атмосферу) руч. Киркирей, который лишь в устьевой части пересекает старую ветку Кругобайкальской железной дороги по специально выстроенному желобу поверх портала тоннеля, и руч. Маркова, протекающий по лишенному населенных пунктов западному гористому склону п-ова Святой Нос. Река Клюевка незначительно подвержена антропогенной нагрузке, поскольку находится на западной окраине одноименного поселка, а р. Максимиха протекает через поселок, население которого в основном обслуживает туристов, и уже несколько лет назад имела измененный химический состав вследствие загрязнения [25].
Картосхема территории расположения точек отбора проб. Кружки – июнь 2018 г., в скобках – шифр пробы: 1 – руч. Киркирей (Кр 3) и м. Киркирей (Кр 4), 2 – р. Клюевка (Кл 12) и Байкал напротив пос. Клюевка (Кл 10), 3 – р. Черемшанка (ГТ 3) и губа Таланка (ГТ 7), 4 – термальный руч. Горячинский (Гор 1) и Байкал напротив пос. Горячинск (Гор 4), 5 – р. Максимиха (М 2) и губа Максимиха (М 5), 6 – руч. Маркова (Св 1) и п-ов Святой Нос южнее м. Маркова (Св 4), 7 – о. Большой Ушканий, южное побережье (Бу 1); крестики – дополнительные точки в августе–сентябре 2019 г.: 8 – Байкал у устья р. Похабихи, 9 – Байкал у устья р. Слюдянки, 10 – Байкал у устья руч. Хакусы, 11 – Байкал в бух. Сеногда, 12 – Байкал у м. Котельниковского.
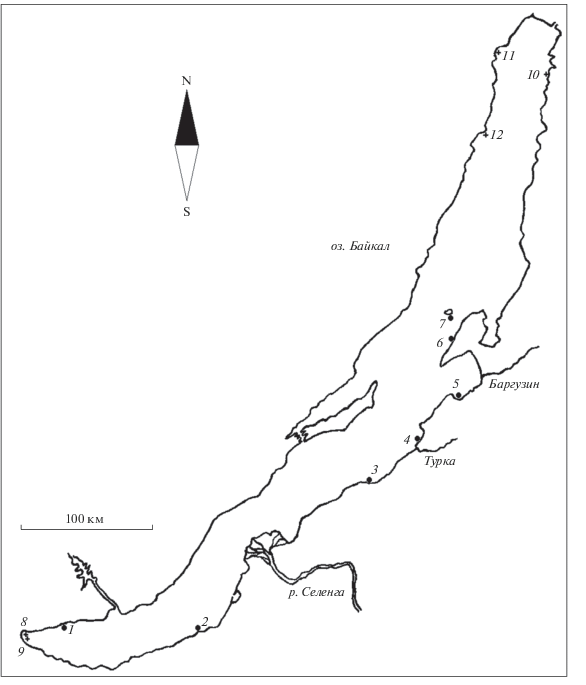
Пробы воды для химического анализа объемом 1.5 л отбирали с 23 по 28 июня 2018 г. в период после весеннего пика развития фитопланктона и до летне-осеннего пика массовой вегетации байкальских планктонных и бентосных водорослей (она начинается в июле и достигает пика в августе–сентябре) на устьевом участке реки или ручья, а также у уреза воды Байкала на расстоянии не далее 100 м от устья водотока.
25.08.2019–03.09.2019 для сопоставления данных за разные биологические сезоны в озере был повторен отбор проб воды на нескольких предыдущих точках (1, 4, 5, 7) и нескольких дополнительных (8–12) (рисунок). Точки 8, 9 и 11 находятся рядом с крупными населенными пунктами (города Слюдянка, Северобайкальск). В р. Похабиху (устье в районе точки 8) к тому же сбрасываются сточные воды с очистных сооружений г. Слюдянки. Точки 10 (бух. Хакусы) и 12 (м. Котельниковский) сравнительно слабо подвержены антропогенному воздействию (на берегу находятся лишь небольшие водолечебницы на горячих источниках).
Химический анализ воды выполняли в аккредитованной лаборатории Института географии СО РАН им. В.Б. Сочавы, согласно руководствам [6, 16]. Определение содержания фосфат-ионов проводили в соответствии с методикой, рекомендованной для целей государственного экологического контроля [7]. Химический элементный состав вод определяли на приборе “Оptima 2000-DV” на основе атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой. Ионно-солевой состав и физические свойства воды выражали в виде формулы М.Г. Курлова [11] (табл. 1). Это псевдодробь, в ее числителе – со-держание анионов в %-эквивалентах, в знаменателе – содержание катионов в %-экв. (указыва-ются только те ионы, содержание которых ≥5%-экв.); M – минерализация воды, г/дм3; T – температура, °C; справа от дроби – pH.
По содержанию в воде фосфора в период его максимальной концентрации (июнь) сделан приблизительный расчет биомассы водорослей к концу лета при его поглощении. Для этого сначала по количеству фосфат-иона рассчитывали количество атомарного фосфора Pатом, мкг на 1 л воды. Затем, пользуясь известными величинами содержания фосфора в талломах доминирующих видов водорослей, образующих в прибрежной зоне Байкала естественные растительные пояса Ulothrix zonata (F. Weber et Mohr.) Kützing, Draparnaldioides baicalensis Meyer et Skabitsch., Tetraspora cylindrica var. bullosa C. Meyer, и неаборигенной Spirogyra sp. [9, 10], вычисляли потенциальный сухой вес водорослей, которые могут развиться на определенном участке прибрежной зоны Байкала. Принято осредненное (по данным [9, 10]) содержание фосфора в этих водорослях – 1500 мкг/г сухой массы. Сухой вес водорослей пересчитан в сырой путем умножения на повышающий коэффициент 3.3, установленный для зеленой водоросли Chlorella vulgaris Beijerinck [4]. Таким образом, потенциальную первичную продукцию, или возможную биомассу водорослей в сыром весе Bсыр (г/л воды), рассчитывали по формуле:
Для расчета возможной продукции водорослей на 100 м береговой линии среднюю ширину прибрежной абразионной платформы Байкала принимали за 100 м, ее максимальную глубину до начала свала – 15 м. Следовательно, напротив 1 м береговой линии от уреза до свала глубин объем водной массы ~750 м3 (или 750 000 л), напротив 100 м побережья – 75 000 м3.РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В табл. 1 представлены общие физико-химические свойства исследованной воды в 2018 г. по формуле М.Г. Курлова, в табл. 2 детализированы сведения о составе главных ионов и общей минерализации.
Таблица 1.
Физико-химические свойства воды в исследованных районах в июне 2018 г.
| Район | Шифр пробы | Место сбора | Формула Курлова |
|---|---|---|---|
| 1 | Кр 3 | Ручей | $M{\text{ 0}}{\text{.05}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{67S}}{{{\text{O}}}_{{\text{4}}}}25{\text{Cl8}}}}{{{\text{Ca}}5{\text{7Mg26Na13}}}}T{\text{ 8}}{\text{.5}}^\circ {\text{ pH 7}}{\text{.23}}$ |
| 1 | Кр 4 | Байкал | $M{\text{ 0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{82S}}{{{\text{O}}}_{{\text{4}}}}{\text{14}}}}{{{\text{Ca65Mg22 Na11}}}}T{\text{ 8}}{\text{.0}}^\circ {\text{ pH 7}}{\text{.86}}$ |
| 2 | Кл 10 | Байкал | $M{\text{ 0}}{\text{.06}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{73S}}{{{\text{O}}}_{{\text{4}}}}{\text{14Cl11}}}}{{{\text{Ca65Mg21Na11}}}}T{\text{ 6}}{\text{.5}}^\circ {\text{ pH 6}}{\text{.53}}$ |
| 2 | Кл 12 | Река | $M{\text{ 0}}{\text{.02}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{73S}}{{{\text{O}}}_{{\text{4}}}}{\text{18Cl}}7}}{{{\text{Ca59Na23Mg}}15}}T{\text{ 10}}{\text{.0}}^\circ {\text{ pH 6}}.45$ |
| 3 | ГТ 3 | Река | $M{\text{ 0}}{\text{.08}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{61S}}{{{\text{O}}}_{{\text{4}}}}34}}{{{\text{Ca53Mg27Na}}1{\text{7}}}}T{\text{ 9}}{\text{.0}}^\circ {\text{ pH 6}}{\text{.45}}$ |
| 3 | ГТ 7 | Байкал | $M{\text{ 0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{80S}}{{{\text{O}}}_{{\text{4}}}}15}}{{{\text{Ca64Mg22Na11}}}}T{\text{ 14}}{\text{.0}}^\circ {\text{ pH 6}}{\text{.43}}$ |
| 4 | Гор 1 | Ручей | $M{\text{ 0}}{\text{.50 }}\frac{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}{\text{81HC}}{{{\text{O}}}_{{\text{3}}}}{\text{13}}}}{{{\text{Na78Ca18}}}}T{\text{ 20}}{\text{.0}}^\circ {\text{ pH 6}}{\text{.92}}$ |
| 4 | Гор 4 | Байкал | $M{\text{ 0}}{\text{.08}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{64S}}{{{\text{O}}}_{{\text{4}}}}{\text{31}}}}{{{\text{Ca53Na27Mg17}}}}T{\text{ 16}}{\text{.5}}^\circ {\text{ pH 7}}{\text{.77}}$ |
| 5 | М 2 | Река | $M{\text{ 0}}{\text{.09}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{72S}}{{{\text{O}}}_{{\text{4}}}}{\text{25}}}}{{{\text{Ca56Mg}}21{\text{Na21}}}}T{\text{ 18}}{\text{.5}}^\circ {\text{ pH 7}}.09$ |
| 5 | М 5 | Байкал | $M{\text{ 0}}{\text{.09}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{72S}}{{{\text{O}}}_{{\text{4}}}}{\text{24}}}}{{{\text{Ca58Mg21Na19}}}}T{\text{ 14}}{\text{.0}}^\circ {\text{ pH 7}}{\text{.41}}$ |
| 6 | Св 1 | Ручей | $M{\text{ 0}}{\text{.08}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{85S}}{{{\text{O}}}_{{\text{4}}}}{\text{13}}}}{{{\text{Ca86Mg}}9}}T{\text{ 8}}{\text{.0}}^\circ {\text{ pH 7}}.89$ |
| 6 | Св 4 | Байкал | $M{\text{ 0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{82S}}{{{\text{O}}}_{{\text{4}}}}{\text{15}}}}{{{\text{Ca69Mg20Na9}}}}T{\text{ 11}}{\text{.0}}^\circ {\text{ pH 8}}{\text{.31}}$ |
| 7 | Бу 1 | Байкал | $M{\text{ 0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{84S}}{{{\text{O}}}_{{\text{4}}}}{\text{1}}2}}{{{\text{Ca66Mg21Na10}}}}T{\text{ 9}}{\text{.0}}^\circ {\text{ pH 7}}{\text{.36}}$ |
Таблица 2.
Содержание основных ионов в воде и ее общая минерализация (M) в июне 2018 г.
| Район | Шифр пробы | рН | ${\text{НСО}}_{3}^{{2 - }}$ | Cl– | ${\text{SO}}_{4}^{{2 - }}$ | ${\text{PO}}_{4}^{{3 - }}$ | ${\text{NO}}_{3}^{ - }$ | Ca2+ | Mg2+ | Na+ | K+ | M |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| мг/дм3 | ||||||||||||
| 1 | Кр 3 | 7.23 | 34.40 | 2.61 | 10.20 | 0.039 | 0.33 | 9.41 | 2.53 | 2.61 | 1.27 | 45.83 |
| 1 | Кр 4 | 7.86 | 65.15 | 1.42 | 8.61 | 0.006 | 0.61 | 18.00 | 3.67 | 3.56 | 1.29 | 69.12 |
| 2 | Кл 10 | 6.53 | 52.70 | 4.61 | 8.18 | 0.009 | 0.79 | 14.03 | 2.62 | 2.82 | 1.05 | 59.65 |
| 2 | Кл 12 | 6.45 | 19.76 | 1.01 | 3.85 | 0.039 | 0.45 | 4.67 | 0.78 | 2.16 | 0.36 | 22.70 |
| 3 | ГТ 3 | 6.45 | 55.88 | 1.77 | 24.90 | 0.045 | 0.99 | 16.23 | 4.99 | 5.91 | 1.73 | 83.48 |
| 3 | ГТ 7 | 6.43 | 67.59 | 2.13 | 10.25 | 0.012 | 0.31 | 19.13 | 3.99 | 3.62 | 1.64 | 74.56 |
| 4 | Гор 1 | 6.92 | 55.63 | 12.76 | 278.50 | 0.120 | 3.18 | 29.10 | 2.74 | 144.91 | 3.28 | 499.26 |
| 4 | Гор 4 | 7.77 | 57.58 | 1.77 | 22.26 | 0.024 | 0.67 | 17.13 | 3.27 | 10.23 | 1.26 | 84.72 |
| 5 | М 2 | 7.09 | 71.98 | 1.06 | 19.71 | 0.094 | 0.48 | 19.04 | 4.34 | 8.11 | 1.25 | 89.50 |
| 5 | М 5 | 7.41 | 71.74 | 1.42 | 19.10 | 0.941 | 0.41 | 19.26 | 4.26 | 7.29 | 1.29 | 88.47 |
| 6 | Св 1 | 7.89 | 78.32 | 1.06 | 8.94 | 0.135 | 0.90 | 30.15 | 1.92 | 1.52 | 0.94 | 83.70 |
| 6 | Св 4 | 8.31 | 63.44 | 1.06 | 9.27 | 0.413 | 0.18 | 20.31 | 3.50 | 3.24 | 1.19 | 70.28 |
| 7 | Бу 1 | 7.36 | 65.88 | 1.42 | 7.63 | 0.458 | 0.61 | 19.37 | 3.74 | 3.45 | 1.21 | 69.76 |
Ионный состав несколько варьировал в разных притоках Байкала. Вода притоков его южной части (Киркирей, Клюевка) очень слабо минерализована, гидрокарбонатно-кальциевого типа, что соответствует фоновым значениям в притоках в докризисное время (середина–конец XX в.) [1, 2] или даже ниже их. В р. Клюевке (хребет Хамар-Дабан) зарегистрирована минимальная минерализация – 0.023 г/л. По-видимому, у многих малых водотоков, стекающих с этого хребта, в целом минерализация гораздо ниже, чем у байкальской воды. Так, по данным авторов, в небольших притоках Байкала, протекающих между г. Байкальскoм и пос. Мурино, летом 2017 и 2018 гг. она варьировала в пределах 0.03–0.07 г/л.
Гидрокарбонатно-кальциевая вода отмечена и для руч. Маркова, но ее минерализация была немного выше, чем в Байкале. В р. Черемшанке наблюдалось то же самое, однако тип воды был сульфатно-гидрокарбонатный магниево-кальциевый (табл. 1). Также в водах этой реки отмечено самое высокое содержание железа (>1 мг/л) (табл. 3), и вода имела оранжевый оттенок. Обогащение железом, как и ионами сульфата и магния, может происходить из-за болота, расположенного рядом с устьевым участком реки. Также значительно более высокое содержание железа свойственно р. Максимихе, образующей в устьевой части озеровидную заводь; вода в ней сульфатно-гидрокарбонатная кальциевая (в 2019 г. – гидрокарбонатная кальциевая), минерализация соответствует таковой на прилегающем участке Байкала.
Таблица 3.
Содержание микрокомпонентов в пробах воды в июне 2018 г. (значения со знаком “<” – микроэлемент не обнаружен, его содержание ниже указанного конструктивного предела обнаружения для использованного аналитического прибора)
| Район | Шифр пробы | Элементы и их концентрация, мг/дм3 | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Mo | Mn | Ba | Al | Pb | Cu | Cr | Fe | Si | Zn | Sr | Ti | Co | Cd | As | ||
| 1 | Кр 3 | 0.022 | 0.003 | 0.003 | 0.116 | <0.001 | <0.001 | <0.001 | 0.101 | 6.586 | <0.005 | 0.024 | 0.004 | 0.005 | <0.0001 | <0.005 |
| 1 | Кр 4 | 0.022 | <0.001 | 0.004 | <0.010 | <0.001 | 0.001 | <0.001 | <0.050 | 0.171 | <0.005 | 0.087 | <0.001 | <0.001 | <0.0001 | <0.005 |
| 2 | Кл 10 | 0.022 | 0.007 | 0.003 | <0.010 | <0.001 | 0.001 | 0.001 | <0.050 | 0.980 | <0.005 | 0.042 | <0.001 | <0.001 | <0.0001 | <0.005 |
| 2 | Кл 12 | 0.016 | 0.002 | 0.001 | <0.010 | <0.001 | <0.001 | <0.001 | <0.050 | 5.257 | <0.005 | 0.020 | <0.001 | <0.001 | <0.0001 | <0.005 |
| 3 | ГТ 3 | 0.013 | 0.012 | 0.005 | 0.027 | 0.005 | 0.001 | 0.001 | 1.070 | 6.517 | 0.005 | 0.037 | 0.001 | <0.001 | <0.0001 | <0.005 |
| 3 | ГТ 7 | 0.023 | 0.009 | 0.006 | <0.010 | <0.001 | 0.001 | <0.001 | <0.050 | 0.304 | <0.005 | 0.077 | <0.001 | <0.001 | <0.0001 | <0.005 |
| 4 | Гор 1 | 0.012 | 0.004 | 0.010 | 0.028 | 0.001 | 0.001 | <0.001 | <0.050 | 18.399 | <0.005 | 0.420 | <0.001 | 0.001 | <0.0001 | <0.005 |
| 4 | Гор 4 | 0.003 | <0.001 | 0.005 | <0.010 | 0.004 | <0.001 | <0.001 | <0.050 | 2.195 | 0.028 | <0.001 | 0.107 | <0.001 | 0.001 | <0.005 |
| 5 | М 2 | 0.016 | 0.010 | 0.007 | 0.086 | 0.008 | <0.001 | <0.001 | 0.577 | 7.724 | 0.070 | 0.105 | 0.003 | <0.001 | <0.0001 | <0.005 |
| 5 | М 5 | 0.012 | 0.003 | 0.008 | 0.035 | <0.001 | 0.002 | 0.001 | 0.293 | 7.742 | <0.005 | 0.042 | 0.109 | 0.001 | <0.0001 | <0.005 |
| 6 | Св 1 | 0.017 | 0.001 | 0.006 | <0.010 | <0.001 | 0.001 | <0.001 | <0.050 | 4.532 | <0.005 | 0.153 | <0.001 | <0.001 | <0.0001 | <0.005 |
| 6 | Св 4 | 0.019 | 0.001 | 0.006 | <0.010 | <0.001 | 0.001 | <0.001 | <0.050 | 1.135 | <0.005 | 0.091 | <0.001 | 0.002 | <0.0001 | <0.005 |
| 7 | Бу 1 | 0.015 | 0.001 | 0.006 | <0.010 | <0.001 | 0.001 | <0.001 | <0.050 | 0.276 | <0.005 | 0.088 | <0.001 | <0.001 | <0.0001 | <0.005 |
Вряд ли можно ожидать существенных сезонных и межгодовых изменений минерализации и химического состава вод малых притоков, поскольку большинство из них (включая исследованные авторами статьи) протекают по очень слабо растворимым кристаллическим горным породам архейского и протерозойского возраста [23].
Таким образом, малые притоки Байкала не могут быть фактором, повышающим минерализацию его вод. Также известно, что в последнее десятилетие суммарное содержание главных ионов в водах р. Селенги – крупнейшего притока озера – повысилось и достигало 119–780 мг/л [17].
Резко выделяется руч. Горячинский, вода в котором имеет гидротермальное происхождение, сульфатно-натриевая, минерализация 0.5–0.6 г/л. Этот ручей – высокотермальный источник с температурой (T) 53.0–54.5°C и расходом воды 13.5 л/с, он берет начало в 1 км от побережья Байкала и впадает в эвтрофированный Горячинский пруд, у которого расположен бальнеологический курорт, затем вытекает из него и по пути до Байкала охлаждается (в день отбора пробы в 2018 г. T = 20°C). Воды этого ручья – типичные по гидрогеологическим характеристикам для азотных термальных вод Горячинского типа, распространенных в Байкальской рифтовой зоне, содержащих кремнекислоту, с преобладанием ионов сульфата и натрия и низким содержанием гидрокарбонатов [12]. По многолетним данным, минерализация термальных вод Горячинского источника варьирует в пределах 0.49–0.65 г/л, pH 7.8–9.7 [3, 12, 14], химический состав отличается постоянством, по данным анализов с 1775 г. [12]. В отобранных авторами статьи пробах pH (6.9–7.2) ниже, чем в истоке, что связано, скорее всего, с закислением воды в вышерасположенном пруде. Содержание кремния – 18.4 мг/л (табл. 3) – на 1–2 порядка выше, чем в Байкале; в пересчете на кремнекислоту H2SiO3 это составляет 51.3 мг/л, что укладывается в многолетние ее колебания от 49 до 88 мг/л [12].
Во всех точках у береговой линии Байкала тип воды был гидрокарбонатно-кальциевый, лишь вблизи устья руч. Горячинского в 2018 г. вода оказалась cульфатно-гидрокарбонатная натриево-кальциевая, на этом сказался разлив в Байкале его вод, имеющих сульфатно-натриевый состав. В 2019 г. по химическим показателям несколько выделялась бух. Хакусы с сульфатно-гидрокарбонатной кальциевой водой; повышенное содержание сульфатов (25 мг/л) в этой точке обусловлено влиянием вод сульфатно-натриевого термального источника, впадающего в Байкал. Величина общей минерализации нигде не была за пределами нормы, кроме района устья р. Похабихи (114 мг/л). Вода имела реакцию от слабокислой до слабощелочной, наиболее высокое значение pH (8.31) отмечено у побережья п-ова Святой Нос. Содержание хлоридов в Байкале в оба года исследований – 2018 и 2019 – было несколько выше (1.06–2.84 мг/л), чем указывалось ранее для поверхностных вод открытой пелагиали (0.5–0.8 мл/л) [1]; в районе пос. Клюевка – заметно выше (4.61 мг/л).
Отметим несколько особенностей микрокомпонетного состава вод (табл. 3). Содержание кремния было в несколько раз выше в притоках, чем в Байкале, кpомe воды термального руч. Горячинского, что вполне соответствует фоновым данным [1]. В Байкале кремний интенсивно потребляется диатомовыми водорослями и губками. Исключение – бух. Максимиха, где содержание этого элемента было повышенным как в реке, так и в Байкале – примерно одинаковым.
Элементы – основные экологические токсиканты (Pb, Zn, Cu, Sr, Co, Cd, As) содержались в пробах либо в малых количествах, либо ниже предела обнаружения метода [6]. Так, кадмий отмечен лишь один раз, мышьяк не был обнаружен во всех пробах. Лишь в р. Максимихе имелось повышенное содержание цинка (0.07 мг/л), в воде руч. Киркирей – алюминия (0.12 мг/л). По содержанию стронция (0.42 мг/л) заметно выделяется вода руч. Горячинского; однако его повышенные концентрации вследствие выщелачивания горных пород свойственны многим термальным и минеральным источникам Байкальского региона, имеющим глубинное происхождение [13, 19].
Особое значение для прогноза экологической ситуации имеют данные по содержанию солей фосфора в воде, поскольку именно это часто бывает основным лимитирующим фактором для развития планктонной альгофлоры и бентосных макрофитов. Полученные результаты выявили довольно парадоксальный факт: в 2018 г. в водах южной (м. Киркирей у пос. Клюевка) и частично – средней (губа Таланка) частей Байкала содержание фосфора было заметно ниже среднемноголетних величин в докризисный период (вторая половина XX в.) и составляло 0.002–0.004 мг/л (табл. 4). Повышенные его концентрации отмечены в протекающей через поселок р. Максимихе и в горно-таежном руч. Маркова; причем, в последнем концентрация фосфора (0.044 мг/л) оказалась даже выше, чем в водах эвтрофированного руч. Горячинского (0.039 мг/л).
Таблица 4.
Количество атомарного фосфора Pатом в пробах воды в июне 2018 г. и расчетная первичная продукция водорослей Bсух, Bсыр, (Bсух – возможная первичная продукция, или потенциальная биомасса водорослей, в сухом весе; Bсыр – то же в воздушно-сыром весе)
| Район | Шифр пробы | Pатом, мкг/л | Bсух, г/л | Bсыр, г/л | Bсыр, г/м3 вод | Bсыр, кг/100 м прибрежной зоны |
|---|---|---|---|---|---|---|
| 1 | Кр 3 | 12.7 | 0.0085 | 0.0280 | 28.0 | 2100 |
| 1 | Кр 4 | 2.0 | 0.0013 | 0.0043 | 4.3 | 323 |
| 2 | Кл 10 | 2.9 | 0.0020 | 0.0065 | 6.5 | 485 |
| 2 | Кл 12 | 12.7 | 0.0085 | 0.0280 | 28.0 | 2100 |
| 3 | ГТ 3 | 14.7 | 0.0098 | 0.0323 | 32.3 | 2423 |
| 3 | ГТ 7 | 3.9 | 0.0026 | 0.0086 | 8.6 | 646 |
| 4 | Гор 1 | 39.2 | 0.0261 | 0.0861 | 86.1 | 6461 |
| 4 | Гор 4 | 7.8 | 0.0052 | 0.0172 | 17.2 | 1292 |
| 5 | М 2 | 30.7 | 0.0204 | 0.0675 | 67.5 | 5061 |
| 5 | М 5 | 307.1 | 0.2047 | 0.6755 | 675.5 | 50 665 |
| 6 | Св1 | 44.1 | 0.0294 | 0.0969 | 96.9 | 7269 |
| 6 | Св 4 | 134.8 | 0.0898 | 0.2965 | 296.5 | 22 237 |
| 7 | Бу 1 | 149.5 | 0.0996 | 0.3288 | 328.8 | 24 660 |
Вместе с тем воды Среднего Байкала в Баргузинском заливе (губа Макcимиха), у п-ова Святой Нос и у о. Большой Ушканий содержали аномально большое количество фосфатного фосфора – 0.413–0.941 мг/л ${\text{PO}}_{4}^{{3 - }}$, или 134.8–307.1 мкг/л Pатом (табл. 3, 4). Это более чем на порядок выше не только многолетних данных за XX в. [1], но и за 2006–2007 гг. для поверхностных вод центральной части Южного Байкала [5]. Для Баргузинского залива в [24] указаны сравнительно высокие концентрации фосфора в августе 2002 г.; однако, по этим данным, они составляли в прибрежной зоне у устья р. Баргузин лишь 0.15–0.16 μmol P L–1, или 4.7–5.0 мкг/л, что в 61–65 раз ниже, чем наблюдалось в июне 2018 г. в бух. Максимихе, и даже ниже среднего фонового содержания в поверхностной воде Байкала в августе при летнем пике биомассы альгофлоры: в 1948–1955 гг. оно составляло 10 мкг/л [1]. В р. Максимихе в день настоящего исследования (27.06.2018) содержание фосфатов было на порядок меньше, чем в водах одноименной бухты.
Для сравнения приведем данные, полученные для придельтового участка у р. Селенги – крупнейшего притока Байкала, протекающего через г. Улан-Удэ и собирающего биогенные элементы со значительной территории. Качество вод этой реки в настоящее время по величине индекса сапробности определяется как “умеренно загрязненные”, в меженные периоды снижается до уровня “загрязненные” [17]. В подледный период концентрация минерального фосфора в воде обычно максимальна. В марте 2002–2007 гг. в устье селенгинской протоки Харауз она менялась от 0.012 до 0.042 мг/л с некоторой тенденцией к повышению; в поверхностных водах Байкала всего в 1 км от устья протоки она снижалась в 3–5 раз [21]. В июле в эти же годы она не превышала 0.005–0.014, в октябре – 0.002 мг/л [21]. В марте 2013 и 2015 гг. содержание минерального фосфора в воде Селенги было не выше 27–35 мкг/л [17].
Даже воды такой крупной и достаточно загрязненной реки привносят в озеро фосфора меньше, чем обнаружено авторами статьи в водах Среднего Байкала. Это, а также значительно меньшее содержание фосфора в р. Максимихе и руч. Маркова в сравнении с прилегающими участками акватории Байкала свидетельствует о том, что высокое насыщение фосфором этой части озера не обусловлено его поступлением из притоков. Регенерация фосфора в таком количестве после весеннего пика развития фитопланктона невозможна; следовательно, он в больших количествах поступает в озеро с его побережий. Определенный вклад в увеличение его количества в озере могла внести и активизация судоходства.
Таким образом, количество фосфатного фосфора, отмеченного в 2018 г. в водах Баргузинского залива и севернее него, способно обеспечить громадную первичную продукцию водорослей (либо совокупности водорослей и высших водных растений), которая привела бы в конце лета к многотонным береговым выбросам отмирающих талломов (табл. 4), запечатленных на фотографиях в [25–27].
В то же время следует отметить, что в середине XX в. соотношение нитратного азота и фосфатного фосфора в водном слое 0–250 м открытого Байкала в районе пос. Большие Коты было в пределах 1.5–1.9, редко поднималось до 2.3–2.5, тогда как для обеспечения баланса этих биогенных элементов в байкальских гидробионтах оно должно быть в пределах 4.7–7.0 [1]; т.е. в чистых байкальских водах наблюдался дефицит азота. По данным авторов статьи (табл. 5), в районах южнее Баргузинского залива в водах как Байкала, так и его малых притоков в 2018 г. соотношение азота и фосфора было значительно выше необходимого – от 8.5 до 101.7. В р. Максимихе и в руч. Маркова оно было в пределах нормы – 5.1–6.7, однако в водах Байкала в бух. Максимихе, у о. Большой Ушканий и особенно у п-ова Святой Нос – очень низким – 0.4–1.3. В этих точках азот был в относительном дефиците, и его недостаток мог ограничивать бурную вегетацию альгофлоры. В то же время следует учитывать, что входящие в ее состав цианопрокариоты, прежде всего массовый в летний период планктонный вид Anabaena lemmermannii P.G. Richter, могут фиксировать молекулярный азот из внешней среды [25] и тем самым восполнять дефицит этого элемента.
Таблица 5.
Количество атомарного азота Nатом в пробах воды в июне 2018 г. и соотношение содержания азота и фосфора N/P
| Район | Шифр пробы | Nатом, мкг/л | N/P |
|---|---|---|---|
| 1 | Кр 3 | 74.6 | 8.5 |
| 1 | Кр 4 | 138.6 | 101.7 |
| 2 | Кл 10 | 179.2 | 87.8 |
| 2 | Кл 12 | 102.2 | 11.5 |
| 3 | ГТ 3 | 224.0 | 22.0 |
| 3 | ГТ 7 | 70.0 | 25.8 |
| 4 | Гор 1 | 718.2 | 26.5 |
| 4 | Гор 4 | 151.2 | 27.9 |
| 5 | М 2 | 109.2 | 5.1 |
| 5 | М 5 | 93.8 | 0.4 |
| 6 | Св1 | 204.4 | 6.7 |
| 6 | Св 4 | 40.6 | 0.4 |
| 7 | Бу 1 | 138.6 | 1.3 |
Поверхностные воды открытого Байкала отличаются очевидным постоянством минерализации и химического состава, что можно видеть при сопоставлении данных за июнь 2018 г. и август–сентябрь 2019 г. (табл. 2, 6). Регулярные штормы в безледный период вызывают перемешивание поверхностных вод и, как следствие, слабую вариабельность их гидрохимических характеристик.
В конце августа – начале сентября 2019 г. картина распределения азота и фосфора была иной. Содержание фосфатов в районе о. Большой Ушканий почти соответствовало среднемноголетнему значению – 0.02 мг/л (табл. 7), в Баргузинском заливе у Максимихи – было повышенным (0.09 мг/л), но все же на порядок ниже, чем в июне 2018 г. При этом концентрация фосфат-иона в р. Максимихе (0.20 мг/л) была выше, чем в Байкале. Заметно повышенным (0.15 мг/л) было содержание фосфатов в районе устья р. Похабихи, принимающей сточные воды от г. Слюдянки. И наиболее высоким оно оказалось в воде руч. Горячинского (1.33 мг/л), что можно связать с активной регенерацией фосфора из отмирающего обильного фитопланктона в эвтрофированном Горячинском пруде.
Таблица 6.
Физико-химические свойства воды в исследованных районах в августе–сентябре 2019 г.
| Район | Место сбора | Формула Курлова |
|---|---|---|
| 1 | Байкал | $M\,\,{\text{0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{83S}}{{{\text{O}}}_{{\text{4}}}}12}}{{{\text{Ca}}5{\text{5Mg21Na21}}}}\,\,{\text{pH 8}}{\text{.20}}$ |
| 4 | Ручей | $M\,\,{\text{0}}{\text{.58}}\frac{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}82{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{13}}}}{{{\text{Na80Ca15}}}}\,\,{\text{pH}}\,\,{\text{7}}{\text{.24}}$ |
| 4 | Байкал | $M\,\,{\text{0}}{\text{.06}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{87}}}}{{{\text{Ca55Na21Mg21}}}}\,\,{\text{pH}}\,\,{\text{8}}{\text{.12}}$ |
| 5 | Река | $M\,\,{\text{0}}{\text{.09}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{75S}}{{{\text{O}}}_{{\text{4}}}}{\text{19}}}}{{{\text{Ca52Na25Mg20}}}}\,\,{\text{pH}}\,\,{\text{8}}{\text{.02}}$ |
| 5 | Байкал | $M\,\,{\text{0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{79S}}{{{\text{O}}}_{{\text{4}}}}{\text{13}}}}{{{\text{Ca59Mg}}21{\text{Na17}}}}\,\,{\text{pH}}\,\,{\text{7}}.88$ |
| 7 | Байкал | $M\,\,{\text{0}}{\text{.06}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{80S}}{{{\text{O}}}_{{\text{4}}}}{\text{13}}}}{{{\text{Ca62Mg21Na15}}}}\,\,{\text{pH}}\,\,{\text{7}}{\text{.89}}$ |
| 8 | Байкал | $M\,\,{\text{0}}{\text{.11}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{84S}}{{{\text{O}}}_{{\text{4}}}}{\text{10}}}}{{{\text{Ca63Mg25Na10}}}}\,\,{\text{pH}}\,\,{\text{8}}{\text{.04}}$ |
| 9 | Байкал | $M\,\,{\text{0}}{\text{.09}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{83S}}{{{\text{O}}}_{{\text{4}}}}13}}{{{\text{Ca62Mg23Na}}1{\text{3}}}}\,\,{\text{pH}}\,\,{\text{8}}{\text{.12}}$ |
| 10 | Байкал | $M\,\,{\text{0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{51S}}{{{\text{O}}}_{{\text{4}}}}43}}{{{\text{Ca64Mg20Na14}}}}\,\,{\text{pH}}\,\,{\text{6}}{\text{.63}}$ |
| 11 | Байкал | $M\,\,{\text{0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{81S}}{{{\text{O}}}_{{\text{4}}}}{\text{13}}}}{{{\text{Ca59Mg22Na17}}}}\,\,{\text{pH}}\,\,{\text{7}}{\text{.92}}$ |
| 12 | Байкал | $M\,\,{\text{0}}{\text{.07}}\frac{{{\text{HC}}{{{\text{O}}}_{{\text{3}}}}{\text{80S}}{{{\text{O}}}_{{\text{4}}}}{\text{15}}}}{{{\text{Ca65Mg21Na13}}}}\,\,{\text{pH}}\,\,{\text{8}}{\text{.18}}$ |
Таблица 7.
Содержание фосфатов и нитратов, атомарного фосфора и азота и их соотношение N/P в исследованных районах в 2019 г.
| Район | Место сбора | ${\text{PO}}_{4}^{{3--}},$ мг/дм3 | Pатом, мкг/л | ${\text{NO}}_{3}^{ - },$ мг/дм3 | Nатом, мкг/л | N/P |
|---|---|---|---|---|---|---|
| 1 | Байкал | 0.005 | 1.63 | 0.07 | 15.8 | 9.7 |
| 4 | Ручей | 1.330 | 434.00 | 0.29 | 65.5 | 0.2 |
| 4 | Байкал | 0.005 | 1.63 | 0.07 | 15.8 | 9.7 |
| 5 | Река | 0.200 | 65.26 | 0.22 | 49.7 | 0.8 |
| 5 | Байкал | 0.090 | 29.37 | 2.39 | 539.7 | 18.4 |
| 7 | Байкал | 0.020 | 6.53 | 0.11 | 24.8 | 3.8 |
| 8 | Байкал | 0.147 | 47.97 | 1.67 | 377.1 | 7.8 |
| 9 | Байкал | 0.004 | 1.31 | 1.94 | 438.1 | 334.4 |
| 10 | Байкал | 0.010 | 3.26 | 0.16 | 36.1 | 11.1 |
| 11 | Байкал | 0.030 | 9.80 | 0.11 | 24.9 | 2.5 |
| 12 | Байкал | 0.008 | 2.61 | 0.07 | 15.8 | 6.1 |
Меньшее содержание фосфора к концу лета – закономерное для Байкала явление. Как отмечал К.К. Вотинцев, во время летней вспышки развития фитопланктона: “чаще всего в августе содержание соединений азота и фосфора в трофогенном слое озера достигает своего летнего минимума” [1]. По предположению авторов настоящей статьи, значительная часть фосфора из вод озера была извлечена в ходе особенно бурного разрастания водорослей (прежде всего спирогиры, а также цианобактерий) в августе–сентябре 2018 г., описанного в [27, 28]. Многотонные выбросы спирогиры отмечены на пляже у пос. Максимиха [27], на севере озера у пос. Заречного, а на побережье о. Большого Ушканьего – обильные выбросы синезеленых (ностоков). Это подтвердило высказанное выше предположение и возможность прогнозировать “урожай” водорослей к концу лета по содержанию фосфора в воде в его начале.
Содержание нитратного азота было очень высоким в районе Максимихи (2.39 мг/л), чуть ниже – в районе г. Слюдянки (1.67–1.94 мг/л). Отношение нитратного азота к фосфатному фосфору (2.5) на уровне фоновых данных XX в. отмечено только в бух. Сеногде (табл. 7), немного выше – у о. Большой Ушканий (точка 7). В остальных точках открытого Байкала отношение намного выше фонового, а в районе устья р. Слюдянки превышение азота над фосфором оказалось экстремальным (334.4 раза).
В целом, по результатам исследований 2018 и 2019 гг., содержание нитратного азота значительно выше фоновых величин как в притоках, так и у уреза воды Байкала. Из притоков наиболее высокой концентрацией нитратов характеризовались удаленные от поселков р. Черемшанка и руч. Маркова; однако особенно резко по этому показателю выделялся руч. Горячинский (3.18 мг/л в 2018 г.), испытывающий сильное антропогенное воздействие.
ЗАКЛЮЧЕНИЕ
Полученные результаты исследований показали, что общая минерализация байкальских вод по-прежнему невысокая и не выходит за пределы фоновых значений с момента начала гидрохимических наблюдений. В малых притоках оз. Байкал она может быть незначительно выше (р. Черемшанка, руч. Маркова), заметно ниже байкальской (руч. Киркирей, р. Клюевка), либо примерно равной ей (р. Максимиха). Исключение составляет руч. Горячинский гидротермального происхождения, но и его минерализация не достигает нижнего порога для вод малой минерализации (1 г/л). Содержание кремния в притоках повышено, часто в несколько раз по сравнению с Байкалом. Особенно богат им термальный руч. Горячинский – содержание на 1–2 порядка выше, чем в водах Байкала.
Содержание элементов – важнейших экотоксикантов – в основном незначительное или ниже предела обнаружения, за исключением повышенного содержания стронция в воде руч. Горячинского, что нормально для термальных и минеральных вод Байкальского региона.
В то же время в водах Байкала значительно возросло содержание биогенных элементов. Содержание нитратного азота в водах лишь в некоторых точках (у п-ова Святой Нос, в губе Таланка в 2018 г., у мысов Киркирей, Котельниковского и в Горячинской губе в 2019 г.) находилось в пределах фонового уровня (0.070–0.075 мг/л), в других точках – превышало его. В водах малых притоков (за исключением руч. Маркова) его количество также выше, чем известно для некоторых небольших рек. Содержание фосфатного фосфора в 2018 г. оказалось ниже среднемноголетних значений для вод Южного (наиболее густонаселенного) и Среднего Байкала и в разы повышенным в районах, удаленных от населенных пунктов (Святой Нос, о. Большой Ушканий). Наиболее высокое содержание отмечено в воде Баргузинского залива, испытывающего антропогенное воздействие, – в 8.8 раз выше такового для открытого Байкала в предыдущие десятилетия.
Таким образом, можно утверждать, что значительное обогащение Байкала биогенными элементами, способное вызывать экстремально большие величины биомассы водорослей, наблюдается не только (и не всегда) вблизи населенных пунктов, но в значительной части акватории Среднего Байкала. Это говорит о необходимости выявления источника поступления биогенов. В частности, поступление возможно с грунтовыми водами в местах значительного сосредоточения населения, туристов и отдыхающих (поселки Горячинск, Максимиха, Усть-Баргузин, Нижнеангарск, г. Северобайкальск, Чивыркуйский залив). В случае выявления антропогенной природы этого явления необходимо принятие срочных мер по снижению данной нагрузки на экосистему озера.
Список литературы
Вотинцев К.К. Гидрохимия озера Байкал. М.: Изд-во АН СССР, 1961. 312 с.
Вотинцев К.К., Глазунов И.В., Толмачева А.П. Гидрохимия рек бассейна озера Байкал. М.: Наука, 1965. 495 с.
Геохимическая деятельность микроорганизмов гидротерм Байкальской рифтовой зоны. Новосибирск: Гео, 2011. 302 с.
Домрачева Л.И. Динамика развития водорослей в дерново-подзолистой почве при ежесуточном определении // Закономерности развития почвенных микроорганизмов. Л.: Зоол. ин-т АН СССР, 1975. С. 38–52.
Домышева В.М., Ходжер Т.В. Гидрохимия Байкала. Химический баланс озера // Байкаловедение. Новосибирск: Наука, 2012. Кн. 1. С. 206–224.
Количественный химический анализ вод. Методика выполнения измерений массовой концентрации элементов в пробах питьевой, природных, сточных вод и атмосферных осадков методом атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой. ПНД Ф 14.1:2:4.135-98. М., 2008. 24 с.
Количественный химический анализ вод. Методика измерений массовой концентрации фосфат-ионов в питьевых, поверхностных и сточных водах фотометрическим методом с молибдатом аммония. Утверждена Министерством охраны окружающей среды и природных ресурсов РФ 21.03.1997. М.: Федеральный центр анализа и оценки техногенного воздействия, 2011. 18 с.
Кравцова Л.С., Ижболдина Л.А., Ханаев И.В., Помазкина Г.В., Домышева В.М., Кравченко О.С., Грачев М.А. Нарушение вертикальной зональности зеленых водорослей в открытом Лиственничном заливе озера Байкал как следствие локального антропогенного воздействия // Докл. РАН. 2012. Т. 447. № 2. С. 227–229.
Куликова Н.Н., Чебыкин Е.П., Волкова Е.А., Бондаренко Н.А., Воднева Е.Н., Сутурин А.Н. Определение элементного состава бентосных макроводорослей для индикации качества воды мелководной зоны залива Лиственничный (Южный Байкал) // Международ. науч.-иссл. журн. 2017. № 12 (66). Ч. 2. С. 166–176.
Куликова Н.Н., Волкова Е.А., Бондаренко Н.А., Чебыкин Е.П., Сайбаталова Е.В., Тимошкин О.А., Сутурин А.Н. Элементный состав и биогеохимические функции водорослей Ulothrix zonata (F. Weber et Mohr) Kützing прибрежной зоны Южного Байкала // Вод. ресурсы. 2018. Т. 45. № 6. С. 656–669.
Курлов М.Г. Классификация сибирских целебных минеральных вод. Томск: Физиотерапевтич. ин-т, 1928. 74 с.
Ломоносов И.С., Кустов Ю.И., Пиннекер Е.В. Минеральные воды Прибайкалья. Иркутск: Вост.-Сиб. кн. изд-во, 1977. 223 с.
Плюснин А.М. Гидрогеохимический режим подземных вод // Байкал: природа и люди. Энциклопедический справочник. Улан-Удэ: ЭКОС; Изд-во БНЦ СО РАН, 2009. С. 263–271.
Плюснин А.М., Замана Л.В., Шварцев С.Л., Токаренко О.Г., Чернявский М.К. Гидрогеохимические особенности состава азотных терм Байкальской рифтовой зоны // Геология и геофизика. 2013. Т. 54. № 5. С. 647–664.
Потемкина Т.Г., Потемкин В.Л., Федотов А.П. Климатические факторы как риски современных экологических изменений в береговой зоне озера Байкал // Геология и геофизика. 2018. Т. 59. № 5. С. 690–702.
Резников А.А., Муликовская Е.П., Соколов И.Ю. Методы анализа природных вод. М.: Недра, 1970. 488 с.
Сороковикова Л.М., Синюкович В.Н., Томберг И.В., Поповская Г.И., Чернышов М.С., Иванов В.Г., Ходжер Т.В. Состояние водной экосистемы дельты реки Селенги в условиях длительного маловодья // География и природ. ресурсы. 2017. № 1. С. 81–89.
Сутурин А.Н., Чебыкин Е.П., Мальник В.В., Ханаев И.В., Минаев А.В., Минаев В.В. Роль антропогенных факторов в развитии экологического стресса в литорали озера Байкал (акватория пос. Листвянка) // География и природ. ресурсы. 2016. № 6. С. 43–54.
Тахтеев В.В., Лопатовская О.Г., Окунева Г.Л., Помазкова Г.И., Самойлова Е.А., Рожкова Н.А. Экологическая характеристика хлоридно-натриевых минеральных источников бассейна реки Киренга и верхнего течения реки Лены. Сообщение 1. Общая характеристика источников и их гидрофауна // Биология внутренних вод. 2017. № 4. С. 3–14.
Тимошкин О.А., Бондаренко Н.А., Волкова Е.А., Томберг И.В., Вишняков В.С., Мальник В.В. Массовое развитие зеленых нитчатых водорослей родов Spirogyra и Stigeoclonium в прибрежной зоне Южного Байкала // Гидробиол. журн. 2014. Т. 50. № 5. С. 15–26.
Томберг И.В., Сороковикова Л.М., Поповская Г.И., Башенхаева Н.В., Синюкович В.Н., Иванов В.Г. Динамика концентраций биогенных элементов и фитопланктона в устье р. Селенги и на Селенгинском мелководье (оз. Байкал) // Вод. ресурсы. 2014. Т. 41. № 6. С. 596–605.
Ханаев И.В., Дзюба Е.В., Кравцова Л.С., Грачев М.А. Влияние массового развития зеленых нитчатых водорослей на воспроизводство желтокрылки Cottocomephorus grewingkii (Dybowski, 1874) (Cottidae) в условиях экологического кризиса озера Байкал // Докл. РАН. 2016. Т. 467. № 1. С. 119–121.
Экологический атлас бассейна озера Байкал. Иркутск: ИГ СО РАН, 2015. 145 с.
Katano T., Nakano Sh., Ueno H., Mitamura O., Anbutsu K., Masayuki K., Satoh Ya., Satoh T., Drucker V.V., Tanaka Yu., Akagashi Yu., Sugiyama M. Abundance and composition of the summer phytoplankton community along a transect from the Barguzin River to the central basin of Lake Baikal // Limnol. 2008. V. 9. P. 243–250.
Kobanova G.I., Takhteev V.V., Rusanovskaya O.O., Timofeyev M.A. Lake Baikal Ecosystem Faces the Threat of Eutrophication // Int. J. Ecol. 2016. Article ID 6058082. 7 p. https://doi.org/10.1155/2016/6058082
Rapid ecological change in the coastal zone of Lake Baikal (East Siberia): Is the site of the world’s greatest freshwater biodiversity in danger? / Eds O.A. Timoshkin, D.P. Samsonov, M. Yamamuro // J. Great Lakes Res. 2016. V. 42. № 3. P. 487–497.
Timoshkin O.A. Coastal zone of the world’s great lakes as a target field for interdisciplinary research and ecosystem monitoring: Lake Baikal (East Siberia) // Limnol. Freshwater Biol. 2018. V. 1. P. 81–97.
www. lin.irk.ru/files/tim.pdf
Дополнительные материалы отсутствуют.


